Esporozorios Reino Protista Subreino Protozoa Filo Apicomplexa Classe
Esporozoários

Reino Protista Sub-reino Protozoa Filo Apicomplexa Classe Sporozoa Ordem Eucoccidiida gondii, hominis = Isospora hominis) belii, cayetanensis) (Cryptosporidium spp. ) Famílias Sarcocystidae (Toxoplasma Sarcocystis Eimeriidae (Isospora Cyclospora Crystosporiidae

Doenças ocasionadas no homem por esporozoários • Toxoplasmose: alta prevalência (50% da população já teve contato – pode chegar a 95% em algumas áreas) • Sarcocistose: rara, mais comum em pessoas que ingerem care crua • Isosporose: rara (prevalência maior entre portadores de HIV – 10 -15%) • Criptosporidiose: prevalência maior em portadores de HIV • Malária: 300 -500 milhões de novos casos por ano; 1, 5 -2, 7 milhões de mortes por ano

Principais características dos esporozoários Tronco de cone ou conóide (Co) ligados entre si por fibras do conóide (Fc) Roptrias (R) e micronemas (produzem materiais para a aderência e a invasão da célulahospedeira Membrana celular externa (Me) e membrana celular interna (Mi), sustentada por microtúbulos do conóide (Mt) O complexo apical Anéis situados no pólo anterior, sob a membrana celular (A)
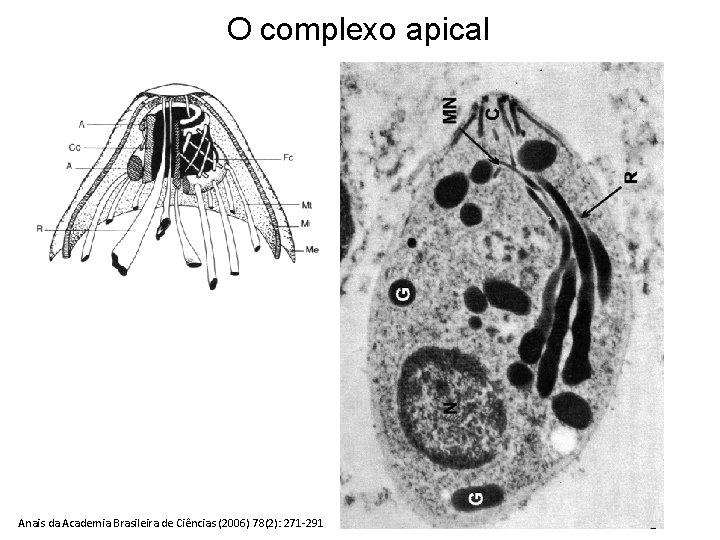
O complexo apical Anais da Academia Brasileira de Ciências (2006) 78(2): 271 -291

Taquizoíta de T. gondii Nature Rev. Microbiol. 4: 621 -628, 2006 Animal Health Research Reviews 6(1); 41– 61
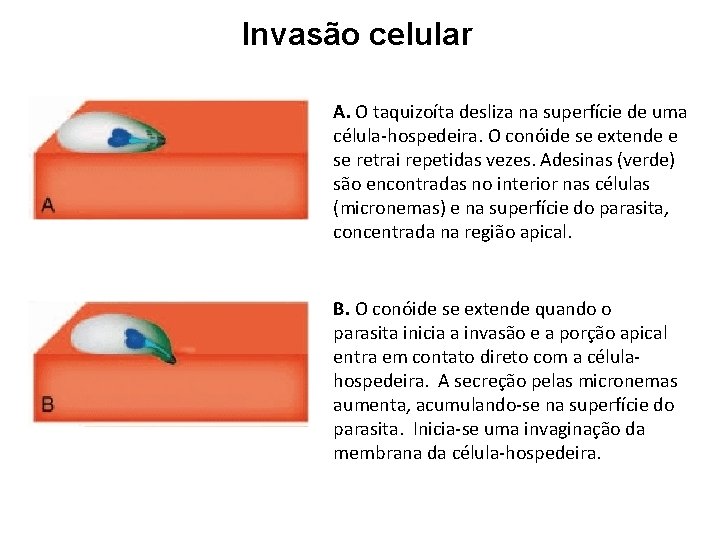
Invasão celular A. O taquizoíta desliza na superfície de uma célula-hospedeira. O conóide se extende e se retrai repetidas vezes. Adesinas (verde) são encontradas no interior nas células (micronemas) e na superfície do parasita, concentrada na região apical. B. O conóide se extende quando o parasita inicia a invasão e a porção apical entra em contato direto com a célulahospedeira. A secreção pelas micronemas aumenta, acumulando-se na superfície do parasita. Inicia-se uma invaginação da membrana da célula-hospedeira.
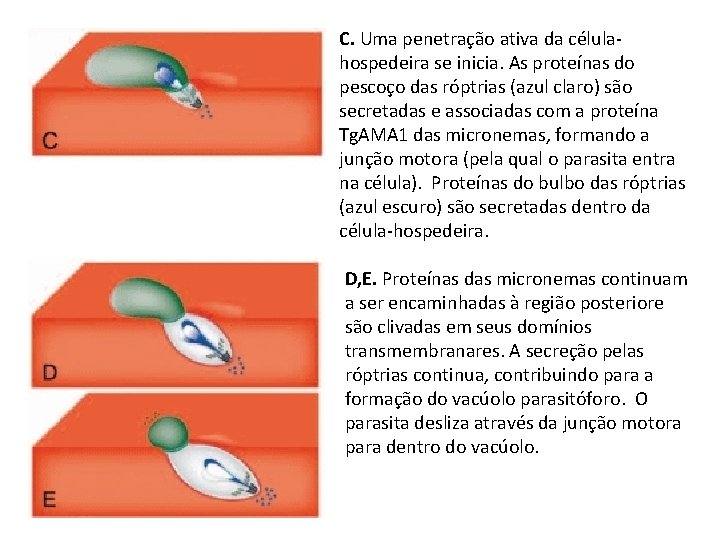
C. Uma penetração ativa da célulahospedeira se inicia. As proteínas do pescoço das róptrias (azul claro) são secretadas e associadas com a proteína Tg. AMA 1 das micronemas, formando a junção motora (pela qual o parasita entra na célula). Proteínas do bulbo das róptrias (azul escuro) são secretadas dentro da célula-hospedeira. D, E. Proteínas das micronemas continuam a ser encaminhadas à região posteriore são clivadas em seus domínios transmembranares. A secreção pelas róptrias continua, contribuindo para a formação do vacúolo parasitóforo. O parasita desliza através da junção motora para dentro do vacúolo.

F. As proteínas das micronemas são descartadas na região posterior do parasita. A invasão se completa quando a membrana do vacíolo parasitóforo se fecha. http: //www. ncbi. nlm. nih. gov/bookshelf/br. fcgi? book=eurekah&part=A 72 483&rendertype=figure&id=A 72486

Reprodução em esporozoários Esquizogonia gametócitos merozoítos esquizonte esporozoítas oocisto Esporogonia

Toxoplasmose v Agente etiológico: Toxoplasma gondii v Hospedeiro definitivo: felídeos v Hospedeiro intermediário: mamíferos (incluindo felídeos) e aves v. Toxoplasma gondii é cosmopolita, sendo encontrado em uma grande diversidade de hospedeiros v Infecção geralmente assintomática (1% dos casos apresenta sintomas) v Complicações em gestantes e portadores de HIV (30% dos soropositivos desenvolvem a doença se contaminados)

Prevalência da toxoplasmose

v 1908: Nicolle e Manceaux identificaram um protozoário no roedor africano Ctenodactylus gundi Toxo = arco; plasma = forma gondii (referente a gundi) v No mesmo ano, Splendori identifica o protozoário em coelhos no Brazil v 1970: Dubley e colaboradores descrevem o ciclo de vida de T. gondii

O ciclo de vida de T. gondii
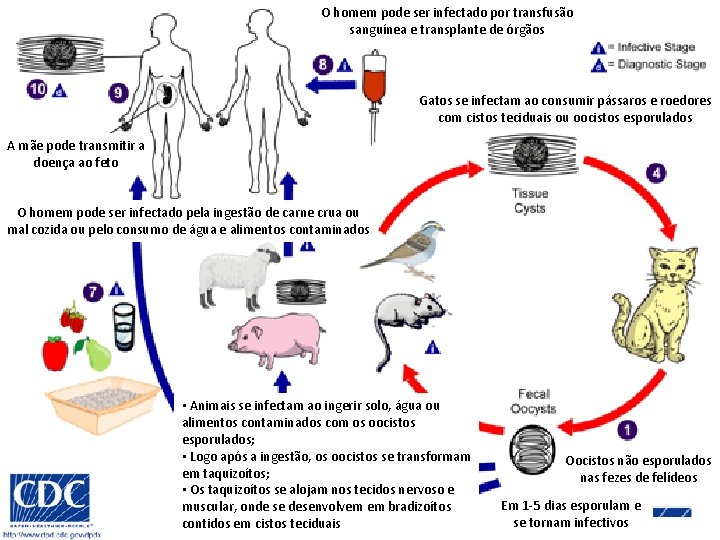
O homem pode ser infectado por transfusão sanguínea e transplante de órgãos Gatos se infectam ao consumir pássaros e roedores com cistos teciduais ou oocistos esporulados A mãe pode transmitir a doença ao feto O homem pode ser infectado pela ingestão de carne crua ou mal cozida ou pelo consumo de água e alimentos contaminados • Animais se infectam ao ingerir solo, água ou alimentos contaminados com os oocistos esporulados; • Logo após a ingestão, os oocistos se transformam em taquizoítos; • Os taquizoítos se alojam nos tecidos nervoso e muscular, onde se desenvolvem em bradizoítos contidos em cistos teciduais Oocistos não esporulados nas fezes de felídeos Em 1 -5 dias esporulam e se tornam infectivos
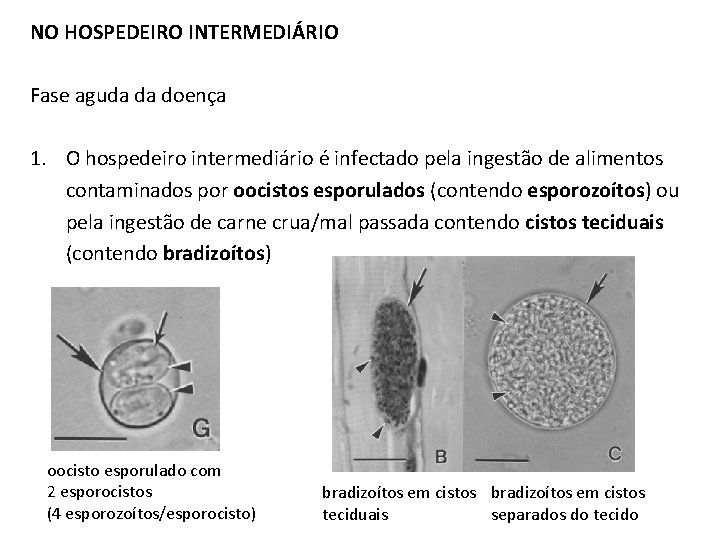
NO HOSPEDEIRO INTERMEDIÁRIO Fase aguda da doença 1. O hospedeiro intermediário é infectado pela ingestão de alimentos contaminados por oocistos esporulados (contendo esporozoítos) ou pela ingestão de carne crua/mal passada contendo cistos teciduais (contendo bradizoítos) oocisto esporulado com 2 esporocistos (4 esporozoítos/esporocisto) bradizoítos em cistos teciduais separados do tecido
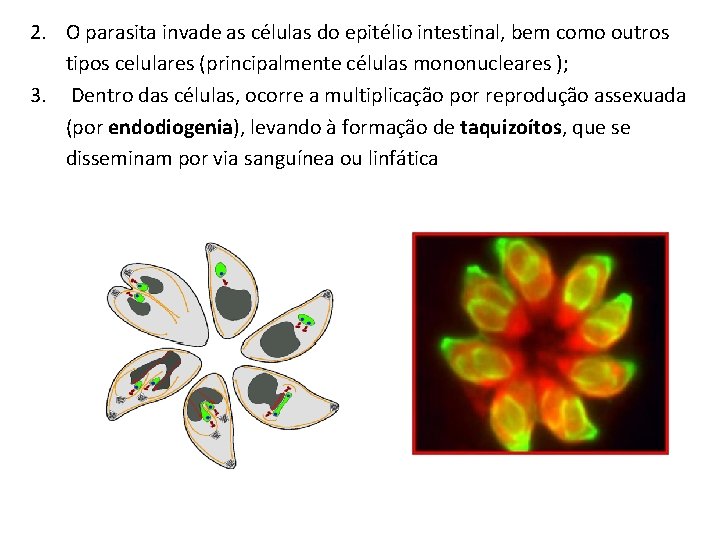
2. O parasita invade as células do epitélio intestinal, bem como outros tipos celulares (principalmente células mononucleares ); 3. Dentro das células, ocorre a multiplicação por reprodução assexuada (por endodiogenia), levando à formação de taquizoítos, que se disseminam por via sanguínea ou linfática
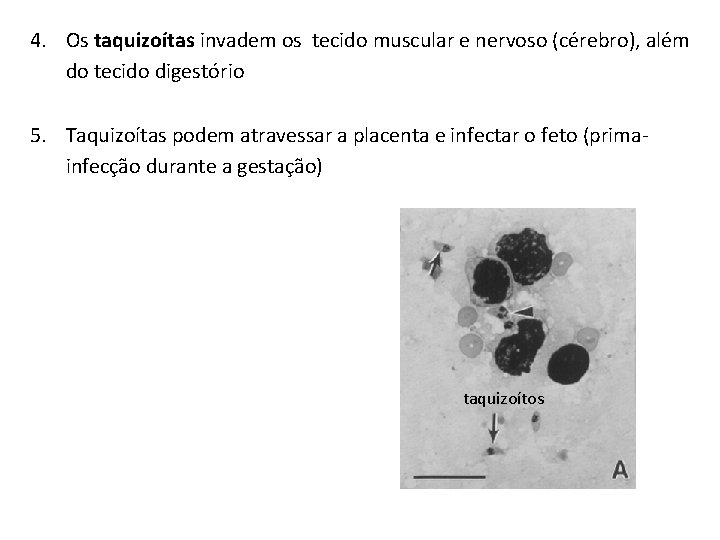
4. Os taquizoítas invadem os tecido muscular e nervoso (cérebro), além do tecido digestório 5. Taquizoítas podem atravessar a placenta e infectar o feto (primainfecção durante a gestação) taquizoítos

NO HOSPEDEIRO INTERMEDIÁRIO Fase crônica da doença 6. Quando a resposta imunitária se torna mais potente, os taquizoítas passam a bradizoítas, que também se reproduzem por endodiogenia 7. Ocorre a formação de cistos (contendo centenas de bradizoítos) nos tecidos muscular e nervoso 8. Cistos permanecem viáveis por anos (no caso de imunodeprimidos podem se romper, liberar os bradizoítos que readquirem capacidade invasiva, ocorrendo uma disseminação fatal do parasita) bradizoítos em cistos teciduais
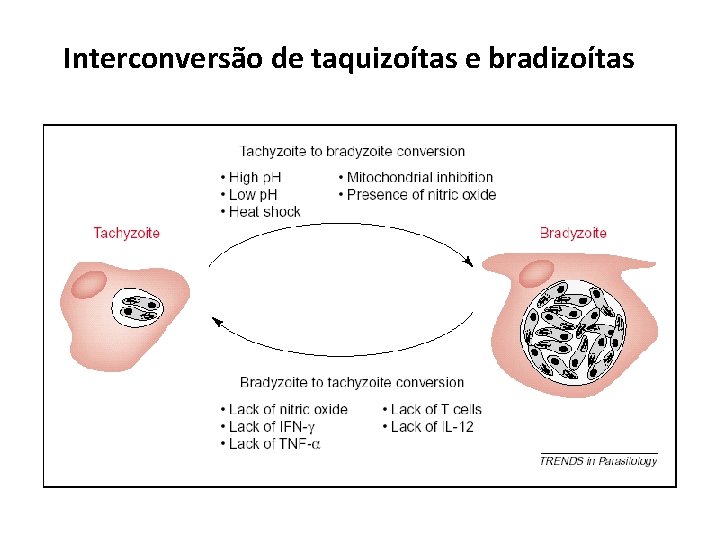
Interconversão de taquizoítas e bradizoítas
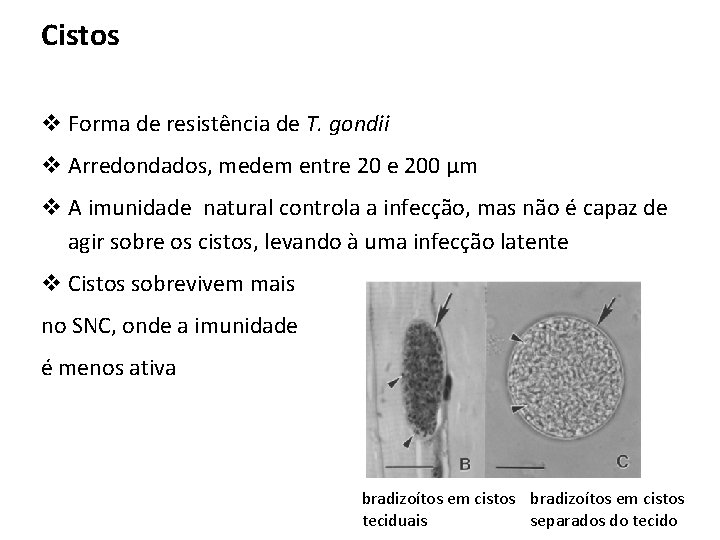
Cistos v Forma de resistência de T. gondii v Arredondados, medem entre 200 μm v A imunidade natural controla a infecção, mas não é capaz de agir sobre os cistos, levando à uma infecção latente v Cistos sobrevivem mais no SNC, onde a imunidade é menos ativa bradizoítos em cistos teciduais separados do tecido

NO HOSPEDEIRO DEFINITIVO 1. O hospedeiro definitivo (felídeo) é infectado pela ingestão de tecidos animais contendo cistos 2. Após a invasão do epitélio digestivo de felídeos, o núcleo do parasita se divide sucessivas vezes formando o esquizonte (esquizogonia) 3. O esquizonte dá origem a merozoítos

NO HOSPEDEIRO DEFINITIVO 4. Os merozoítos podem invadir novas células ou se desenvolver em gametócitos 5. A reprodução sexuada também ocorre no epitélio do trato digestório do hospedeiro definitivo 6. O zigoto se desenvolve em um oocisto não esporulado que é eliminado com as fezes 7. Em 1 -5 dias, o oocisto se desenvolve em oocisto esporulado (esporogonia) com 2 espocistos (4 esporozoítos/esporocisto)

Oocistos v Correspondem à forma infectante do parasita, que é produzida somente no intestino dos felinos (eliminados com as fezes) v Esporogonia: em condições ambientais adequadas de temperatura e umidade ocorre a esporulação do oocisto v Oocistos esporulados podem sobreviver por longos períodos de tempos em condições moderadas de temperatura e umidade v Podem ser mecanicamente transmitidos por moscas, besouros e também podem sobreviver por longo períodos de tempo sobre frutas e vegetais

v O período para o aparecimento de esporocistos nas fezes de felídeos varia de acordo com o estágio do parasita ingerido: • Oocisto: mais de 20 dias • Taquizoítos: mais de 19 dias • Bradizoítos: entre 3 -10 dias e continua por até 14 dias (imunidade mais efetiva) v Menos de 50% dos gatos eliminam oocistos após a ingestão de taquizoítos e quase 100% dos gatos que ingerem bradizoítos eliminam oocistos. v Ratos experimentalemnte infectados com T. gondii têm seu comportamento alterado, adquirindo hábitos mais “ousados” e, portanto, são mais sujeitos à predação

Patogenia e Sintomatologia v Cerca de 1% dos indivíduos infectados apresentam sintomas clínicos v Importância em imunocomprometidos Sintomas: cefaléia, febre, mialgia, dor nas articulações, lesão ocular, convulsões, coma, morte

Infecção congênita: ocorre pela prima-infecção de gestantes v Risco de transmissão aumenta com o tempo de gravidez Primeiro trimestre – 25% Segundo trimestre – 40% Terceiro trimestre – 65% v Gravidade da doença no feto é inversamente proporcional ao tempo de gestação § § § retardo mental problemas de visão hidrocefalia estrabismo problemas de audição

Diagnóstico Clínico: apenas sugestivo Laboratorial v Pesquisa do parasita: § coloração de cortes de tecidos § cultivo celular § inoculação em camundongos (avaliação de soroconversão) § PCR (líquido aminiótico, líquido céfalo-raquidiano) v Pesquisa de anticorpos (teste de Sabin-Feldman, ELISA, IFA, aglutinação, Western Blot)
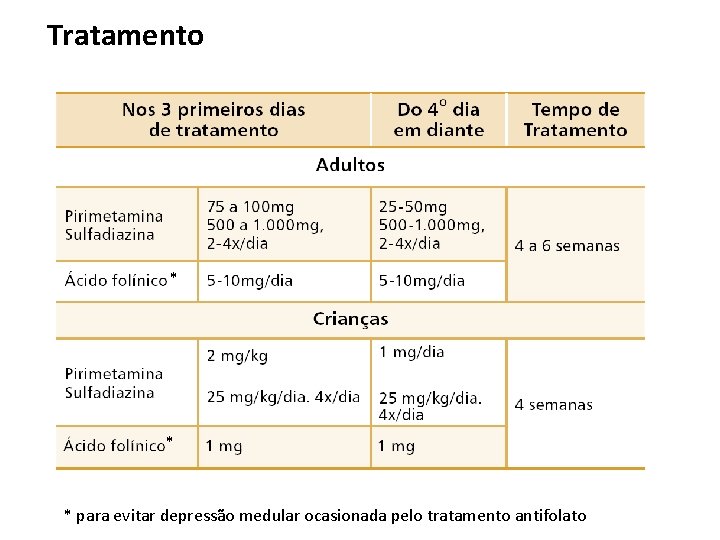
Tratamento * * * para evitar depressão medular ocasionada pelo tratamento antifolato
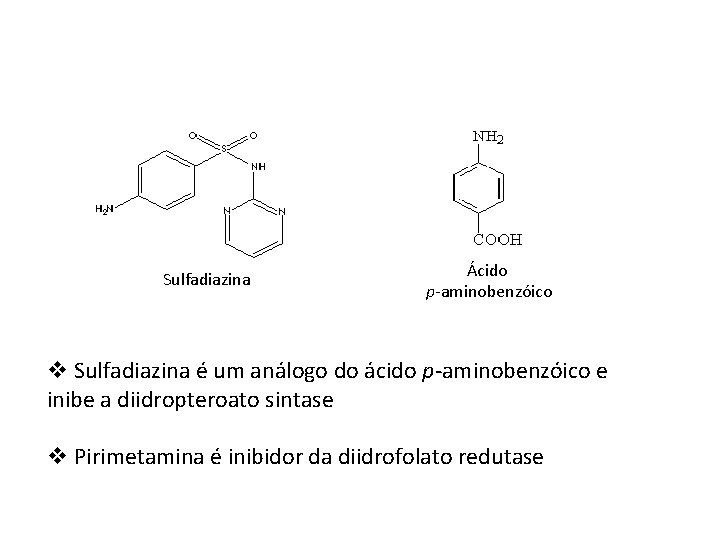
Sulfadiazina Ácido p-aminobenzóico v Sulfadiazina é um análogo do ácido p-aminobenzóico e inibe a diidropteroato sintase v Pirimetamina é inibidor da diidrofolato redutase
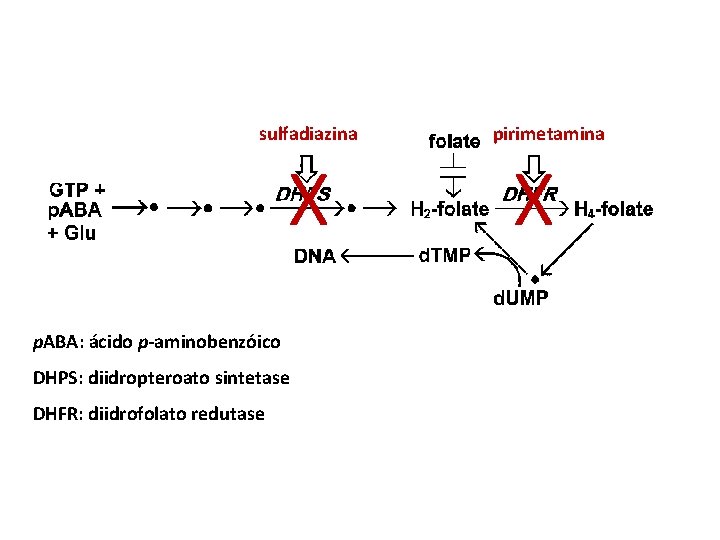
sulfadiazina X p. ABA: ácido p-aminobenzóico DHPS: diidropteroato sintetase DHFR: diidrofolato redutase pirimetamina X

Tratamento Gestantes: o uso de pirimetamina no 1º trimestre é contraindicado, pois é teratogênica Espiramicina, 750 a 1. 000 mg, VO, a cada 8 horas Clindamicina, VO, na dose de 600 mg a cada 6 horas Na forma ocular utiliza-se 40 mg/dia de prednisona, por 1 semana, e 20 mg/dia, por outras 7 semanas para reduzir a necrose e inflamação e minimizar a cicatriz Não há nenhuma droga que aja contra os cistos

Controle v Higiene pessoal v Limpeza de caixas de areia v Evitar contato com fezes de gatos (principalmente durante gestação) v Controle de roedores e de insetos v Não ingerir leite cru, nem carne crua ou mal cozida (nem oferecer aos gatos) v Lavar frutas e verduras e tratar água antes do consumo Vacinação: comercial somente para ovinos (com cistos vivos)

Coccídios intestinais: Cryptosporidium parvum Isospora belli Cyclospora cayetanensis

Criptosporidiose v Agente etiológico: Cryptosporidium parvum v 1976: primeiro relato de infecção humana v 1982: relato como doença oportunista em HIV positivos (prevalência de 5 -10%)

Ciclo de Vida

Patogenia e sintomatologia v Imunocompetentes: maioria dos casos é assintomática v Sintomas incluem diarréia, dor abdominal, náuseas e vômitos, perda de peso, desidratação
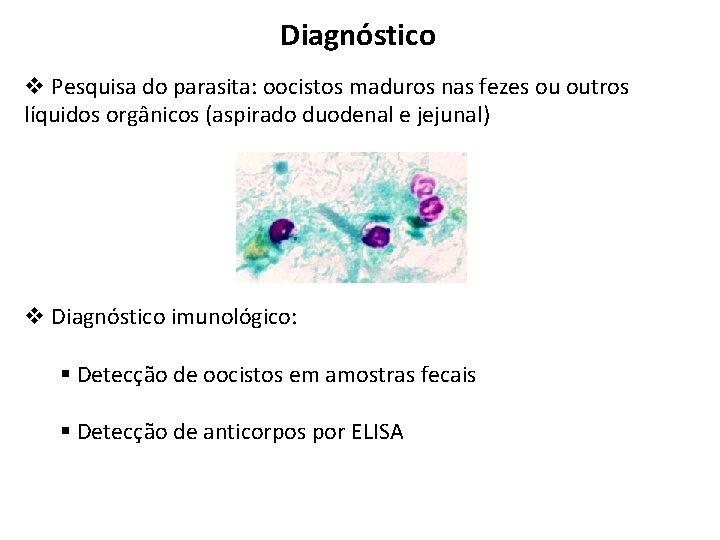
Diagnóstico v Pesquisa do parasita: oocistos maduros nas fezes ou outros líquidos orgânicos (aspirado duodenal e jejunal) v Diagnóstico imunológico: § Detecção de oocistos em amostras fecais § Detecção de anticorpos por ELISA
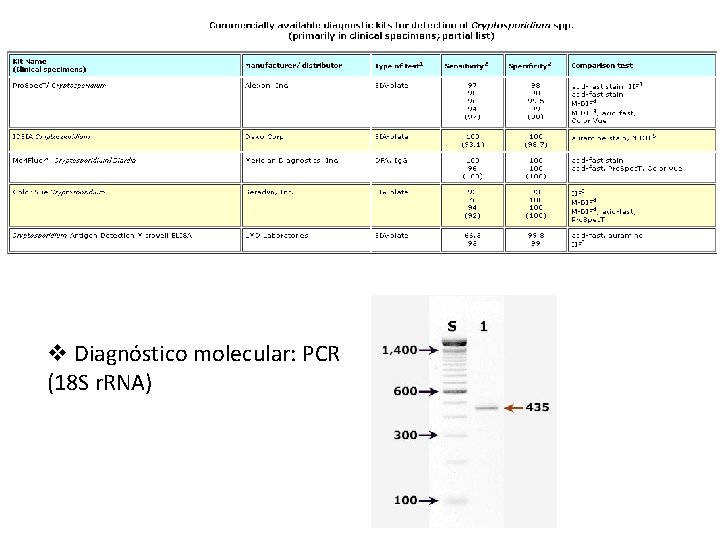
v Diagnóstico molecular: PCR (18 S r. RNA)

Tratamento v Reposição de sais v. Nitazoxanida (inibição da piruvato oxido-redutase) em imonucompetentes Obs. : eficácia não completamente elucidada em imunodeprimidos v Tratamento de imunodeprimidos com retrovirais diminui excreção de oocistos

Isosporose v Agente etiológico: Isospora belli v Cosmopolita, com maior prevalência em regiões tropicais e subtropicais v Prevalência chega a 15% em indivíduos com HIV
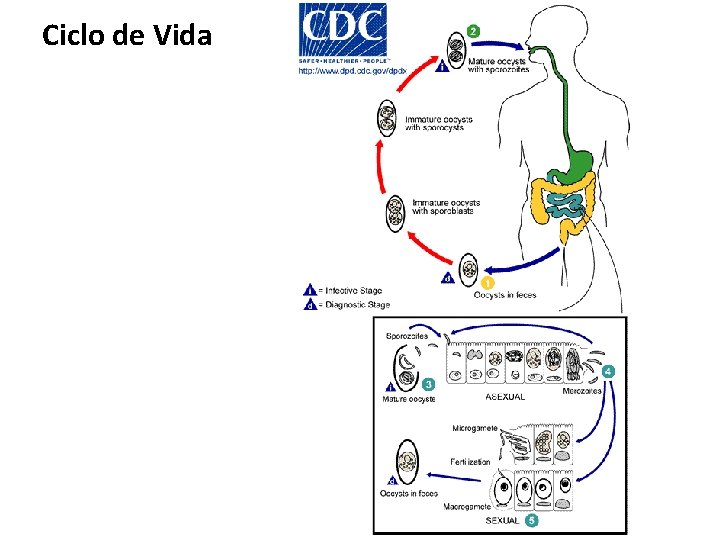
Ciclo de Vida

Patogenia e Sintomatologia v Imunocompetentes: geralmente assintomática ou diarréia com dor abdominal e perda de peso por mal-absorção v Imunocomprometidos: quadro diarréico grave (várias evacuações/dia), febre, cólicas intestinais, vômitos e emagrecimento por mal-absorção v Pode apresentar quadros de disseminação extraintestinal (linfonodos, fígado e baço)
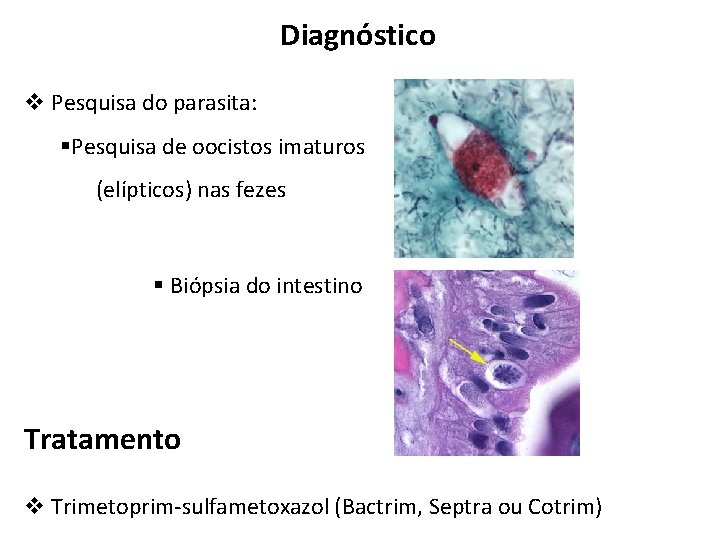
Diagnóstico v Pesquisa do parasita: §Pesquisa de oocistos imaturos (elípticos) nas fezes § Biópsia do intestino Tratamento v Trimetoprim-sulfametoxazol (Bactrim, Septra ou Cotrim)

Ciclosporose v Agente etiológico: Cyclospora cayetanensis v 1979: primeiro relato de infecção em humanos
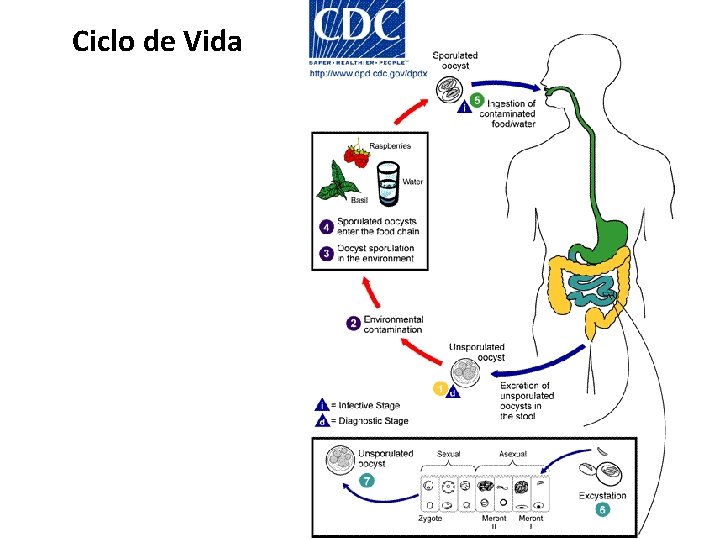
Ciclo de Vida

Patogenia e Sintomatologia v Maioria dos casos é assintomática v Sintomas incluem diarréia líquida, dor abdominal, náuseas e vômitos, anorexia, perda de peso, mialgia, fadiga e febre baixa v Em indivíduos imunocomprometidos o quadro diarréico é crônico e intermitente
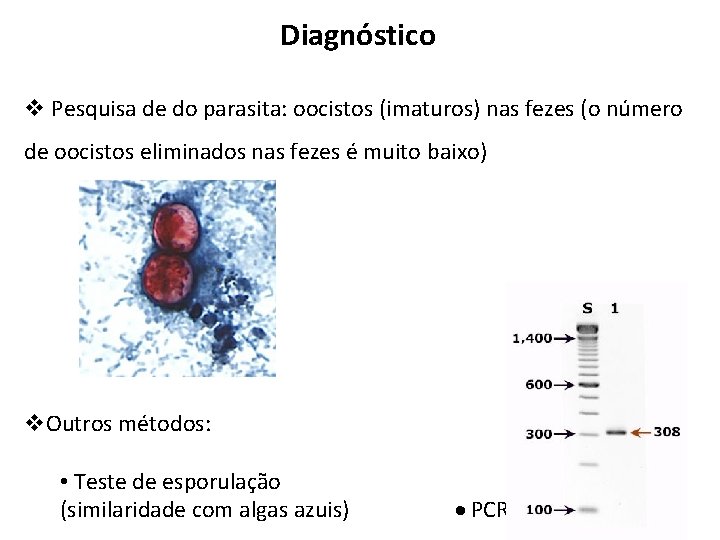
Diagnóstico v Pesquisa de do parasita: oocistos (imaturos) nas fezes (o número de oocistos eliminados nas fezes é muito baixo) v. Outros métodos: • Teste de esporulação (similaridade com algas azuis) PCR
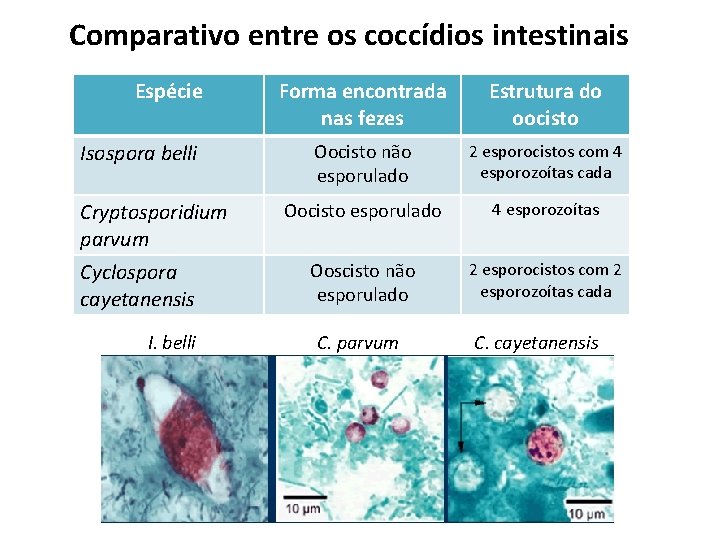
Comparativo entre os coccídios intestinais Espécie Isospora belli Cryptosporidium parvum Cyclospora cayetanensis I. belli Forma encontrada nas fezes Estrutura do oocisto Oocisto não esporulado 2 esporocistos com 4 esporozoítas cada Oocisto esporulado 4 esporozoítas Ooscisto não esporulado 2 esporocistos com 2 esporozoítas cada C. parvum C. cayetanensis

Microsporidiose v Integrantes do Filo Microspora v 14 espécies descritas como patógenos humanos: Brachiola algerae, B. connori, B. vesicularum Encephalitozoon cuniculi, E. hellem, E. intestinalis Enterocytozoon bieneusi Microsporidium ceylonensis, M. africanum Nosema ocularum Pleistophora sp. Trachipleistophora hominis, T. anthropophthera Vittaforma corneae

Epidemiologia v 1959: primeiro relato de infecção por Encephalitozoon spp. v 1985: relato de infecção por Enterocytozoon bieneusi em um indivíduo infectado pelo HIV v Atualmente os microsporídeos são reconhecidos como agentes etiológicos de infecções oportunistas em pacientes com AIDS e transplantados v Relatos de infecção em diversos países
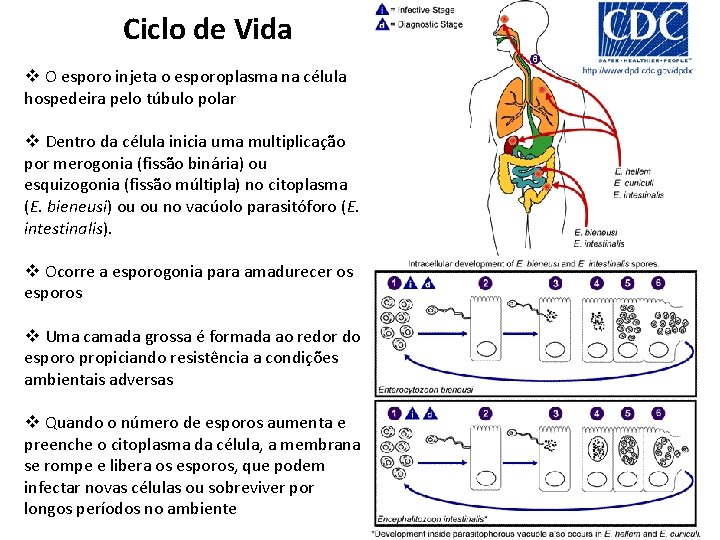
Ciclo de Vida v O esporo injeta o esporoplasma na célula hospedeira pelo túbulo polar v Dentro da célula inicia uma multiplicação por merogonia (fissão binária) ou esquizogonia (fissão múltipla) no citoplasma (E. bieneusi) ou ou no vacúolo parasitóforo (E. intestinalis). v Ocorre a esporogonia para amadurecer os esporos v Uma camada grossa é formada ao redor do esporo propiciando resistência a condições ambientais adversas v Quando o número de esporos aumenta e preenche o citoplasma da célula, a membrana se rompe e libera os esporos, que podem infectar novas células ou sobreviver por longos períodos no ambiente

Patogenia e Sintomatologia v Geralmente assintomática em imunocompetentes v Sintomas incluem:

Diagnóstico v Pesquisa do parasita por microscopia: busca de esporos nas fezes v Métodos imunológicos : IFA v Métodos moleculares: PCR

Tratamento v Microsporidiose ocular (Brachiola algerae, Encephalitozoon hellem, E. cuniculi, Vittaforma corneae): albendazol (oral) + fumagilina (inibição de síntese de RNA – uso tópico) Obs. : Infecções com V. corneae geralmente não respondem a quimioterapia e necessitam de ceratoplastia v Gastroenterite (Encephalitozoon intestinalis), microsporidiose disseminada (E. hellem, E. cuniculi, E. intestinalis, Pleistophora sp. , Trachipleistophora sp. , Brachiola vesicularum), infecções de pele e musculares (Brachiola algerae): albendazol

Controle de coccídeos e microsporídeos v Saneamento básico e educação sanitária v Filtração da água (oocistos resistem ao cloro) v Evitar a ingestão de alimentos crus ou mal cozidos

Parasitoses em indivíduos imunocomprometidos
indivíduo imunocomprometido v disfunção das defesas específicas de determinado órgão ou sistema v anormalidade sistêmica da imunidade celular ou humoral microrganismos oportunistas v patógenos comumente conhecidos v microrganismos não considerados normalmente virulentos (microbiota, vida livre)

Algumas causas de imunodeficiência Doenças hereditárias e metabólicas: • Diabetes • Insuficiência renal • Desnutrição • Anemia Substâncias químicas e tratamentos que inibem o sistema imunitário: • Quimioterapia • Corticosteróides • Medicamentos imunossupressores • Radioterapia Infecções : • Varicela • Infecção por citomegalovírus • Rubéola • Infecção pelo vírus da imunodeficiência adquirida (AIDS) • Mononucleose infecciosa • Sarampo • Infecção bacteriana grave • Infecção fúngica grave • Tuberculose grave

Algumas causas de imunodeficiência Patologias: • Agranulocitose • Tumores malignos • Anemia aplásica • Leucemia • Linfoma • Mielofibrose • Mieloma Cirurgia e traumas: • Queimaduras • Extirpação do baço Outras causas: • Cirrose alcoólica • Hepatite crônica • Envelhecimento normal • Sarcoidose • Lupus eritematoso sistêmico

Defesa imune contra protozoários v defesa celular http: //clientes. netvisao. pt/freiremj/t_particulas_endo. html v defesa humoral
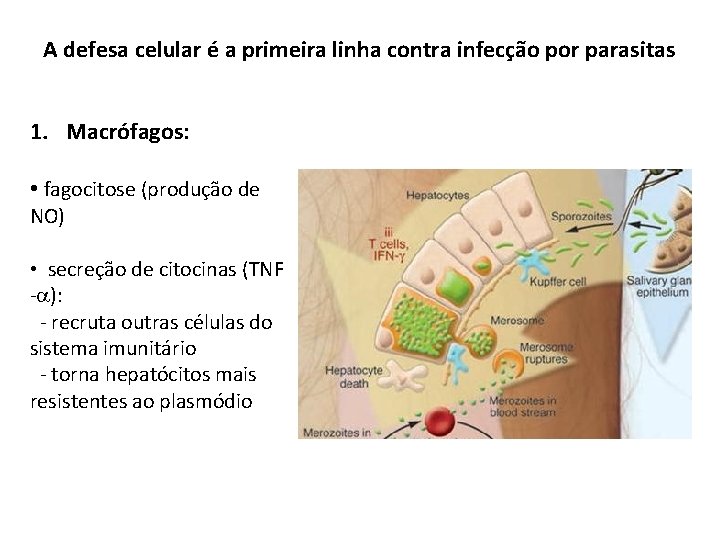
A defesa celular é a primeira linha contra infecção por parasitas 1. Macrófagos: • fagocitose (produção de NO) • secreção de citocinas (TNF -a): - recruta outras células do sistema imunitário - torna hepatócitos mais resistentes ao plasmódio

2. Neutrófilos: • fagocitose (mecanismos independentes ou dependentes de O 2) • destruição extracelular por H 2 O 2 • presentes nos sítios inflamatórios infectados por parasitas para a eliminação dos parasitas liberados pelas células rompidas

3. Eosinófilos: associados às infecções helmínticas 4. Plaquetas: atividade citotóxica potencializada pela ativação por citocinas (TNF-a, INF-g)

Os linfócitos T são essenciais na imunidade contra protozoários: produção de citocinas e perforinas • Citocinas: recrutamento de células, aumento da atividade citotóxica e promoção do aumento do número de células • Populações de células T CD 4+ e CD 8+: atuam em diferentes fases do ciclo de vida dos protozoários Exemplo: Plasmodium - CD 4+ : atua contra fase eritrocítica - CD 8+ : atua contra fase hepática

Ação de anticorpos específicos sobre os protozoários • neutralização: bloqueio da ligação do protozoário com a célulaalvo • ação direta ou mediando ação do sistema complemento
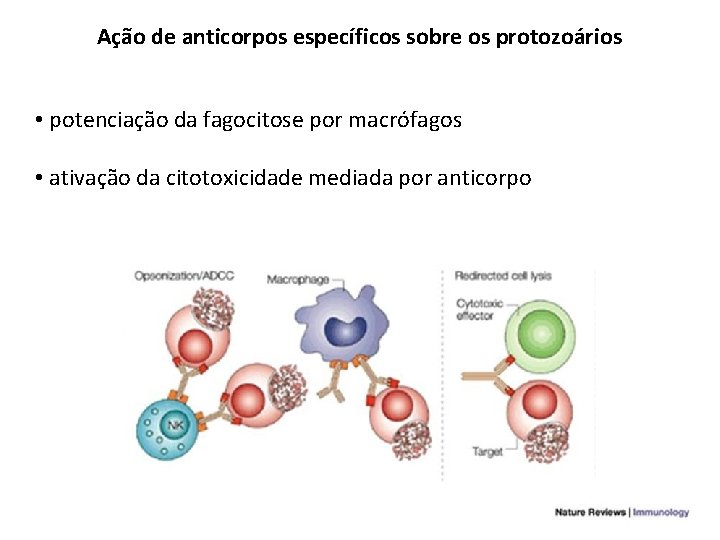
Ação de anticorpos específicos sobre os protozoários • potenciação da fagocitose por macrófagos • ativação da citotoxicidade mediada por anticorpo

A maior susceptibilidade à infecção está relacionada com o processo do sistema imunitário que se encontra comprometido Exemplos: • agamaglobulinemia: maior susceptibilidade à microrganismos extracelulares • falhas na imunidade celular: maior susceptibilidade a microrganismos intracelulares
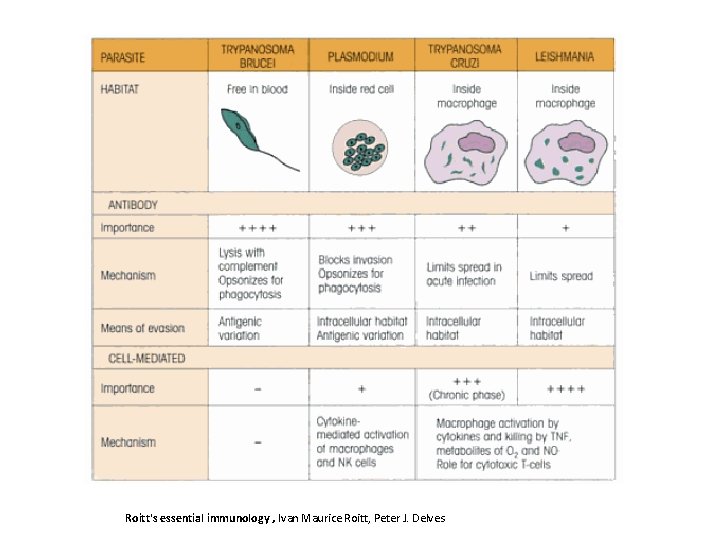
Roitt's essential immunology , Ivan Maurice Roitt, Peter J. Delves

Os protozoários e as infecções oportunistas v Toxoplasma gondii v Cryptosporidium parvum e Cyclospora cayetanensis v Isospora beli, Sarcocystis e microsporídeos v Pnemocystis carinii v Balantidium coli

Toxoplasma gondii v parasitose comum (cerca de 50% da população mundial é soropositiva) v imunidade depende de células T (CD 8+ e CD 4+) e de macrófagos; secreção de INF-g e TNF-a (aumentam a produção de NO)
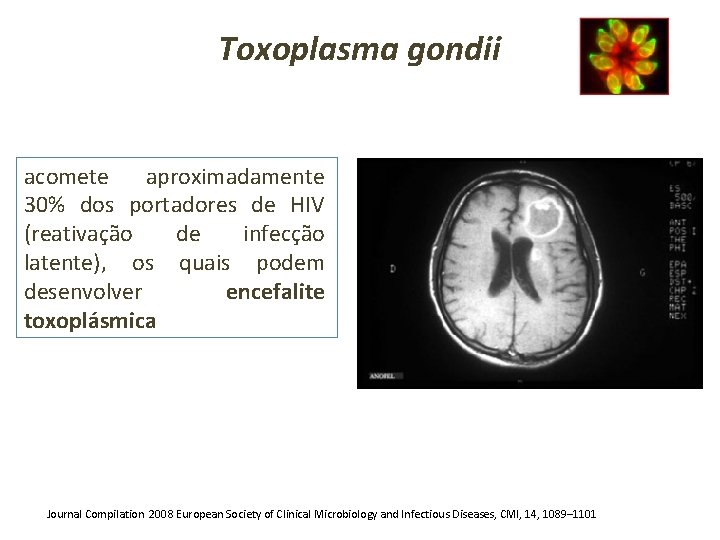
Toxoplasma gondii acomete aproximadamente 30% dos portadores de HIV (reativação de infecção latente), os quais podem desenvolver encefalite toxoplásmica Journal Compilation 2008 European Society of Clinical Microbiology and Infectious Diseases, CMI, 14, 1089– 1101

Toxoplasma gondii v principal parasitose relacionada ao transplante de órgãos (agravada pelo tratamento com imunossupressores): infecção pelo órgão recebido por um receptor negativo (R-) de um doador positivo (D+) ou por reativação de infecção crônica no receptor positivo (R+) v importância da análise da presença de infecção no doador e no receptor antes e depois do transplante e quimioprofilaxia (sulfonamidas e pirimetamina; atovaquona – AIDS)

Cryptosporidium parvum v alta prevalência em indivíduos com AIDS (30 -50% em países tropicais), ocasionando diarréia intensa e perda de peso diarréia intensa = aumento da liberação de oocistos Assim, portadores de HIV atuam como reservatórios amplificadores Chieffi, Revista Brasileira de Medicina

Cryptosporidium parvum v “clearance” da infecção relacionado com a preservação das funções das células T CD 4+ : indivíduos com AIDS, que possuem número reduzidos dessas células (< 200 células/mm 3), não conseguem controlar a infecção

Isospora beli, Sarcocystis e microsporídeos v infecção rara (1/1000) em imunocompetentes, mas crônica e intermitente em indivíduos com AIDS v prevalência de 2 -50% dos indivíduos com AIDS v diarréia intensa*, perda de peso

Pnemocystis carinii e Balantidium coli Pneumocystis carinii: cerca de 80 -90% dos portadores do HIV contraem pneumonia ocasionada por P. carinii v também ocasionar pneumonia em indivíduos transplantados, sob tratamento com corticóides ou ainda em indivíduos com leucemias, linfomas, ausência congênita de imunidade do sistema linfocitário Balantidium coli: indivíduos imunocomprometidos e idosos são mais susceptíveis (infecções intestinais)

Parasitoses com gravidade exacerbada pela depressão do sistema imunitário v Leishmania v Trypanosoma v Plasmodium

Leishmania, Trypanosoma e Plasmodium v Quadros severos em indivíduos com AIDS v HIV: destroem linfócitos CD 4+, alterando a ativação de macrófagos, que ficam mais susceptíveis à infecção por Leishmania v comprometimento de CD 4+ também compromete a ação contra Trypanosoma cruzi e contra a fase eritrocítica de Plasmodium
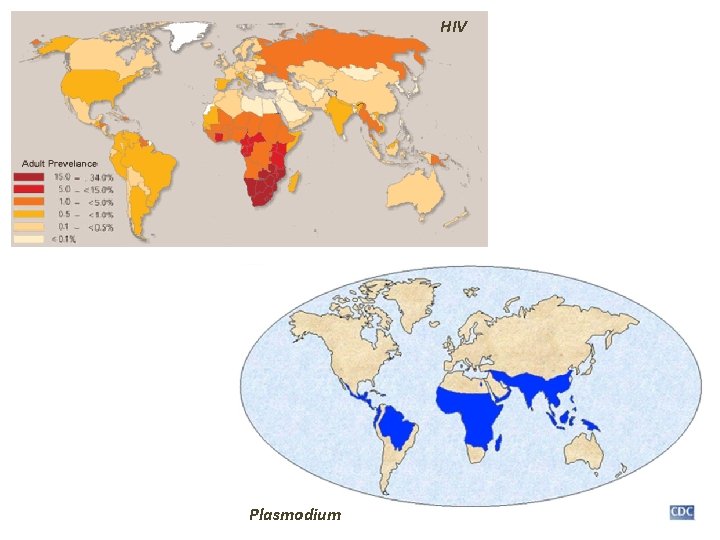
HIV Plasmodium

Outras infecções v Giardia: prevalência de aproximadamente 16% em indivíduos com AIDS v também apresenta alta prevalência em indivíduos com produção reduzida de anticorpos v Babesia: indivíduos esplenectomizados v Amebíases

v Poliparasitismo Rev. Soc. Bras. Med. Trop. v. 32 n. 2 Uberaba mar. /abr. 1999

Fatores que influenciam a gravidade das infecções v patogenicidade das cepas v fatores de predisposição do hospedeiro
Infecções por helmintos v Raras complicações imunopatológicas: doença granulomatosa e falência de órgãos v Normalmente a relação helminto-hospedeiro é harmônica e assintomática reservatórios de transmissão Aproximadamente 2 bilhões de pessoas no mundo apresentam-se infectadas por helmintos

Infecção por helmintos 1. Vias de infecção: oral (Ascaris spp. ), penetração direta pele (S. mansoni, N. americanus), picada do inseto-vetor (Onchocerca volvulus); 2. Fases de vida: ovos, larvas e adultos; 3. Órgãos afetados: intestino grosso, intestino delgado, órgãos linfáticos, pulmões, fígado. http: //www. path. cam. ac. uk/~schisto/general_parasitology/index. html

Helmintos e o sistema imunitário As infecções por helmintos são caracterizadas por: 1. Fase aguda: resposta intensa de linfócitos Th 2 2. Fase crônica: depressão do sistema imune → resposta antiinflamatória

Linfócitos Th 1: produzem citocinas pró-inflamatórias (majoritariamente INF-g) Linfócitos Th 2 produzem citocinas antiinflamatórias (IL-4, IL-5, IL-13 e IL-10) Balanço entre as citocinas: importante para controlar a infecção e, ao mesmo tempo, evitar danos aos tecidos
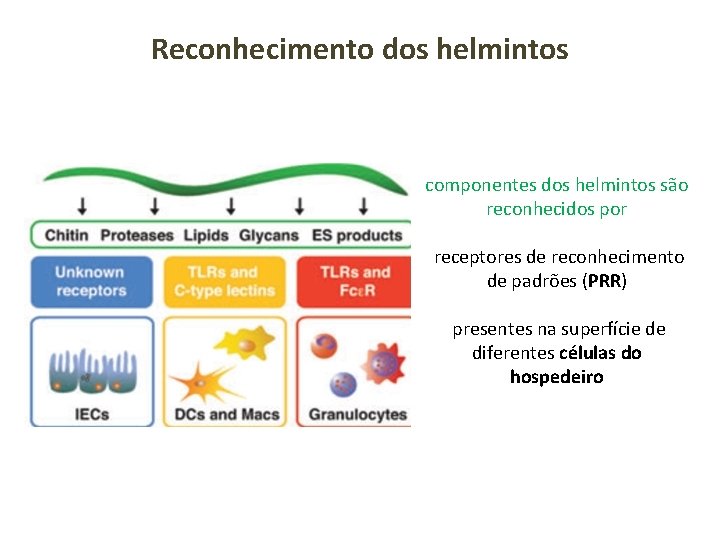
Reconhecimento dos helmintos componentes dos helmintos são reconhecidos por receptores de reconhecimento de padrões (PRR) presentes na superfície de diferentes células do hospedeiro

1. As células dendríticas ativadas pela infecção por helmintos estimulam a diferenciação de linfócitos Th naive (Th 0) em Th 2 2. Os linfócitos Th 2 ativados produzem citocinas (IL-4 e IL-5) 3. IL-4 ativa a produção de Ig. E por infócitos B e 4. Ig. E leva à desgranulação de mastócitos e a IL-5 de eosinófilos, os quais liberam substâncias tóxicas aos helmintos 5. As células dendríticas também levam à ativação de células T-regulatórias que regulam uma resposta excessiva
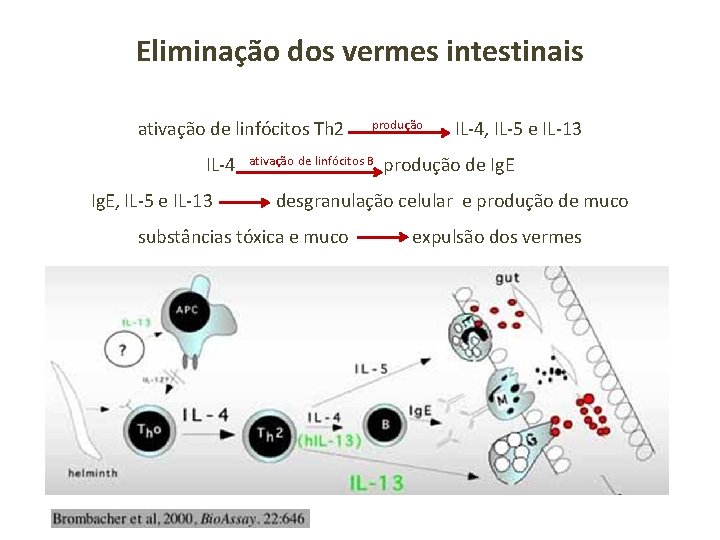
Eliminação dos vermes intestinais ativação de linfócitos Th 2 produção IL-4, IL-5 e IL-13 IL-4 ativação de linfócitos B produção de Ig. E, IL-5 e IL-13 desgranulação celular e produção de muco substâncias tóxica e muco expulsão dos vermes
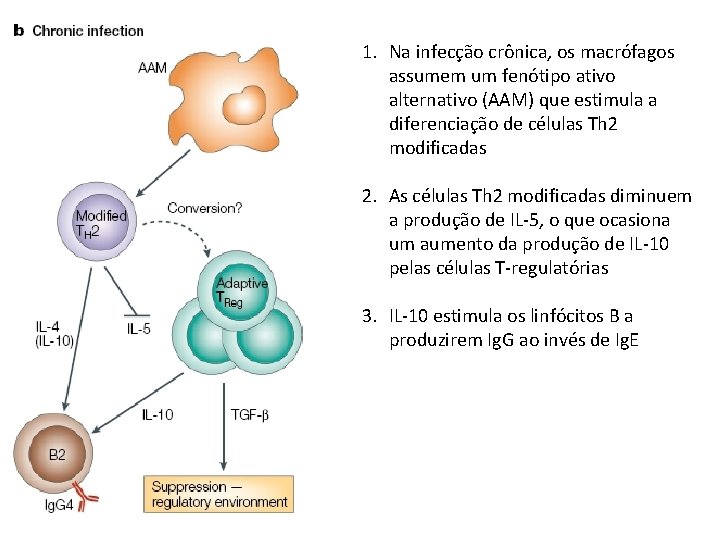
1. Na infecção crônica, os macrófagos assumem um fenótipo ativo alternativo (AAM) que estimula a diferenciação de células Th 2 modificadas 2. As células Th 2 modificadas diminuem a produção de IL-5, o que ocasiona um aumento da produção de IL-10 pelas células T-regulatórias 3. IL-10 estimula os linfócitos B a produzirem Ig. G ao invés de Ig. E

Mecanismos de escape dos helmintos ao sistema imune do hospedeiro Problemas encontrados para a evasão do sistema imune do hospedeiro: • podem viver muitos anos no hospedeiro vertebrado sem se multiplicar: a variação antigênica não é possível; • são muito grandes para ocuparem nichos protegidos do ataque do sistema imune

Mecanismos de escape dos helmintos ao sistema imune do hospedeiro Porém: üpodem comprometer a função do complemento e levar à degradação de imunoglobulinas (Schistosoma spp. ); üsão capazes de utilizar moléculas de superfície do hospedeiro (mimetismo), por exemplo, lectinas üresposta antiinflamatória/depressão global do sistema imunitário

Resposta imunitária aos helmintos Benefícios: v a resposta antiinflamatória reduz a doença inflamatória ocasionada por Helicobacter pylori e Plasmodium falciparum; v infecção crônica: redução de alergias e de doenças auto-imunes

Resposta imunitária aos helmintos Prejuízos: v prejudica vacinação, que depende de resposta Th 1; v afeta a resposta imune contra os agentes etiológicos (incluindo HIV e Mycobacterium)

Helmintos e Mycobacterium A resposta contra Mycobacterium depende da atividade de linfócitos Th 1 Hipótese: presença de helmintos, que estimula a resposta de linfócitos Th 2, prejudicaria a resposta contra a bactéria Área hiperendêmica para oncocercíase apresenta incidência duas vezes maior de Mycobacterium leprae

Helmintos e Plasmodium A resposta imune à malária também depende da atividade de linfócitos Th 1 Hipótese: presença de helmintos, que estimula a resposta de linfócitos Th 2, prejudicaria a resposta contra o plasmódio No entanto: • crianças na África infectadas por Schistosoma mansoni têm uma incidência menor de malária; • Ascaris: proteção contra malária cerebral e falência renal associada com citocinas pró-inflamatórias, diminuídas pela produção de IL-10

Helmintos e HIV A resposta imune contra vírus depende de linfócitos T CD 8+ Hipótese: presença crônica de helmintos, que deprime o sistema imune do hospedeiro, prejudicaria a resposta contra o HIV Uma menor carga viral é necessária para a infecção de macacos previamente infectados por Schistosoma

Helmintos e HIV infecta linfócitos T CD 4+ Hipótese: a infecção pelo HIV prejudicaria a imunidade contra helmintos, a qual depende de linfócitos T CD 4+ Indivíduos HIV-positivos apresentam altas taxas de infecção por parasitas (protozoários e helmintos)
- Slides: 99