Espontaneidad y Equilibrio CONTENIDO 1 Condiciones generales de

Espontaneidad y Equilibrio

CONTENIDO 1. - Condiciones generales de equilibrio y espontaneidad. 2. - Funciones de Helmholtz y de Gibbs. 3. - Relaciones termodinámicas de un sistema cerrado en equilibrio 4. - Potencial químico

La masa como variable termodinámica Cualquier tipo de trabajo puede expresarse de la forma d. W = Σi yi d. Xi donde yi es una variable intensiva cualquiera y Xi la variable extensiva conjugada correspondiente. La masa se introduce utilizando el potencial químico μ como variable intensiva conjugada (GIBBS) d. W = Σi μi dni, Por lo tanto, d. U = Td. S – pd. V + Σi μi dni donde ni = número de moles del componente i μi = potencial químico del componente i μi = ( ∂U/ ∂ni) S, V, nj
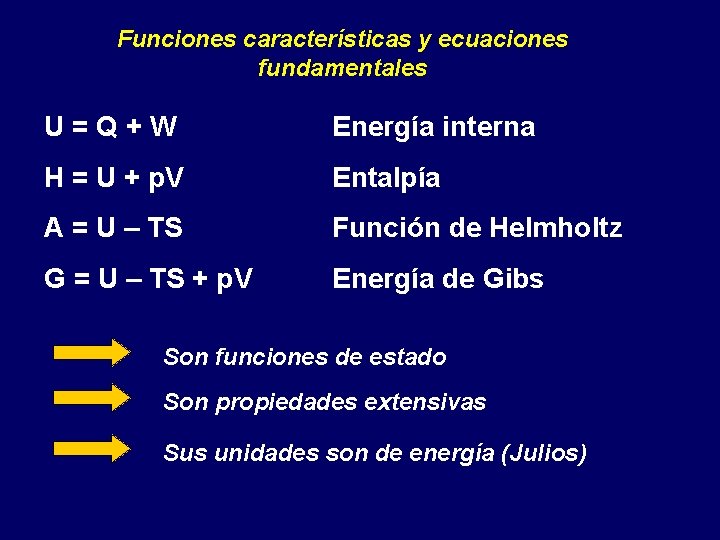
Funciones características y ecuaciones fundamentales U=Q+W Energía interna H = U + p. V Entalpía A = U – TS Función de Helmholtz G = U – TS + p. V Energía de Gibs Son funciones de estado Son propiedades extensivas Sus unidades son de energía (Julios)

Operando y sustituyendo el valor de d. U obtenemos las siguientes ecuaciones fundamentales Sistemas cerrados, en equilibrio, de una sola fase, solo trabajo P-V U = U (S, V, ni) H = H (S, p, ni) A = A (T, V, ni) G = G (T, p, ni)

Pueden obtenerse relaciones de gran interés. d. A = (∂A/∂T)V, nid. T + (∂A/∂V)T, ni d. V + (∂A/∂ni)V, T, nj dni d. A = -Sd. T -pd. V + Σiμi dni de donde: S = - (∂A/∂T)V, ni ; p = - (∂A/∂V)T, ni ; μi = (∂A/∂ni)V, T, nj Lo mismo se puede hacer con todas las ecuaciones fundamentales: μi = (∂U/∂ni)S, V, nj = (∂H/∂ni)S, p, nj = (∂A/∂ni)V, T, nj = (∂G/∂ni)p, T, nj Potencial químico G

El potencial químico: Es una función de estado Es una propiedad intensiva Sus unidades son julios/mol Para una sustancia pura el potencial químico es la energía de Gibbs molar

Si el sistema está constituido por varias fases, en cada una de ellas se puede asignar un valor a las propiedades extensivas, de forma que el valor total de estas será la suma de los valores en las distintas fases y cualquier variación vendrá dado por ejemplo por: De forma global para el sistema d. G -Sd. T Vd. P

Todas las ecuaciones de Gibbs pueden reescribirse del siguiente modo: Sistemas en equilibrio, con varias fases, solo trabajo P-V

Condición de equilibrio material Cuando el sistema alcanza el equilibrio material no hay cambio macroscópico en la composición a lo largo del tiempo, y no hay transporte de materia de una parte a otra del sistema

Condiciones de equilibrio y espontaneidad Variables extensivas Habíamos visto que: d. S = d. Se + d. Si d. S – d. Q/T = d. Si ≥ 0 (1) Td. S – d. U + d. W ≥ 0 d. U – Td. S + pd. V ≤ 0 Sistema aislado: d. S = d. Si ≥ 0 S y V = ctes d. U ≤ 0 S y p = ctes d(U + p. V) = d. H ≤ 0 T y V = ctes d(U – TS) = d. A ≤ 0 T y P = ctes d(U – TS + p. V) = d. G ≤ 0 (2)
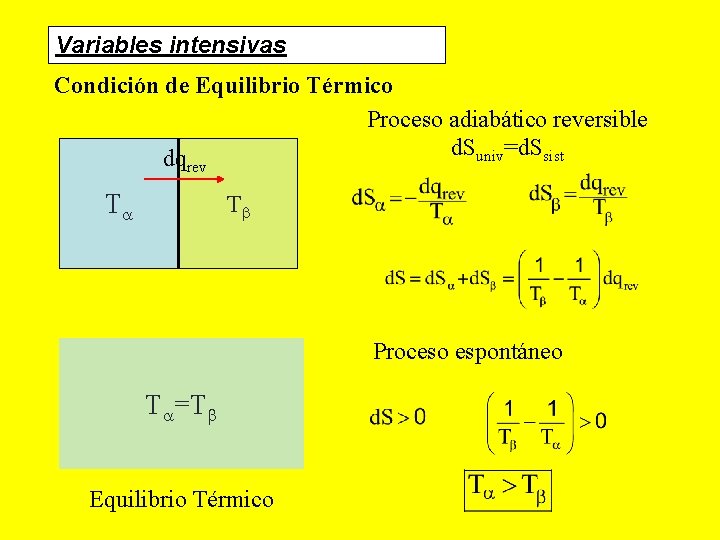
Variables intensivas Condición de Equilibrio Térmico Proceso adiabático reversible d. Suniv=d. Ssist dq rev T T Proceso espontáneo T =T Equilibrio Térmico
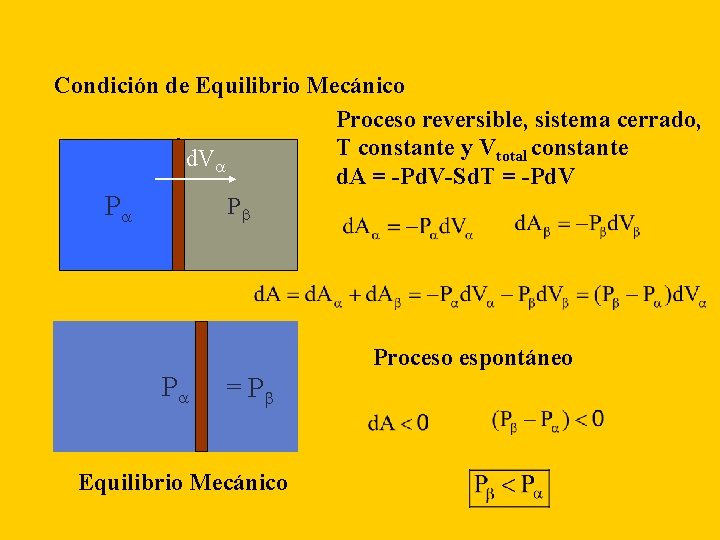
Condición de Equilibrio Mecánico Proceso reversible, sistema cerrado, T constante y Vtotal constante d. V d. A = -Pd. V-Sd. T = -Pd. V P P Proceso espontáneo P = P Equilibrio Mecánico
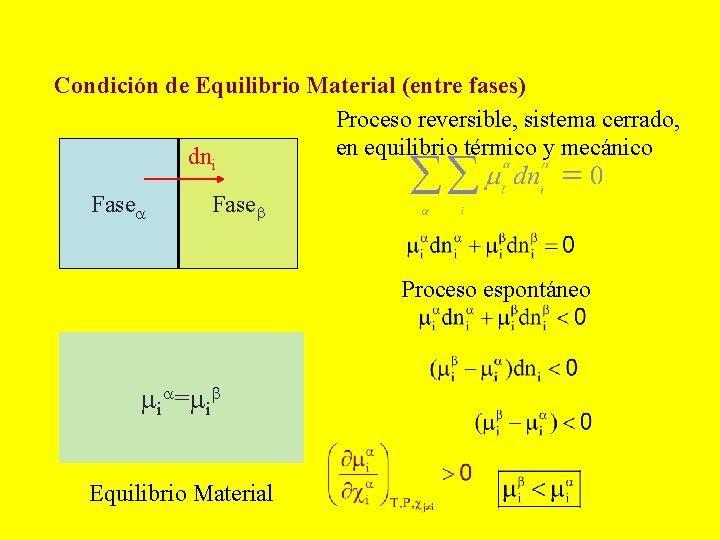
Condición de Equilibrio Material (entre fases) Proceso reversible, sistema cerrado, en equilibrio térmico y mecánico dn i Fase Proceso espontáneo i = i Equilibrio Material

POTENCIAL QUÍMICO DE UN GAS IDEAL Propiedad intensiva, (solo depende de T y P). ¿Como varía el potencial químico con la presión si se mantiene la temperatura constante? . dividiendo por el número de moles y siendo T constante G. I.

Si el gas sufre una transformación desde P 1 a una presión P 2 Si P 1 es 1 bar, podemos definir el potencial químico normal del Gas Ideal puro como:

POTENCIAL QUÍMICO DE UNA MEZCLA DE GASES IDEALES ¿cuáles son las propiedades de una mezcla de gases ideales? Cuando la mezcla de gases se realiza mezclando isotérmicamente los componentes puros, no hay transferencia de energía en forma de calor (suponiendo que no ocurre ninguna reacción química)

Para conocer el potencial químico de cada uno de los gases en la mezcla se hace el mismo razonamiento que para un gas puro donde el miembro de la izquierda representa el potencial químico del gas i en la mezcla a la temperatura T y a la presión parcial Pi donde
- Slides: 18