ESF ldzfinansts Rgas domes Izgltbas kultras un sporta

ESF līdzfinansēts Rīgas domes Izglītības, kultūras un sporta departamenta projekts, , Inovatīvi risinājumi sociālās atstumtības mazināšanai sociālā riska grupas jauniešiem” līguma Nr. 2009/0318/1 DP/1. 2. 2. 4. 2/09/APIA/VIAA/116, ID: 2278 Ķīmija 8. klase Vielu oksidēšanās 4. 1. Skābekļa ķīmiskās īpašības. Oksīdi. Reakciju vienādojumi. 1

Kas kopīgs ir attēlos redzamām vielām? Krāsu pigmenti Mn. O 2(melns) Zn. O (balts) CO (tvana gāze) Cr 2 O 3 (zaļš) Fe 2 O 3 (brūns) H 2 O (ūdens) CO 2 (ogļskābā gāze) Si. O 2 (smilts) Si. O 2 (kvarcs) 2
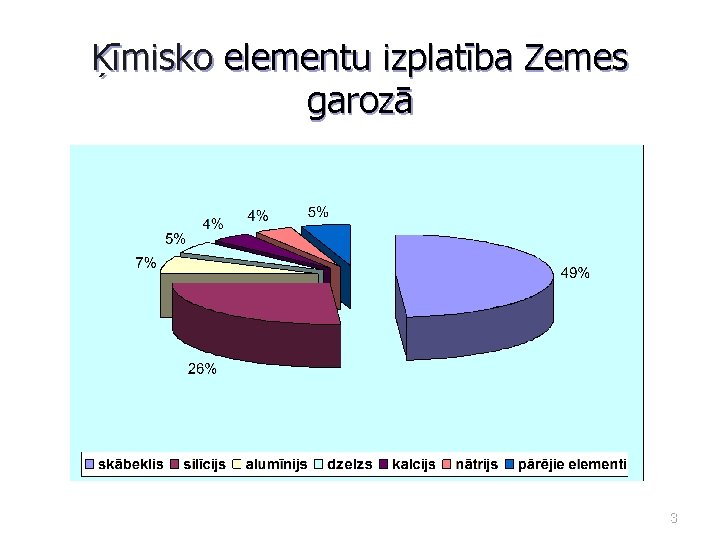
Ķīmisko elementu izplatība Zemes garozā 3

Skābekļa ķīmiskās īpašības gš de Reakcija starp skābekli an a rū sē ša na Skābeklis enerģiski reaģē ar daudzām vielām. Vielu reakcijas ar skābekli sauc par oksidēšanās reakcijām. Šajās reakcijās rodas oksīdi. un vielu var notikt lēni vai ātri. 4

Oksīdi ir ķīmiskie savienojumi, kas sastāv no diviem elementiem, no kuriem viens ir skābeklis. Li 2 O 5

Oksīdu nosaukumu veidošana • Ja elementam ir viena vērtība: Na 2 O –nātrija oksīds Zn. O – cinka oksīds 6

Oksīdu nosaukumu veidošana Ja elementam ir vairākas vērtības: Fe. O – dzelzs (II) oksīds (dzelzs divi oksīds) Fe 2 O 3 – dzelzs (III) oksīds (dzelzs trīs oksīds) SO 3 – sēra (VI) oksīds (sēra seši oksīds) 7

Oksīdu nosaukumu veidošana Kā arī var norādīt atomu skaitu molekulā ar grieķu skaitļa vārdiem: P 2 O 5 – fosfora (V) oksīds, vai difosfora pentoksīds CO – tvana gāze CO 2 – ogļskābā gāze 8

Pārbaudi sevi! Oksīda nosaukums Litija oksīds Sēra dioksīds Kalcija oksīds Fosfora (V) oksīds Oglekļa (II) oksīds Alumīnija oksīds Oksīda formula Li 2 O SO 2 Ca. O P 2 O 5 CO Al 2 O 3 9
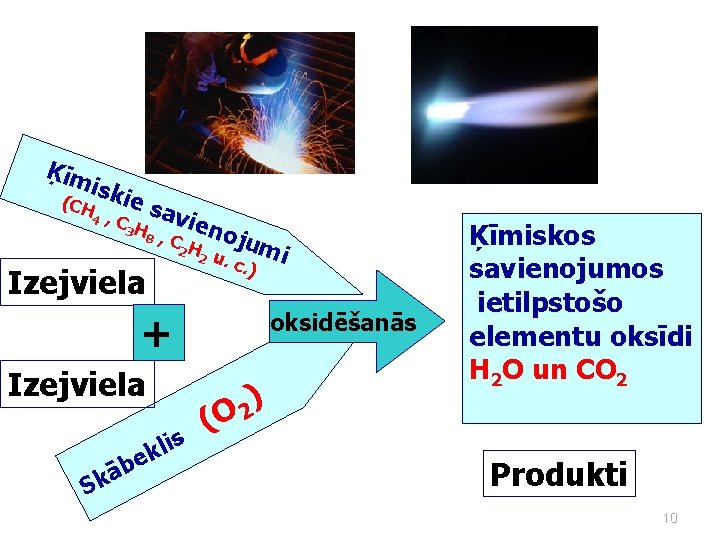
Ķīm iski (CH 4 , C e sa 3 H 8 vie , C Izejviela 2 H 2 noj u u. c . ) mi oksidēšanās + Izejviela s b ā Sk li k e (O ) 2 Ķīmiskos savienojumos ietilpstošo elementu oksīdi H 2 O un CO 2 Produkti 10

Ķīmisko reakciju vienādojumi • Oksīdi rodas ķīmisko pārvērtību rezultātā • Ķīmiskās pārvērtības apraksta ar ķīmisko reakciju vienādojumiem 11

Ķīmisko reakciju vienādojumus var sastādīt tāpēc, ka • Ķīmiskajās pārvērtībās atomi nezūd un nerodas no jauna, bet tikai pārgrupējas, kā rezultātā rodas jaunas vielas ar citām īpašībām • Katrai ķīmiski tīrai vielai ir tikai viena formula • Izejvielu un reakcijas produktu masas ir vienādas 12
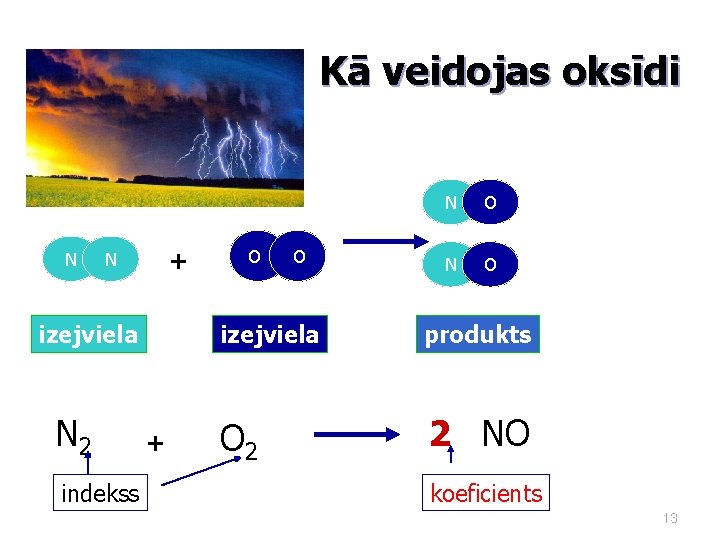
Kā veidojas oksīdi N + N izejviela N 2 indekss + O O N O izejviela produkts O 2 2 NO koeficients 13
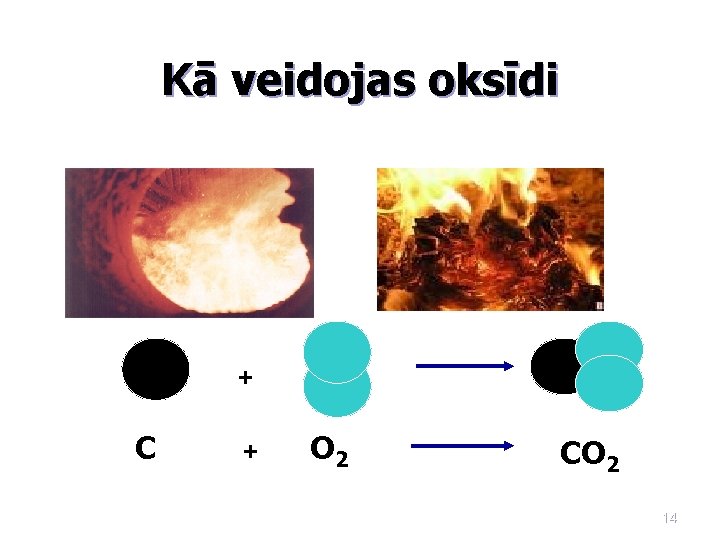
Kā veidojas oksīdi + C + O 2 CO 2 14
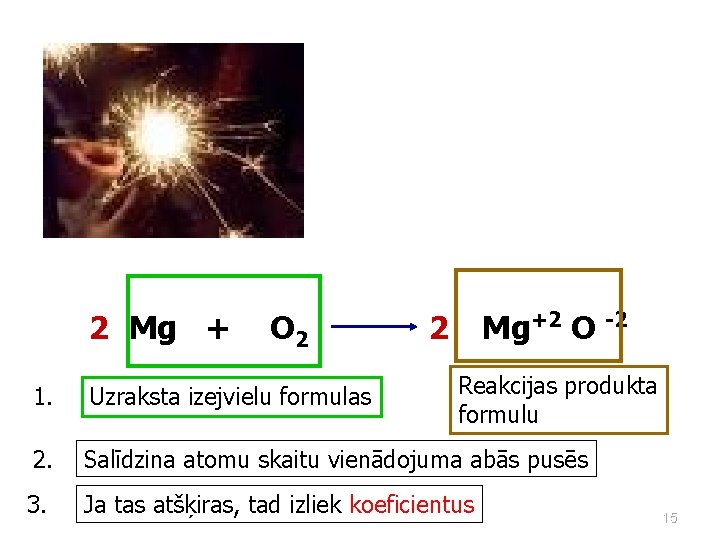
2 Mg + O 2 Mg+2 O -2 2 Reakcijas produkta formulu 1. Uzraksta izejvielu formulas 2. Salīdzina atomu skaitu vienādojuma abās pusēs 3. Ja tas atšķiras, tad izliek koeficientus 15
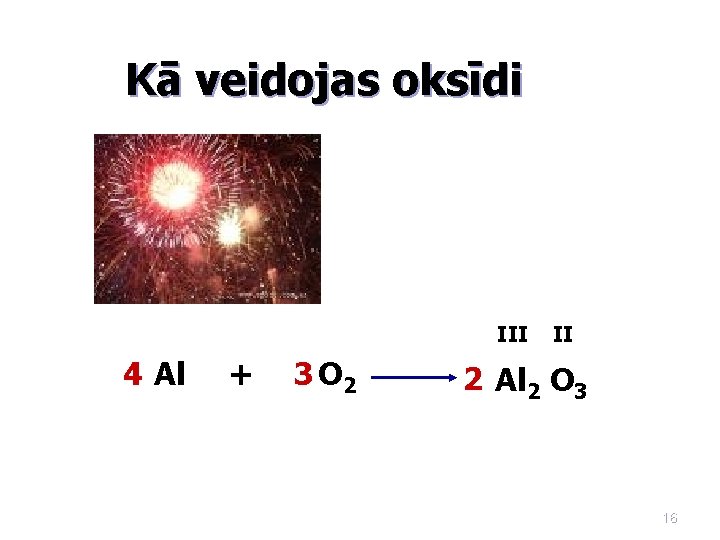
Kā veidojas oksīdi III 4 Al + 3 O 2 II 2 Al 2 O 3 16
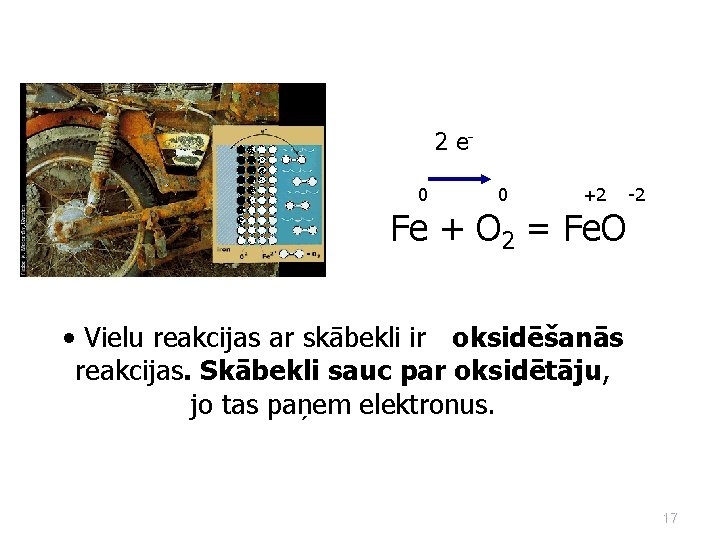
2 e 0 0 +2 -2 Fe + O 2 = Fe. O • Vielu reakcijas ar skābekli ir oksidēšanās reakcijas. Skābekli sauc par oksidētāju, jo tas paņem elektronus. 17

Metālu griešanai un metināšanai izmanto acetilēnu ( C 2 H 2) kopā ar skābekli. C 2 H 2 + 2, 5 O 2 2 CO 2 + H 2 O Ja vienādojumā labajā pusē kopējais skābekļa atomu skaits nav pāra skaitlis, tad visus koeficientus dubulto. 2 C 2 H 2 + 5 O 2 4 CO 2 + 2 H 2 O 18

Pārbaudi sevi! Ievērojot iepriekšējā slaida norādījumus, sastādiet • metāna – CH 4 degšanas reakciju vienādojumus. 19
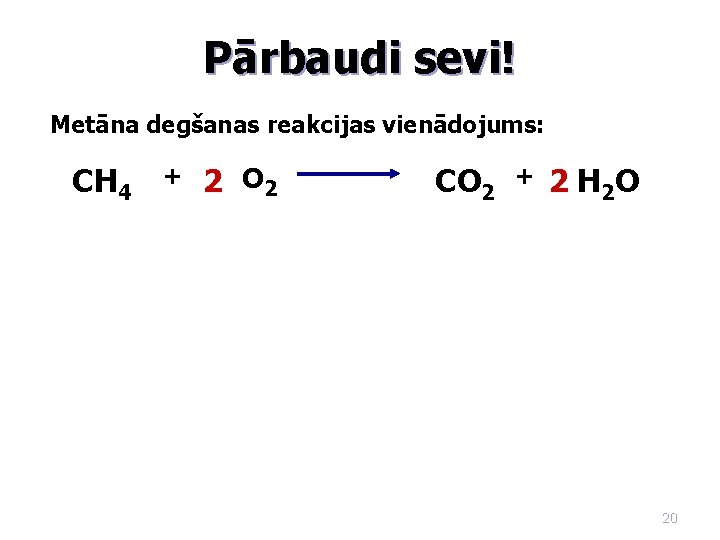
Pārbaudi sevi! Metāna degšanas reakcijas vienādojums: CH 4 + 2 O 2 CO 2 + 2 H 2 O 20
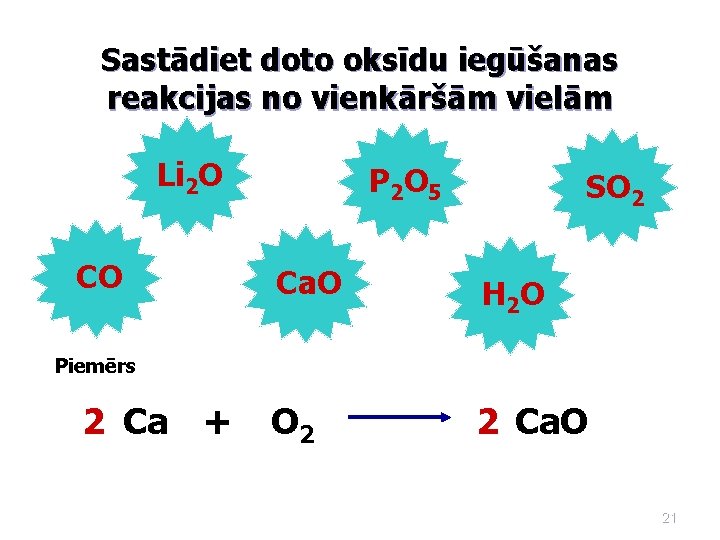
Sastādiet doto oksīdu iegūšanas reakcijas no vienkāršām vielām Li 2 O CO P 2 O 5 Ca. O Piemērs 2 Ca + SO 2 H 2 O II O 2 II 2 Ca. O 21
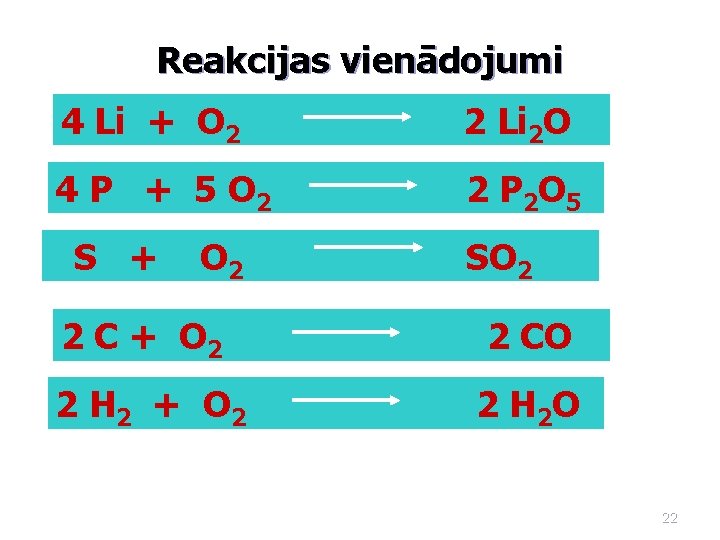
Reakcijas vienādojumi 4 Li + O 2 2 Li 2 O 4 P + 5 O 2 2 P 2 O 5 S + O 2 SO 2 2 C + O 2 2 CO 2 H 2 + O 2 2 H 2 O 22

Kurā gadījumā reakcijas vienādojumā nav kļūdas? A. 2 Na + O 2 B. Hg + O 2 C. 4 Ca + O 2 D. 2 Zn + O 2 2 Na 2 O Hg. O 2 Ca 2 O 2 Zn. O 23

Paldies par uzmanību! Izmantoti Nataļjas Kirsanovas materiāli 24
- Slides: 24