ESF ldzfinansts Rgas domes Izgltbas kultras un sporta

ESF līdzfinansēts Rīgas domes Izglītības, kultūras un sporta departamenta projekts, , Inovatīvi risinājumi sociālās atstumtības mazināšanai sociālā riska grupas jauniešiem” līguma Nr. 2009/0318/1 DP/1. 2. 2. 4. 2/09/APIA/VIAA/116, ID: 2278 Ķīmija 8. klase Ieskats vielu mikropasaulē(6+1) 2. 4. ķīmiskā saite, vērtība, oksidēšanās pakāpe, joni 1
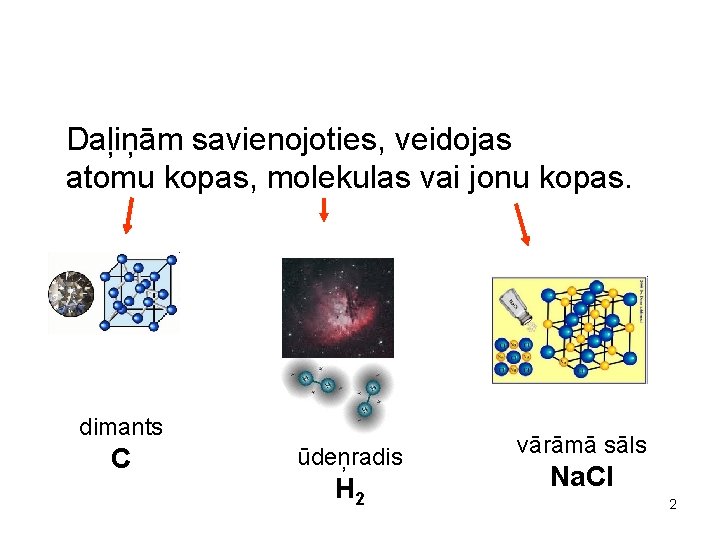
Daļiņām savienojoties, veidojas atomu kopas, molekulas vai jonu kopas. dimants C ūdeņradis H 2 vārāmā sāls Na. Cl 2

Vārāmās sāls jeb nātrija hlorīda Na. Cl vielas kristāli Na. Cl Jonu kopa Na http: //www. bio. miami. edu/~cmallery/150/chemistry/chem. htm + Cl - Nātrija Na atoms Hlora Cl atoms Na Cl 3

Atomi un joni atšķiras pēc izmēriem un īpašībām Na Metāliskais nātrijs rada ķīmiskus apdegumus Cl Hlors ir dzeltenzaļa, indīga gāze Na+ Cl- Vārāmo sāli Na. Cl lietojam uzturā 4
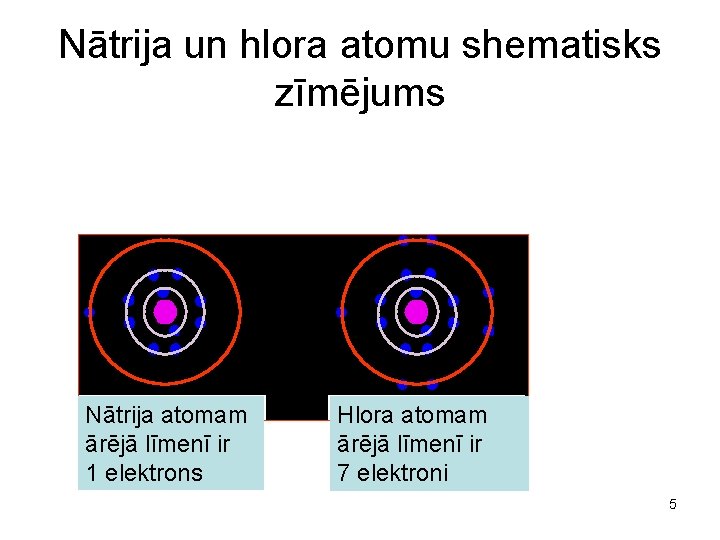
Nātrija un hlora atomu shematisks zīmējums Nātrija atomam ārējā līmenī ir 1 elektrons Hlora atomam ārējā līmenī ir 7 elektroni 5
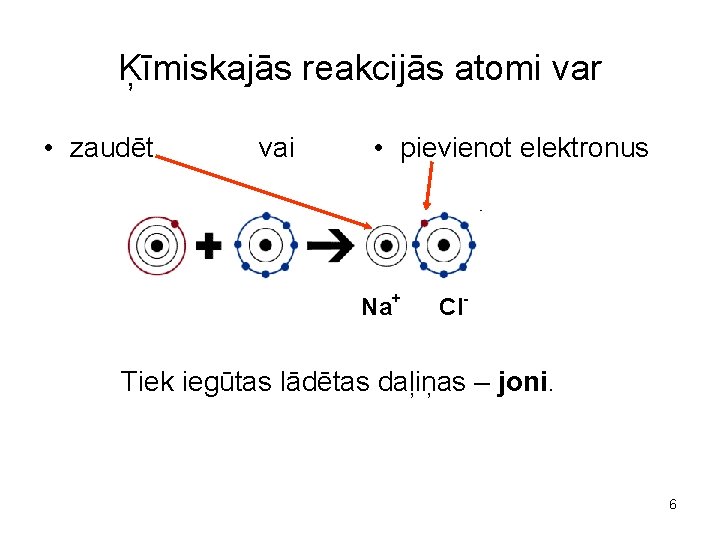
Ķīmiskajās reakcijās atomi var • zaudēt vai • pievienot elektronus Na+ Cl- Tiek iegūtas lādētas daļiņas – joni. 6
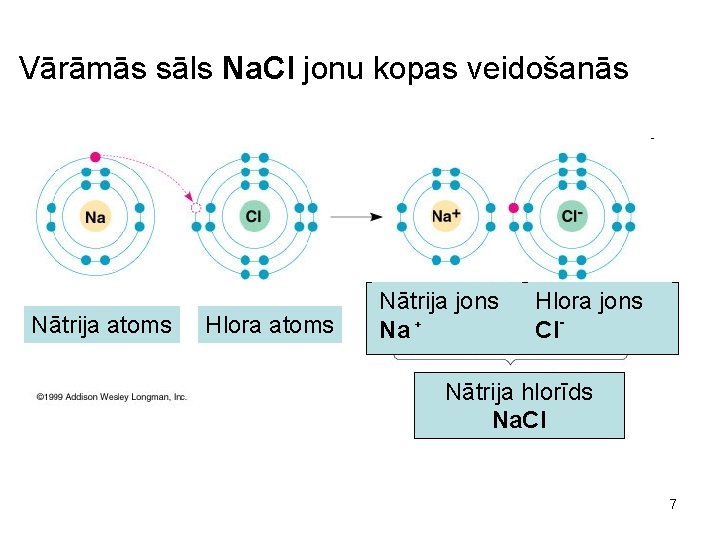
Vārāmās sāls Na. Cl jonu kopas veidošanās Nātrija atoms Hlora atoms Nātrija jons Na + Hlora jons Cl- Nātrija hlorīds Na. Cl 7
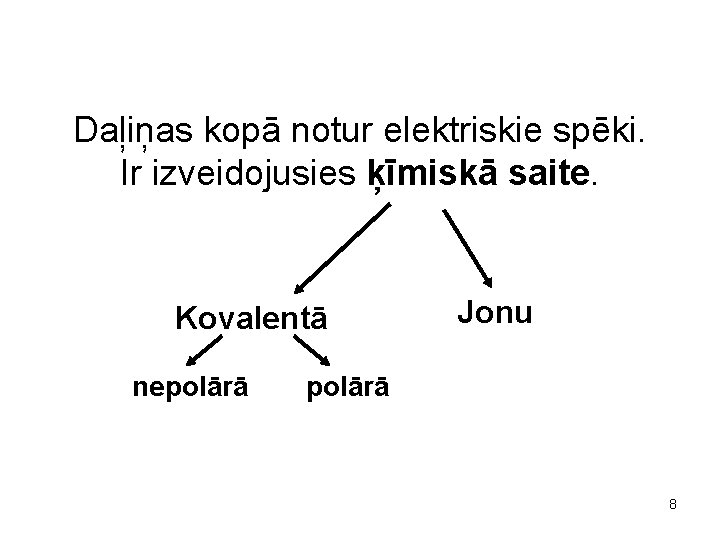
Daļiņas kopā notur elektriskie spēki. Ir izveidojusies ķīmiskā saite. Kovalentā nepolārā Jonu polārā 8
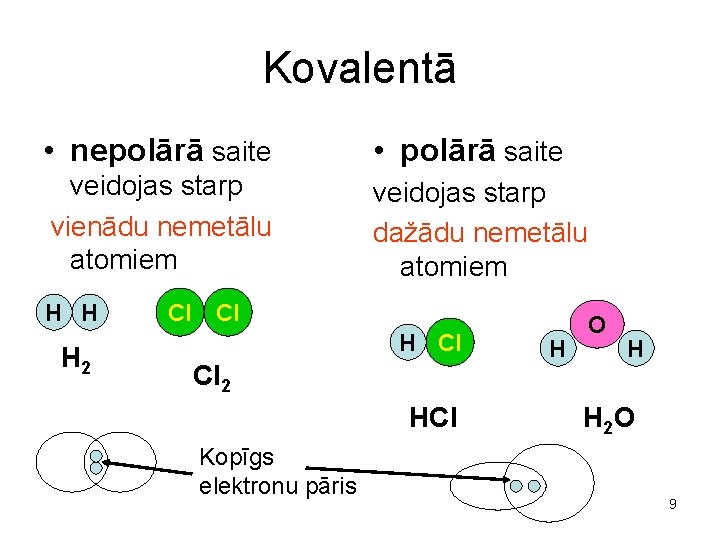
Kovalentā • nepolārā saite • polārā saite veidojas starp vienādu nemetālu atomiem veidojas starp dažādu nemetālu atomiem H H H 2 Cl Cl H Cl Cl 2 HCl Kopīgs elektronu pāris H O H H 2 O 9
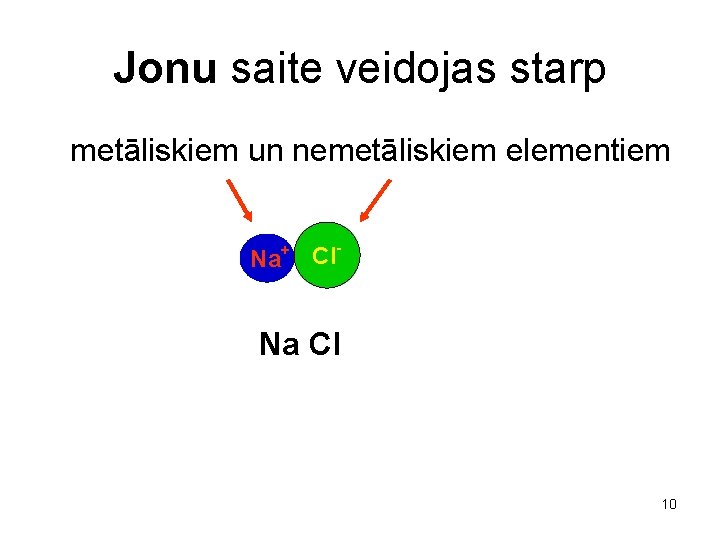
Jonu saite veidojas starp metāliskiem un nemetāliskiem elementiem Na+ Cl Na Cl 10

Saites veidošanās • Ķīmiskās saites veidošanā piedalās ārējās kārtas elektroni. • Veidojoties ķīmiskajai saitei, katrs atoms iegūst ārējā līmenī stabilu struktūru 2 vai 8 elektronus. 11
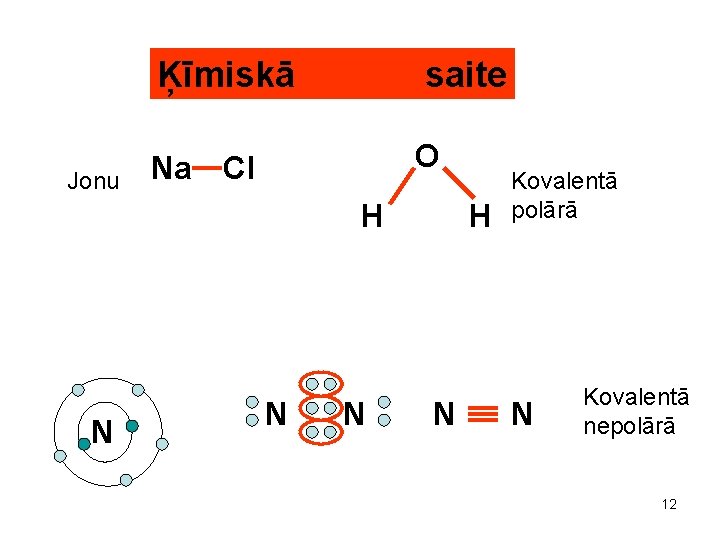
Ķīmiskā Jonu saite O Na Cl H N N N H N Kovalentā polārā N Kovalentā nepolārā 12
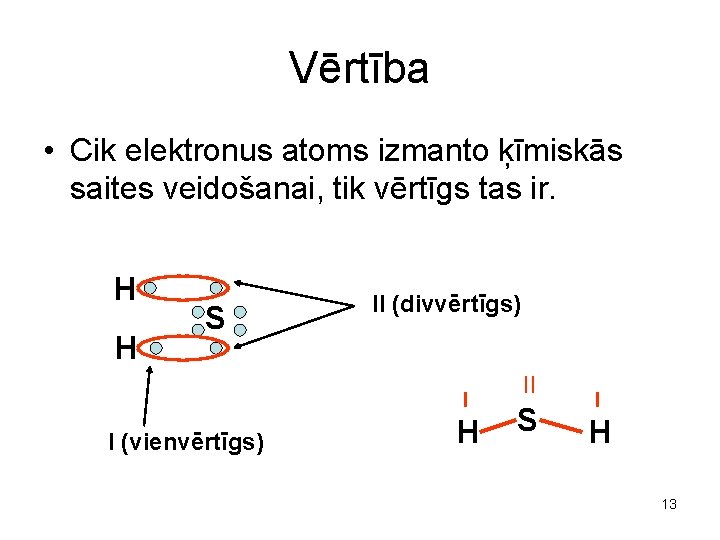
Vērtība • Cik elektronus atoms izmanto ķīmiskās saites veidošanai, tik vērtīgs tas ir. H H S II (divvērtīgs) I I (vienvērtīgs) H II S I H 13
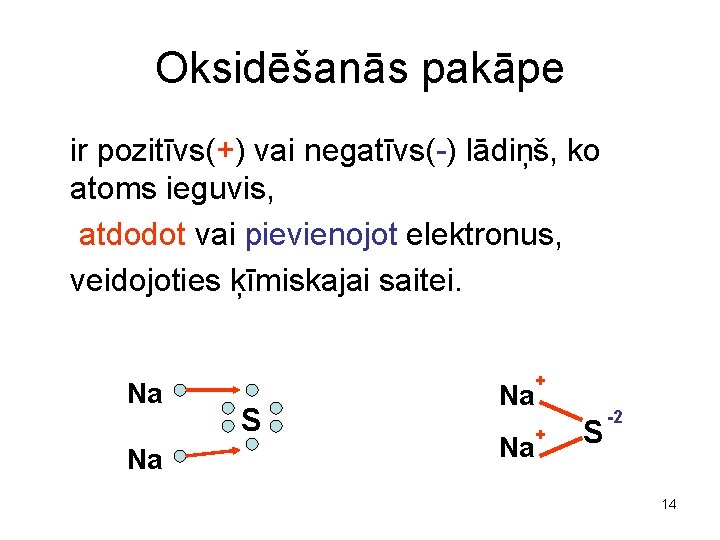
Oksidēšanās pakāpe ir pozitīvs(+) vai negatīvs(-) lādiņš, ko atoms ieguvis, atdodot vai pievienojot elektronus, veidojoties ķīmiskajai saitei. Na Na S Na + S -2 14
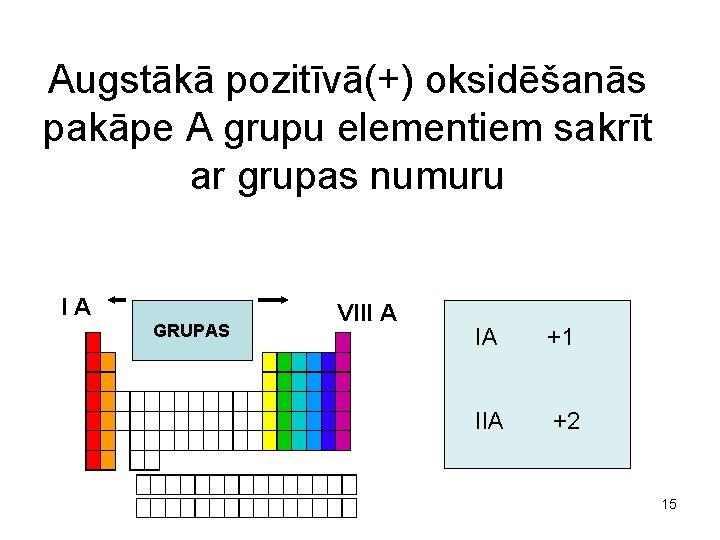
Augstākā pozitīvā(+) oksidēšanās pakāpe A grupu elementiem sakrīt ar grupas numuru IA GRUPAS VIII A IA +1 IIA +2 15
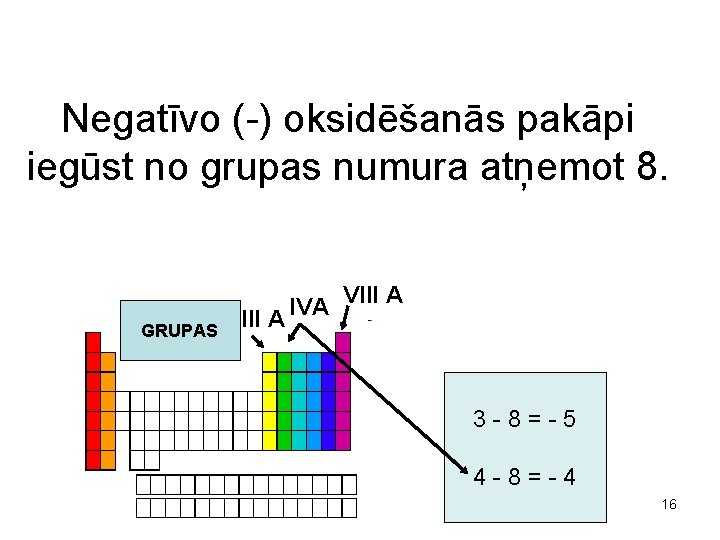
Negatīvo (-) oksidēšanās pakāpi iegūst no grupas numura atņemot 8. GRUPAS VIII A IVA III A 3 -8=-5 4 -8=-4 16
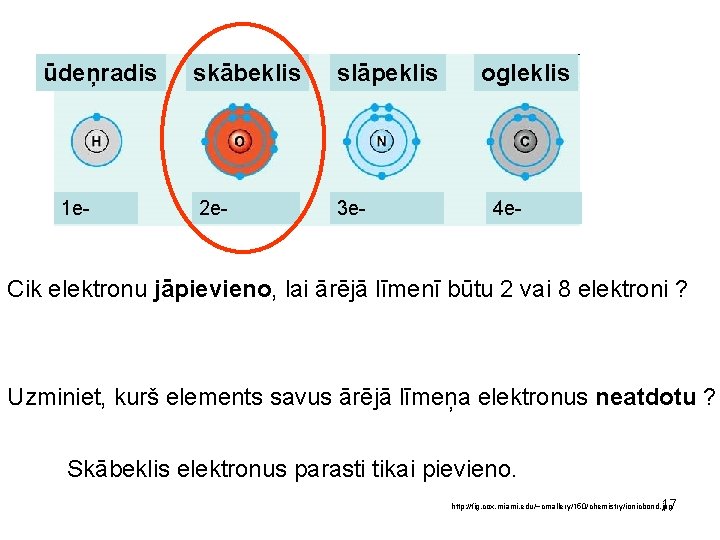
ūdeņradis 1 e- skābeklis slāpeklis 2 e- 3 e- ogleklis 4 e- Cik elektronu jāpievieno, lai ārējā līmenī būtu 2 vai 8 elektroni ? Uzminiet, kurš elements savus ārējā līmeņa elektronus neatdotu ? Skābeklis elektronus parasti tikai pievieno. 17 http: //fig. cox. miami. edu/~cmallery/150/chemistry/ionicbond. jpg

Elektronus atdodot, atomi pārvēršas par + lādētiem joniem - Be - 2 e Ba - 2 e Li -1 e- 2+ Be 2+ Ba 1+ Li 18
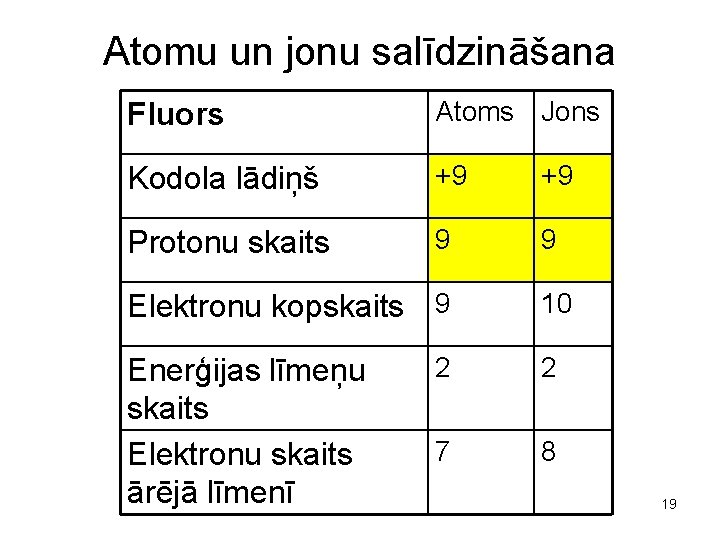
Atomu un jonu salīdzināšana Fluors Atoms Jons Kodola lādiņš +9 +9 Protonu skaits 9 9 Elektronu kopskaits 9 Enerģijas līmeņu skaits Elektronu skaits ārējā līmenī 10 2 2 7 8 19
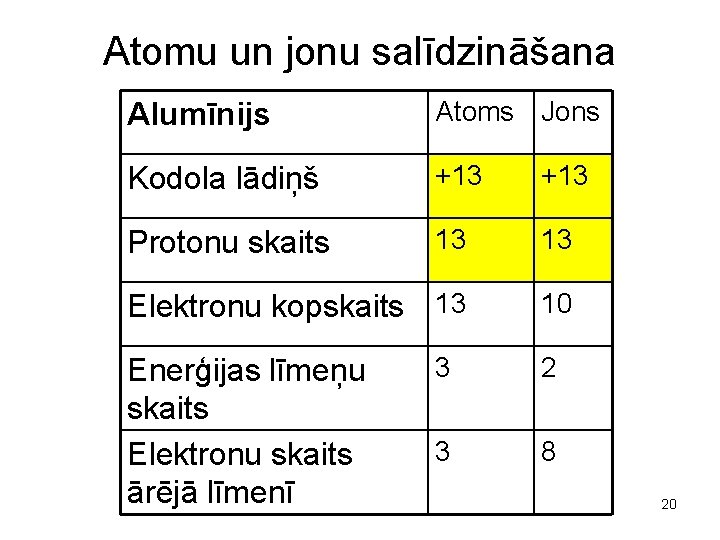
Atomu un jonu salīdzināšana Alumīnijs Atoms Jons Kodola lādiņš +13 Protonu skaits 13 13 Elektronu kopskaits 13 10 Enerģijas līmeņu skaits Elektronu skaits ārējā līmenī 3 2 3 8 20
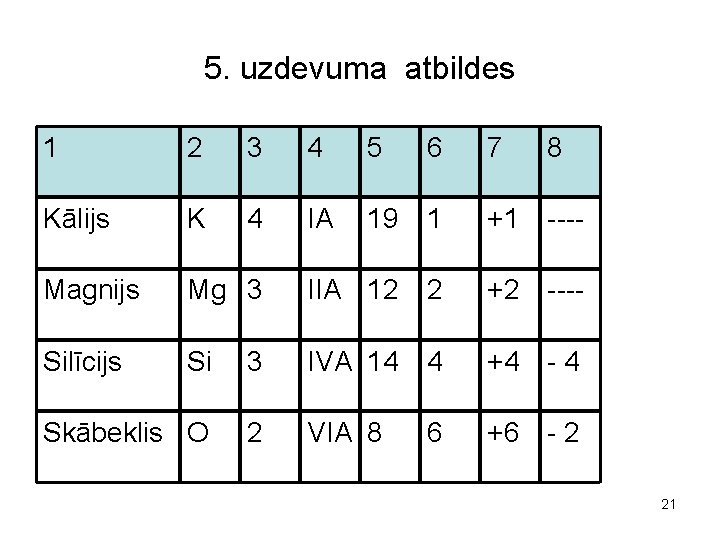
5. uzdevuma atbildes 1 2 3 4 5 6 7 8 Kālijs K 4 IA 19 1 +1 ---- Magnijs Mg 3 IIA 12 2 +2 ---- Silīcijs Si 3 IVA 14 4 +4 -4 Skābeklis O 2 VIA 8 6 +6 -2 21

Paldies! 22
- Slides: 22