ESF ldzfinansts Rgas domes Izgltbas kultras un sporta

ESF līdzfinansēts Rīgas domes Izglītības, kultūras un sporta departamenta projekts, , Inovatīvi risinājumi sociālās atstumtības mazināšanai sociālā riska grupas jauniešiem” līguma Nr. 2009/0318/1 DP/1. 2. 2. 4. 2/09/APIA/VIAA/116, ID: 2278 Ķīmija 8. klase Vielu oksidēšanās 4. 2. Oksidēšanās procesi dabā. Oksīdi. Aprēķini pēc reakcijas vienādojuma. 1

Oksidēšanās veidi • Ātra – Degšana • Ļoti ātra – Eksplozija • Lēna – – Elpošana Rūsēšana (korozija) Pūšana Trūdēšana 2

elpošana 3

elpošana Arī raugi elpo. 4

Trūdēšana 5

Pūšana 6

Rūsēšana http: //content 9 -foto. inbox. lv/albums 102192022/ichtus/20090620_Laboratorija/Laboratorija-20090620 -029. sized. jpg 7

Eksplozija 8

Degšana Deg kūla. Vilciena avārija Ventspilī, kuras rezultātā aizdegās deviņas cisternas ar degvielu. 2008. 9

Degšanā radušos siltumu izmanto lai sasildītos. Rīgas otrā termoelektrocentrāle (Rīgas TEC-2) ir lielākā Latvijas termoelektrostacija. Kā galveno kurināmo izmanto dabasgāzi, savukārt kā rezerves kurināmais ir paredzēta dīzeļdegviela. 10

Oksidēšanās procesos rodas oksīdi 11
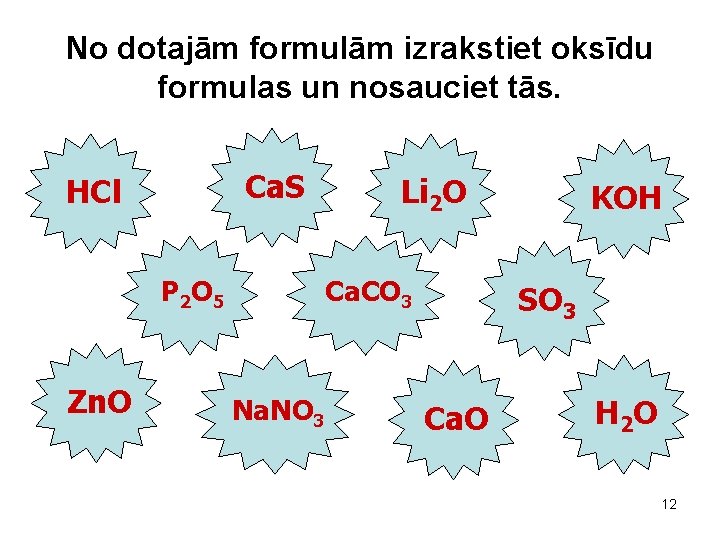
No dotajām formulām izrakstiet oksīdu formulas un nosauciet tās. Ca. S HCl P 2 O 5 Zn. O Li 2 O Ca. CO 3 Na. NO 3 KOH SO 3 Ca. O H 2 O 12
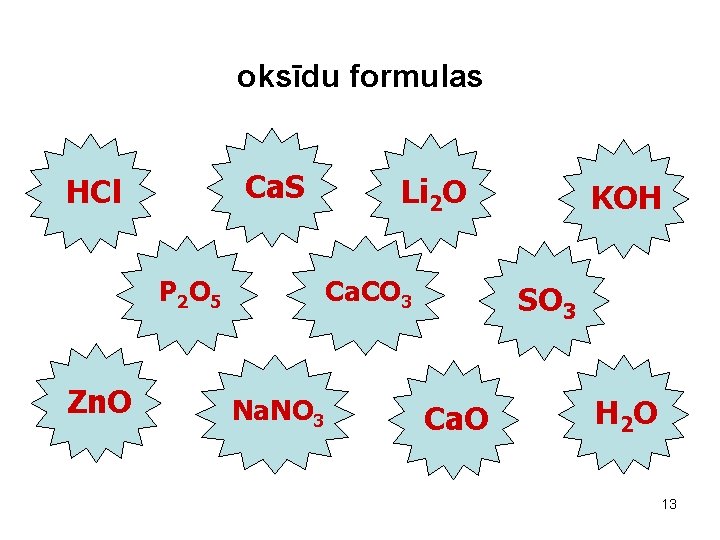
oksīdu formulas Ca. S HCl Ca. CO 3 P 2 O 5 Zn. O Li 2 O Na. NO 3 KOH SO 3 Ca. O H 2 O 13

Li 2 O SO 3 Sēra(VI) oksīds Sēra trioksīds Litija oksīds Zn. O Ūdeņraža oksīds H 2 O (ūdens) Cinka oksīds Ca. O P 2 O 5 Fosfora (V) oksīds Kalcija oksīds Fosfora pentoksīds 14
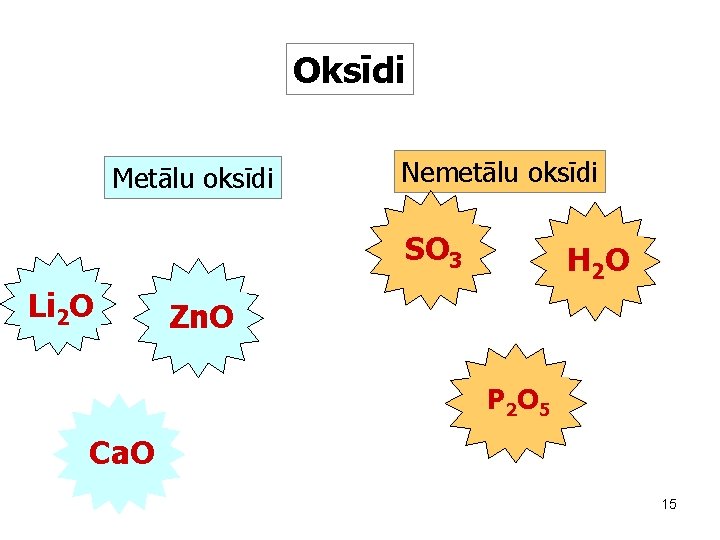
Oksīdi Metālu oksīdi Nemetālu oksīdi SO 3 Li 2 O H 2 O Zn. O P 2 O 5 Ca. O 15
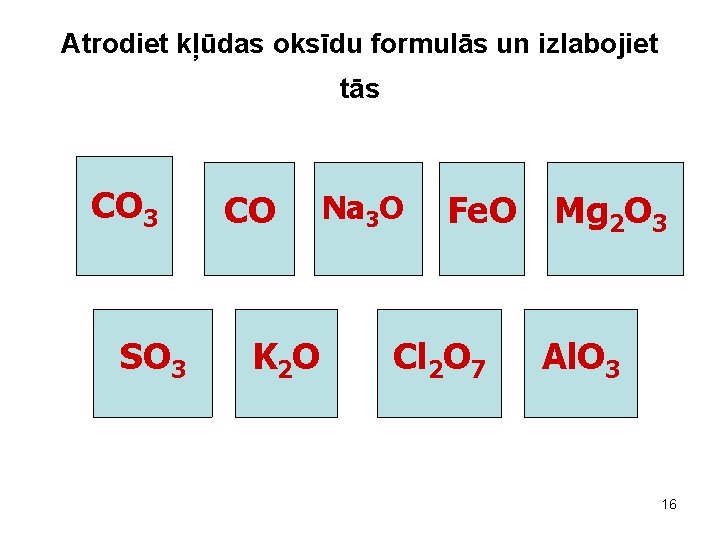
Atrodiet kļūdas oksīdu formulās un izlabojiet tās CO CO 33 SO 3 CO K 2 O Na 3 O Fe. O Cl 2 O 7 Mg 2 O 3 Al. O 3 16
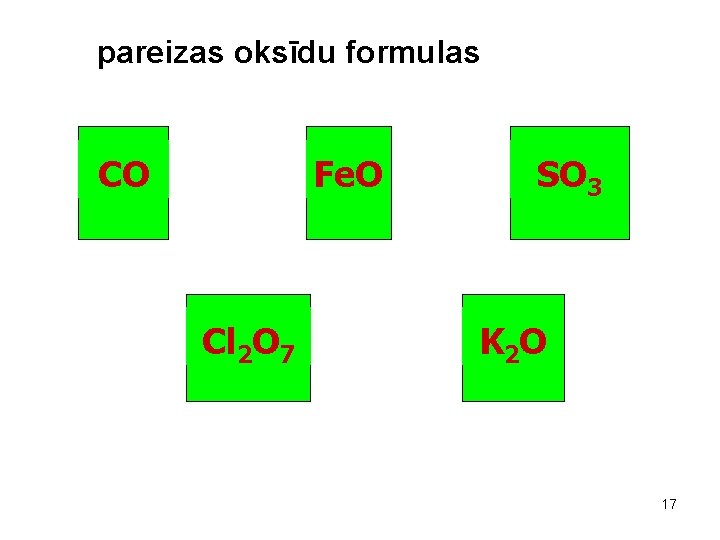
pareizas oksīdu formulas CO Fe. O Cl 2 O 7 SO 3 K 2 O 17
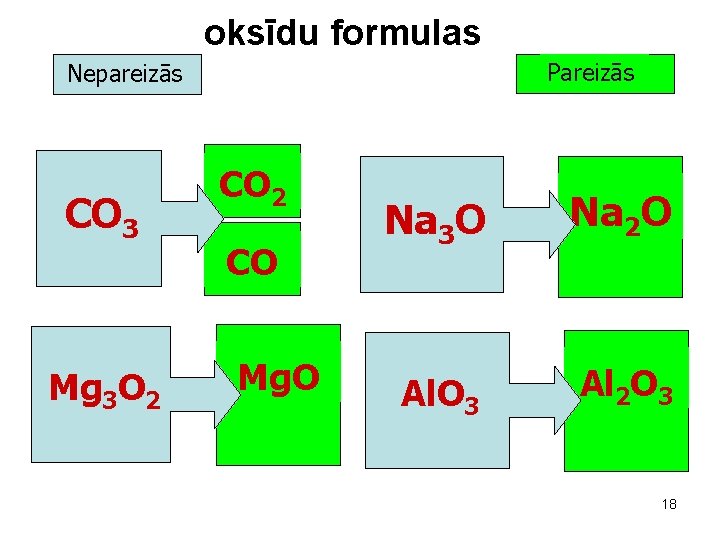
oksīdu formulas Pareizās Nepareizās CO 3 Mg 3 O 2 CO Mg. O Na 3 O Na 2 O Al. O 3 Al 2 O 3 18

Vielas daudzuma aprēķināšana • Cik daudz tvana gāzes rodas, ja ogleklis izreaģē ar 2 moliem skābekļa? 19
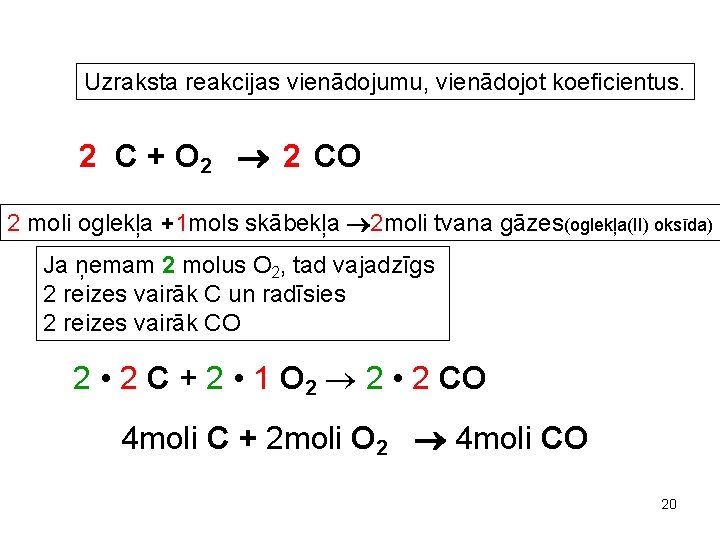
Uzraksta reakcijas vienādojumu, vienādojot koeficientus. 2 C + O 2 2 CO 2 moli oglekļa +1 mols skābekļa 2 moli tvana gāzes(oglekļa(II) oksīda) Ja ņemam 2 molus O 2, tad vajadzīgs 2 reizes vairāk C un radīsies 2 reizes vairāk CO 2 • 2 C + 2 • 1 O 2 2 • 2 CO 4 moli C + 2 moli O 2 4 moli CO 20

Paldies! 21
- Slides: 21









































