ESCURECIMENTO NOENZIMTICO ESCURECIMENTO NOENZIMTICO Podem ser divididos em














- Slides: 27

ESCURECIMENTO NÃOENZIMÁTICO

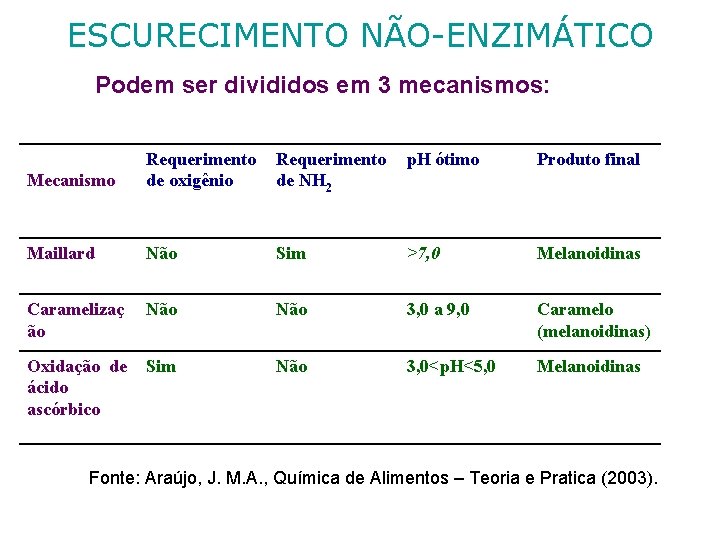
ESCURECIMENTO NÃO-ENZIMÁTICO Podem ser divididos em 3 mecanismos: Requerimento de NH 2 p. H ótimo Produto final Mecanismo Requerimento de oxigênio Maillard Não Sim >7, 0 Melanoidinas Caramelizaç ão Não 3, 0 a 9, 0 Caramelo (melanoidinas) Oxidação de ácido ascórbico Sim Não 3, 0<p. H<5, 0 Melanoidinas Fonte: Araújo, J. M. A. , Química de Alimentos – Teoria e Pratica (2003).

CARAMELIZAÇÃO • Durante o aquecimento de carboidratos, particularmente açúcares e xaropes de açúcares, ocorre uma série de reações que resultam no seu escurecimento, denominada de caramelização. • Degradação de açúcares na ausência de aminoácidos e proteínas. • Os açúcares no estado sólido são relativamente estáveis ao aquecimento moderado, mas em temperaturas maiores que 120 ºC são pirolisados para diversos produtos de degradação de alto peso molecular e escuros, denominados caramelos.

A composição química do pigmento é complexa e pouco conhecida, embora caramelos obtidos de diferentes açúcares sejam similares em composição. As frações de baixo peso molecular presentes na mistura caramelizada contêm, além do açúcar que não reagiu, ácido pirúvico e aldeídos.

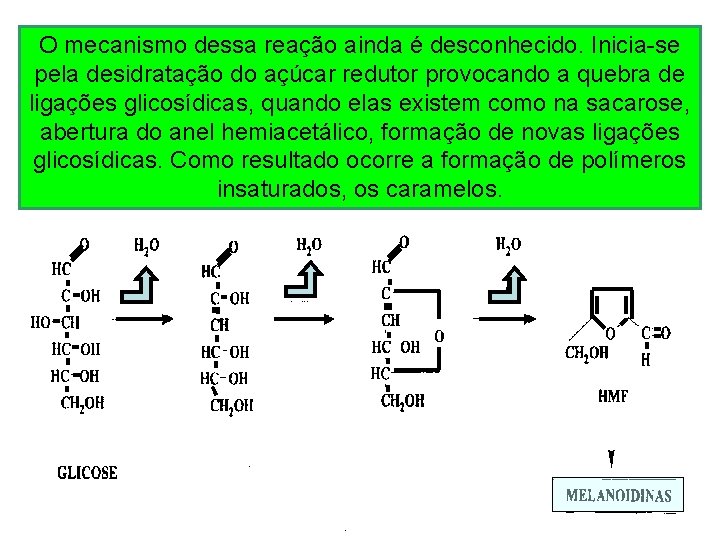
O mecanismo dessa reação ainda é desconhecido. Inicia-se pela desidratação do açúcar redutor provocando a quebra de ligações glicosídicas, quando elas existem como na sacarose, abertura do anel hemiacetálico, formação de novas ligações glicosídicas. Como resultado ocorre a formação de polímeros insaturados, os caramelos.

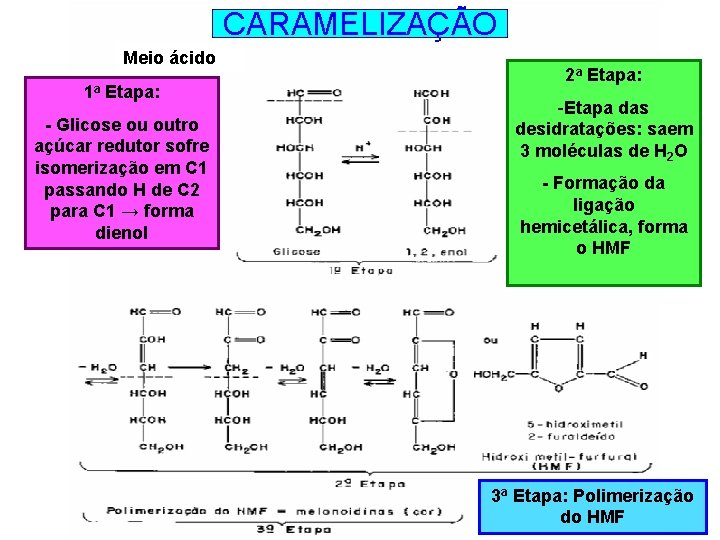
CARAMELIZAÇÃO Meio ácido 1 a Etapa: - Glicose ou outro açúcar redutor sofre isomerização em C 1 passando H de C 2 para C 1 → forma dienol 2 a Etapa: -Etapa das desidratações: saem 3 moléculas de H 2 O - Formação da ligação hemicetálica, forma o HMF 3 a Etapa: Polimerização do HMF

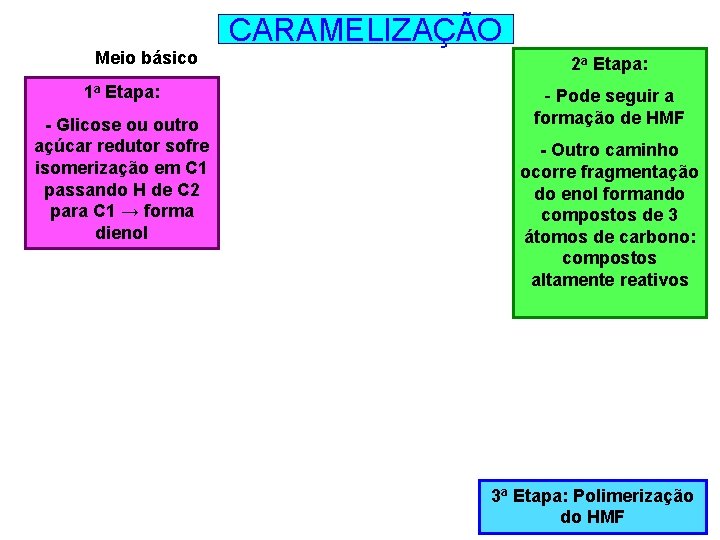
CARAMELIZAÇÃO Meio básico 1 a Etapa: - Glicose ou outro açúcar redutor sofre isomerização em C 1 passando H de C 2 para C 1 → forma dienol 2 a Etapa: - Pode seguir a formação de HMF - Outro caminho ocorre fragmentação do enol formando compostos de 3 átomos de carbono: compostos altamente reativos 3 a Etapa: Polimerização do HMF

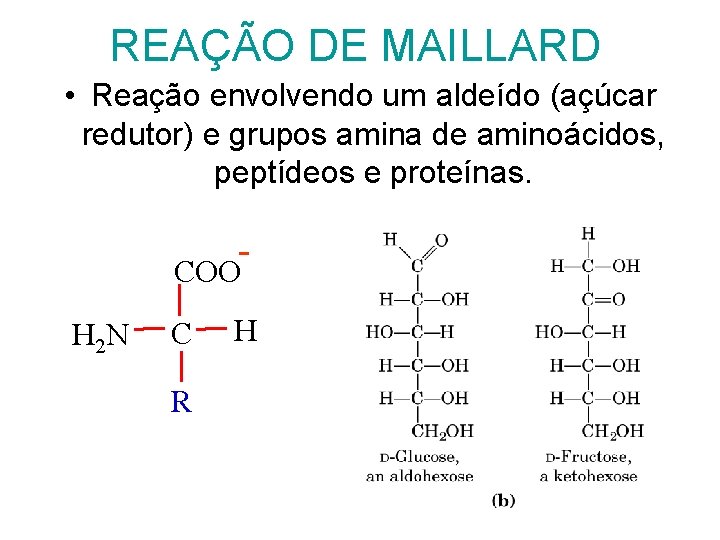
REAÇÃO DE MAILLARD • Reação envolvendo um aldeído (açúcar redutor) e grupos amina de aminoácidos, peptídeos e proteínas. COO H 2 N C R H

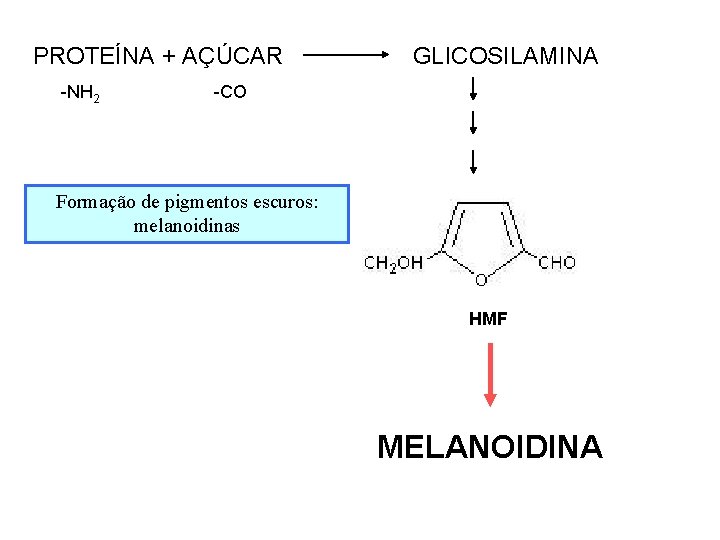
PROTEÍNA + AÇÚCAR -NH 2 GLICOSILAMINA -CO Formação de pigmentos escuros: melanoidinas HMF MELANOIDINA

Etapas da Reação de Maillard • 1 a Etapa: 1. Condensação do açúcar redutor com o aminoácido 2. Desidratação formando uma Base de Schiff 3. Rearranjo para a forma cíclica formando a glicosilamina


Etapas da Reação de Maillard • 2 a Etapa (Rearranjo de Amadori): 1. Ocorre entrada e saída de um próton (H+), inicialmente formando o catiônico da Base de Schiff 2. Isomerização formando a forma mais estável ceto (cetosaminas)


Etapas da Reação de Maillard • 3 a Etapa: 1. Conversão destes produtos em HMF: o HMF reage com os compostos iniciais, polimeriza-se e forma melanoidinas

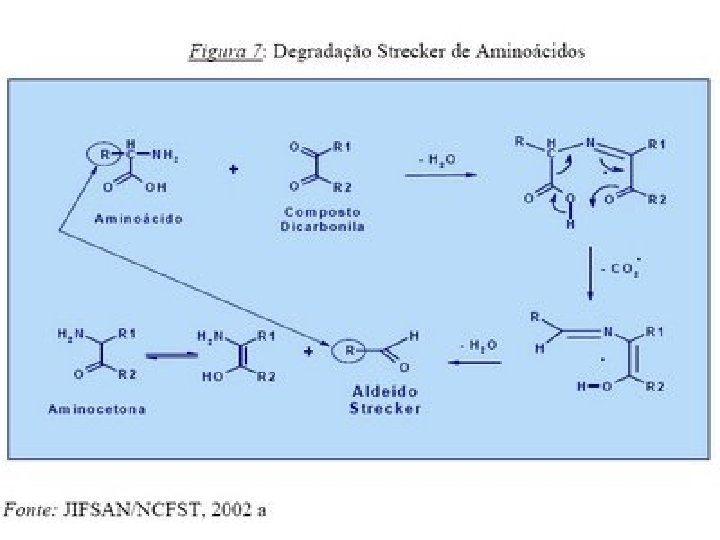
Etapas da Reação de Maillard • Degradação de Strecker: 1. Compostos α-dicarbonila reagem com aminoácidos, produzindo sua degradação 2. Ocorre produção de CO 2 3. Ocorre produção de compostos voláteis aromáticos como as pirazinas (dimetilpirazina é responsável pelo aroma das batatas chips)


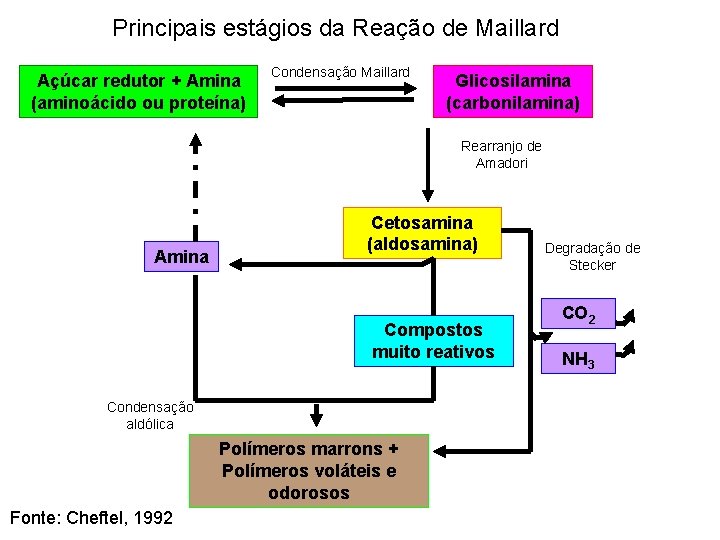
Principais estágios da Reação de Maillard Açúcar redutor + Amina (aminoácido ou proteína) Condensação Maillard Glicosilamina (carbonilamina) Rearranjo de Amadori Amina Cetosamina (aldosamina) Compostos muito reativos Condensação aldólica Polímeros marrons + Polímeros voláteis e odorosos Fonte: Cheftel, 1992 Degradação de Stecker CO 2 NH 3

REAÇÃO DE MAILLARD • Diminui a digestibilidade da proteína • Inibe a ação de enzimas digestivas • Destrói aminoácidos essenciais como a lisina • Promove alterações desejáveis de cor e flavor: crosta do pão, carne cozida, doce de leite, etc.

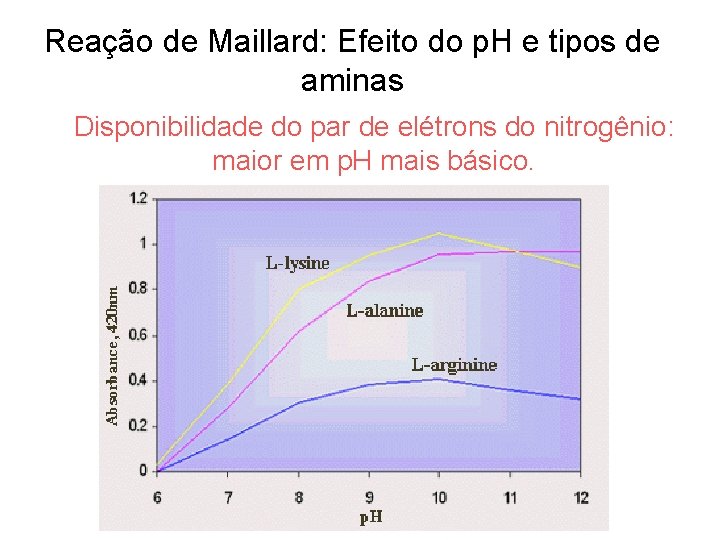
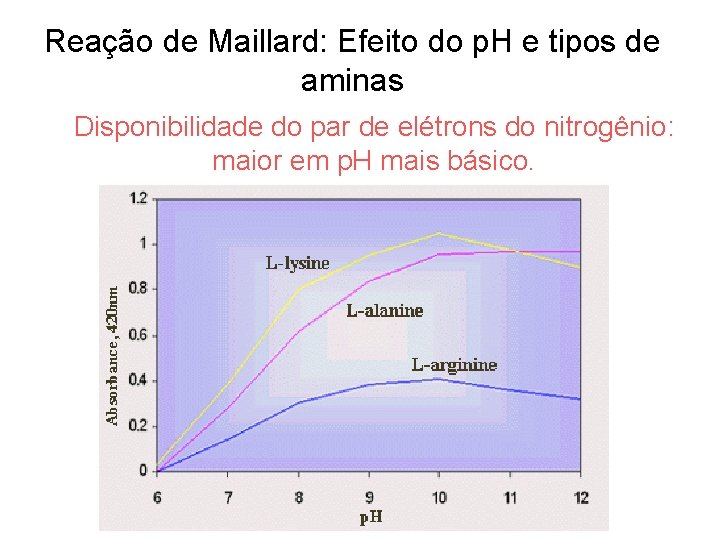
Reação de Maillard: Efeito do p. H e tipos de aminas Disponibilidade do par de elétrons do nitrogênio: maior em p. H mais básico.

Oxidação do ácido ascórbico • A vitamina C oxida rapidamente em solução aquosa Geralmente ocorre em sucos de frutas como o limão, laranjas • Exposição ao ar, calor e luz e metais (cobre, ferro)


CONTROLE DO ESCURECIMENTO • Temperatura: - As reações se intensificam com o aumento da temperatura. - Portanto, refrigeração as inibirá. - A sacarose é inerte a baixas temperaturas.

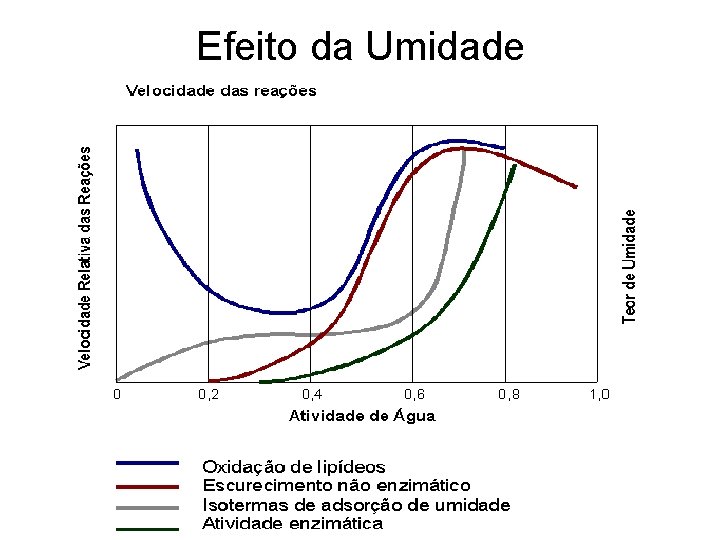
CONTROLE DO ESCURECIMENTO • Umidade - A água catalisa as reações. - O escurecimento aumenta com o aumento da umidade relativa, depois diminui. - Leite em pó: Aw = 0, 6 – escurecimento mais intenso Aw<0, 4 e >0, 7 – escurecimento não ocorre

Efeito da Umidade

Reação de Maillard: Efeito do p. H e tipos de aminas Disponibilidade do par de elétrons do nitrogênio: maior em p. H mais básico.

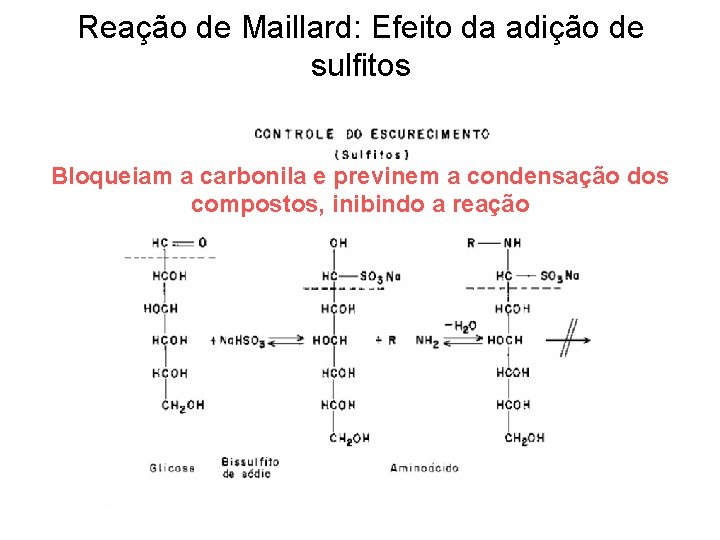
CONTROLE DO ESCURECIMENTO • Adição de aditivos - Sulfitos: bloqueiam a carbonila de açucares redutores e previnem a reação de Maillard.

Reação de Maillard: Efeito da adição de sulfitos Bloqueiam a carbonila e previnem a condensação dos compostos, inibindo a reação