ESCUELA POLITCNICA DEL EJRCITO DEPARTAMENTO DE CIENCIAS DE










![Fase de inducción de brotes P / A de brotes vs interacción [BAP] * Fase de inducción de brotes P / A de brotes vs interacción [BAP] *](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-21.jpg)
![Longitud de los brotes vs [BAP] y [ANA] Gráfico de longitud de los brotes Longitud de los brotes vs [BAP] y [ANA] Gráfico de longitud de los brotes](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-22.jpg)

![Número de entrenudos vs [BAP] y [ANA] Gráfico del número de entrenudos con respecto Número de entrenudos vs [BAP] y [ANA] Gráfico del número de entrenudos con respecto](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-24.jpg)


![Número de entrenudos vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Gráfico Número de entrenudos vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Gráfico](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-27.jpg)

![Longitud de los brotes vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Longitud de los brotes vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-29.jpg)

![Enraizamiento en medio Murashige y Skoog (M&S) Longitud de los brotes vs [ANA] Gráfico Enraizamiento en medio Murashige y Skoog (M&S) Longitud de los brotes vs [ANA] Gráfico](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-32.jpg)
![Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-33.jpg)
![Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-34.jpg)
![Enraizamiento en medio de cultivo B 5 Longitud de los brotes vs [ANA] Gráfico Enraizamiento en medio de cultivo B 5 Longitud de los brotes vs [ANA] Gráfico](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-35.jpg)
![Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-36.jpg)
![Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-37.jpg)
![Enraizamiento con carbón activado Longitud de los brotes vs [ANA] Gráfica de la longitud Enraizamiento con carbón activado Longitud de los brotes vs [ANA] Gráfica de la longitud](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-38.jpg)
![Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-39.jpg)
![Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-40.jpg)
![Enraizamiento en medio líquido Longitud de los brotes vs [ANA] Gráfica de la longitud Enraizamiento en medio líquido Longitud de los brotes vs [ANA] Gráfica de la longitud](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-41.jpg)
![Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-42.jpg)
![Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-43.jpg)



- Slides: 46

ESCUELA POLITÉCNICA DEL EJÉRCITO DEPARTAMENTO DE CIENCIAS DE LA VIDA INGENIERÍA EN BIOTECNOLOGÍA «EVALUACIÓN DEL EFECTO DE ÁCIDO α- NAFTALENACÉTICO (ANA), 6 - BENCILAMINOPURINA (BAP) Y ÁCIDO GIBERÉLICO (GA 3) EN LAS FASES DE INDUCCIÓN, MULTIPLICACIÓN Y ENRAIZAMIENTO IN VITRO A PARTIR DE YEMAS APICALES DE Valeriana scandens Previo a la obtención del título de: INGENIERA EN BIOTECNOLOGÍA MARIA JOSE BASANTES MANTILLA SANGOLQUÍ, NOVIEMBRE DE 2011

INTRODUCCIÓN especies mas distintivas del género valeriana Valeriana scandens extensivo uso en la elaboración de fitomedicinas CONTROL Ansiedad Insomnio Tensión nerviosa (principalmente) INVIMA aprobadas 2 especies V. officinalis L. (origen europeo) V. scandens abundantes en los Andes del Ecuador y Perú

Tiempos memorables virtudes medicinales Valeriana rizoma reequilibradores generales del sistema nervioso ésteres de iridoides bicíclicos valepotriatos (0, 5 -2 %) Páramo Andino afectado prácticas antropogénicas Quemas Sobrepastoreo Introducción animales ESPECIES deterioran la capa superficial del suelo alto grado de vulnerabilidad

Plantas Presentan características valiosas En la industria explotadas sin que haya un control VALERIANA no cuenta con prácticas de cultivo programado vital importancia recuperarla su distribución con los años ha llegado a ser escasa Repoblarla Extraer sus metabolitos secundarios Gran herramienta para la industria medicinal.

Valeriana scandens: Características de la planta Enredadera perenne Muy ramificada, con presencia de entrenudos Hojas: Opuestas y c/par en dirección perpendicular al par que sigue, compuestas de folíolos Flores: Pequeñas, numerosas, agrupadas en inflorescencias grandes, ramificadas, con presencia de brácteas Presentan dos tipos de flores, bisexuales y femeninas Fruto: Aquenio oblongo-linear u oval, con segmentos largos y plumosos que representan el cáliz desplegado

PROPAGACION CLONAL 1 Preparación y selección de plantas donadoras Establecimiento del cultivo aséptico Inducción de brotes 6 5 4 Multiplicación de brotes 3 2 Enraizamiento Aclimatación

OBJETIVOS Evaluar el efecto de ácido α naftalenacético (ANA), 6 - bencilaminopurina (BAP) y ácido giberélico (GA 3) en las fases de inducción, multiplicación y enraizamiento in vitro a partir de yemas apicales de Valeriana scandens Específicos • Establecer un método de desinfección para las yemas apicales de Valeriana scandens a fin de controlar los agentes contaminantes. • Evaluar la concentración de ANA y BAP adecuada para la inducción de brotes. • Evaluar la concentración de ANA y BAP adecuada para la etapa de multiplicación. • Evaluar el efecto de GA 3 en el alargamiento de brotes previo al enaizamiento. • Evaluar la concentración ideal de ANA para utilizarla como hormona de enraizamiento in vitro en los medios de cultivo M&S y B 5

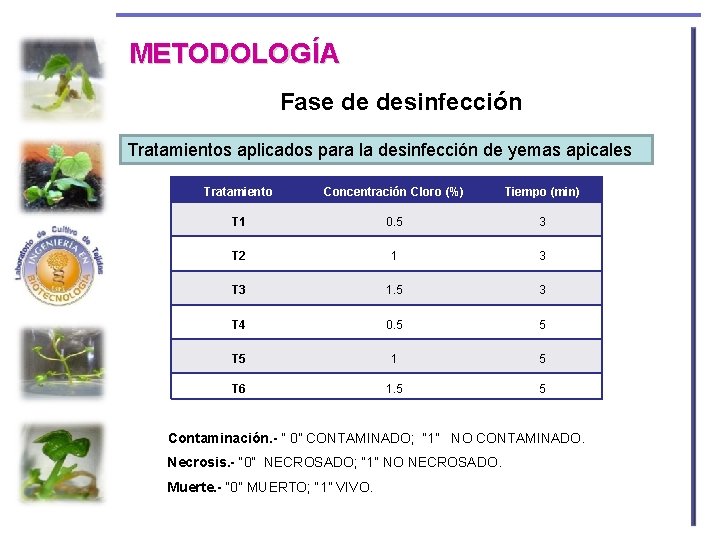
METODOLOGÍA Fase de desinfección Tratamientos aplicados para la desinfección de yemas apicales Tratamiento Concentración Cloro (%) Tiempo (min) T 1 0. 5 3 T 2 1 3 T 3 1. 5 3 T 4 0. 5 5 T 5 1 5 T 6 1. 5 5 Contaminación. - ” 0” CONTAMINADO; “ 1” NO CONTAMINADO. Necrosis. - “ 0” NECROSADO; “ 1” NO NECROSADO. Muerte. - “ 0” MUERTO; “ 1” VIVO.

A B D E C F Figura 1 (A) Yemas que van a ser sometidas a desinfección, (B) Lavado con detergente por 10 minutos (C) lavado con agua estéril por 5 minutos (D) Lavado con fungicida por 10 minutos (E) Inmersión en alcohol por 1 minuto (F) Inmersión en hipoclorito de sodio por 5 minutos

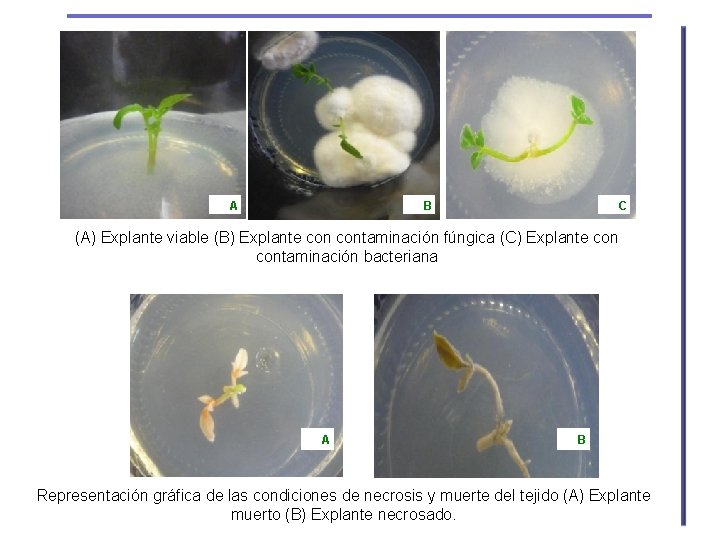
A B C (A) Explante viable (B) Explante contaminación fúngica (C) Explante contaminación bacteriana A B Representación gráfica de las condiciones de necrosis y muerte del tejido (A) Explante muerto (B) Explante necrosado.

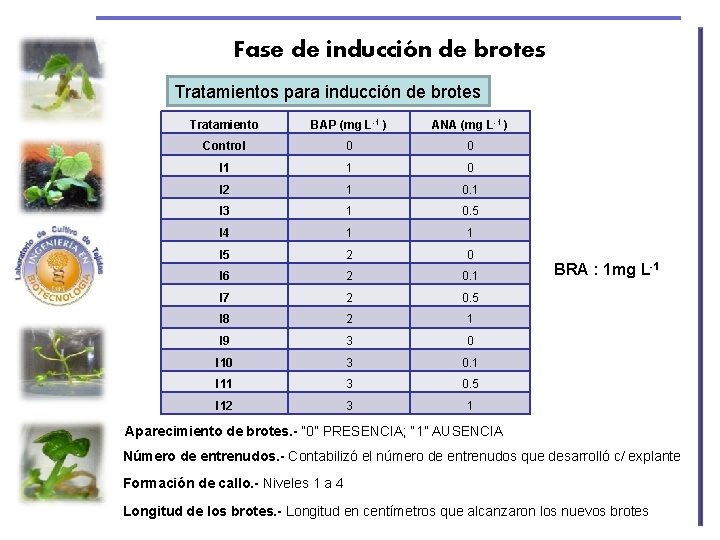
Fase de inducción de brotes Tratamientos para inducción de brotes Tratamiento BAP (mg L-1 ) ANA (mg L-1 ) Control 0 0 I 1 1 0 I 2 1 0. 1 I 3 1 0. 5 I 4 1 1 I 5 2 0 I 6 2 0. 1 I 7 2 0. 5 I 8 2 1 I 9 3 0 I 10 3 0. 1 I 11 3 0. 5 I 12 3 1 BRA : 1 mg L-1 Aparecimiento de brotes. - “ 0” PRESENCIA; “ 1” AUSENCIA Número de entrenudos. - Contabilizó el número de entrenudos que desarrolló c/ explante Formación de callo. - Niveles 1 a 4 Longitud de los brotes. - Longitud en centímetros que alcanzaron los nuevos brotes

A B C D (A) Ausencia de callo (B) Poca formación de callo (C) Mediana formación de callo (D) Abundante formación de callo.

Fase de multiplicación de brotes Tratamientos aplicados en la etapa de multiplicación Tratamiento BAP (mg L-1) ANA (mg L-1) M 1 0 0 M 2 0, 5 0, 05 M 3 1 0, 1 M 4 0, 5 0, 1 Número de entrenudos. - Contabilizó el número de entrenudos que desarrolló c/explante Vigorosidad de los nuevos brotes. - Se estableció niveles del 1 al 4, siendo “ 1” un brote débil y “ 4” un brote vigoroso Longitud de los brotes. - Se midió la longitud en centímetros

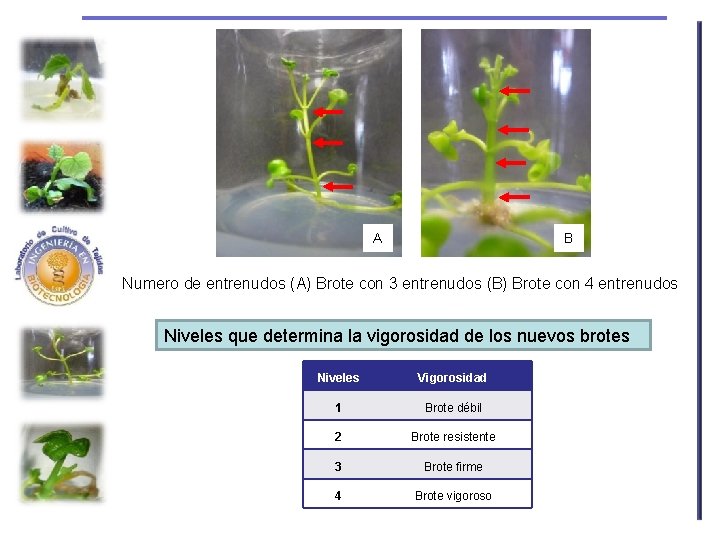
A B Numero de entrenudos (A) Brote con 3 entrenudos (B) Brote con 4 entrenudos Niveles que determina la vigorosidad de los nuevos brotes Niveles Vigorosidad 1 Brote débil 2 Brote resistente 3 Brote firme 4 Brote vigoroso

A C B D Niveles de vigorosidad (A) Brote débil (B) Brote resistente (C) Brote firme (D) Brote vigoroso.

Longitud de la planta tomada en centímetros Subcultivos sucesivos A B C (A) Entrenudos obtenido después del primer subcultivo (B) y (C) Nuevos brotes generados en los subcultivos subsiguientes

Etapa de enraizamiento Tratamientos para alargamiento de brotes Tratamiento GA 3 (mg L-1 ) A 1 1 A 2 2 A 3 3 Respuesta de crecimiento. - Se midió la longitud alcanzada por los brotes al cabo de dos semanas Elaboración de medios de cultivo con GA 3

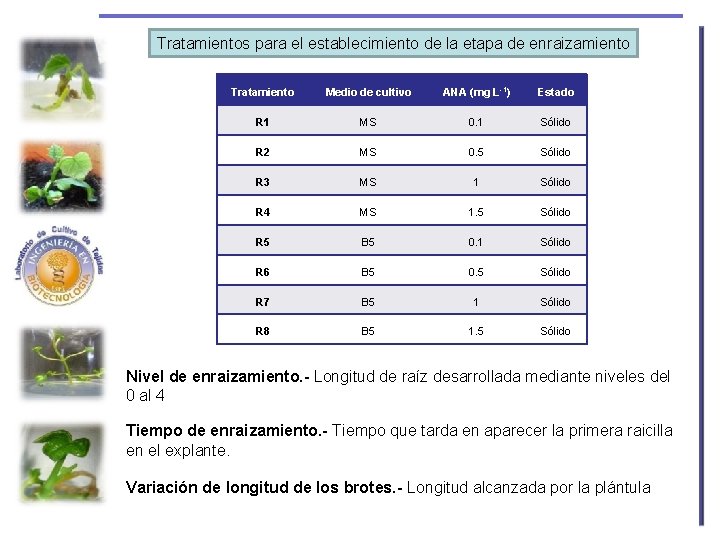
Tratamientos para el establecimiento de la etapa de enraizamiento Tratamiento Medio de cultivo ANA (mg L-1) Estado R 1 MS 0. 1 Sólido R 2 MS 0. 5 Sólido R 3 MS 1 Sólido R 4 MS 1. 5 Sólido R 5 B 5 0. 1 Sólido R 6 B 5 0. 5 Sólido R 7 B 5 1 Sólido R 8 B 5 1. 5 Sólido Nivel de enraizamiento. - Longitud de raíz desarrollada mediante niveles del 0 al 4 Tiempo de enraizamiento. - Tiempo que tarda en aparecer la primera raicilla en el explante. Variación de longitud de los brotes. - Longitud alcanzada por la plántula

A B E C D Niveles de enraizamiento (A) Sin raíz (B) Raíz desarrollada al 25% (C) Raíz desarrollada al 50% (D) Raíz desarrollada al 75% (D) Raíz desarrollada al 100%.

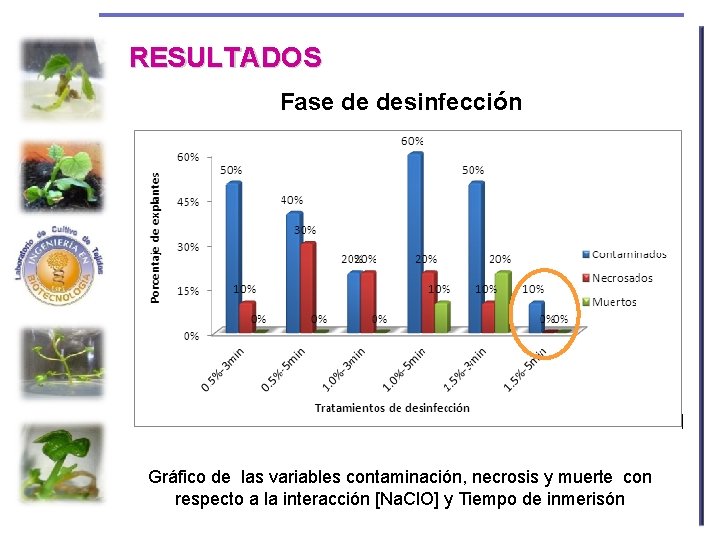
RESULTADOS Fase de desinfección Gráfico de las variables contaminación, necrosis y muerte con respecto a la interacción [Na. Cl. O] y Tiempo de inmerisón
![Fase de inducción de brotes P A de brotes vs interacción BAP Fase de inducción de brotes P / A de brotes vs interacción [BAP] *](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-21.jpg)
Fase de inducción de brotes P / A de brotes vs interacción [BAP] * [ANA] Gráfico de presencia/ausencia de brotes encontrados al usar la interacción ANA y BAP en el medio de cultivo
![Longitud de los brotes vs BAP y ANA Gráfico de longitud de los brotes Longitud de los brotes vs [BAP] y [ANA] Gráfico de longitud de los brotes](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-22.jpg)
Longitud de los brotes vs [BAP] y [ANA] Gráfico de longitud de los brotes con respecto a la interacción de las hormonas ANA y BAP

Análisis de varianza y prueba LSD Fisher para la longitud de brotes con respecto a la interacción de las hormonas ANA y BAP Se rechaza la hipótesis de igualdad de medias de tratamientos Existen diferencias estadísticamente significativas entre las combinaciones de BAP y ANA
![Número de entrenudos vs BAP y ANA Gráfico del número de entrenudos con respecto Número de entrenudos vs [BAP] y [ANA] Gráfico del número de entrenudos con respecto](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-24.jpg)
Número de entrenudos vs [BAP] y [ANA] Gráfico del número de entrenudos con respecto a la interacción de hormonas ANA y BAP

Análisis de varianza y prueba LSD Fisher para la variable número de entrenudos con respecto a la interacción hormonal ANA y BAP. Rechazo de la hipótesis de igualdad de medias de tratamientos Existen diferencias estadísticamente significativas entre las combinaciones de BAP y ANA

Fase de multiplicación de brotes 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO P / A de brotes vs [BAP] y [ANA]
![Número de entrenudos vs BAP y ANA 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Gráfico Número de entrenudos vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Gráfico](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-27.jpg)
Número de entrenudos vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Gráfico del número de entrenudos con respecto a la interacción hormonal de ANA y BAP

Análisis de varianza y prueba LSD Fisher para variable número de entrenudos con respecto a la interacción hormonal. se sugiere el rechazo de la hipótesis de igualdad de medias de tratamientos. existen diferencias estadísticamente significativas entre las combinaciones de BAP Y ANA
![Longitud de los brotes vs BAP y ANA 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Longitud de los brotes vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-29.jpg)
Longitud de los brotes vs [BAP] y [ANA] 3º SUBCULTIVO 2º SUBCULTIVO 1º SUBCULTIVO Gráfico de la longitud de brotes con respecto a la interacción hormonal de ANA y BAP

Análisis de varianza y prueba LSD Fisher para la variable longitud de brotes con respecto a la interacción hormonal de ANA y BAP. se sugiere el rechazo de la hipótesis de igualdad de medias de tratamientos existen diferencias estadísticamente significativas entre las combinaciones de BAP y ANA

Fase de enraizamiento Alargamiento de brotes usando ácido giberélico (GA 3) 1, 2 y 3 mg. L-1 Esta fitohormona no tuvo ningún efecto sobre los brotes, es decir que no existe un efecto significativo. respuesta de crecimiento
![Enraizamiento en medio Murashige y Skoog MS Longitud de los brotes vs ANA Gráfico Enraizamiento en medio Murashige y Skoog (M&S) Longitud de los brotes vs [ANA] Gráfico](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-32.jpg)
Enraizamiento en medio Murashige y Skoog (M&S) Longitud de los brotes vs [ANA] Gráfico de longitud de brotes con respecto a la concentración de ANA en medio M&S
![Nivel de enraizamiento vs ANA Gráfico del nivel de enraizamiento con respecto a la Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-33.jpg)
Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la concentración de ANA en el medio M&S.
![Tiempo de enraizamiento vs ANA Gráfica del tiempo de enraizamiento con respecto a la Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-34.jpg)
Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la concentración de ANA aplicada en el medio M&S.
![Enraizamiento en medio de cultivo B 5 Longitud de los brotes vs ANA Gráfico Enraizamiento en medio de cultivo B 5 Longitud de los brotes vs [ANA] Gráfico](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-35.jpg)
Enraizamiento en medio de cultivo B 5 Longitud de los brotes vs [ANA] Gráfico de longitud de brotes con respecto a la concentración de ANA en medio B 5.
![Nivel de enraizamiento vs ANA Gráfico del nivel de enraizamiento con respecto a la Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-36.jpg)
Nivel de enraizamiento vs [ANA] Gráfico del nivel de enraizamiento con respecto a la concentración de ANA en el medio B 5.
![Tiempo de enraizamiento vs ANA Gráfica del tiempo de enraizamiento con respecto a la Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-37.jpg)
Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto a la concentración de ANA aplicada en el medio B 5.
![Enraizamiento con carbón activado Longitud de los brotes vs ANA Gráfica de la longitud Enraizamiento con carbón activado Longitud de los brotes vs [ANA] Gráfica de la longitud](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-38.jpg)
Enraizamiento con carbón activado Longitud de los brotes vs [ANA] Gráfica de la longitud de brotes con respecto al uso de carbón activado en el medio de cultivo M&S
![Nivel de enraizamiento vs ANA Gráfica del nivel de enraizamiento con respecto al uso Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-39.jpg)
Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso de carbón activado en el medio de cultivo M&S
![Tiempo de enraizamiento vs ANA Gráfica del tiempo de enraizamiento con respecto al uso Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-40.jpg)
Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso de carbón activado en el medio de cultivo M&S
![Enraizamiento en medio líquido Longitud de los brotes vs ANA Gráfica de la longitud Enraizamiento en medio líquido Longitud de los brotes vs [ANA] Gráfica de la longitud](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-41.jpg)
Enraizamiento en medio líquido Longitud de los brotes vs [ANA] Gráfica de la longitud de brotes con respecto al uso de medio M&S líquido.
![Nivel de enraizamiento vs ANA Gráfica del nivel de enraizamiento con respecto al uso Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-42.jpg)
Nivel de enraizamiento vs [ANA] Gráfica del nivel de enraizamiento con respecto al uso de medio M&S líquido.
![Tiempo de enraizamiento vs ANA Gráfica del tiempo de enraizamiento con respecto al uso Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso](https://slidetodoc.com/presentation_image/4c872282e40ef31a5799f5520f40b54f/image-43.jpg)
Tiempo de enraizamiento vs [ANA] Gráfica del tiempo de enraizamiento con respecto al uso de medio M&S líquido.

CONCLUSIONES 1. 5% de hipoclorito de sodio por un tiempo de 5 minutos de inmersión permite obtener explantes libres de contaminación. El medio de cultivo sin suplemento hormonal, presentó la mayor cantidad de brotes largos y la producción de un mayor número de entrenudos El GA 3 aplicado en la etapa previa al enraizamiento, no produjeron ningún efecto sobre el alargamiento de brotes. La adición de brasinolida permitió un mejor desarrollo de los explantes, tanto en esa etapa como en las posteriores por la acción residual Baja concentración de auxina o en su defecto, la no adición de la misma, si existe endógenamente, es suficiente para la generación de raíces. El medio de cultivo B 5 no es eficiente para la rizogénesis, debido a la reducción de la concentración de nitratos en su composición. El uso de carbón activado provee de un ambiente de oscuridad al medio de cultivo, aumentando en gran manera la rizogénesis

RECOMENDACIONES Utilizar plantas jóvenes para iniciar con los procesos in vitro ya que estos tienen una mayor capacidad de regeneración Probar la utilización de otro componente para el alargamiento de tallos en la etapa previa al enraizamiento como la zeatina o el 2 -i. P. Utilizar una auxina débil como el AIA o en su defecto una combinación de auxinas (IBA y ANA) en las etapas para ver su respuesta in vitro. Evaluar el comportamiento de los explantes después del tercer subcultivo y de ser necesario añadir suplemento hormonal al medio de cultivo, de manera que se mantenga su capacidad de regeneración. Realizar análisis de modelos de regresión logístico binomial y multinomial, según corresponda, para los datos obtenidos. Continuar con la investigación, analizando más especies de esta familia, ya que este trabajo constituye una premisa para posteriormente crear bancos de germoplasma, estudios de genética poblacional etc.

GRACIAS