ESCSFEPECS SES DF Amniorrexe Prematura Dbora Pompeu Martins

ESCS/FEPECS – SES DF Amniorrexe Prematura Débora Pompeu Martins / Janice Bauab de Assis Orientadores : Dr. Paulo Sérgio França Dra. Denise Cidade Dr. Paulo R. Margotto Colaboradores : Lenira Silva Valadão /Roberta T. Talarico Escola Superior de Ciências da Saúde(ESCS)/SES/DF- HRAS – 04/11/2005

Relato de Caso ANAMNESE (24/08/05) Identificação: Z. B. A. , 38 anos, 1 filha, casada, supervisora de produção de produtos cosméticos, natural de Tianguá-CE, procedente do Guará I-DF. Queixa Principal: Perda de líquido pela vagina há 4 dias.

Relato de Caso História da Doença Atual: Paciente refere perda de líquido transvaginal aprox. às 9 h 30 do dia 20/08/05, em quantidade moderada. Relata que vem perdendo líquido de modo intermitente. Nega contrações ou sangramento transvaginal. Chegou à emergência obstétrica do HRAS, encaminhada do HRGu, 8 horas após o ocorrido.

Relato de Caso Antecedentes Ginecológicos: Menarca: 12 anos; Coitarca: 13 anos; Uso de ACHO (Microvlar) durante 18 anos;

Relato de Caso Antecedentes Obstétricos: G 2 C 1 AØ DUM: ? IG (eco 31/03/05 → 10 s + 4 d): 31 s + 3 d 1ª gestação (1995), PCAT sem intercorrências, feminino , 3065 g, viva e saudável. Parto cesárea por ausência de passagem (sic). Realizou 4 consultas de pré-natal.

Relato de Caso Antecedentes Patológicos: Nega doenças prévias significativas, cirurgias (além da casárea), traumas, internações anteriores, transfusão de hemoderivados e alergia medicamentosa. Antecedentes Familiares: mãe - HAS e AVC.

Relato de Caso Exame Físico (20/08): Ao exame especular, observou-se perda de líquido claro pelo colo, que se encontrava fechado. AFU: 32 cm DU: Ø BCF: 144 bpm Toque: evitado.
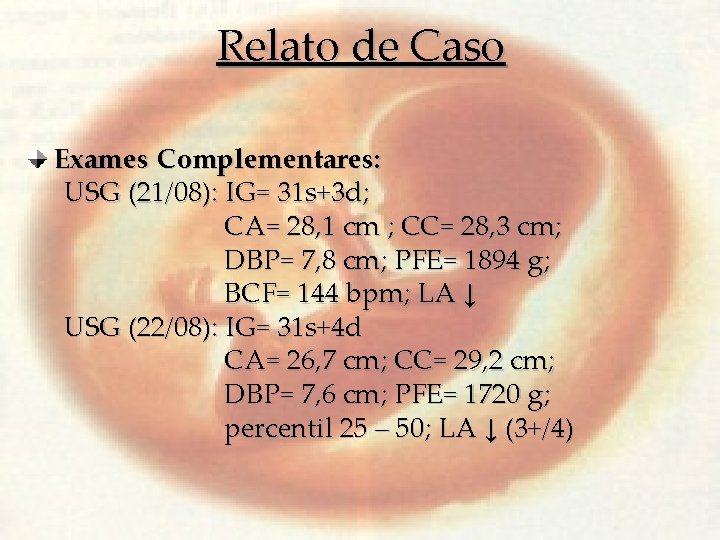
Relato de Caso Exames Complementares: USG (21/08): IG= 31 s+3 d; CA= 28, 1 cm ; CC= 28, 3 cm; DBP= 7, 8 cm; PFE= 1894 g; BCF= 144 bpm; LA ↓ USG (22/08): IG= 31 s+4 d CA= 26, 7 cm; CC= 29, 2 cm; DBP= 7, 6 cm; PFE= 1720 g; percentil 25 – 50; LA ↓ (3+/4)

Relato de Caso Exames Complementares: Hemograma Hematócrito Hemácias Hemoglobina Leucócitos 20/08 36, 7 % 3, 61 x 106/mm 3 12, 7 g/dl 14. 900 Segmentados 67 % Linfócitos 24 % Bastões 2% Monócitos 4% Eosinófilos 3% Plaquetas 257. 000
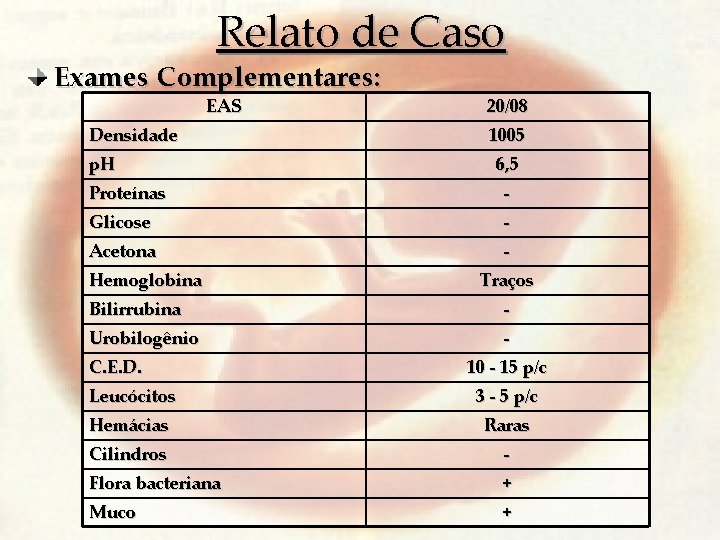
Relato de Caso Exames Complementares: EAS Densidade p. H 20/08 1005 6, 5 Proteínas - Glicose - Acetona - Hemoglobina Traços Bilirrubina - Urobilogênio - C. E. D. 10 - 15 p/c Leucócitos 3 - 5 p/c Hemácias Raras Cilindros - Flora bacteriana + Muco +

Relato de Caso Exames Complementares: VDRL (20/08): não reagente.

Relato de Caso Diagnósticos: # Gestação única tópica de 31 s + 3 d; # ROPREMA; # Oligodrâmnio.
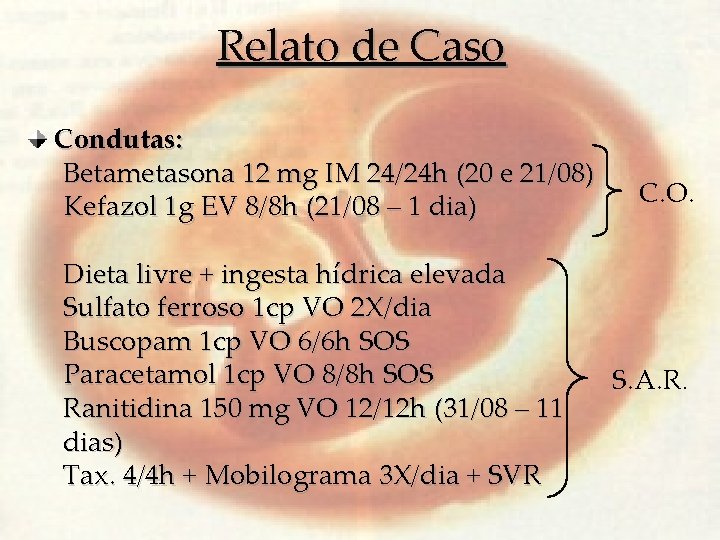
Relato de Caso Condutas: Betametasona 12 mg IM 24/24 h (20 e 21/08) Kefazol 1 g EV 8/8 h (21/08 – 1 dia) Dieta livre + ingesta hídrica elevada Sulfato ferroso 1 cp VO 2 X/dia Buscopam 1 cp VO 6/6 h SOS Paracetamol 1 cp VO 8/8 h SOS Ranitidina 150 mg VO 12/12 h (31/08 – 11 dias) Tax. 4/4 h + Mobilograma 3 X/dia + SVR C. O. S. A. R.
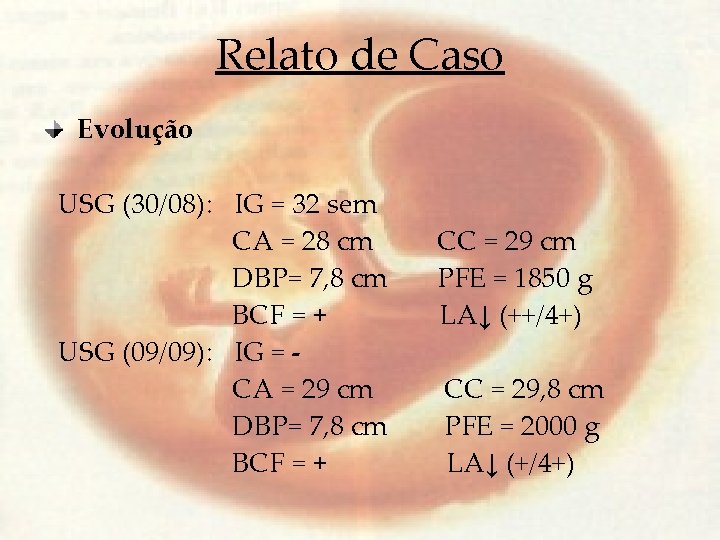
Relato de Caso Evolução USG (30/08): IG = 32 sem CA = 28 cm DBP= 7, 8 cm BCF = + USG (09/09): IG = CA = 29 cm DBP= 7, 8 cm BCF = + CC = 29 cm PFE = 1850 g LA↓ (++/4+) CC = 29, 8 cm PFE = 2000 g LA↓ (+/4+)

Relato de Caso Evolução CTB (25/08): padrão reativo, linha de base com taquicardia (FCF=160 bpm c/ duração > 10 min); CTB (26/08): padrão reativo umbilical; CTB (31/08): padrão inconclusivo; CTB (06/09): padrão reativo; CTB (08/09): padrão reativo.

Relato de Caso Evolução: Paciente fez uso de estearato de eritromicina, 500 g, 1 cp VO 6/6 h por 10 dias (30/08 – EAS: numerosos leucócitos, bacteriúria: +++); Aciclovir tópico (27/08 - suspeita de Herpes Zoster); Redução das perdas líquidas transvaginais; Contrações esporádicas e diminuição dos movimentos fetais (sic); Exame físico normal; Manutenção da gestação (23 dias) com feto em boas condições.

Relato de Caso Evolução 11/09 → metrossístoles; Dieta zero; Ampicilina 1 g EV 6/6 h; Gentamicina 240 mg 1 x/dia. 12/09 → IG = 34 s+ 5 d; parto cesáreo às 9 h 56, sem intercorrências. LA claro, RN cefálico, vivo, masculino, sem malformações aparentes e em boas condições vitais.

Relato de Caso Evolução 12 a 14/09 → puerpério sem intercorrências; 14/09 → alta hospitalar.
Amniorrexe Prematura

Amniorrexe Prematura Definições: Amniorrexe Prematura: rotura das membranas corioamnióticas antes da deflagração do trabalho de parto, independente da idade gestacional. Amniorrexe Prematura Pretermo: rotura das membranas antes do termo. Período de Latência: intervalo entre a rotura das membranas e o início do trabalho de parto.

Amniorrexe Prematura Epidemiologia: A incidência de AP varia de 3 a 18, 5% Aproximadamente 8 a 10% das pacientes com gestação a termo apresentam AP AP pretermo corresponde a 25% de todos os casos de AP e é responsável por cerca de 30% de todos os partos prematuros É maior e contribui mais para partos prematuros em populações de baixo nível sócio econômico e maiores índices de DSTs

Amniorrexe Prematura Importância das membranas fetais: Barreira física que separa o feto e o líquido amniótico estéreis do canal vaginal contaminado Importância para o desenvolvimento do feto - o líquido amniótico é necessário para o desenvolvimento dos sistemas respiratório, gastrintestinal e urinário, além de permitir a movimentação fetal, contribuindo para o desenvolvimento normal da musculatura, e proteger o feto de lesões traumáticas e de lesões isquêmicas, por compressão do cordão umbilical

Amniorrexe Prematura Importância das membranas fetais: Previne o prolapso de qualquer estrutura intra-amniótica pela cérvix, que frequentemente sofre dilatação antes da deflagração do trabalho de parto franco Depósito de substratos para processos bioquímicos

Amniorrexe Prematura Etiologia: Rotura Fisiológica: com a aproximação do termo, as membranas vão se tornando cada vez mais susceptíveis à rotura devido ao estiramento causado pelo crescimento fetal e contrações uterinas, além da diminuição do seu conteúdo de colágeno Rotura patológica: Causa intrínseca: constituição defeituosa, polidrâmnio, incompetência cervical Causa extrínseca: infecção ascendente - gonococo, estreptococos do grupo B, Gardnerella vaginalis; após procedimento – cerclagem ou amniocentese

Amniorrexe Prematura Etiologia: Fatores de risco: fumo, gestações múltiplas, descolamento prematuro da placenta, uso de cocaína, antecedente de rotura prematura pretermo, procedimentos ou lacerações cervicais, fadiga e longas horas de trabalho, deficiência de vitamina C e E.

Amniorrexe Prematura Complicações: Parto Prematuro Infecção materna, fetal ou neonatal Hipoxia e asfixia secundárias à compressão ou prolapso de cordão umbilical Deformação fetal com restrição de crescimento, compressão de partes fetais e hipoplasia pulmonar (Potterlike síndrome) Maiores taxas de cesáreas

Amniorrexe Prematura Complicações: Parto prematuro: É a maior causa de morbidade e mortalidade perinatal nos casos de amniorrexe prematura A duração do período de latência é inversamente proporcional à idade gestacional > 37 s – TP dentro de 24 h em 90% dos casos 28 -34 s – TP dentro de 1 semana em 80 -90% dos casos < 26 s – TP dentro de 1 semana em 50% dos casos Complicações da prematuridade: SAR, hemorragia intraventricular e enterocolite necrosante

Amniorrexe Prematura Complicações: Infecção: Quanto menor a idade gestacional, maior a probabilidade de infecção e esta tende a ser de maior gravidade Materna: corioamnionite Fetal ou neonatal: septicemia, pneumonia, infecção do trato urinário Complicações da infecção para o feto: SAR, dano ao sistema nervoso central

Amniorrexe Prematura Avaliação da paciente: Confirmação do diagnóstico: história clínica; exame especular; teste do p. H vaginal; teste de ferning; USG; amniocentese Determinação da idade gestacional: DUM, pré-natal, USG precoce; dosagem de fosfatidilglicerol e relação L/E no líquido amniótico Investigação de infecção materno-fetal: sintomas e sinais clínicos, leucograma, cultura, amniocentese, USG Estabelecer se a paciente está em trabalho de parto: dinâmica, dilatação cervical, CTB Excluir sofrimento fetal: ecodoppler

Amniorrexe Prematura Condutas: Hospitalização até o parto Interrupção imediata da gravidez em caso de em trabalho de parto avançado, corioamnionite ou sofrimento fetal Tocolíticos: Não são efetivos em prolongar a gestação em casos de amniorrexe prematura Corticóides: Antecipam a maturidade fetal e diminuem a hemorragia intraventricular, mas podem aumentar o risco de infecção materna e neonatal

Amniorrexe Prematura Condutas: Antibióticos: Reduzem o risco de infecção materna e perinatal e também mostram-se eficazes em aumentar o período de latência provavelmente por tratar uma infecção que foi a causa da rotura Antibioticoprofilaxia para estreptococos do grupo B é mandatória quando do trabalho de parto para pacientes com AP pretermo ou prolongada, exceto se a paciente tiver uma cultura recente negativa

Amniorrexe Prematura Condutas: IG > 34 semanas: ≤ 12 h: conduta expectante para parto espontâneo >12 h: indução – ocitocina 5 UI 1 amp, precedida de misoprostol 25 -50 mg 1 cp se índice de Bishop < 5 cesárea – indicações formais ou falha de indução >18 h: antibioticoterapia – penicilina G cristalina 5. 000 UI + 2. 500. 000 UI 4/4 h

Amniorrexe Prematura Condutas: 24 < IG > 34 semanas: Corticoideterapia: betametasona 12 mg IM 24/24 h (2 doses) dexametasona 6 mg IM 12/12 h (4 doses) Antibióticoprofilaxia/terapia: ampicilina 2 g + eritromicina 250 mg EV 6/6 h p/ 48 h amoxicilina 250 mg + eritromicina 500 mg VO 8/8 h p/ 5 dias Tratamentos de vanguarda

Obrigada!

Referências Bibliográficas DINSMOOR, M. J. ; BACHMAN, R. ; et al. Outcomes after expectant management of extremaly preterm rupture of the membranes. American Journal of Obstetrics and Gynecology. vol. 190 p. 183 -187. 2004 GARITE, T. G. Premature rupture of the membranes. In: CRCASY, R. K. ; RESNIK, R. ; IAMS, J. D. Fetal Medicine Principles and Practice. 5 ed. Sauders, 2004. cap. 38 p. 723 -739. HNAT, M. D; MERCER, B. M; et al. Perinatal outcomes in women with preterm rupture of the membranes between 24 and 32 weeks of gestation and a history of vaginal bleeding. American Journal of Obstetrics and Gynecology. vol. 193 p. 164168. 2005 LEVENO, K. J. Preterm Birth. In: CUNNINGHAM, F. G; GANT, N. F. Williams Obstetrics. 21 ed. Mc. Graw-Hill, 2001. cap. 27 p. 689 -728 MERCER, B. M. Preterm premature rupture of the membranes: current approaches to evaluation and management. Obstetrics and Gynecology Clinics of North America. vol. 32 p. 411 -418. 2005 REZENDE, J. ; MONTENEGRO, C. A. Amniorrexe prematura. Obstetrícia Fundamental. 9 ed. Rio de Janeiro: Guanabara Koogan, 2005. cap. 26 p. 317 -321

Caso Clínico • Rn de Zilmar Benedita Alves Reg: 151166 -2 • Dados maternos: - Idade: 38 anos - Procedência: Guará - Tipagem sangüínea: O+ - G: II P: 0 C: I A: 0 - N° de consultas de pré-natal: 4 • Dados do parto: Cesárea por presença de aminiorexe desde 29° semana. • Bolsa rota em 20/08/05 às 9: 30 hs Data de nascimento: 12/09/05 as 10: 17 hs

Caso Clínico • Dados do RN: - Idade gestacional: 34 semanas - Sexo: Masculino - Apgar: 9 e 10 NÃO NECESSITOU DE NA SALA - Peso ao nascimento: 2145 g REANIMAÇÃO DE PARTO - Estatura: 43 cm - Perímetro Cefálico: 31 cm - Placenta: 505 g - Classificação do RN: AIG • Conduta ao nascimento: - Solicitado TORCH e Hemocultura - Prescrito Cefepime + Amicacina

Evolução Clínica • 12/09/05 RN em berço aquecido, eupneico, corado, boa perfusão. Conduta: Colhidos Hemograma e Hemocultura. Colher HMG de novo e PCR com 2 normais suspender ATB

Evolução Clínica • 13/09/05 RN em berço aquecido, ar ambiente, dieta por SOG (20 ml) – sem resíduos. TIG 4 mg/kg/min, temperatura de 37, 8 – 35°C. Eliminações ausentes Ao exame: corado, hidratado, eupneico, iniciando icterícia (? ), acianótico, reativo. Fontanela plana Pulmões limpos Ap. Card. : RCR 2 T, sem sopros, pulsos presentes Abdômen: flácido, sem VMG, RH presente. Perfusão: OK Dx : 88 mg% Conduta: Seio Materno + LHB no copo Diminuir TIG para 3 mg/kg/dia Colhido HC, PCR e Bilirrubina Total e Frações

Evolução Clínica • 14/09/05 IGPC: 34 + 2 Idade: 50 hs Peso atual: 2050 g D 2 de Cefepime + Amicacina RN em berço aquecido, ar ambiente, evolui sem distermias, sugando melhor o seio materno. FR= ok Diurese= 2, 2 ml/kg/h Ao exame: corado, eupneico, ictérico (+/4+), boa perfusão. ACP e abdome: NDN Edema em MSD por infiltração por necrólise. Dx : 70 mg% Conduta: Suspensa hidratação venosa Colhido 3°HC, PCR e avaliar suspensão de ATB Às 16 hs: Resgate de exames Bilirrubina Total: 12, 8 BI: 12, 3 BD: 0, 5 Conduta: Fototerapia

Evolução Clínica • 15/09/05 IGPC: 34 + 3 Idade 73 hs D 3 de Cefepime + Amicacina RN em berço aquecido, foto halógena. Pico febril isolado de 37, 8°C. Evacuando. Sugando bem. FR= ok Dieta= 2 ml/kg/h Ao exame: corado, eupneico, excelente atividade, ictérico leve zona III ACP e abdome: NDN Sem edema. Recebido resultado de Sorologias: todas negativas

Evolução Clínica • 16/09/05 IGPC: 34 + 4 D 4 de Cefepime + Amicacina Icterícia RN em berço aquecido, foto halógena. Suga bem Ao exame: BEG, corado, eupneico, ictérico até zona III ACP e abdome: normal Conduta: Foto Azul PCR de 14/09: 0, 1 (negativo) Aguardando hemocultura

Evolução Clínica • 17/09/05 RNPT, 34 s, no 5° dia de vida com: Icterícia neonatal IGPC: 34+6 Sepse suspeita Peso atual: 2050 g ( ↑ 15 g) D 5 de Cefepime + Amicacina Evoluindo bem, em fototerapia azul. No momento não observei qualquer icterícia. Boa aceitação do seio, com ganho ponderal. Diurese e dejeções preservados. Curva térmica normal. Ao exame: BEG, corado, eupneico, afebril, ativo, reativo, bem perfundido. AR: MVF sem RA ACV: BNF 2 T, sem sopros Abdome: flácido, sem VMG Ext. : perfundidas sem deformidades Resgate de exames Bilirrubina Total: 16 BI: 15, 2 BD: 0, 8 Conduta: Fototerapia mantida

Evolução Clínica • 18/09/05 Pré Termo: 34 s 6 dias de vida Icterícia neonatal IGPC: 34+6 Infecção suspeita não confirmada D 6 de Cefepime + Amicacina Ao exame: bebê parece bem, pouco ictérico, em foto azul, hidratado, corado, acianótico. AR: MVF sem RA ACV: BNF 2 T, sem sopros Abdome: flácido, sem VMG Ext. : sem edemas Conduta: Suspenso ATB

Evolução Clínica • 19/09/05 Infecção suspeita usou ATB por 5 dias Hemocultura: negativa IGPC: 34 + 2 Idade: 8 dias Peso atual: 2075 g (↑ 15 g) Icterícia: Mãe O+ RN em berço aquecido e foto azul. Suga bem. Ao exame: corado, eupneico, icterícia leve zona II ACP e abdome: NDN Sem edema Resultado de exames: Tipagem sangüínea do RN - B+ Coombs direto negativo Conduta: Desligada fototerapia (praticamente ictérico) Alta com orientação e retorno em 48 hs para avaliar icterícia
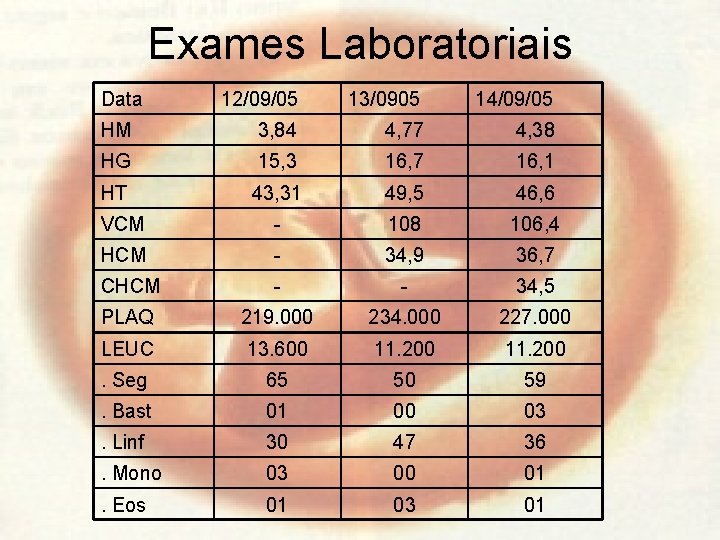
Exames Laboratoriais Data 12/09/05 13/0905 14/09/05 HM 3, 84 4, 77 4, 38 HG 15, 3 16, 7 16, 1 HT 43, 31 49, 5 46, 6 VCM - 108 106, 4 HCM - 34, 9 36, 7 CHCM - - 34, 5 PLAQ 219. 000 234. 000 227. 000 LEUC 13. 600 11. 200 . Seg 65 50 59 . Bast 01 00 03 . Linf 30 47 36 . Mono 03 00 01 . Eos 01 03 01
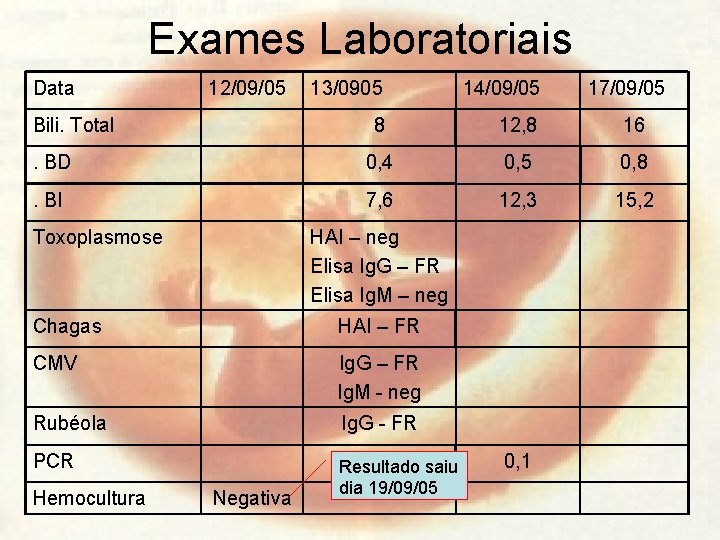
Exames Laboratoriais Data 12/09/05 13/0905 14/09/05 8 12, 8 16 . BD 0, 4 0, 5 0, 8 . BI 7, 6 12, 3 15, 2 Bili. Total Toxoplasmose HAI – neg Elisa Ig. G – FR Elisa Ig. M – neg Chagas HAI – FR CMV Ig. G – FR Ig. M - neg Rubéola Ig. G - FR PCR negativo saiu Resultado dia 19/09/05 Hemocultura Negativa 0, 1 17/09/05

Discussão • Infecção perinatal constitui causa importante de morbi-mortalidade; • Até a década de 60 para evitar-se a infecção segregava-se o recém-nascido • Contudo o Rn infectado é isolado para evitar a contaminação de outros RNs – o que exalta a necessidade de cuidados vigorosos com a assepsia

Vias de infecção fetal • Os principais mecanismos de infecção fetal são via transplacentária e via ascendente • Raramente, o feto pode se infectar por extensão de áreas adjacentes (peritônio e genitália) ou como conseqüência de métodos invasivos e para diagnóstico ou terapêutica intra uterina;

Vias de infecção fetal Por via transplacentária, o germe que atingiu diretamente a corrente sanguínea materna pode levar a: • Infecção placentária sem infecção fetal • Infecção fetal sem infecção placentária • Infecção placentária e fetal • ausência de infecção placentária e fetal

Vias de infecção fetal • A via ascendente é a seguida por agentes bacterianos encontrados na flora vaginal ou digestiva materna; • As infecções ascendentes são observadas , principalmente após a ruptura prematura de membranas, sendo a incidência aumentada em proporção direta ao tempo de bolsa rota; • São bastante conhecidos os trabalhos de Gosselin, relacionando a presença de bactérias na cavidade amniótica com o tempo de bolsa rota, chegando a quase 100% após 24 horas de bolsa rota.

Vias de infecção fetal • A manipulação excessiva da gestante também favorece a contaminação da cavidade amniótica, mas não implica obrigatoriamente o comprometimento fetal • Em apenas 5 -10% doa casos de amnionite se observa infecção fetal • Pode-se encontrar bactérias no líquido amniótico, com bolsa íntegra, em 5% dos casos.

Vias de infecção fetal • Nos casos em que houve comprometimento fetal a porta de entrada pode ter sido: pele, cordão umbilical e as cavidades naturais (ouvido, narinas , olhos e boca). Por aspiração ou deglutição, o líquido amniótico contaminado atinge a árvore respiratória ou o aparelho digestivo fetal, podendo por aí disseminar-se hematogenicamente ou produzir pneumonias ou gastrenterites.

Introdução • O risco para infecção bacteriana perinatal é 100 x maior na amnionite e rotura prematura de mebranas • Sepse neonatal – incidência : 1 – 10 casos / 1000 nascidos vivos a presença de RPM aumenta 5 x • A corioamnionite ocorre em 28% das infecções associadas ao óbito em RN baixo peso

Discussão • A causa da ruptura prematura de membranas é desconhecida e é uma complicação freqüente na gestação. • A infecção pode preceder a RPM (neutrófilos, bactérias e proteases) • A incidência de RPM pode ser de 3 -18% • Blott observou: todas as mães com infecção entram em trabalho de parto em 48 hs devido a ação das citocinas, o aumento de prostaglandinas que induz contração uterina.

• O risco de amnionite aumenta quanto mais prolongada a RPM. • A infecção ocorreu em 5 -44% dos casos • Incidência de infecção é maior nos RN até 34 semanas. A partir de 34 semanas há o aparecimento de substâncias protetoras do líquido amniótico (LA) como peptídeos catiônicos, betalisina, complexo de Zinco, transferrina, peroxidase e imunoglobulinas; isto confirma porque os RN a termo são de menor risco de desenvolver seqüelas de corioamnionite.

• Em estudo de Mataloum e cols, dentre os fatores de risco considerados, apenas a IG < ou =34 semanas, hemograma de 24 hs alterado e hemocultura positiva selecionaram de forma significante os casos de risco para infecção neonatal.

• No estudo de Bomela e cl, realizado na África do Sul (Pediatr Infect Dis J 2000; 19: 531 -5), envolvendo 100 RN com suspeita de sepses, o antibiótico foi suspenso se PCR 10 mg/l e apenas 1 retornou ao antibiótico (hemocultura ). O valor preditivo negativo foi de 99%, ou seja, a PCR repetida estimou corretamente 99 de 100 RN neste estudo como não requerendo antibioticoterapia posterior. • a dosagem da PCR auxilia no diagnóstico da sepses 2448 hs após o seu início. • a presença de hemocultura é fundamental no diagnóstico de sepses comprovada.
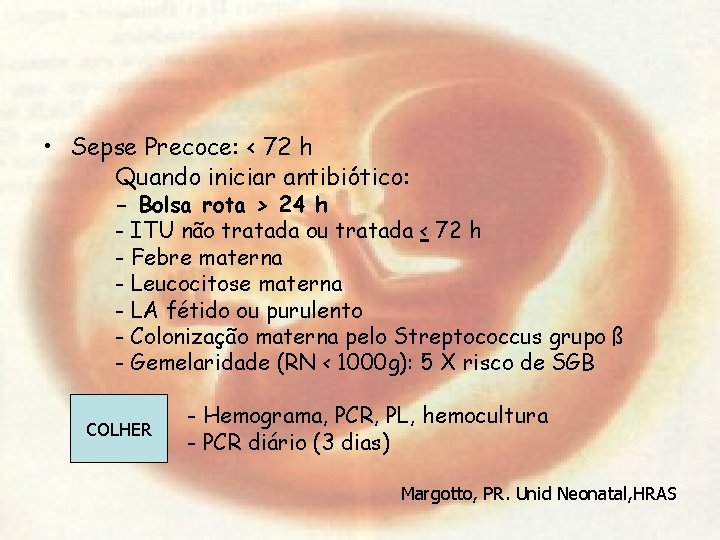
• Sepse Precoce: < 72 h Quando iniciar antibiótico: - Bolsa rota > 24 h - ITU não tratada ou tratada < 72 h - Febre materna - Leucocitose materna - LA fétido ou purulento - Colonização materna pelo Streptococcus grupo ß - Gemelaridade (RN < 1000 g): 5 X risco de SGB COLHER - Hemograma, PCR, PL, hemocultura - PCR diário (3 dias) Margotto, PR. Unid Neonatal, HRAS

• RN assintomático com IG >34 semanas com ou sem fatores de risco clássicos: • Não iniciamos o antibiótico • Hemograma com 12 - 24 - 48 h • PCR seriado (3 dias) Margotto, PR. Unid Neonatal, HRAS
Antibioticoterapia SEPSES PRECOCE AMPICILINA + GENTAMICINA AGUARDAR RESULTADO DE HEMOCULTURA NEGATIVA HEMOCULTURA POSITIVA + EVOLUÇÃO RUIM AJUSTAR (ANTIBIÓTICO SENSÍVEL) Margotto, PR. Unid Neonatal, HRAS

Antibioticoterapia • • • Observar as condições clínicas e optar por drogas mais específicas segundo o perfil hospitalar Cefepime + amicacina Vancomicina +(Piperacilina+Tazobactan) Meropenen Ciproflaxacin Trimetoprim Astreonam Margotto, PR. Unid Neonatal, HRAS

• Após resultados de cultura, PCR diário (3 dias) e conforme evolução clínico/laboratorial (hemograma, plaquetas) suspender o antibiótico • A decisão mais difícil tem que ser a RETIRADA do antibiótico e NÃO a sua introdução ( a briga tem que ser para suspender) Margotto, PR. Unid Neonatal, HRAS

• A Infecção intra-útero / nosocomial: aumenta 3 vezes mais o risco de Displasia Broco Pulmonar(DBP). Ela é fundamental na DBP. Muitos fatores pró-inflamatórios e quimiotácticos estão presentes no espaço aéreo de animais prematuros ventilados e os mesmos fatores são achados em elevadas concentrações em crianças que posteriormente irão desenvolver DBP. Margotto, PR. Unid Neonatal, HRAS

• Fatores inflamatórios como a proteína inflamatória dos macrófagos e interleucina-8 (IL 8) persistem no espaço aéreo, enquanto citocinas contrarreguladoras como a IL-10 podem diminuir, resultando num processo inflamatório desregulado e persistente. RN expostos a infecção/inflamação pré-natal ou colonização fetal por Ureaplasma urealyticum têm indicadores pró-inflamatórios no espaço aéreo ao nascer. Células inflamatórias estão presentes no espaço aéreo e no interstício e ainda as células epiteliais pulmonares podem sintetizar mediadores inflamatórios. Margotto, PR. Unid Neonatal, HRAS

Corticóide pré natal e lesão neurológica Cursos múltiplos de esteróide pré-natal ≥ 3 cursos): Banks e cl relataram maior risco de displasia broncopulmonar severa e precoce (OR= 3, 3 – p 0, 001) no RN cujas mães receberam mais do que 3 cursos de esteróide pré-natal, além de maior risco de morte (OR= 3, 2 – p 0, 003). A supressão adrenal por múltiplos cursos pode ter contribuído, uma vez que há evidências, a partir dos estudos de Watterberg e cl, que menor nível sérico de cortisol nos primeiros dias de vida associa-se com aumento de interleucinas (1 beta e 8) e persistência do canal arterial. , ambos fatores altamente associado a DBP. Margotto, PR. Unid Neonatal, HRAS

O Papel das Citocinas na lesão neurológica • Na lesão oligodendroglial, as citocinas exercem papel de grande importância. Yoon et al. Evidenciaram aumento na concentração de várias citocinas no líquido amniótico (interleucina-1β, interleucina 6 e o fator de necrose tumoral alfa) de RN pré-termo com lesões na substância branca. Margotto, PR. Unid Neonatal, HRAS

O Papel das Citocinas na lesão neurológica • Há evidências, de que a infecção de endotoxina leva à lesão na substância branca, provavelmente por um efeito direto na mielinização periventricular das células gliais ou devido a efeito no endotélio vascular, com impacto secundário nas células gliais. • A endotoxina estimula a produção, a partir dos leucócitos e de células endoteliais, de várias citocinas, como o fator de necrose tumoral alfa e a interleucina-2, que são altamente tóxicos à oligodendróglia. • Um pequeno número de citocinas é considerado antiinflamatório (p. ex. , fatores de crescimento, alguns dos quais protegem o desenvolvimento dos oligodendrócitos). Citocinas que aumentam a inflamação são identificadas como pró-inflamatórias (como vimos, estão muito aumentadas no líquido amniótico e cordão umbilical de mães que deram à luz RN pré-termo com lesão na substância branca). Margotto, PR. Unid Neonatal, HRAS

O Papel das Citocinas na lesão neurológica • Entre as citocinas pró-inflamatórias, as mais importantes são: o fator de necrose tumoral alfa (TNF – alfa e a interleucina-2, interleucina-1β e interleucina-6). O TNF – alfa (fator mielotóxico) induz a degeneração da mielina e apoptose oligodendrócita, exercendo também efeitos na maturação dos precursores dos oligodendrócitos, pela inibição da sua diferenciação, explicando assim a hipomielinização nos cérebros dos RN com lesão na substância branca. Margotto, PR. Unid Neonatal, HRAS

O Papel das Citocinas na lesão neurológica • Assim, há evidências atuais de que as citocinas podem ser mediadoras da lesão neuronal e da substância branca. Kadhim et al. detectaram alta expressão de TNF -alfa nos cérebros dos RN com LPV, principalmente no grupo com infecções bacterianas, assim como alta expressão de interleucina-2, que por sua vez poderia induzir a produção de citocinas pró-inflamatórias neurotóxicas (TNF-alfa e interleucina -1β). • Estudos têm evidenciado a relação entre LPV, infecção e citocinas. Perlman et al. relataram, numa análise de 632 RN < 1. 750 g (14 -2, 3% com LPV cística), que a ruptura prolongada de membranas (OR = 6, 9 – IC 95%: 1, 96 -22, 10) e a corioamnionite (6, 77 –IC 95%: 1, 7725, 93) foram predictores significativos de LPV. Margotto, PR. Unid Neonatal, HRAS

O Papel das Citocinas na lesão neurológica • Spinillo et al. relataram aumento de 5, 75 vezes na incidência de deficiência neurocomportamental severa nos RN de mães com ruptura prematura prolongada de membranas (idade gestacional entre 24 -34 semanas), havendo inclusive significativa relação entre a duração da ruptura de membranas e a ocorrência de hemorragia intraventricular severa, leucomalácia periventricular cística e deficiência neurocomportamental moderada a severa. Em outro estudo, estes autores relatam uma associação significativa entre infecção do trato urinário materno na admissão e leucomalácia cística (OR = 5, 71 - IC 95%: 1, 91 -17, 07). Margotto, PR. Unid Neonatal, HRAS

O Papel das Citocinas na lesão neurológica • Zupan et al. relataram que a infecção intrauterina, em combinação com a ruptura prematura de membranas, esteve associada com leucomalácia periventricular em 22%, sendo considerada fator de risco muito elevado. • Grether e Nelson relataram, em RN de peso normal ao nascer, maior risco de paralisia cerebral (PC) espástica quando ocorreu exposição intra-uterina à infecção materna em 22% das crianças com paralisia cerebral espástica, a PC foi relacionada a infecção. Margotto, PR. Unid Neonatal, HRAS

Obrigada!!!!
- Slides: 73