ESCOLA SECUNDRIA FRANCISCO RODRIGUES LOBO NCLEOS ATMICOS E

ESCOLA SECUNDÁRIA FRANCISCO RODRIGUES LOBO NÚCLEOS ATÓMICOS E RADIOACTIVIDADE INTRODUÇÃO 2011/2012 Professoras Cacilda Ferreira e Paula Sousa

ÍNDICE A. Energia de ligação nuclear e estabilidade dos núcleos. B. Processos de estabilização dos núcleos. C. Emissões radioactivas Propriedades. D. Lei do decaimento radioactivo e período de decaimento. E. Efeitos biológicos da radioactividade. F. Aplicações da radiação ionizante. G. Detectores de radiação ionizante. H. Reacções nucleares: fissão; fusão. 2
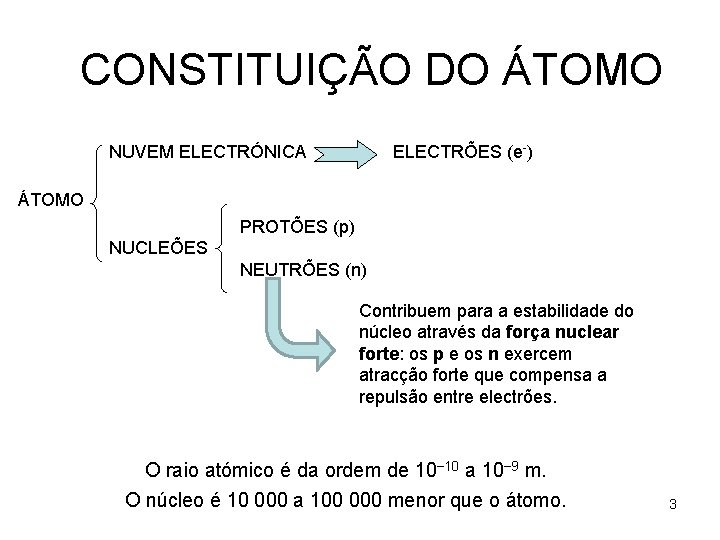
CONSTITUIÇÃO DO ÁTOMO NUVEM ELECTRÓNICA ELECTRÕES (e-) ÁTOMO PROTÕES (p) NUCLEÕES NEUTRÕES (n) Contribuem para a estabilidade do núcleo através da força nuclear forte: os p e os n exercem atracção forte que compensa a repulsão entre electrões. O raio atómico é da ordem de 10− 10 a 10− 9 m. O núcleo é 10 000 a 100 000 menor que o átomo. 3

PARTICULAS ELEMENTARES Barião – partícula constituída por 3 quarks ligados por gluões. Ex. : protão; neutrão. Mesão – partículas constituídas por 1 quark e 1 antiquark ligados por gluões. Gluão – partícula mediadora de força nuclear forte. São os quanta do campo forte. bosões quarks leptões 4

FORÇAS FUNDAMENTAIS Na natureza existem 4 tipos de interacções fundamentais: gravitacional; electromagnética; nuclear fraca; nuclear forte. Força Nuclear Forte : interacção forte que se estabelece entre bariões e mesões. Força Nuclear Fraca: interacção que afecta todos os leptões e quarks. É mediada pelos bosões W e Z. As forças nucleares fraca e forte actuam apenas dentro do núcleo atómico e na sua vizinhança imediata. força nuclear forte força nuclear electromagnética fraca força gravitacional 10 3 1 10 -39 10 -11 5
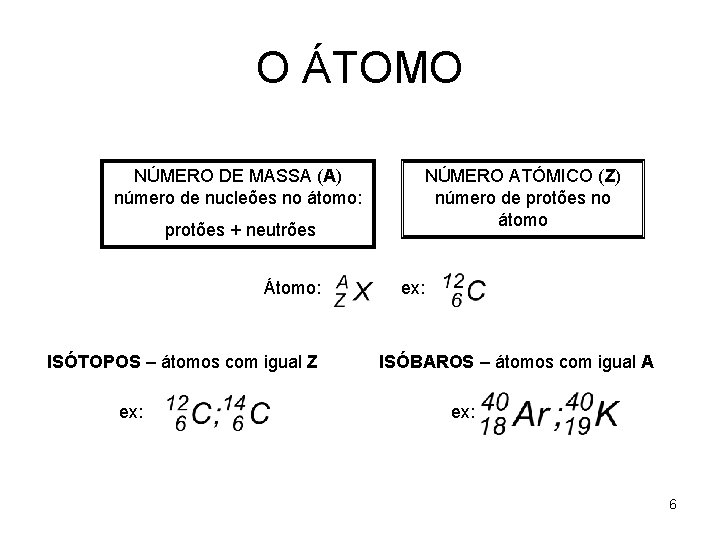
O ÁTOMO NÚMERO DE MASSA (A) número de nucleões no átomo: protões + neutrões Átomo: ISÓTOPOS – átomos com igual Z ex: NÚMERO ATÓMICO (Z) número de protões no átomo ex: ISÓBAROS – átomos com igual A ex: 6
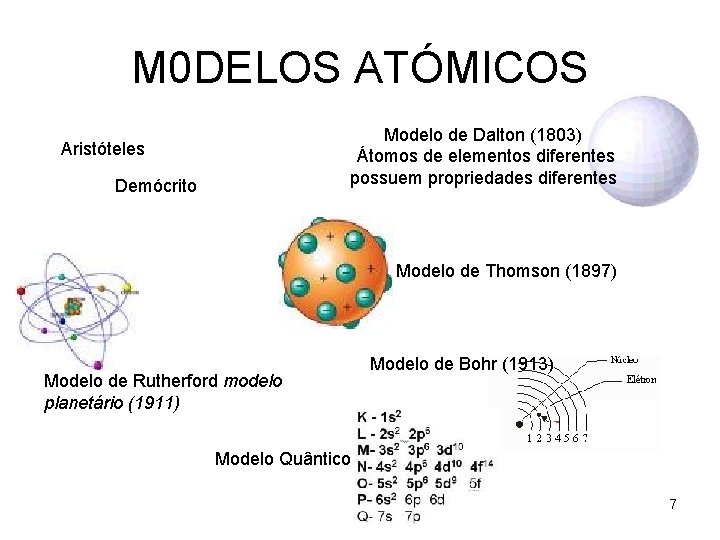
M 0 DELOS ATÓMICOS Modelo de Dalton (1803) Átomos de elementos diferentes possuem propriedades diferentes Aristóteles Demócrito Modelo de Thomson (1897) Modelo de Rutherford modelo planetário (1911) Modelo de Bohr (1913) Modelo Quântico 7
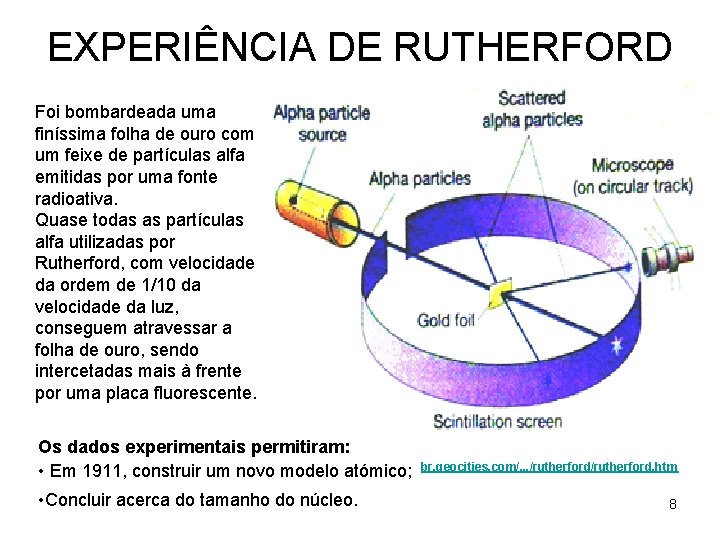
EXPERIÊNCIA DE RUTHERFORD Foi bombardeada uma finíssima folha de ouro com um feixe de partículas alfa emitidas por uma fonte radioativa. Quase todas as partículas alfa utilizadas por Rutherford, com velocidade da ordem de 1/10 da velocidade da luz, conseguem atravessar a folha de ouro, sendo intercetadas mais à frente por uma placa fluorescente. Os dados experimentais permitiram: • Em 1911, construir um novo modelo atómico; • Concluir acerca do tamanho do núcleo. br. geocities. com/. . . /rutherford. htm 8
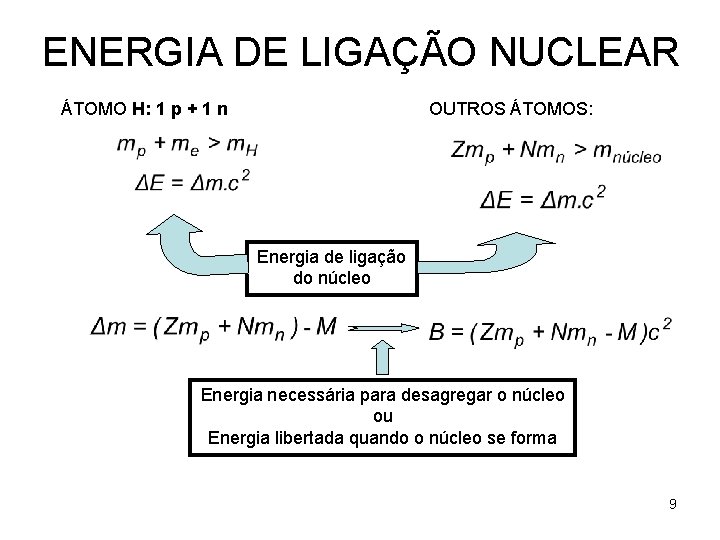
ENERGIA DE LIGAÇÃO NUCLEAR OUTROS ÁTOMOS: ÁTOMO H: 1 p + 1 n Energia de ligação do núcleo Energia necessária para desagregar o núcleo ou Energia libertada quando o núcleo se forma 9

ENERGIA DE LIGAÇÃO NUCLEAR Energia de ligação do núcleo de carbono 10

ESTABILIDADE DOS NÚCLEOS Os nucleões são mantidos juntos pela interação nuclear forte, de carácter atrativo, apesar do efeito contrário da interação coulombiana, de carácter repulsivo, entre os protões. Esta interação tem um alcance muito pequeno, da ordem de 10 -15 m, e é independente da carga elétrica, isto é, atua igualmente entre dois protões, dois neutrões ou um protão e um neutrão. O curto alcance da interação nuclear forte faz com que cada nucleão atraia apenas os nucleões mais próximos. Cada protão interage com todos os outros protões do núcleo - interação coulombiana. A interação nuclear forte contribui para a estabilidade do núcleo; a interação coulombiana contribui para a sua 11 desestabilização.
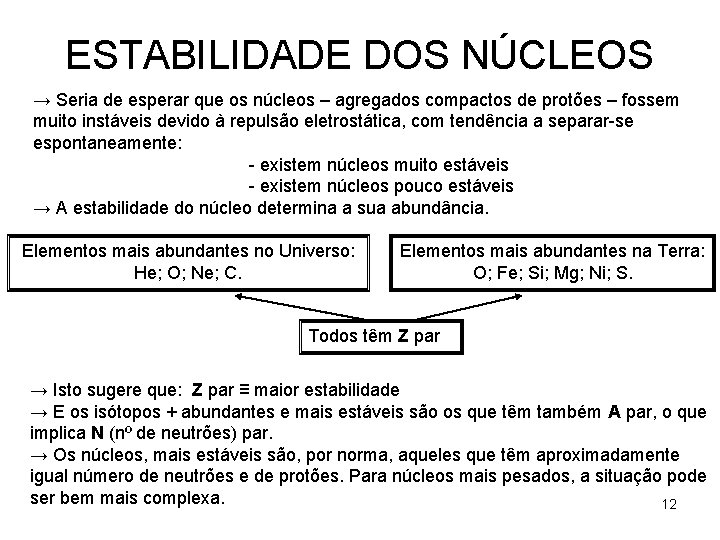
ESTABILIDADE DOS NÚCLEOS → Seria de esperar que os núcleos – agregados compactos de protões – fossem muito instáveis devido à repulsão eletrostática, com tendência a separar-se espontaneamente: - existem núcleos muito estáveis - existem núcleos pouco estáveis → A estabilidade do núcleo determina a sua abundância. Elementos mais abundantes no Universo: He; O; Ne; C. Elementos mais abundantes na Terra: O; Fe; Si; Mg; Ni; S. Todos têm Z par → Isto sugere que: Z par ≡ maior estabilidade → E os isótopos + abundantes e mais estáveis são os que têm também A par, o que implica N (nº de neutrões) par. → Os núcleos, mais estáveis são, por norma, aqueles que têm aproximadamente igual número de neutrões e de protões. Para núcleos mais pesados, a situação pode ser bem mais complexa. 12
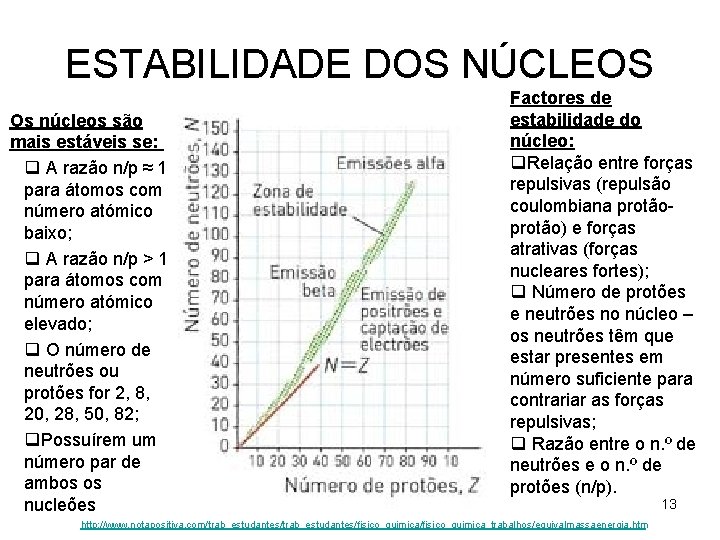
ESTABILIDADE DOS NÚCLEOS Os núcleos são mais estáveis se: q A razão n/p ≈ 1 para átomos com número atómico baixo; q A razão n/p > 1 para átomos com número atómico elevado; q O número de neutrões ou protões for 2, 8, 20, 28, 50, 82; q. Possuírem um número par de ambos os nucleões Factores de estabilidade do núcleo: q. Relação entre forças repulsivas (repulsão coulombiana protão) e forças atrativas (forças nucleares fortes); q Número de protões e neutrões no núcleo – os neutrões têm que estar presentes em número suficiente para contrariar as forças repulsivas; q Razão entre o n. º de neutrões e o n. º de protões (n/p). http: //www. notapositiva. com/trab_estudantes/fisico_quimica_trabalhos/equivalmassaenergia. htm 13
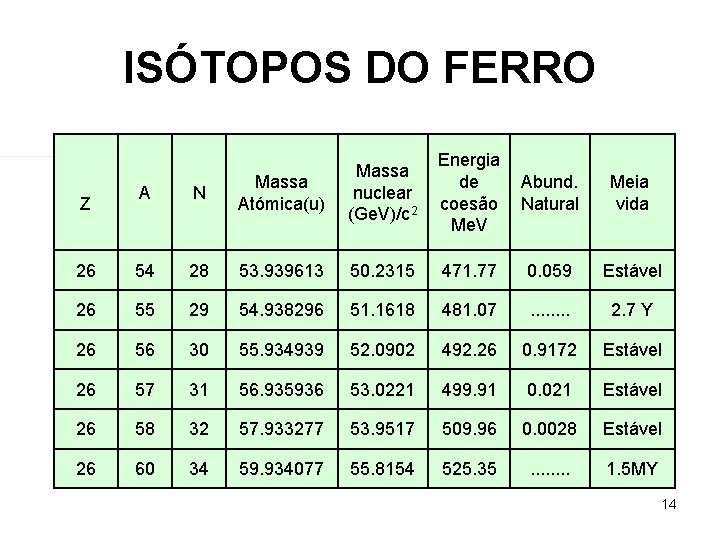
ISÓTOPOS DO FERRO Energia de coesão Me. V Abund. Natural Meia vida A N Massa Atómica(u) Massa nuclear (Ge. V)/c 2 26 54 28 53. 939613 50. 2315 471. 77 0. 059 Estável 26 55 29 54. 938296 51. 1618 481. 07 . . . . 2. 7 Y 26 56 30 55. 934939 52. 0902 492. 26 0. 9172 Estável 26 57 31 56. 935936 53. 0221 499. 91 0. 021 Estável 26 58 32 57. 933277 53. 9517 509. 96 0. 0028 Estável 26 60 34 59. 934077 55. 8154 525. 35 . . . . 1. 5 MY Z 14
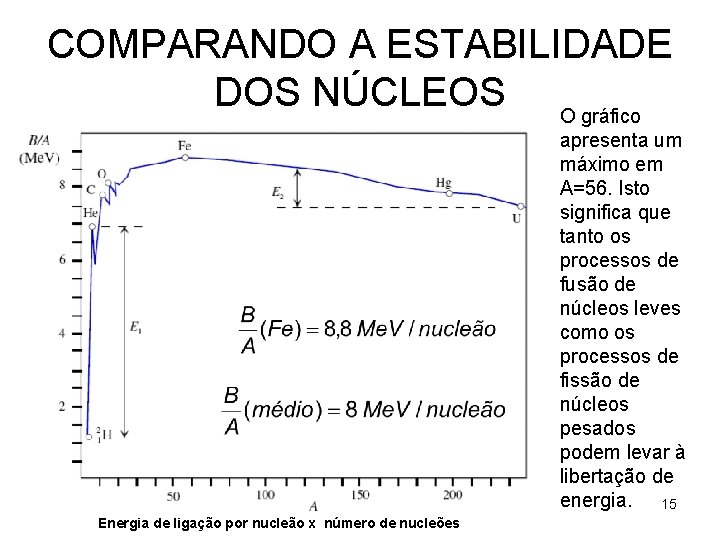
COMPARANDO A ESTABILIDADE DOS NÚCLEOS O gráfico apresenta um máximo em A=56. Isto significa que tanto os processos de fusão de núcleos leves como os processos de fissão de núcleos pesados podem levar à libertação de energia. 15 Energia de ligação por nucleão x número de nucleões

PROCESSOS DE ESTABILIZAÇÃO DOS NÚCLEOS A estabilização dos núcleos faz-se à custa de emissões de radiação ou partículas que caracterizam uma dada espécie ou elemento radioactivo. Estas emissões dependem das características de cada nuclídeo número de nucleões e as interacções a que estão sujeitos. RADIOACTIVIDADE – Os núcleos emitem partículas ou radiação, dando origem a outros núcleos Naturais (todos os elementos c/ Z>83) SUBST NCIAS RADIOACTIVAS Artificiais Conservação de carga NUM DECAIMENTO RADIOACTIVO HÁ Conservação do n. º de nucleões 16

EMISSÕES RADIOACTIVAS (a) Partículas α (b) Partículas β (β- + antineutrino) EMISSÕES NUCLEARES: (c) Partículas β (β+ + neutrino) (d) Radiação γ (e) Captura electrónica OUTRAS EMISSÕES NUCLEARES: • Emissão de protões • Emissão de neutrões • Emissão de deuterões 17

EMISSÕES RADIOACTIVAS (a) Decaimento α – emissão de partículas α (núcleos de 4 2 He) O decaimento α ocorre essencialmente devido ao efeito repulsivo de Coulomb, pelo que é mais provável ocorrer em núcleos pesados. A partícula α é uma partícula muito leve comparada com os núcleos radioactivos pesados. Por isso é emitida com velocidades elevadas, e isto faz com que seja uma forma de radiação importante. O núcleo descendente, , tem energia de ligação superior, pelo que o decaimento conduz a uma situação mais estável e libertação de energia. Este ganho de energia é dado pela diferença de massas relativistas nos dois membros da reacção, Exemplo: 18

EMISSÕES RADIOACTIVAS (b) Decaimento - emissão de electrão + anti neutrino Este tipo de decaimento resulta da transformação de um neutrão num protão, de modo que o núcleo descendente pertence já a um elemento diferente Exemplo: 19

EMISSÕES RADIOACTIVAS (c) Decaimento - emissão de positrão + neutrino Este tipo de decaimento ou declínio, resulta da transformação de um protão num neutrão, de modo que o núcleo descendente pertence já a uma espécie diferente Exemplo: 20

EMISSÕES RADIOACTIVAS (d) Decaimento - emissão de radiação Exemplo: 21

EMISSÕES RADIOACTIVAS (d) Captura electrónica - um electrão (K) é captado pelo núcleo Esta captura electrónica é acompanhada pela emissão de RX quando um electrão mais exterior ocupa a lacuna deixada pelo electrão capturado. Exemplo: 22

PROPRIEDADES DAS EMISSÕES RADIOACTIVAS A capacidade de ionização das diferentes emissões e seu poder de penetração na matéria estão de uma certa forma relacionados: § Partículas de massa e carga elevadas têm o poder de ionização elevada na matéria com a qual interagem e baixo poder de penetração. § Partículas de massa e carga pequena produzem fraca ionização da matéria e têm maior poder de penetração. § Radiação electromagnética, sem carga e massa associadas, produzem ionização pequena da matéria e elevado poder de penetração. O efeito biológico da emissão radioactiva está relacionado com a natureza da própria emissão e também com a natureza do tecido vivo que a absorve. 23

PROPRIEDADES DAS EMISSÕES RADIOACTIVAS Emissões α • Grande poder ionizante (podem provocar danos) • Pequeno poder de penetração (≈5 cm no ar) • Ligeiramente deflectidas por um campo magnético Emissões β • Baixo poder ionizante • Grande poder de penetração (alguns metros no ar; ≈2 cm no tecido humano) • Fortemente deflectidas pelo campo magnético Emissões γ • Baixo poder ionizante, • Elevado poder de penetração • Não são deflectidas no campo magnético (s/ carga) 24

LEI DO DECAIMENTO RADIOACTIVO Decaimento Radioactivo Actividade de uma amostra (R) • É um processo estatístico • Apenas existe uma probabilidade de ocorrência do processo • Mede a rapidez da desintegração • Taxa de decaimento • Indica o n. º de decaimentos/Δt n. º de núcleos alterados ≡ Actividade de 1 g de 1 Ci(Curie) = 37 GBq 25
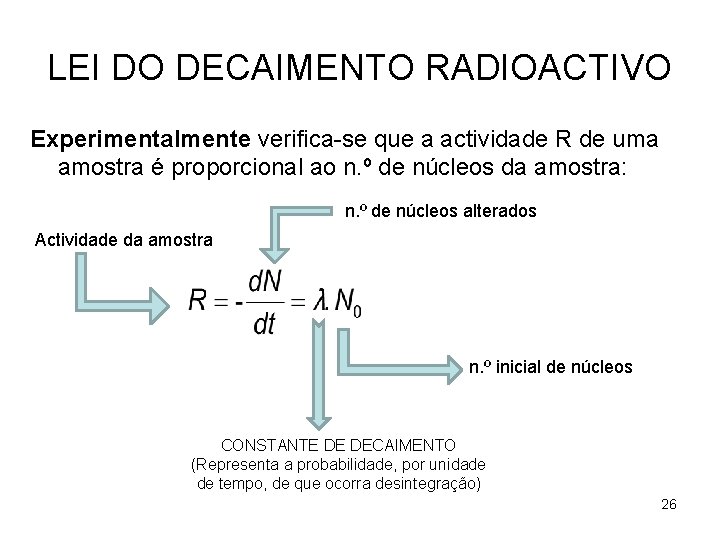
LEI DO DECAIMENTO RADIOACTIVO Experimentalmente verifica-se que a actividade R de uma amostra é proporcional ao n. º de núcleos da amostra: n. º de núcleos alterados Actividade da amostra n. º inicial de núcleos CONSTANTE DE DECAIMENTO (Representa a probabilidade, por unidade de tempo, de que ocorra desintegração) 26
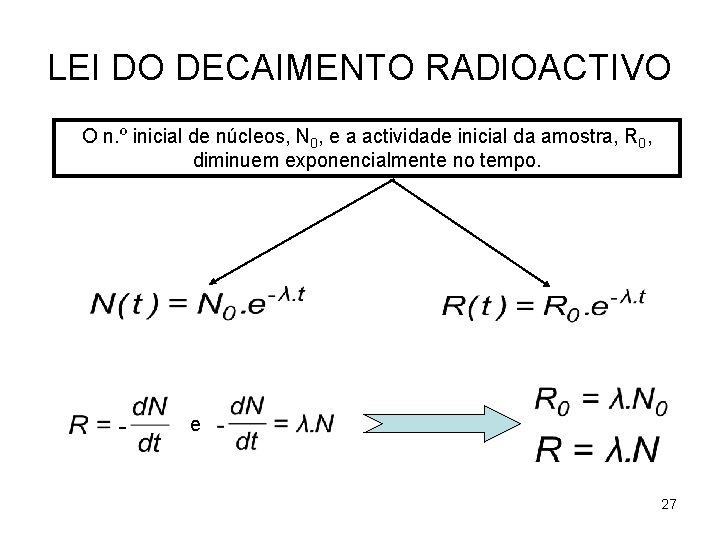
LEI DO DECAIMENTO RADIOACTIVO O n. º inicial de núcleos, N 0, e a actividade inicial da amostra, R 0, diminuem exponencialmente no tempo. e 27
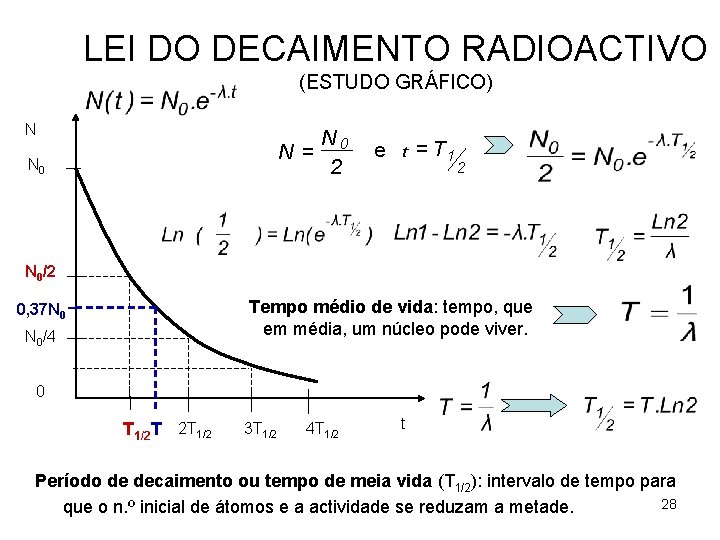
LEI DO DECAIMENTO RADIOACTIVO (ESTUDO GRÁFICO) N N = N 0 2 e t = T 1 2 N 0/2 Tempo médio de vida: tempo, que em média, um núcleo pode viver. 0, 37 N 0 N 0/4 0 T 1/2 T 2 T 1/2 3 T 1/2 4 T 1/2 t Período de decaimento ou tempo de meia vida (T 1/2): intervalo de tempo para 28 que o n. º inicial de átomos e a actividade se reduzam a metade.
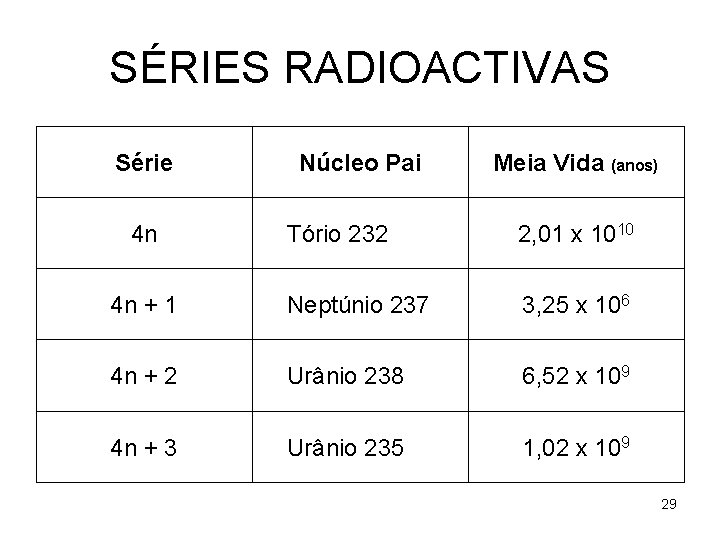
SÉRIES RADIOACTIVAS Série 4 n Núcleo Pai Meia Vida (anos) Tório 232 2, 01 x 1010 4 n + 1 Neptúnio 237 3, 25 x 106 4 n + 2 Urânio 238 6, 52 x 109 4 n + 3 Urânio 235 1, 02 x 109 29
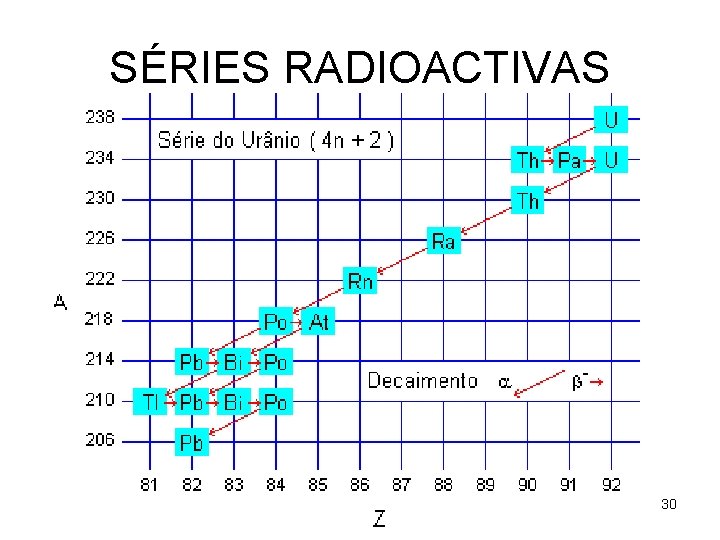
SÉRIES RADIOACTIVAS 30
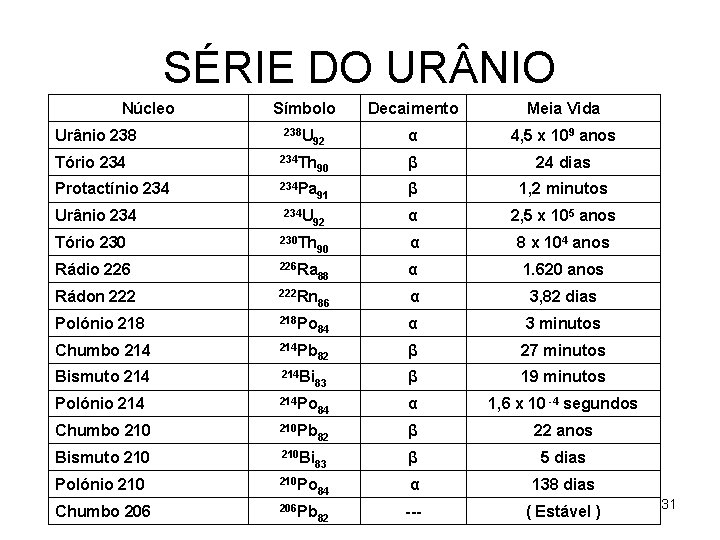
SÉRIE DO UR NIO Núcleo Urânio 238 Símbolo 238 U 92 Decaimento Meia Vida α 4, 5 x 109 anos Tório 234 Th 90 β 24 dias Protactínio 234 Pa 91 β 1, 2 minutos α 2, 5 x 105 anos α 8 x 104 anos α 1. 620 anos 86 α 3, 82 dias Urânio 234 U 92 Tório 230 Th Rádio 226 Ra Rádon 222 Rn Polónio 218 Po 84 α 3 minutos Chumbo 214 Pb 82 β 27 minutos Bismuto 214 Bi 83 β 19 minutos Polónio 214 Po 84 α 1, 6 x 10 -4 segundos Chumbo 210 Pb 82 β 22 anos Bismuto 210 Bi 83 β 5 dias Polónio 210 Po 84 α 138 dias Chumbo 206 Pb 82 --- ( Estável ) 90 88 31
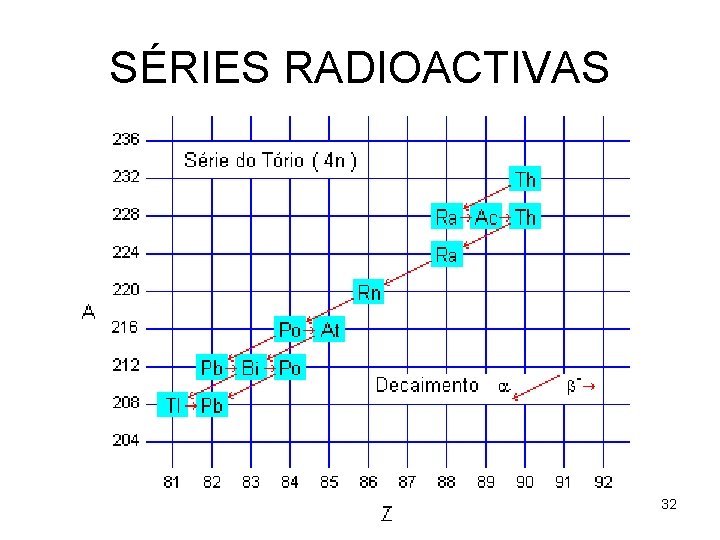
SÉRIES RADIOACTIVAS 32

EFEITOS BIOLÓGICOS DA RADIOACTIVIDADE É importante observar que radiações de diferentes naturezas ( raios-X, raios γ , partículas α e β), de mesmas intensidades, têm capacidades diferentes de lesar o mesmo tipo de matéria viva. 3 exemplos: • 1 g de água absorve aproximadamente 90 x 10− 7 J de energia de uma radiação. • 1 g de tecido não-ósseo absorve aproximadamente 97 x 10− 7 J de energia da mesma radiação. • 1 g de tecido ósseo absorve uma quantidade muito maior de energia da mesma radiação — aproximadamente o dobro de energia absorvida por tecidos não-ósseos. 33

EFEITOS BIOLÓGICOS DA RADIOACTIVIDADE EXPOSIÇÃO: A Exposição é uma medida da quantidade de radiação, definida como a carga liberada por unidade de massa de ar. Unidade SI: C/kg (Coulomb/quilograma). A unidade antiga é o Röntgen (R), 1 R= 2, 5 x 10− 4 C/kg. INTENSIDADE: A da radiação (I) mede a quantidade de energia transferida por unidade de área exposta, na unidade de tempo. A intensidade I é proporcional à actividade da fonte radioactiva, multiplicada pela energia da radiação incidente por unidade de área, na unidade de tempo. Unidade SI de intensidade é J. m− 2. s− 1. 34

EFEITOS BIOLÓGICOS DA RADIOACTIVIDADE Energia transferida DOSE ABSORVIDA: Dose = intensidade da radiação x tempo de exposição Unidade SI de dose absorvida: Gray (Gy). 1 Gy equivale à quantidade de radiação que provoca a absorção de 1 J por kg de matéria exposta à radiação. 1 Gy = 1 J/kg = 100 rad Massa do corpo FACTOR DE QUALIDADE: Q O factor de qualidade (Q) é uma constante que depende do tipo de radiação absorvida. http: //www. educacao. te. pt/jovem/index. jsp? p=117&id. Artigo=293 Radiação Q β 1 RX, Rγ 1 α 20 Protões 5 Neutrões 3 a 20 35

EFEITOS BIOLÓGICOS DA RADIOACTIVIDADE DOSE EQUIVALENTE: Dose equivalente absorvida mede os danos que uma determinada radiação pode provocar. H = Q. D Unidade SI de dose equivalente: Sivert (Sv). 1 Sv equivale à quantidade de radiação que provoca a absorção da energia de 1 J por kg de matéria exposta à radiação. DOSE LETAL: >10 Sv O limite máximo de radiação recomendado para pessoas que estão expostas à actividade de isótopos radioactivos é 0, 05 Sv http: //www. biossegurancahospitalar. com. br/rx/Curso_de_Biosseguranca_cap_4_Grandezas_e_Unidades. pdf 36
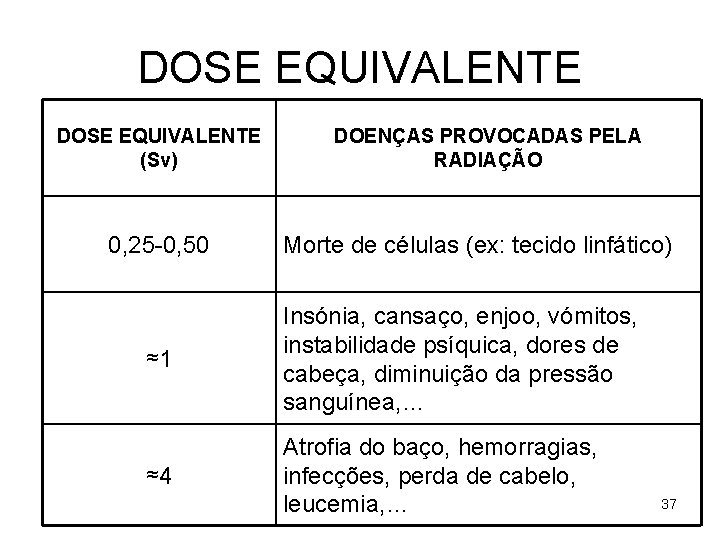
DOSE EQUIVALENTE (Sv) 0, 25 -0, 50 DOENÇAS PROVOCADAS PELA RADIAÇÃO Morte de células (ex: tecido linfático) ≈1 Insónia, cansaço, enjoo, vómitos, instabilidade psíquica, dores de cabeça, diminuição da pressão sanguínea, … ≈4 Atrofia do baço, hemorragias, infecções, perda de cabelo, leucemia, … 37
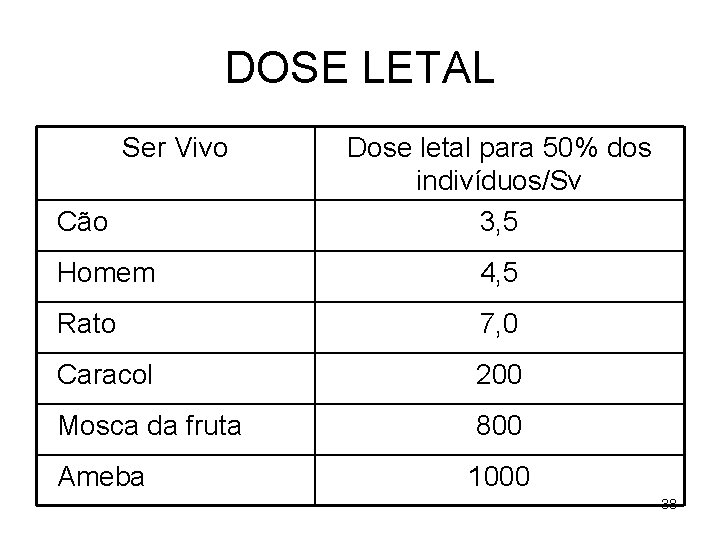
DOSE LETAL Ser Vivo Cão Dose letal para 50% dos indivíduos/Sv 3, 5 Homem 4, 5 Rato 7, 0 Caracol 200 Mosca da fruta 800 Ameba 1000 38

RADIAÇÃO IONIZANTE A emissão de ondas electromagnéticas ou de partículas de um núcleo instável, com energia suficiente para ionizar átomos ou moléculas. Feixes de partículas de elevada energia: • neutrões, protões, partículas alfa, partículas beta (electrões positrões). São as radiações de alta frequência: • ultravioleta (excluindo a faixa inicial), raios X, raios Gama (emitidos por materiais radioactivos) e os raios cósmicos. Ionizar significa tornar electricamente carregado. Quando a ionização acontece dentro de uma célula viva a sua estrutura química pode ser modificada. A exposição à radiação ionizante pode danificar as células e afectar o material 39 genético (DNA), causando doenças graves, levando até à morte.

RADIAÇÃO IONIZANTE APLICAÇÕES MEDICINA Meios de diagnóstico: Radiografia; ressonância magnética nuclear; PET-tomografia por emissão de positrões; … Tratamento: Radiofármacos; cardiologia nuclear; … ALIMENTAÇÃO Conservação de alimentos AGRICULTURA Controlo de pragas; … AMBIENTE Investigação relativa a poluição; … ARQUEOLOGIA Datação; … INVEST. CRIMINAL Análise por activação de neutrões; … Um corpo pode ser irradiado sem ficar contaminado – só existe contaminação 40 quando a substância radioactiva permanece em contacto directo com o corpo.
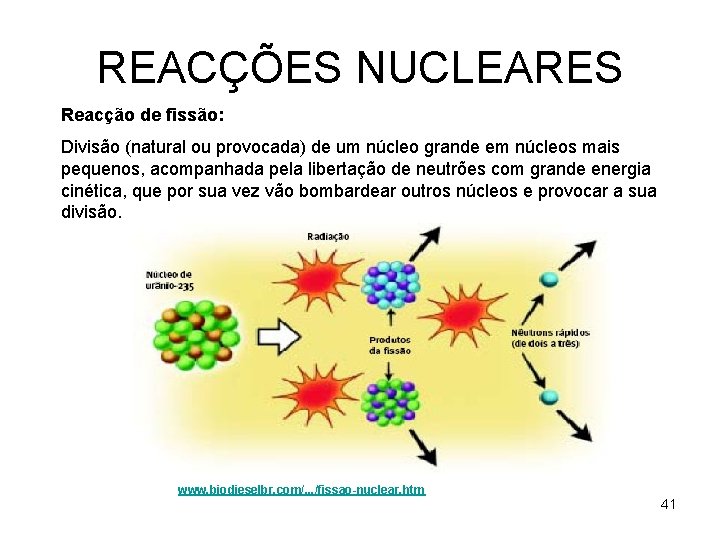
REACÇÕES NUCLEARES Reacção de fissão: Divisão (natural ou provocada) de um núcleo grande em núcleos mais pequenos, acompanhada pela libertação de neutrões com grande energia cinética, que por sua vez vão bombardear outros núcleos e provocar a sua divisão. www. biodieselbr. com/. . . /fissao-nuclear. htm 41
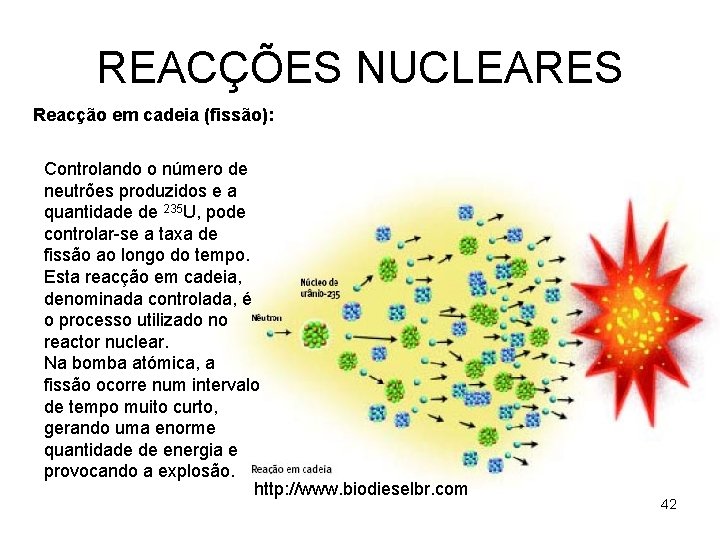
REACÇÕES NUCLEARES Reacção em cadeia (fissão): Controlando o número de neutrões produzidos e a quantidade de 235 U, pode controlar-se a taxa de fissão ao longo do tempo. Esta reacção em cadeia, denominada controlada, é o processo utilizado no reactor nuclear. Na bomba atómica, a fissão ocorre num intervalo de tempo muito curto, gerando uma enorme quantidade de energia e provocando a explosão. http: //www. biodieselbr. com 42
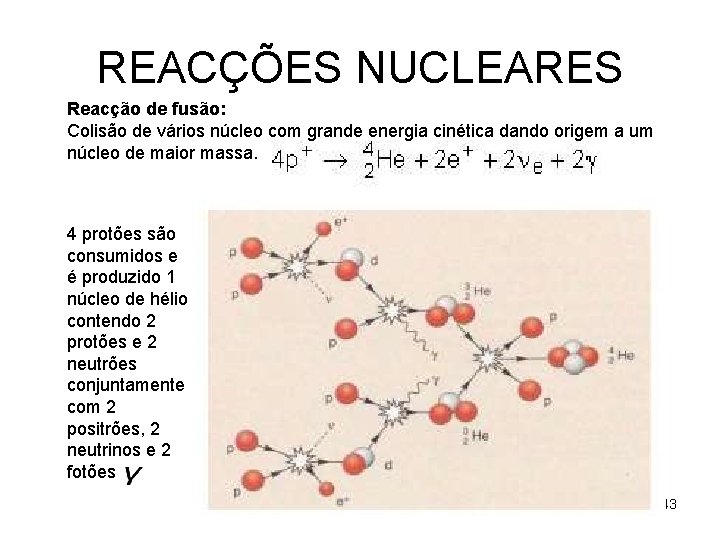
REACÇÕES NUCLEARES Reacção de fusão: Colisão de vários núcleo com grande energia cinética dando origem a um núcleo de maior massa. 4 protões são consumidos e é produzido 1 núcleo de hélio contendo 2 protões e 2 neutrões conjuntamente com 2 positrões, 2 neutrinos e 2 fotões 43
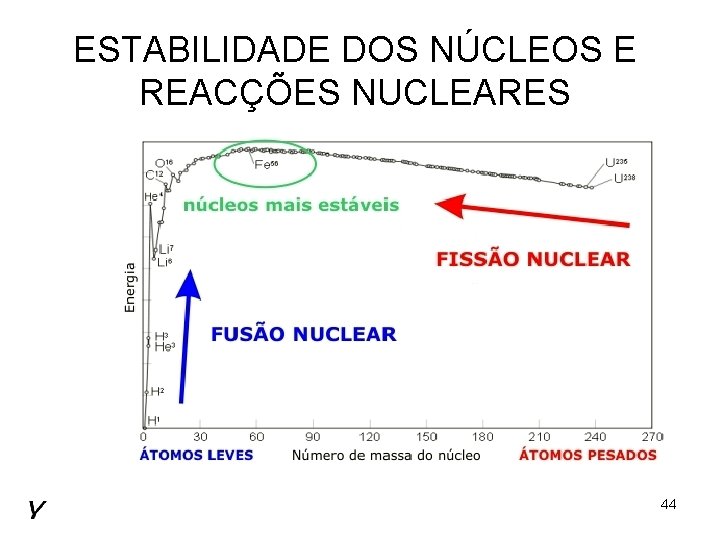
ESTABILIDADE DOS NÚCLEOS E REACÇÕES NUCLEARES 44
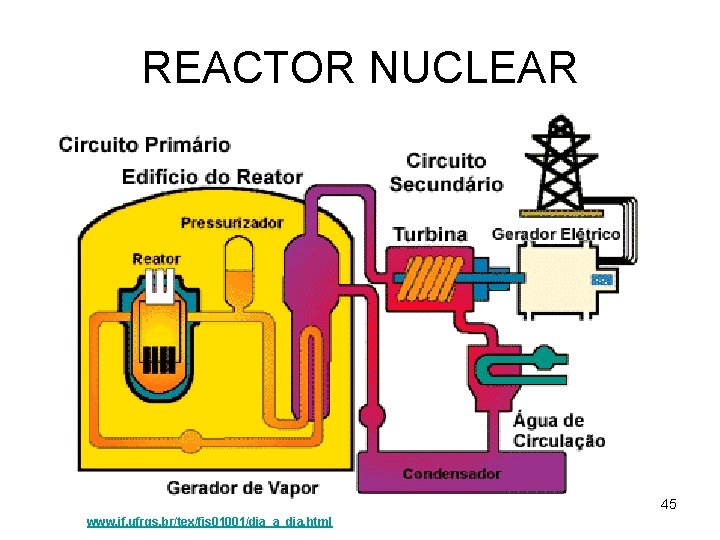
REACTOR NUCLEAR 45 www. if. ufrgs. br/tex/fis 01001/dia_a_dia. html
- Slides: 45