EQUILIBRIO QUMICO REACCIONES CIDO BASE cidos Caractersticas Tienen

EQUILIBRIO QUÍMICO REACCIONES ÁCIDO BASE Ácidos Características Tienen sabor agrio Se encuentran en muchas frutas y en productos de fermentaciones como el vinagre y el yogur Hacen que el papel tornasol cambie de azul a rojo Reaccionan con algunos metales (Mg, Zn, Fe) liberando hidrógeno (H 2) Reacciona con las bases formando sal y agua En solución acuosa dejan pasar la corriente eléctrica Ejemplos Limón, bebidas carbónicas, café negro, Aspirina, vinagre.

Bases o hidróxidos Características Sabor amargo Poseen tacto grasiento Las propiedades básicas desaparecen al reaccionar con las ácidos Reacciona con los ácidos formando sal y agua En solución acuosa dejan pasar la corriente eléctrica Ejemplos Amoniaco, jabón, detergente, limpiadores, sosa cáustica
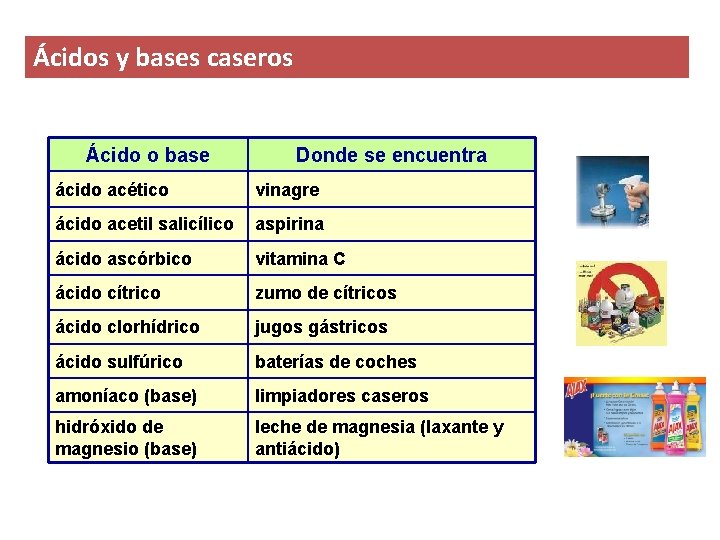
Ácidos y bases caseros Ácido o base Donde se encuentra ácido acético vinagre ácido acetil salicílico aspirina ácido ascórbico vitamina C ácido cítrico zumo de cítricos ácido clorhídrico jugos gástricos ácido sulfúrico baterías de coches amoníaco (base) limpiadores caseros hidróxido de magnesio (base) leche de magnesia (laxante y antiácido)

Arrhenius Ácidos Liberan iones hidrógeno (H+) en agua HA A- + H+ Bases - Liberan iones hidróxido (OH ) en agua BOH B- + OH- La teoría de Arrhenius para ácidos y bases se aplica a soluciones acuosas
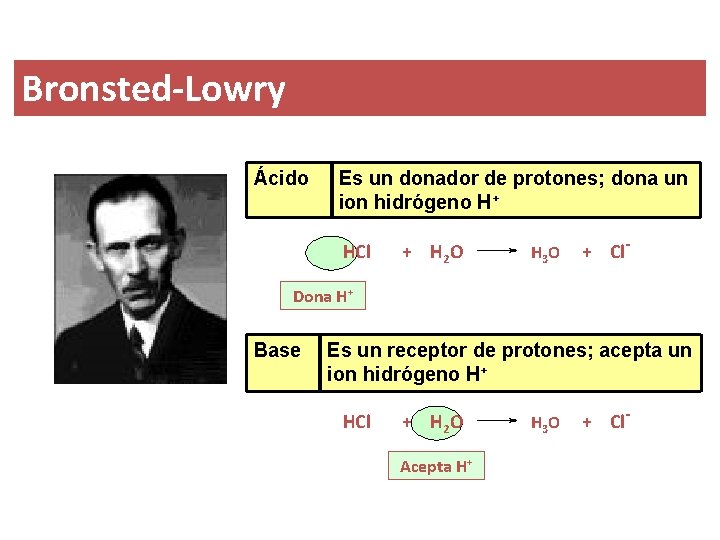
Bronsted-Lowry Ácido Es un donador de protones; dona un ion hidrógeno H+ HCl + H 2 O H 3 O + Cl- Dona H+ Base Es un receptor de protones; acepta un ion hidrógeno H+ HCl + H 2 O H 3 O + Cl- Acepta H+
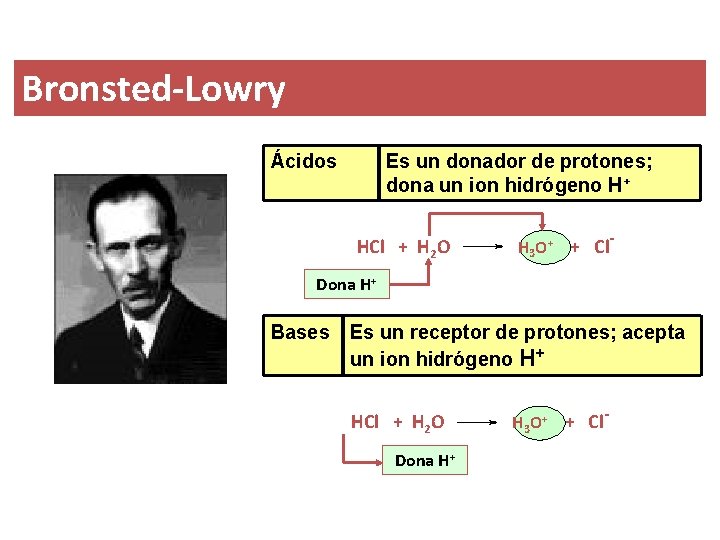
Bronsted-Lowry Ácidos Es un donador de protones; dona un ion hidrógeno H+ HCl + H 2 O H 3 O+ + Cl- Dona H+ Bases Es un receptor de protones; acepta un ion hidrógeno H+ HCl + H 2 O H 3 O+ + Cl- Dona H+

Teorías Ácido-Base Ácidos de Lewis BrÖnsted y Lowry Ácido de Arrhenius

Reacciones de neutralización Arrhenius Ácido + Base Sal + Agua
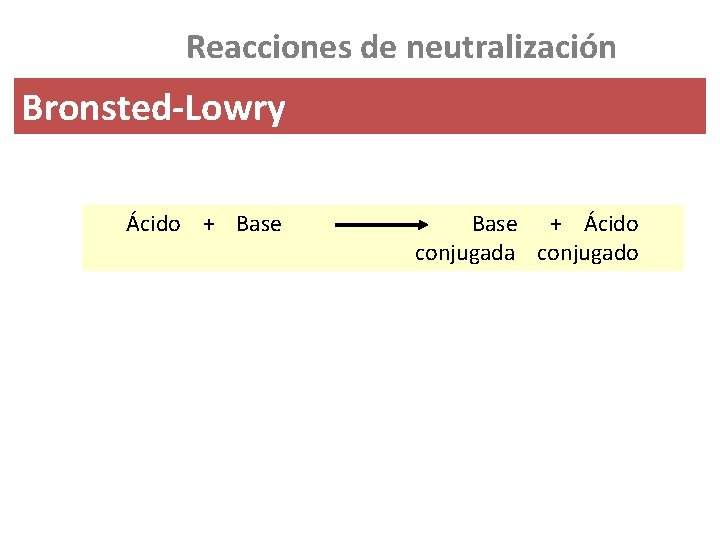
Reacciones de neutralización Bronsted-Lowry Ácido + Base + Ácido conjugada conjugado
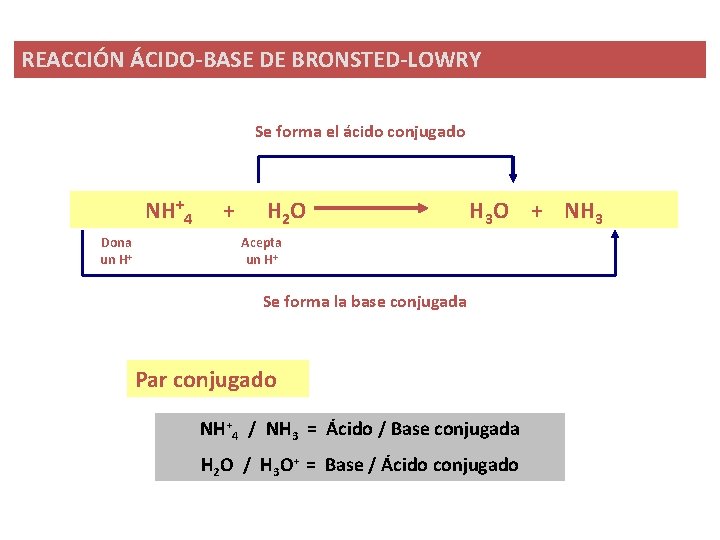
REACCIÓN ÁCIDO-BASE DE BRONSTED-LOWRY Se forma el ácido conjugado NH+4 + H 2 O H 3 O + NH 3 Dona un H+ Acepta un H+ Se forma la base conjugada Par conjugado NH+4 / NH 3 = Ácido / Base conjugada H 2 O / H 3 O+ = Base / Ácido conjugado
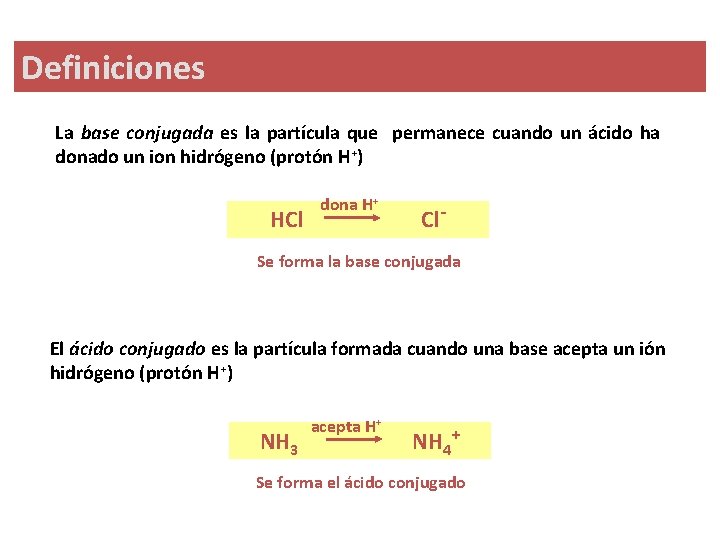
Definiciones La base conjugada es la partícula que permanece cuando un ácido ha donado un ion hidrógeno (protón H+) dona H+ HCl Cl. Se forma la base conjugada El ácido conjugado es la partícula formada cuando una base acepta un ión hidrógeno (protón H+) acepta H+ NH 3 NH 4+ Se forma el ácido conjugado
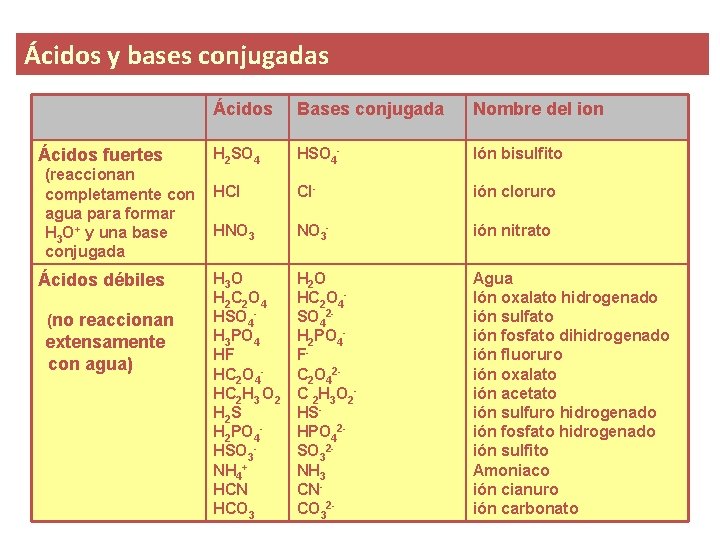
Ácidos y bases conjugadas Ácidos Bases conjugada Nombre del ion Ácidos fuertes H 2 SO 4 HSO 4 - Ión bisulfito Cl- ión cloruro NO 3 - ión nitrato H 2 O HC 2 O 4 SO 42 H 2 PO 4 F- C 2 O 42 C 2 H 3 O 2 HS- HPO 42 SO 32 - NH 3 CNCO 32 - Agua Ión oxalato hidrogenado ión sulfato ión fosfato dihidrogenado ión fluoruro ión oxalato ión acetato ión sulfuro hidrogenado ión fosfato hidrogenado ión sulfito Amoniaco ión cianuro ión carbonato (reaccionan completamente con HCl agua para formar HNO 3 H 3 O+ y una base conjugada Ácidos débiles (no reaccionan extensamente con agua) H 3 O H 2 C 2 O 4 HSO 4 H 3 PO 4 HF HC 2 O 4 HC 2 H 3 O 2 H 2 S H 2 PO 4 HSO 3 - NH 4+ HCN HCO 3

Fortaleza de los ácidos ÁCIDOS FUERTES ÁCIDOS DÉBILES Son los ácidos minerales: HCl, HBr, HI. Son los ácidos minerales: HF, H 2 S, HCN. Los ácidos que tienen una diferencia entre oxígeno e hidrógeno de 2 o más: Los ácidos que tienen una diferencia entre oxígeno e hidrógeno de 1 o menos: H 2 CO 3, H 3 PO 4, HNO 2, H 2 SO 4, HCLO 4, HNO 3,
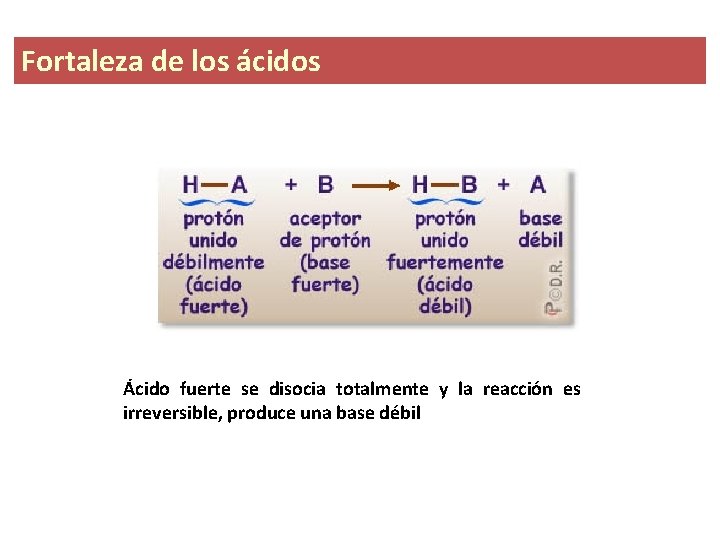
Fortaleza de los ácidos Ácido fuerte se disocia totalmente y la reacción es irreversible, produce una base débil
Fortaleza de las bases BASES FUERTES Son las bases de la familia IA y algunas de la familia II excepto la de berilio: Na. OH, KOH, Li. OH, Ca(OH)2 BASES DÉBILES Be(OH)2, NH 3

Acidos Monopróticos Son los ácidos que tienen un solo protón en la fórmula. Ejemplos HCl, HBr, HI, HCl. O, HMn. O 4

Acidos Polipróticos Son los ácidos que tienen un dos o más protones en la fórmula. Ejemplos H 2 SO 4, H 2 CO 3, H 3 PO 4

Disociación y Ionización Disociación Es la separación de los iones existentes en una sustancia iónica, cuando se encuentran en solución acuosa o en un estado líquido. Ionización Es el proceso mediante el cual una molécula se separa en una parte positiva y en una negativa, por separación asimétrica de los pares de electrones.
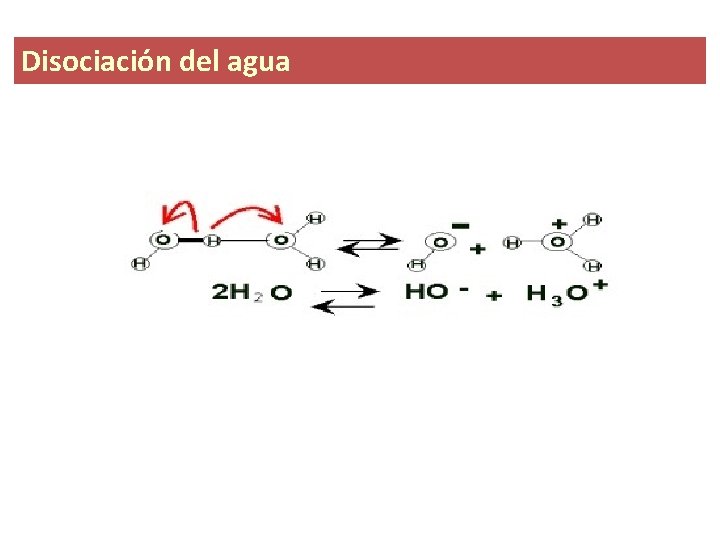
Disociación del agua
- Slides: 19