EQUILIBRIO QUMICO Objetivos Definicin de equilibrio qumico constante

EQUILIBRIO QUÍMICO Objetivos: • Definición de equilibrio químico, constante de equilibrio. • Identifican toda reacción química como un proceso que tiende a una situación de equilibrio.

¿Qué es el equilibrio químico? n n Estado del sistema: No se observan cambios a medida que transcurre el tiempo. Proceso dinámico. a A + b B c C + d D Las velocidades directas e inversas se igualan y las concentraciones netas de reactivos y productos se mantienen constantes
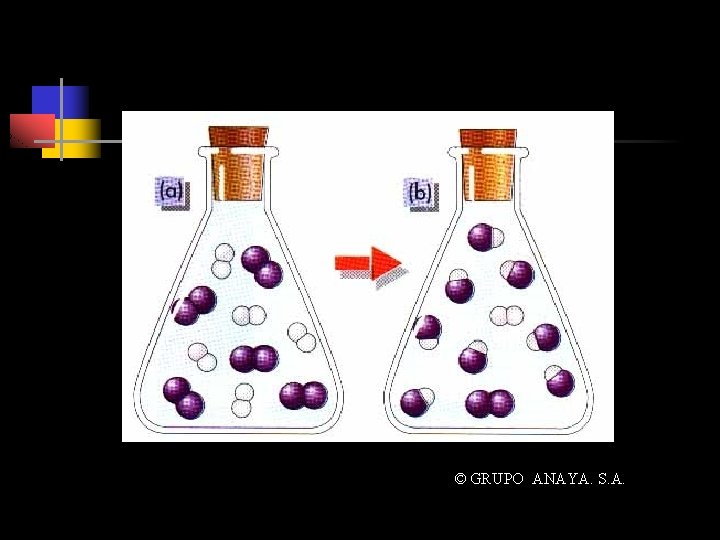
© GRUPO ANAYA. S. A.

Expresión para la constante de equilibrio, Kc Kc representa: La tendencia de una reacción hacia los productos o los reactantes. Es equivalente a las concentraciones de productos y reactantes. En la reacción: a A + b B c C + d D Kc se expresa así:

Ley de acción de masas
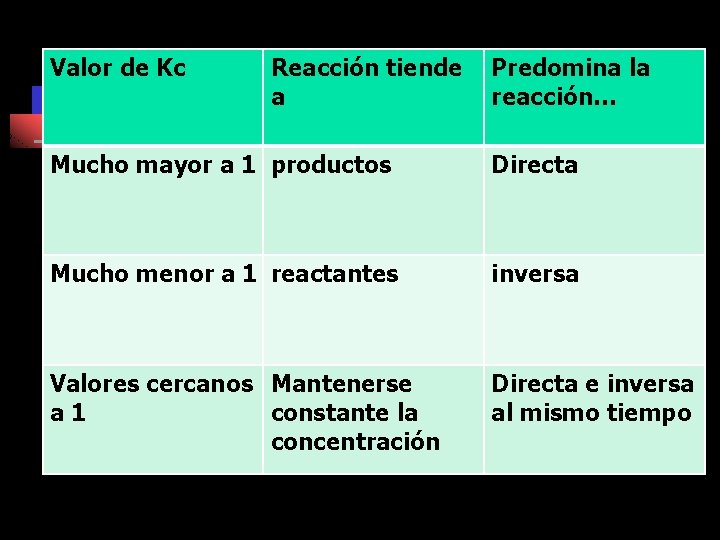
Valor de Kc Reacción tiende a Predomina la reacción… Mucho mayor a 1 productos Directa Mucho menor a 1 reactantes inversa Valores cercanos Mantenerse a 1 constante la concentración Directa e inversa al mismo tiempo
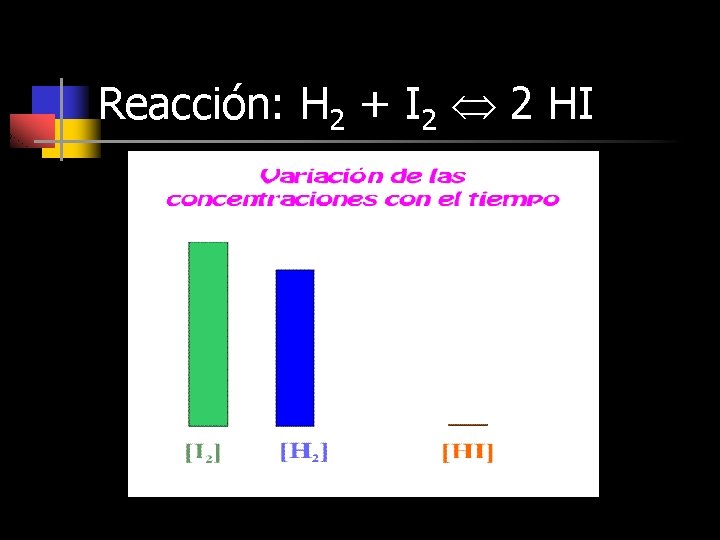
Reacción: H 2 + I 2 2 HI

Cuociente de reacción n n Q = Relación entre los reactivos y los productos al inicio de la reacción Q = Kc sistema en equilibrio Q > Kc predomina la reacción inversa hasta alcanzar el equilibrio Q < Kc predomina la reacción directa hasta alcanzar el equilibrio

Kp n En gases es mas sencillo medir presiones parciales que concentraciones: a. A+b. B c. C+d. D y se observa la constancia de Kp viene definida por:
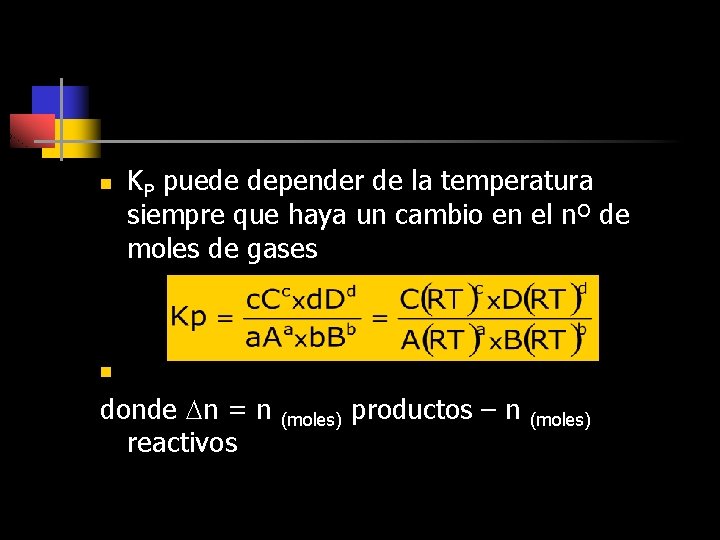
n KP puede depender de la temperatura siempre que haya un cambio en el nº de moles de gases n donde n = n reactivos (moles) productos – n (moles)

Principio de Le Chatelier n “Un cambio o perturbación en cualquiera de las variables que determinan el estado de equilibrio químico produce un desplazamiento del equilibrio en el sentido de contrarrestar o minimizar el efecto causado por la perturbación”.

Cambio en la concentración de alguno de los reactivos o productos. n n Si a un equilibrio se varía la concentración (reactivo o producto) el equilibrio desaparece y se tiende hacia un nuevo equilibrio. Las concentraciones iniciales de este nuevo equilibrio son las del equilibrio anterior con las variaciones que se hayan introducido.

n La constante del nuevo equilibrio es la misma, por lo que: n n n si aumenta [ reactivos], Q y se vuelve a igualar a KC los [ reactivos] (en cantidades estequiométricas) [productos] . Significa que si aumenta la concentración de reactivos, el equilibrio se desplaza a los productos.

Cambio en la presión n El equilibrio se desplaza hacia donde hay menor cantidad de moles, generalizable para cualquier equilibrio en el que intervengan gases. si la presión disminuye, se desplaza hacia donde hay mayor cantidad de moles Si el número de moles total de reactivos es igual al de productos (a+b =c+d), entonces no afecta.

Cambio en la temperatura n n n Para reacciones endotérmicas: Se observa que, al aumentar T el sistema se desplaza hacia donde se consuma calor, es decir, hacia la derecha Si disminuye T el sistema se desplaza hacia donde se desprenda calor, izquierda.

n n n Para reacciones exotérmicas: Se observa que, al aumentar T el sistema se desplaza hacia donde se consuma calor, es decir hacia la izquierda en las reacciones exotérmicas Si disminuye T el sistema se desplaza hacia donde se desprenda calor, derecha.
- Slides: 16