EQUILIBRIO QUMICO ESTUDIO ESPECTROFOTOMTRICO esdelibro Equilibrio qumico 201000938

EQUILIBRIO QUÍMICO ESTUDIO ESPECTROFOTOMÉTRICO esdelibro; Equilibrio químico. 201000938 1

OBJETIVO Determinar el valor de la constante del equilibrio entre el Fe 3+ y SCN- para formar Fe. SCN 2+ , en disolución acuosa Fe 3+ + SCN- ↔Fe. SCN 2+ esdelibro; Equilibrio químico. 201000938 2

EQUILIBRIO QUÍMICO • ¿Qué es un equilibrio químico? Es el estado en el que las concentraciones de los reactivos y los productos de una reacción química permanecen constantes en el tiempo. esdelibro; Equilibrio químico. 201000938 3

CONSTANTE DE EQUILIBRIO Es el producto de las concentraciones de los productos, dividido entre el producto de las concentraciones de los reactivos, elevada cada una a un exponente igual a su coeficiente en la ecuación química ajustada. esdelibro; Equilibrio químico. 201000938 4

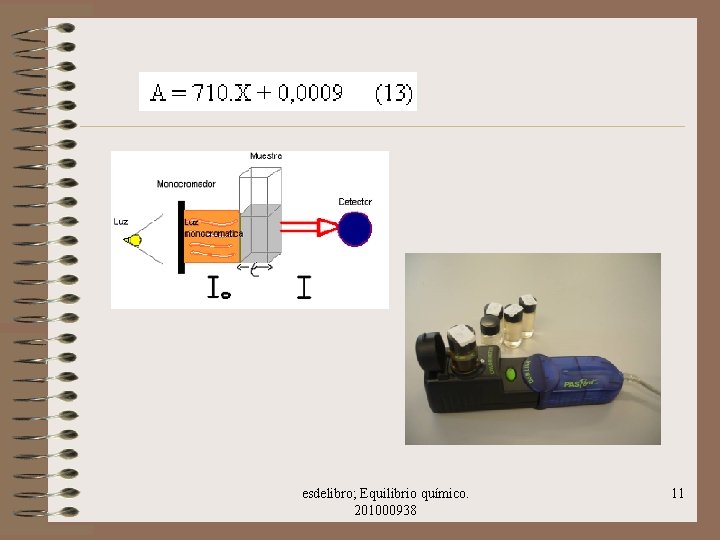
DETERMINACIÓN DE LA CONCENTRACIÓN DEL COMPLEJO EN EL EQUILIBRIO • La ley de Beer-Lambert relaciona la concentración de una sustancia en disolución, con la disminución en la intensidad de la luz que la atraviesa. La cantidad de luz de una determinada longitud de onda, absorbida por una muestra, depende de la concentración. A = absorbancia; E = absortividad (L/cm. mol) c = concentración de la especie absorbente en la disolución (mol/L) l = longitud de la celda (cm) esdelibro; Equilibrio químico. 201000938 5

MATERIALES • • • balanza electrónica buretas de 50 m. L (4) cuentagotas embudo (4) espátula guantes de látex matraz aforado de 100 m. L matraz aforado de 1000 m. L matraz aforado de 500 m. L (3) nueces (4) ordenador programa “Data Studio” PASCO© esdelibro; Equilibrio químico. 201000938 6

MATERIALES • sensor colorimétrico, PS-2121 PASCO© • soportes (4) • tapones de matraces • USB link PASCO© • varilla • vasos de precipitados de 250 m. L (6) • vidrio de reloj • KSCN (0, 29 g) • HNO 3 al 60% (52, 508 g) • H 2 O • Fe(NO 3)3 * 9 H 2 O (24, 24 g) esdelibro; Equilibrio químico. 201000938 7

PROCEDIMIENTO EXPERIMENTAL Pincha sobre el video esdelibro; Equilibrio químico. 201000938 8

PROCEDIMIENTO EXPERIMENTAL 1º. Obtención de la recta de calibrado (relación que permite determinar la concentración del Fe. SCN 2+ a partir de la absorbancia) esdelibro; Equilibrio químico. 201000938 9

PROCEDIMIENTO EXPERIMENTAL 2º. Cálculo de la constante de equilibrio, a partir de la absorbancia de las mezclas preparadas esdelibro; Equilibrio químico. 201000938 10
esdelibro; Equilibrio químico. 201000938 11
esdelibro; Equilibrio químico. 201000938 12

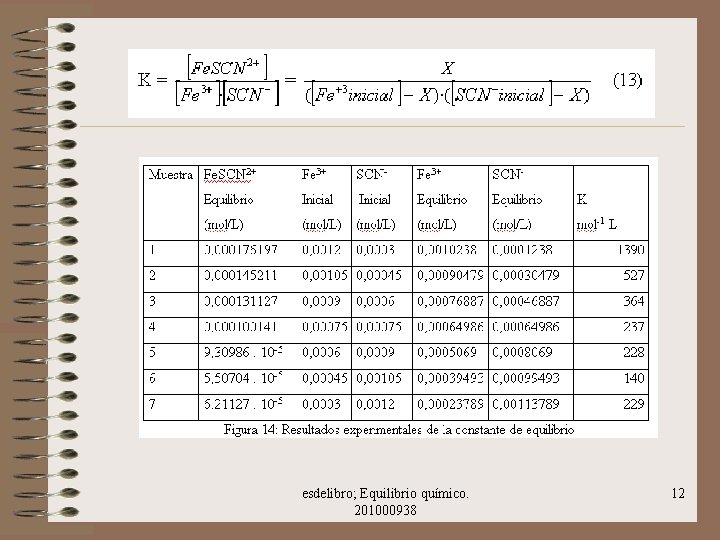
RESULTADOS - Los datos de la bibliografía muestran una gran variedad en el valor de la constante de este equilibrio. Nosotros tomamos como referencia el de Burriel Martí (1985) igual a 158 L/mol - Nuestro resultado experimental ha sido: K = 240 L/ mol a 19 ºC - Las posibles causas de la discrepancia son múltiples esdelibro; Equilibrio químico. 201000938 13

BIBLIOGRAFÍA - Baeza, J. El equilibrio químico. Departamento de Química Analítica, Universidad de Valencia. Disponible en http: //www. uv. es/baeza/equili. html Burriel Martí, F. , Lucena Conde, F. , Arribas Jimeno, S. , Hernández Méndez, J. (1985). Química Analítica Cualitativa. Madrid: Paraninfo. Págs. 348 -49. - Marín García, M. L. (2004) Bases químicas del medio ambiente: manual de laboratorio. Página 41. Disponible en Internet - http: //books. google. es/books? id=Mp- HKee. Rzb. AC&lpg=PA 43&ots=d. Zky. Czk. DTl&dq=constante%20 de%20 equilibrio%20 hierro%20 sulfocianuro&p g=PA 46#v=onepage&q=constante%20 de%20 equilibrio%20 hierro%20 sulfocianuro&f=false Masjuan, M. D. , Pelegrín, J. (2009). Química 2 Bachillerato. Barcelona: Casals. Tema 6: Páginas. 147 -184. esdelibro; Equilibrio químico. 201000938 14

BIBLIOGRAFÍA - Oro, L. A. , Andreu, J. L. , Fernández, M. C. , Pérez-Torrente, J. (1997). Química. Madrid: Santillana. Páginas: 65, 67 y 69. - Petrucci, R. H. , Harwood, W. S. , Herring, F. G. (2003). Química General. Madrid: Prentice Hall. Páginas: 627 -629. - Práctica 2. Determinación espectrofotométrica de Mn. O 4 -. Laboratorio integrado E. P. S. de Algeciras. Universidad de Cádiz Disponible en Internet. http: //www. uca. es/grup-invest/corrosion/integrado/P 2. pdf - Práctica nº 7, Equilibrio químico. 1 er cuatrimestre de 2004. Química General e Inorgánica I. Universidad de Buenos Aires. Disponible en: www. q 1. fcen. uba. ar/materias/qi 1/doc/GTP 07 mod. pdf - PASCO® (2009/2010). Physics & Engineering Education. California (USA). Página 46. esdelibro; Equilibrio químico. 201000938 15

ESPERANDO QUE OS HAYA GUSTADO SALUDOS DEL EQUIPO “LOS ALQUIMISTAS” esdelibro; Equilibrio químico. 201000938 16
- Slides: 16































