EQUILIBRIO QUMICO Cuando ocurre una reaccin qumica termina

EQUILIBRIO QUÍMICO Cuando ocurre una reacción química, ¿termina agotándose siempre, al menos, uno de los reactivos? Dpto. Física y Química IES Turaniana

ÍNDICE 1. DEFINICIÓN EQUILIBRIO QUÍMICO 2. EQUILIBRIO HOMOGÉNEO 2. 1. CONSTANTE DE EQUILIBRIO Kc 2. 2 GRADO DE DISOCIACIÓN 2. 3. COCIENTE DE REACCIÓN 2. 4. CONSTANTE DE EQUILIBRIO Kp 3. FACTORES QUE AFECTAN AL EQUILIBRIO 3. 1. CONCENTRACIÓN 3. 2. PRESIÓN 3. 3. TEMPERATURA 4. EQUILIBRIOS HETEROGÉNEOS 4. 1. EFECTO DEL ION COMÚN 4. 2. EFECTO DEL p. H Dpto. Física y Química IES Turaniana
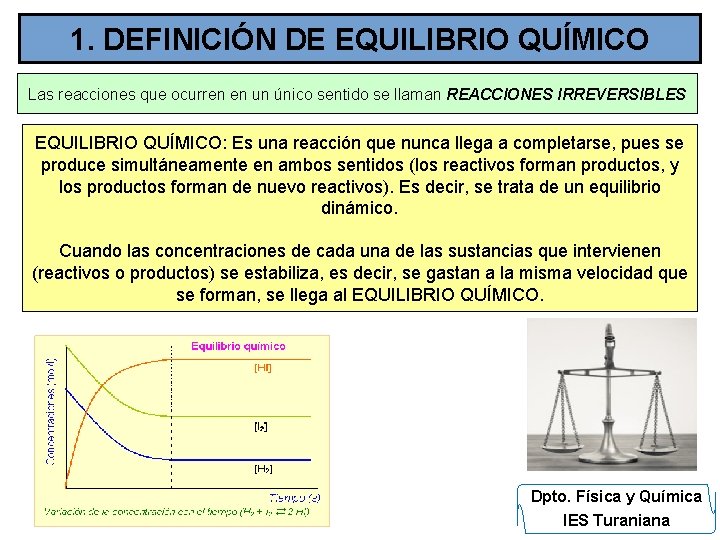
1. DEFINICIÓN DE EQUILIBRIO QUÍMICO Las reacciones que ocurren en un único sentido se llaman REACCIONES IRREVERSIBLES EQUILIBRIO QUÍMICO: Es una reacción que nunca llega a completarse, pues se produce simultáneamente en ambos sentidos (los reactivos forman productos, y los productos forman de nuevo reactivos). Es decir, se trata de un equilibrio dinámico. Cuando las concentraciones de cada una de las sustancias que intervienen (reactivos o productos) se estabiliza, es decir, se gastan a la misma velocidad que se forman, se llega al EQUILIBRIO QUÍMICO. Dpto. Física y Química IES Turaniana
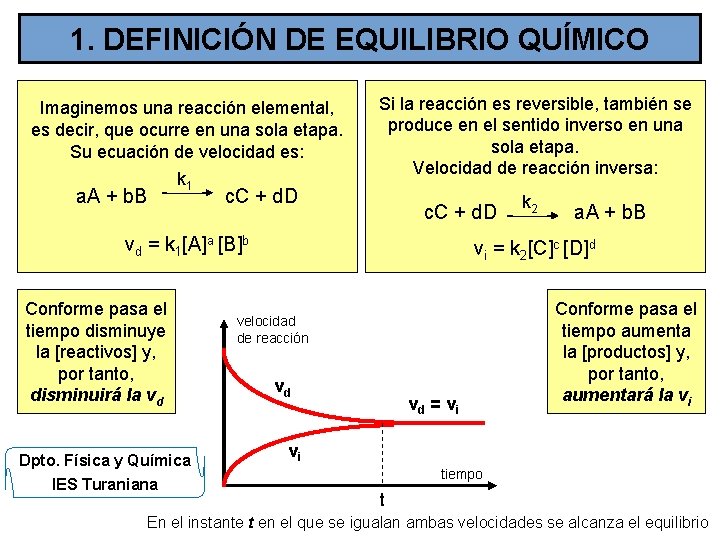
1. DEFINICIÓN DE EQUILIBRIO QUÍMICO Imaginemos una reacción elemental, es decir, que ocurre en una sola etapa. Su ecuación de velocidad es: a. A + b. B k 1 Si la reacción es reversible, también se produce en el sentido inverso en una sola etapa. Velocidad de reacción inversa: c. C + d. D vd = k 1[A]a [B]b Conforme pasa el tiempo disminuye la [reactivos] y, por tanto, disminuirá la vd Dpto. Física y Química IES Turaniana k 2 a. A + b. B vi = k 2[C]c [D]d velocidad de reacción vd vd = v i Conforme pasa el tiempo aumenta la [productos] y, por tanto, aumentará la vi vi tiempo t En el instante t en el que se igualan ambas velocidades se alcanza el equilibrio
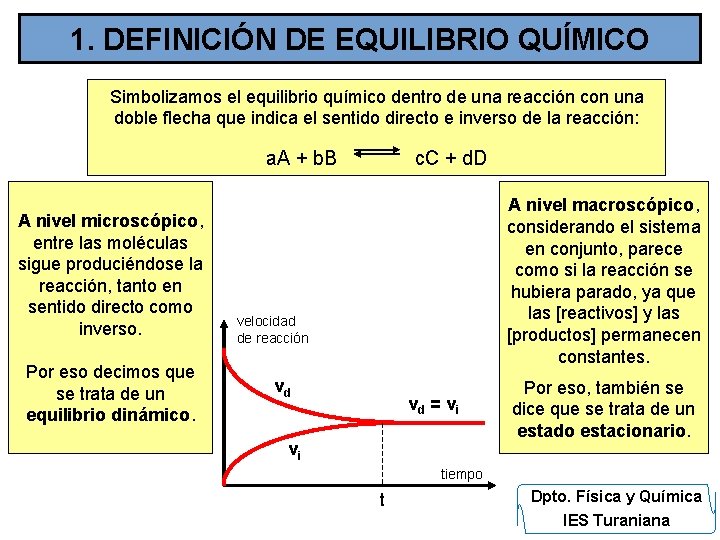
1. DEFINICIÓN DE EQUILIBRIO QUÍMICO Simbolizamos el equilibrio químico dentro de una reacción con una doble flecha que indica el sentido directo e inverso de la reacción: a. A + b. B A nivel microscópico, entre las moléculas sigue produciéndose la reacción, tanto en sentido directo como inverso. Por eso decimos que se trata de un equilibrio dinámico. c. C + d. D A nivel macroscópico, considerando el sistema en conjunto, parece como si la reacción se hubiera parado, ya que las [reactivos] y las [productos] permanecen constantes. velocidad de reacción vd vd = v i vi Por eso, también se dice que se trata de un estado estacionario. tiempo t Dpto. Física y Química IES Turaniana
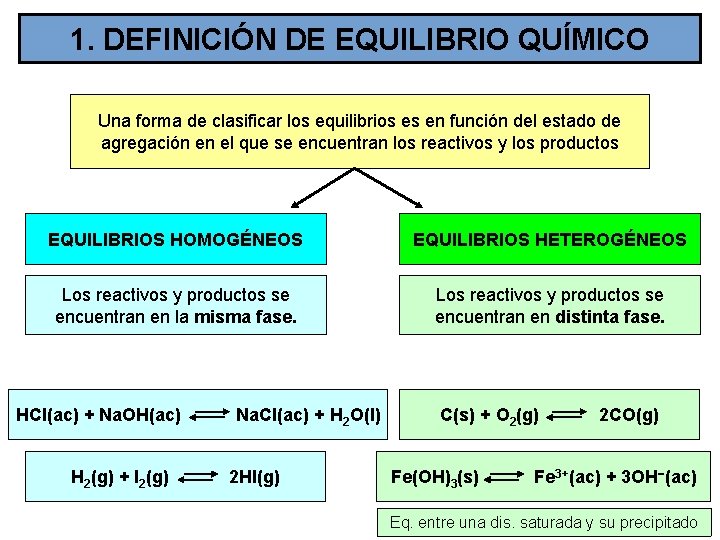
1. DEFINICIÓN DE EQUILIBRIO QUÍMICO Una forma de clasificar los equilibrios es en función del estado de agregación en el que se encuentran los reactivos y los productos EQUILIBRIOS HOMOGÉNEOS EQUILIBRIOS HETEROGÉNEOS Los reactivos y productos se encuentran en la misma fase. Los reactivos y productos se encuentran en distinta fase. HCl(ac) + Na. OH(ac) H 2(g) + I 2(g) Na. Cl(ac) + H 2 O(l) 2 HI(g) C(s) + O 2(g) Fe(OH)3(s) 2 CO(g) Fe 3+(ac) + 3 OH (ac) Eq. entre una dis. saturada y su precipitado
Responde: 1. ¿Qué significa que una reacción química está en equilibrio? 2. ¿Cuándo una reacción está en equilibrio [reactivos]=[productos]? 3. ¿Por qué se dice que el equilibrio es dinámico? Dpto. Física y Química IES Turaniana
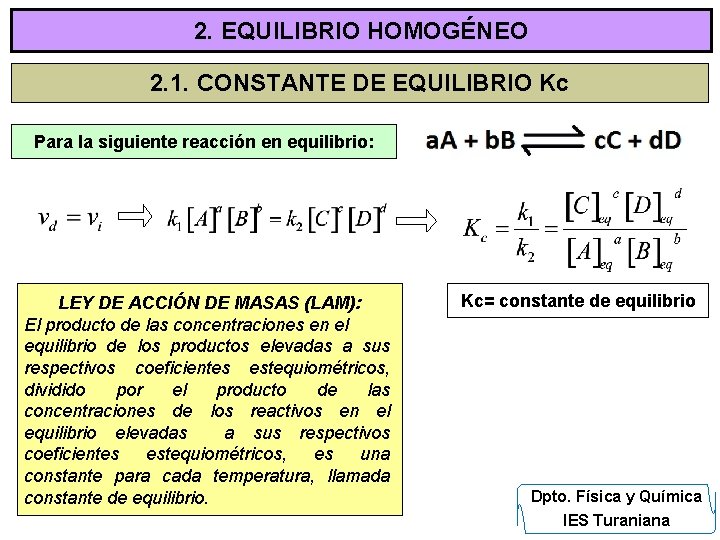
2. EQUILIBRIO HOMOGÉNEO 2. 1. CONSTANTE DE EQUILIBRIO Kc Para la siguiente reacción en equilibrio: LEY DE ACCIÓN DE MASAS (LAM): El producto de las concentraciones en el equilibrio de los productos elevadas a sus respectivos coeficientes estequiométricos, dividido por el producto de las concentraciones de los reactivos en el equilibrio elevadas a sus respectivos coeficientes estequiométricos, es una constante para cada temperatura, llamada constante de equilibrio. Kc= constante de equilibrio Dpto. Física y Química IES Turaniana

2. EQUILIBRIO HOMOGÉNEO 2. 1. CONSTANTE DE EQUILIBRIO Kc El valor de Kc es específico de cada reacción e independiente de las concentraciones iniciales de reactivos y productos. ¡¡ El valor de Kc sólo depende de la temperatura !! [ ]eq representa la concentración molar (en moles/L) en el equilibrio. Sin embargo, Kc se considera adimensional: ¡¡no tiene unidades!! En la expresión de Kc sólo se incluyen las especies gaseosas o en disolución. Sólidos puros, Líquidos puros y disolventes no aparecen en la expresión de K. Ya que sus [ ] son constantes y, por tanto, se integrarán en la constante de equilibrio. Pero esto será cuando estudiemos los equilibrios heterogéneos. Si para una reacción de izquierda a derecha se define Kp o Kc, para la reacción de derecha a izquierda será 1/Kp o 1/Kc Si una reacción representa la suma de varias reacciones, la constante de equilibrio para la reacción global se expresa como el producto de cada constante de equilibrio. K global = K’. K”. Kn.

2. EQUILIBRIO HOMOGÉNEO 2. 1. CONSTANTE DE EQUIIBRIO Kc Conociendo el valor de la constante de equilibrio se puede juzgar cualitativamente en que forma se desplaza la reacción antes de alcanzar el equilibrio, es decir si la reacción es o no favorable para la obtención de productos. Tres situaciones posibles: La K > 1 entonces: [productos] > [reactivos] Favorable para productos. La K ≈1 entonces [productos]≈ [reactivos]. La K < 1 entonces [productos] < [reactivos]: Desfavorable para productos. Dpto. Física y Química IES Turaniana

2. EQUILIBRIO HOMOGÉNEO 2. 1. 2. 2. CONSTANTEDE DEEQUILIBRIO EQUIIBRIO Kc Kc Si la escribimos como: Por ejemplo: ¡¡ Sólo depende de la Tª !! Tª (K) Kc 298 794 500 160 764 46 1100 25 Dpto. Física y Química IES Turaniana
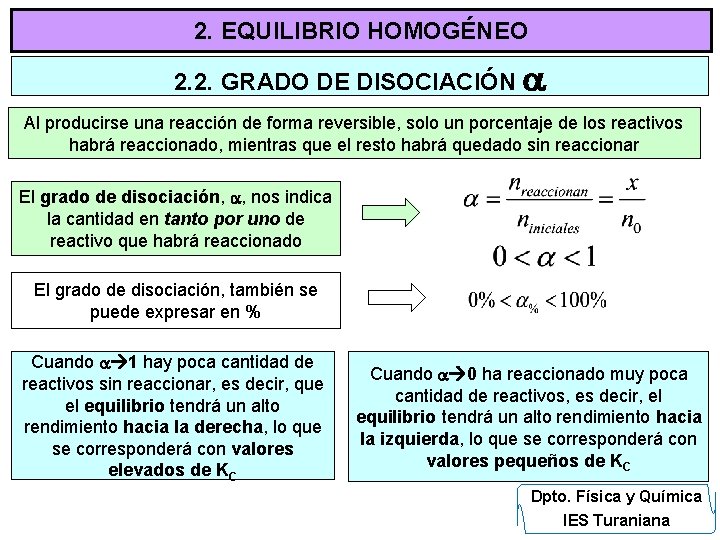
2. EQUILIBRIO HOMOGÉNEO 2. 2. GRADO DE DISOCIACIÓN Al producirse una reacción de forma reversible, solo un porcentaje de los reactivos habrá reaccionado, mientras que el resto habrá quedado sin reaccionar El grado de disociación, , nos indica la cantidad en tanto por uno de reactivo que habrá reaccionado El grado de disociación, también se puede expresar en % Cuando 1 hay poca cantidad de reactivos sin reaccionar, es decir, que el equilibrio tendrá un alto rendimiento hacia la derecha, lo que se corresponderá con valores elevados de KC Cuando 0 ha reaccionado muy poca cantidad de reactivos, es decir, el equilibrio tendrá un alto rendimiento hacia la izquierda, lo que se corresponderá con valores pequeños de KC Dpto. Física y Química IES Turaniana

2. EQUILIBRIO HOMOGÉNEO 2. 3. COCIENTE DE REACCIÓN QC Al comparar Qc con KC, se puede saber cómo evolucionará una reacción química reversible cuando los reactivos y los productos se encuentren en unas concentraciones cualesquiera diferentes de las que tienen en el equilibrio. Si QC=KC, la reacción está en el equilibrio. Si QC<KC, la reacción no está en el equilibrio, pues hay menos concentración de productos de la que hay en el equilibrio. Por tanto, la reacción evolucionará hacia la derecha hasta alcanzar el equilibrio. Si QC>KC, la reacción no está en el equilibrio, pues hay más concentración de productos de la que hay en el equilibrio. Por tanto, la reacción evolucionará hacia la izquierda hasta alcanzar el equilibrio.

1. En el proceso de formación del amoniaco, realizado a 500 °C en un recipiente de 10 litros, se ha encontrado en el equilibrio la presencia de 6 moles de N 2, 4 moles de H 2 y 1, 12 moles de NH 3. ¿Cómo será el rendimiento de esa reacción a 500 °C? 2. A una temperatura determinada, la Kc para la descomposición del fluoruro de hidrógeno 2 HF (g) ⇌ H 2 (g) + F 2 (g) vale: Kc= 1, 0· 10 -13. Al cabo de cierto tiempo se encuentran las siguientes concentraciones: [HF] = 0, 5 M; [H 2] =1· 10 -3; [F 2] = 4· 10 -3. Indica si el sistema se encuentra en equilibrio. En caso contrario, ¿qué debe ocurrir para que se alcance dicho equilibrio? 3. Para la reacción: A + B ⇌ C + D, el valor de la constante de equilibrio a una determinada temperatura es Kc = 56, 0. Si inicialmente se ponen 1, 00 mol de A y 2, 00 moles de B en un recipiente de 10 litros, ¿cuál será la concentración de todas las especies cuando se alcance el equilibrio? 4. Calcula los valores de Kc y Kp a 250 °C en la reacción de formación del amoniaco, sabiendo que si partimos de dos moles de N 2 y cinco moles de H 2, obtenemos tres moles de amoniaco. El volumen del recipiente de reacción es de 10 L

2. EQUILIBRIO HOMOGÉNEO 2. 4. CONSTANTE DE EQUILIBRIO Kp Cuando las reacciones son homogéneas y transcurren en fase gaseosa, se puede expresar el estado de los gases con sus presiones parciales expresadas en atm. Para una mezcla gaseosa: Dpto. Física y Química IES Turaniana
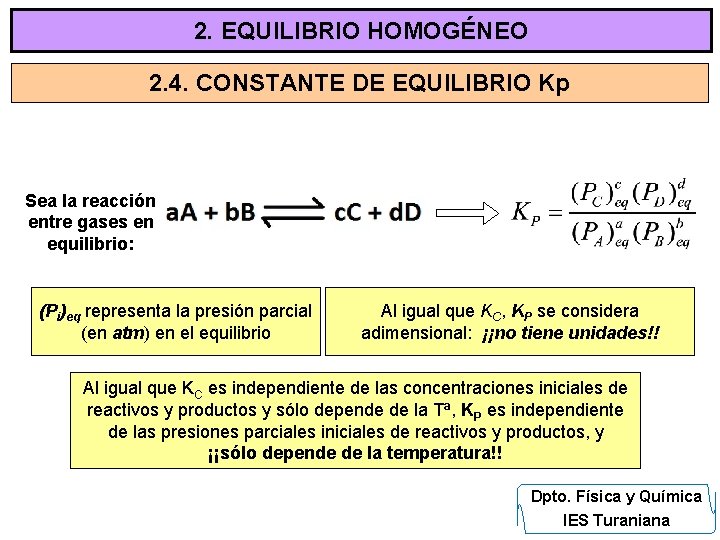
2. EQUILIBRIO HOMOGÉNEO 2. 4. CONSTANTE DE EQUILIBRIO Kp Sea la reacción entre gases en equilibrio: (Pi)eq representa la presión parcial (en atm) en el equilibrio Al igual que KC, KP se considera adimensional: ¡¡no tiene unidades!! Al igual que KC es independiente de las concentraciones iniciales de reactivos y productos y sólo depende de la Tª, KP es independiente de las presiones parciales iniciales de reactivos y productos, y ¡¡sólo depende de la temperatura!! Dpto. Física y Química IES Turaniana
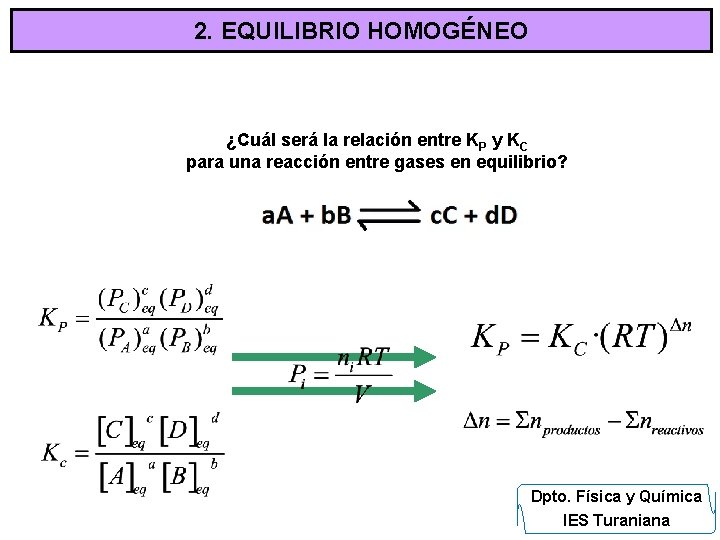
2. EQUILIBRIO HOMOGÉNEO ¿Cuál será la relación entre KP y KC para una reacción entre gases en equilibrio? Dpto. Física y Química IES Turaniana

3. FACTORES QUE AFECTAN AL EQUILIBRIO PRINCIPIO DE LE CH TELIER El principio de Le Chatelier nos permite predecir cuál será el sentido del desplazamiento del equilibrio de un modo cualitativo cuando se altera alguno de los factores que le afectan APRENDER Cuando se produce una variación de las condiciones de un sistema en equilibrio químico, el sistema tiende a recuperar el equilibrio oponiéndose a la causa que lo ha modificado. Dpto. Física y Química IES Turaniana
3. FACTORES QUE AFECTAN AL EQUILIBRIO PRINCIPIO DE LE CH TELIER 3. 1. CAMBIO CONCENTRACIÓN DE REACTIVOS O PRODUCTOS Al aumentar la concentración de una sustancia, el equilibrio evoluciona oponiendose a dicho cambio haciendo disminuir la cantidad presente de esa sustancia. Al disminuir la concentración de una sustancia, el equilibrio evoluciona oponiendose a dicho cambio haciendo aumentar la cantidad presente de esa sustancia. PCl 3(g) + Cl 2 (g) ⇌ PCl 5 (g) Si se aumenta la concentración de Cl 2, el sistema alcanzará un nuevo equilibrio produciendo más cantidad de PCl 5. Si se disminuye la concentración de PCl 3, el equilibrio se desplazará hacia la formación de PCl 3 y Cl 2 oponiendose a la variación introducida. Dpto. Física y Química IES Turaniana

Suponga el siguiente sistema en equilibrio: UO 2(s) + 4 HF(g) ⇌ UF 4(g) + 2 H 2 O(g) Explique hacia donde se desplaza el equilibrio cuando: a) Se adiciona UO 2(s) al sistema. b) Se elimina HF(g) Dpto. Física y Química IES Turaniana
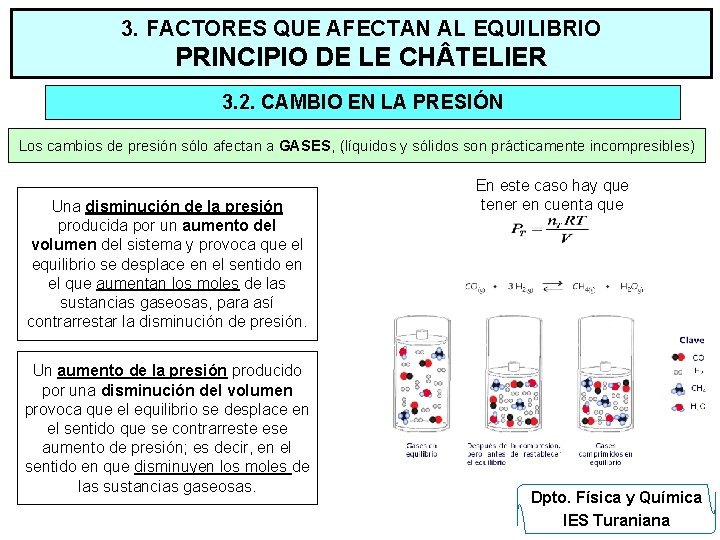
3. FACTORES QUE AFECTAN AL EQUILIBRIO PRINCIPIO DE LE CH TELIER 3. 2. CAMBIO EN LA PRESIÓN Los cambios de presión sólo afectan a GASES, (líquidos y sólidos son prácticamente incompresibles) Una disminución de la presión producida por un aumento del volumen del sistema y provoca que el equilibrio se desplace en el sentido en el que aumentan los moles de las sustancias gaseosas, para así contrarrestar la disminución de presión. Un aumento de la presión producido por una disminución del volumen provoca que el equilibrio se desplace en el sentido que se contrarreste ese aumento de presión; es decir, en el sentido en que disminuyen los moles de las sustancias gaseosas. En este caso hay que tener en cuenta que Dpto. Física y Química IES Turaniana

EJEMPLO: 3 H 2 (g) + N 2 (g) ⇌ 2 NH 3 (g) Un aumento de la presión exterior desplaza el equilibrio hacia la formación de amoniaco pues en ese término hay un menor número de moles de sustancias gaseosas. Una disminución de la presión exterior desplaza el equilibrio hacia la producción de una mayor cantidad de sustancias gaseosas, es decir hacia la producción de nitrógeno e hidrógeno. Para la reacción en equilibrio: 4 NH 3 (g) + 5 O 2 (g) ⇌ 4 NO(g) + 6 H 2 O(g) Explique el efecto que sobre la cantidad de NO(g) en el equilibrio tendrá: a) Una disminución de la [O 2] manteniendo constante el volumen del recipiente. b) Transferir la mezcla en equilibrio a un recipiente cuyo volumen es la mitad del volumen del recipiente original, a la misma temperatura. Dpto. Física y Química IES Turaniana

3. FACTORES QUE AFECTAN AL EQUILIBRIO PRINCIPIO DE LE CH TELIER 3. 3. CAMBIO EN LA TEMPERATURA Al aumentar la temperatura, el equilibrio se desplaza en el sentido en que se absorba calor (reacción endotérmica) para contrarrestar dicho aumento. Al disminuir la temperatura, el equilibrio se desplaza en el sentido en que se desprenda calor (reacción exotérmica) para contrarrestar dicha disminución. CH 2=CH 2(g) + H 2(g) ⇌ CH 3 -CH 3(g) ΔH= -136 KJ/mol Si se aumenta la temperatura, el sistema evolucionará en el sentido en que se oponga absorbiendo calor; por tanto se desplazará hacia la izquierda en el sentido de la regeneración de etileno e hidrógeno. Si se disminuye la temperatura, el sistema se opondrá desprendiendo calor y desplazándose hacia la formación de etano. Dpto. Física y Química IES Turaniana

Consideremos el sistema: 4 HCl(g) + O 2 (g) ⇌ 2 H 2 O(g) + 2 Cl 2 (g) ΔHº = - 114 k. J Razona qué sucede al: a) añadir O 2 (manteniendo constante el volumen) b) extraer Cl 2 (manteniendo constante el volumen) c) si disminuimos la temperatura d) si disminuimos la presión Dpto. Física y Química IES Turaniana

3. FACTORES QUE AFECTAN AL EQUILIBRIO PRINCIPIO DE LE CH TELIER 3. 4. ADICIÓN DE UN CATALIZADOR La adición de un catalizador produce la misma variación en la velocidad del proceso directo y del inverso y, por tanto, no afecta al equilibrio, aunque sí modifica el tiempo que tarda en alcanzarse el estado de equilibrio Dpto. Física y Química IES Turaniana

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN Las sustancias reaccionantes no se encuentran en el mismo estado físico, en la expresión de su constante de equilibrio no se incluyen ni las [ ] ni las presiones parciales de los sólidos o líquidos puros EJEMPLOS: Ca. CO 3 (s) ⇌ Ca. O(s) + CO 2(g) Kc = [CO 2 ] Kp = PCO 2 Dpto. Física y Química IES Turaniana

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN Nosotros vamos a estudiar los equilibrios que se producen entre solutos sólidos poco solubles y sus iones en disolución. Es lo que llamamos reacciones de precipitación Cuando formamos una disolución saturada de Aa. Bb se produce un equilibrio heterogéneo entre la sal no disuelta (en estado sólido) y los iones en disolución La constante de equilibrio referida alas concentraciones de una sal poco soluble en disolución se denomina producto de solubilidad Dpto. Física y Química IES Turaniana

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN Dpto. Física y Química IES Turaniana Los valores del producto de solubilidad son muy pequeños para sales poco solubles Recordemos que la solubilidad s de una sal es la concentración de sal disuelta en una disolución saturada de la misma, y que se expresa en gsoluto/Ldisolución ó molessoluto/Ldisolución Dpto. Física y Química IES Turaniana Conviene recordar que tanto la solubilidad como el producto de solubilidad dependen sólo de la temperatura
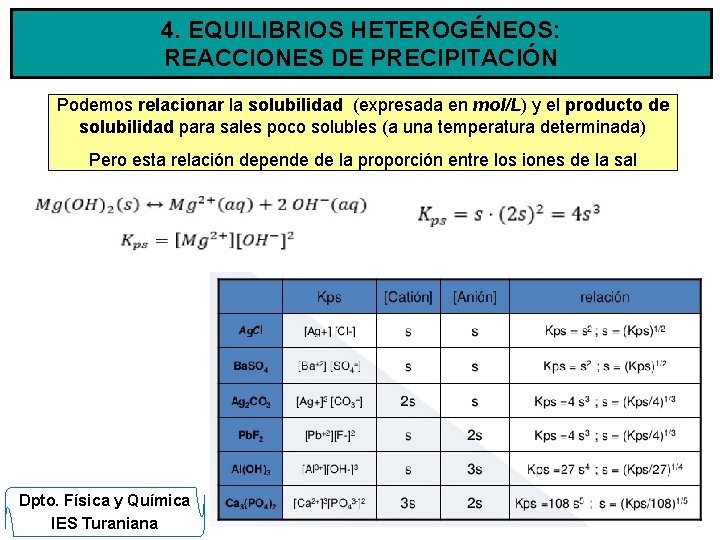
4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN Podemos relacionar la solubilidad (expresada en mol/L) y el producto de solubilidad para sales poco solubles (a una temperatura determinada) Pero esta relación depende de la proporción entre los iones de la sal Dpto. Física y Química IES Turaniana

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN Gracias al producto de solubilidad también podemos predecir si precipitará o no una sal cuando tengamos unas determinadas concentraciones de los iones de la sal Para ello se define el producto iónico, de la misma manera que definíamos el cociente de reacción para un equilibrio homogéneo, y compararlo con el producto de solubilidad PRODUCTO IÓNICO, Q: producto de las concentraciones de los iones en disolución en cualquier instante. Q= [Ab+]ta. [Ba-]tb Ks= [Ab+]eqa. [Ba-]eqb Disolución saturada: El sistema está en equilibrio Disolución sobresaturada La reacción se desplaza hacia la izquierda. Se formará precipitado. Disolución insaturada. La reacción se desplaza hacia la derecha. Se disolverá precipitado.

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN 4. 1. Efecto del ion común en los equilibrios de solubilidad Si a un equilibrio de solubilidad le añadimos una cierta cantidad de uno de los iones, mediante la adición de una segunda disolución que lo contiene, se producirá un aumento en la concentración de dicho ion. La presencia de este ion común creará una situación en la que el producto iónico supere el producto de solubilidad (Q>Ks) Como consecuencia, el equilibrio se desplazará hacia la izquierda formando más precipitado, es decir, más sal en estado sólido La solubilidad de un compuesto poco soluble disminuye en presencia de un segundo soluto que proporcione un ion común Dpto. Física y Química IES Turaniana

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN EJEMPLO ION COMÚN Ag. I (s)⇌ Ag+ (ac) + I - (ac) ion común Adición: KI (s)⇌ K+ (ac) + I - (ac) El equilibrio se desplaza hacia la izquierda y precipita Ag. I(s) La solubilidad de un compuesto poco soluble disminuye en presencia de un segundo soluto que proporcione un ion común Dpto. Física y Química IES Turaniana

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN 4. 2. El efecto del p. H en los equilibrios de solubilidad Si a un equilibrio de solubilidad le añadimos cierta cantidad de un ácido que aporte iones H+, estos iones H+ pueden reaccionar con los iones negativos de la sal disuelta para formar otra especie, disminuyendo así la concentración de dicho ión negativo La presencia de estos iones H+ creará una situación en la que el producto iónico sea menor el producto de solubilidad (Q<Ks) Como consecuencia, el equilibrio se desplazará hacia la derecha disolviéndose más precipitado, es decir, más sal se disolverá La solubilidad de un compuesto poco soluble puede aumentar en presencia de una disolución ácida que aporte iones H+ Dpto. Física y Química IES Turaniana

4. EQUILIBRIOS HETEROGÉNEOS: REACCIONES DE PRECIPITACIÓN 4. 2. El efecto del p. H en los equilibrios de solubilidad EJEMPLO Mg(OH)2 (s)⇌ Mg 2+ (ac) + OH - (ac) H+ (ac) + OH- (ac) ⇌ H 2 O (l) Se añade: HCl (ac)⇌ Cl- (ac) + H + (ac) El equilibrio se desplaza hacia la derecha y se disuelve más Mg(OH)2(s) Disminuye la [OH-] y, como consecuencia, Q<Ks La solubilidad de un compuesto poco soluble puede aumentar en presencia de una disolución ácida que aporte iones H+ Dpto. Física y Química IES Turaniana
- Slides: 34