EQUILIBRIO QUMICO Contenidos n 1 Describir Concepto de

EQUILIBRIO QUÍMICO

Contenidos n 1. -Describir Concepto de Equilibrio Químico. n 2. -Plantear Constante de equilibrio termodinámica. n 3. -Relacionar Kp y Kc n 4. -Equilibrio Homogéneo.

Equilibrio Químico n La velocidad de reacción directa se iguala a la velocidad de reacción inversa. n Las concentraciones de cada especie NO cambian en el tiempo. n El avance de la reacción, está controlado por una Constante de Equilibrio. n Depende de la Temperatura. . 3

n Todos los sistemas químicos alcanzan en el tiempo la condición de equilibrio n El estado de equilibrio químico es de naturaleza dinámica y no estática. . 4

Reacciones Reversibles n Finalmente, las dos reacciones evolucionan de modo tal que sus velocidades se igualan, estableciéndose un equilibrio químico. n Bajo estas condiciones la reacción es reversible y se representa de la siguiente manera: 2 N 2 O 5(g) O 2(g) + 4 NO 2(g) n En una reacción reversible, la reacción ocurre simultáneamente en ambas direcciones. n Lo anterior se indica por medio de una doble flecha n En principio, casi todas las reacciones son reversibles en cierta medida. Prof. S. Casas-Cordero E. 5
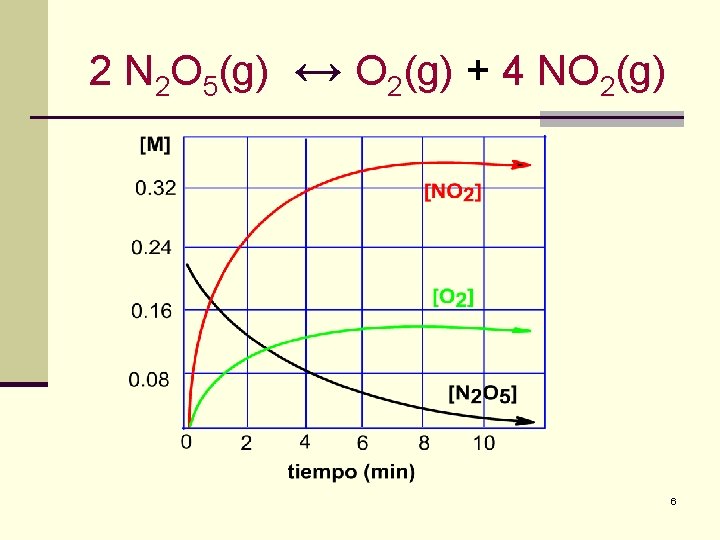
2 N 2 O 5(g) ↔ O 2(g) + 4 NO 2(g) 6
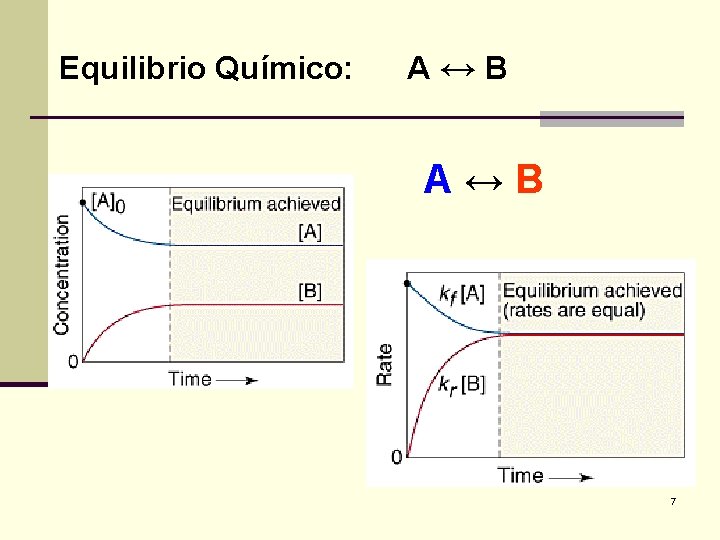
Equilibrio Químico: A↔B 7
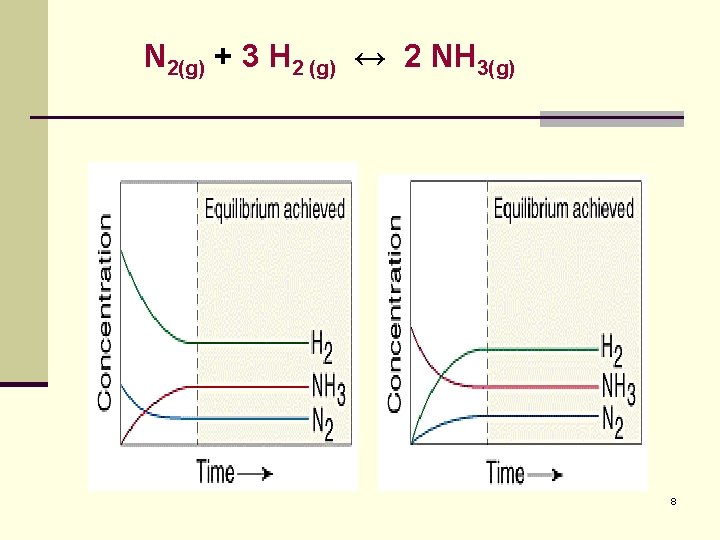
N 2(g) + 3 H 2 (g) ↔ 2 NH 3(g) 8

Forma general de la Keq 9

Constante de Equilibrio 2 N 2 O 5(g) ↔ O 2(g) + 4 NO 2(g) 10

Constante de Equilibrio N 2(g) + 3 H 2 (g) ↔ 2 NH 3(g) 11

Reacciones en fase gaseosa n En un recipiente cerrado, cada especie puede cuantificarse por la concentración molar y también por la Presión Parcial. n La Keq puede escribirse en función de la Concentración Molar o bien en función de la Presión Parcial. n Kc representará a la Keq escrita concentraciones molares n Kp representará a la Keq escrita con presiones parciales 12
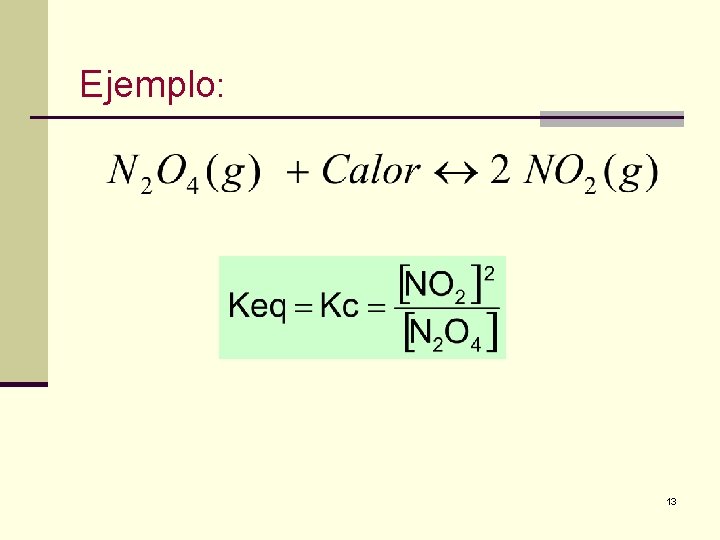
Ejemplo: 13
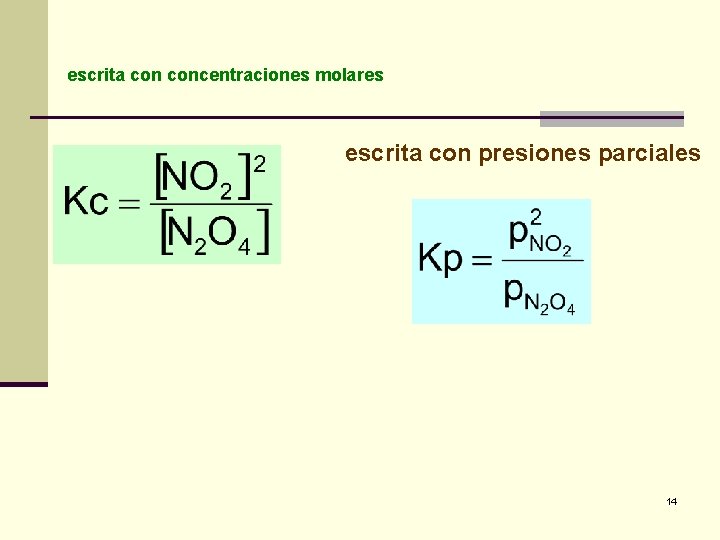
escrita concentraciones molares escrita con presiones parciales 14
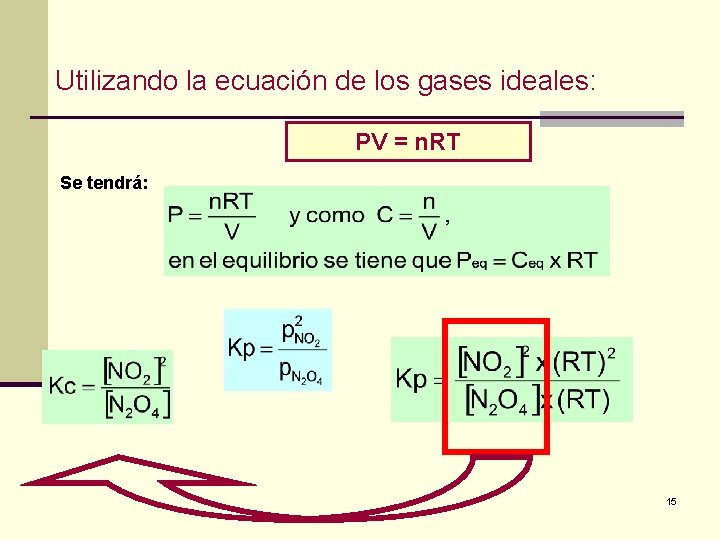
Utilizando la ecuación de los gases ideales: PV = n. RT Se tendrá: 15
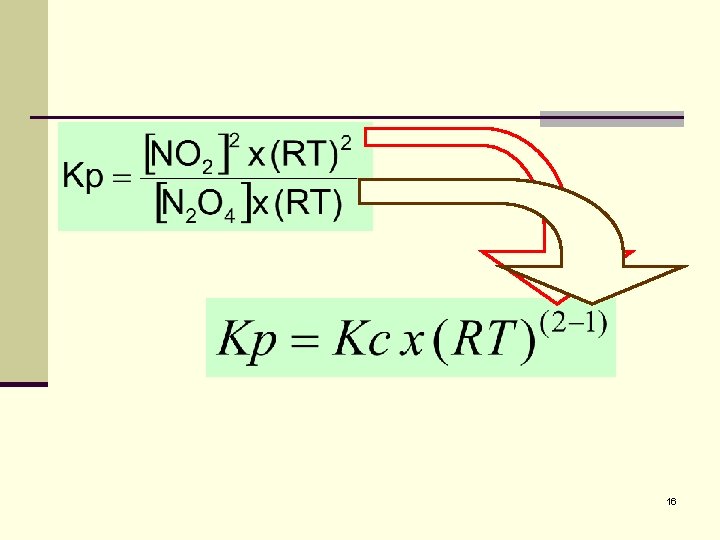
16
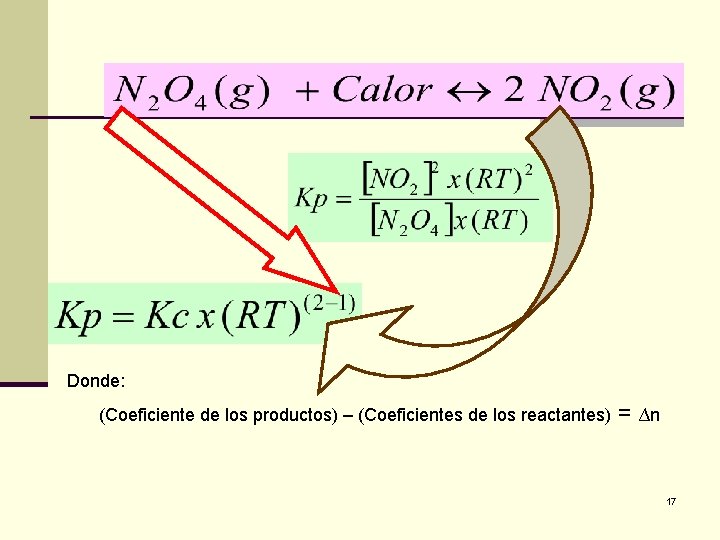
Donde: (Coeficiente de los productos) – (Coeficientes de los reactantes) = ∆n 17

Constante de Equilibrio a A(g) + b B(g) ↔ y P(g) + z Q(q) Kp = Kc x ∆n (RT) 18

Equilibrio Homogéneo y Heterogéneo Si todos los reactivos y productos están en una sola fase, el equilibrio es homogéneo. Si uno o más reactivos o productos están en una fase diferente, el equilibrio es heterogéneo. 19

Criterios para representar la Keq n Los líquidos y los sólidos puros no se incluyen en la constante de equilibrio. n Si una ecuación se invierte, el valor de la nueva Keq, será el inverso del valor anterior. n El valor de la Keq de toda ecuación que se amplifique por un número, cambiará a la potencia del número por el cual se amplificó. n Si una reacción se realiza en etapas sucesivas, la Keq de la reacción global corresponde a la multiplicación de las Keq de todas las etapas. 20
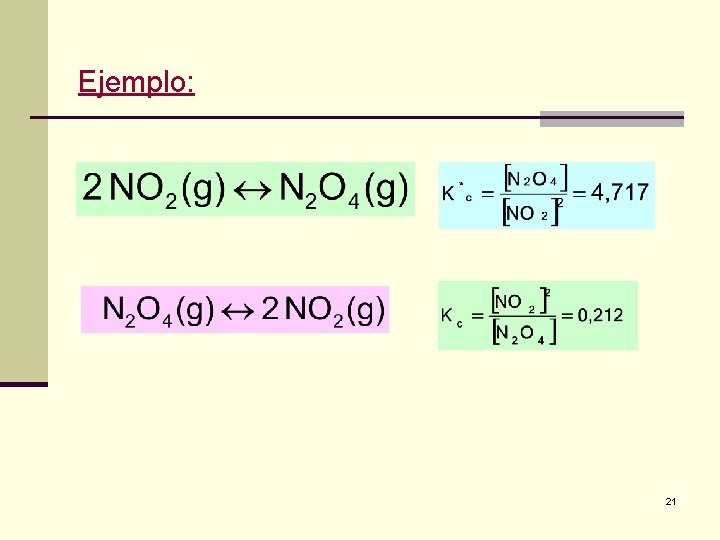
Ejemplo: 21
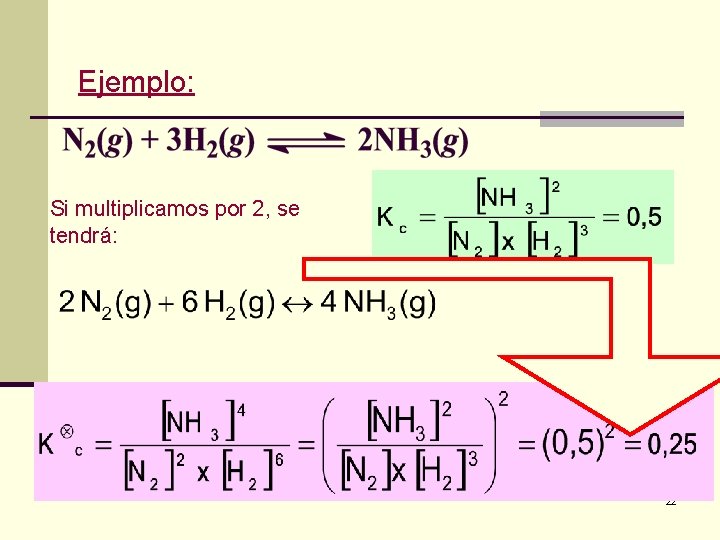
Ejemplo: Si multiplicamos por 2, se tendrá: 22
Magnitud de las constantes de equilibrio 23

Predicción del sentido de una reacción 24
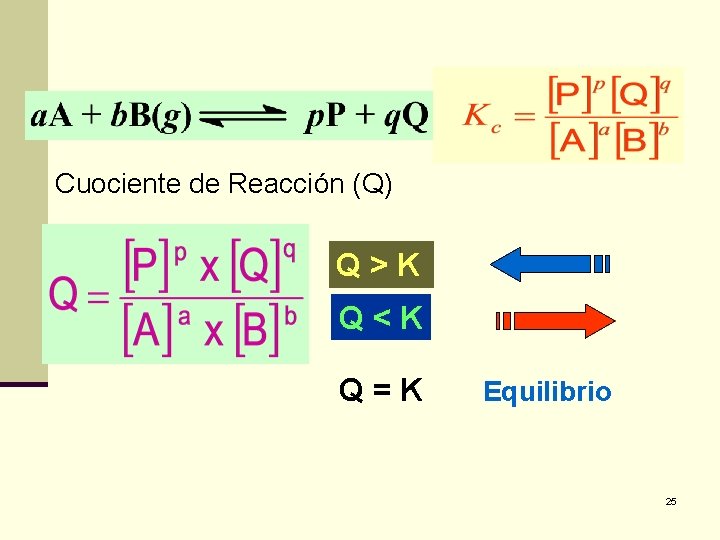
Cuociente de Reacción (Q) Q>K Q<K Q=K Equilibrio 25

Principio de Le Chatelier n Establece que si un sistema en equilibrio es sometido a una perturbación o tensión, el sistema reaccionará de tal manera que disminuirá el efecto de la tensión. n Hay 3 formas de alterar la composición en el equilibrio de una mezcla de reacción en estado gaseoso para mejorar el rendimiento de un producto: 26
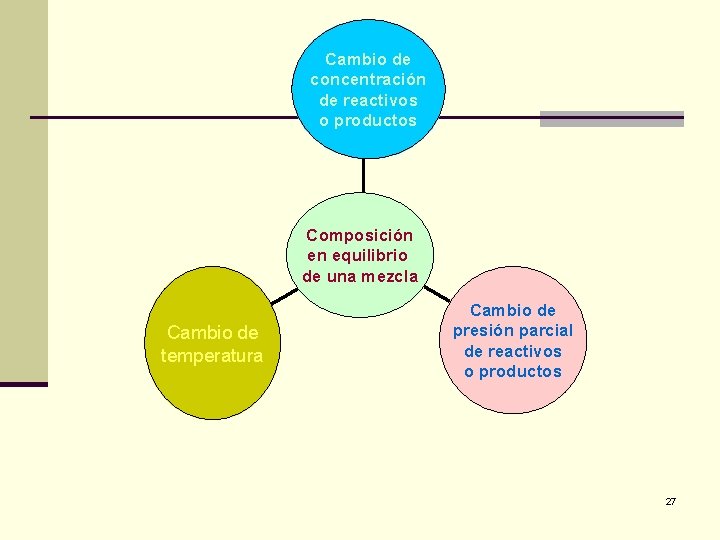
Cambio de concentración de reactivos o productos Composición en equilibrio de una mezcla Cambio de temperatura Cambio de presión parcial de reactivos o productos 27
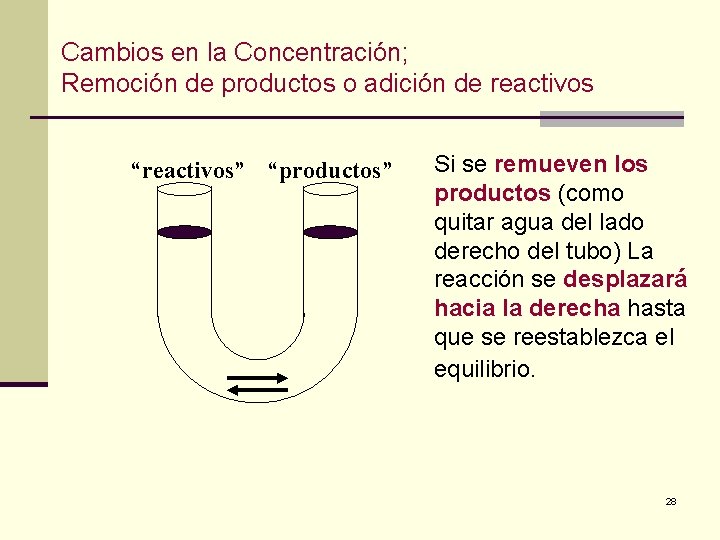
Cambios en la Concentración; Remoción de productos o adición de reactivos “reactivos” “productos” Si se remueven los productos (como quitar agua del lado derecho del tubo) La reacción se desplazará hacia la derecha hasta que se reestablezca el equilibrio. 28
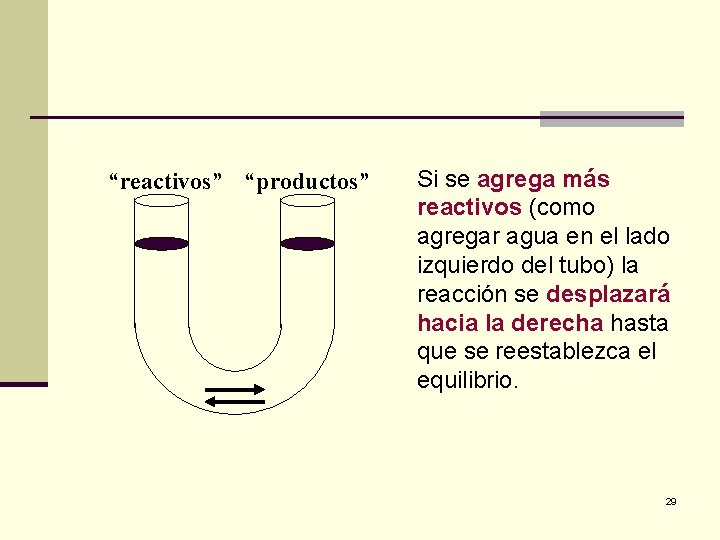
“reactivos” “productos” Si se agrega más reactivos (como agregar agua en el lado izquierdo del tubo) la reacción se desplazará hacia la derecha hasta que se reestablezca el equilibrio. 29
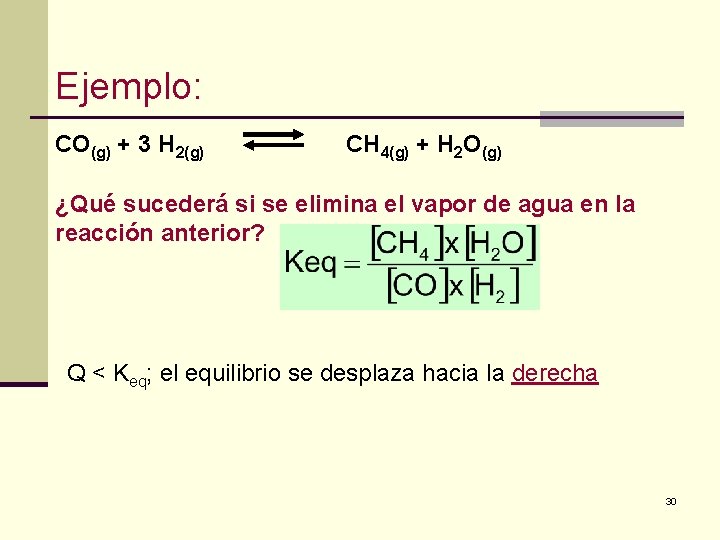
Ejemplo: CO(g) + 3 H 2(g) CH 4(g) + H 2 O(g) ¿Qué sucederá si se elimina el vapor de agua en la reacción anterior? Q < Keq; el equilibrio se desplaza hacia la derecha 30

Efecto del cambio de temperatura n La temperatura afecta de modo diferente si la reacción es exotérmica o endotérmica. n La velocidad de reacción normalmente se incrementa al aumentar la temperatura. n Se alcanza más rápidamente el equilibrio. n Cambia el valor de la constante de equilibrio, Keq. 31

32

Co(H 2 O)62+ + 4 Cl 1 - ↔ Co. Cl 42 - + 6 H 2 O n Efecto del cambio de temperatura sobre el equilibrio químico. Prof. S. Casas-Cordero E. 33
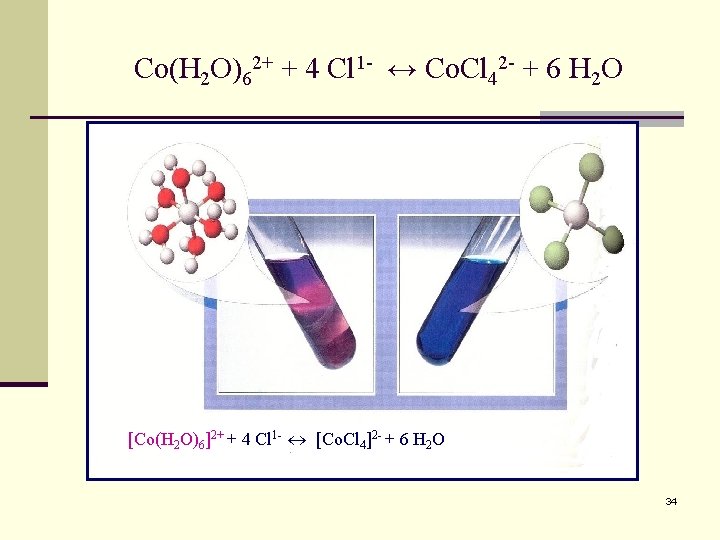
Co(H 2 O)62+ + 4 Cl 1 - ↔ Co. Cl 42 - + 6 H 2 O [Co(H 2 O)6]2+ + 4 Cl 1 - [Co. Cl 4]2 - + 6 H 2 O 34
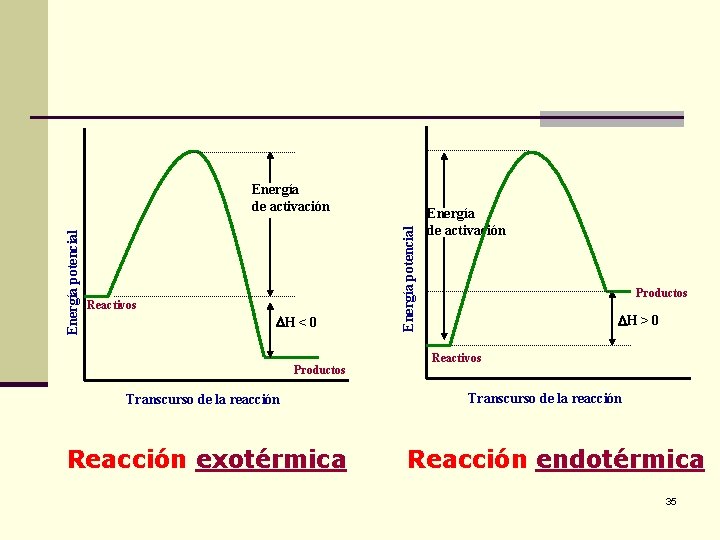
Reactivos H < 0 Productos Transcurso de la reacción Reacción exotérmica Energía potencial Energía de activación Productos H > 0 Reactivos Transcurso de la reacción Reacción endotérmica 35

Efecto del cambio de presión n Los cambios de presión pueden afectar los sistemas gaseosos homogéneos en equilibrio. n Los cambios de presión no afectan sistemas homogéneos sólidos o líquidos, pero afectan los sistemas heterogéneos en los que interviene uno o más gases. n Los cambios que se producen en la presión interna no afectan el equilibrio. 36

n Un aumento en la presión externa hace evolucionar al sistema en la dirección del menor número de moles de gas. Una disminución lo hace reaccionar hacia donde existen mayor cantidad. n Un aumento en la presión del siguiente sistema: CO(g) + 3 H 2(g) CH 4(g) + H 2 O(g) obliga a que el sistema se desplace hacia la derecha, hay cuatro moles a la izquierda y solo dos a la derecha. 37
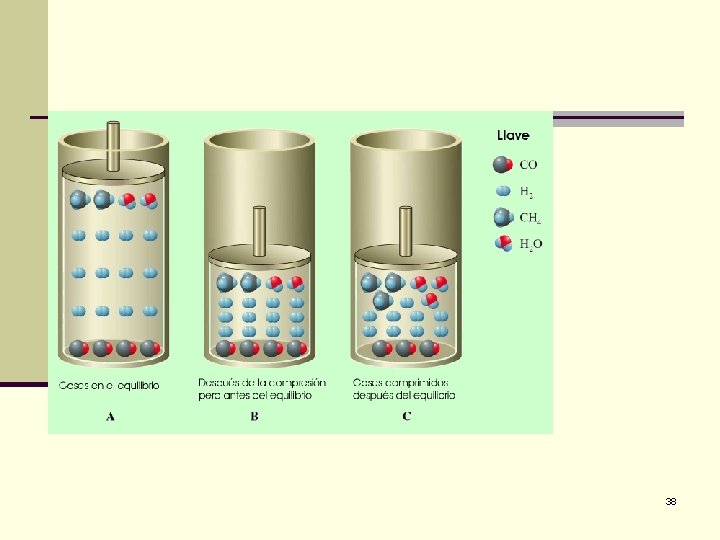
38
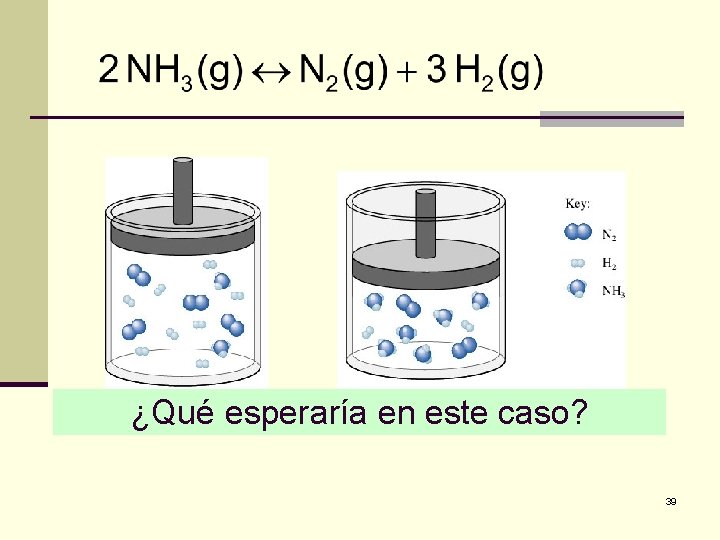
¿Qué esperaría en este caso? 39

n Ciertamente la reacción se favorece hacia reactante. n La formación de Amoniaco es un proceso industrial que se realiza a alta presión n Se conoce como proceso Haber 40
- Slides: 40