Equilibrio qumico Captulo 14 Copyright The Mc GrawHill

Equilibrio químico Capítulo 14 Copyright © The Mc. Graw-Hill Companies, Inc. Permission required for reproduction or display.

El equilibrio es un estado en que no hay ningún cambio notable mientras transcurre el tiempo. Equlibrio químico se alcanza cuando: • las velocidades de las reacciones directa e inversa se igualan y • las concentraciones de los reactivos y productos permanecen constantes Equilibrio físico H 2 O (l) H 2 O (g) Equilibrio químico N 2 O 4 (g) 2 NO 2 (g) 14. 1
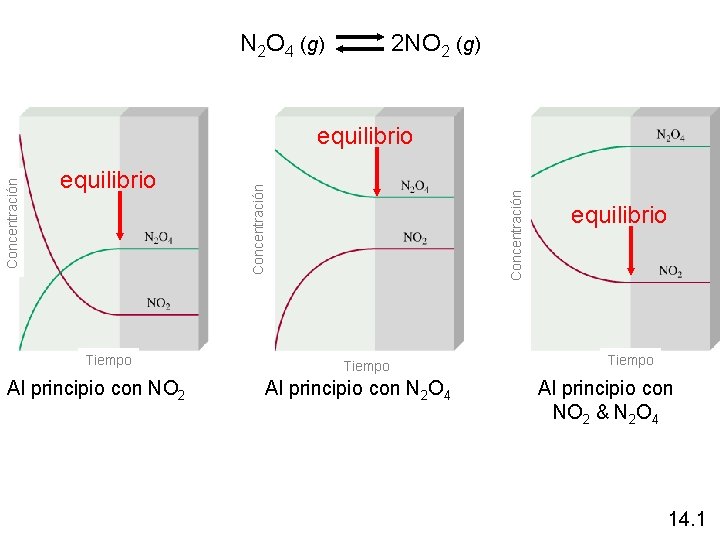
N 2 O 4 (g) 2 NO 2 (g) Tiempo Al principio con NO 2 Concentración equilibrio Tiempo Al principio con N 2 O 4 equilibrio Tiempo Al principio con NO 2 & N 2 O 4 14. 1
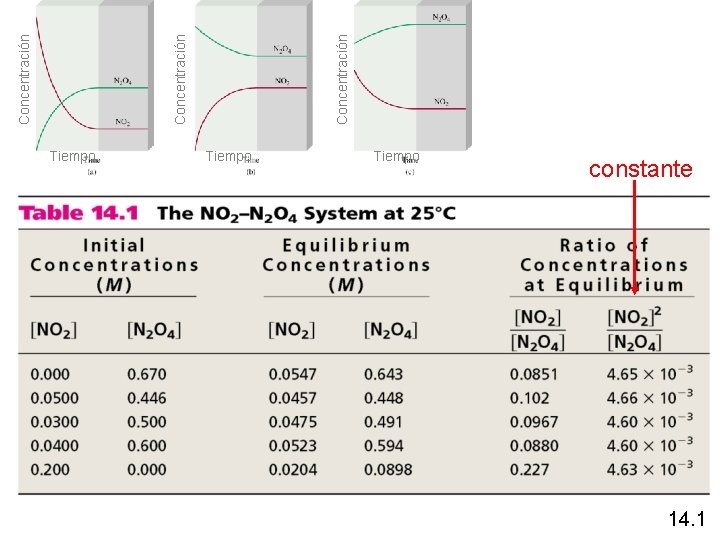
Tiempo constante 14. 1 Concentración
![N 2 O 4 (g) 2 NO 2 (g) K = [NO 2]2 [N N 2 O 4 (g) 2 NO 2 (g) K = [NO 2]2 [N](http://slidetodoc.com/presentation_image/1f1f94a4231bb6898151a60f10fea36f/image-5.jpg)
N 2 O 4 (g) 2 NO 2 (g) K = [NO 2]2 [N 2 O 4] = 4. 63 x 10 -3 a. A + b. B c. C + d. D K = [C]c[D]d [A]a[B]b Ley de acción de masa El equilibrio será K >> 1 K << 1 Desplaza a la derecha Favorece a los productos Desplaza a la derecha Favorece a las productos 14. 1
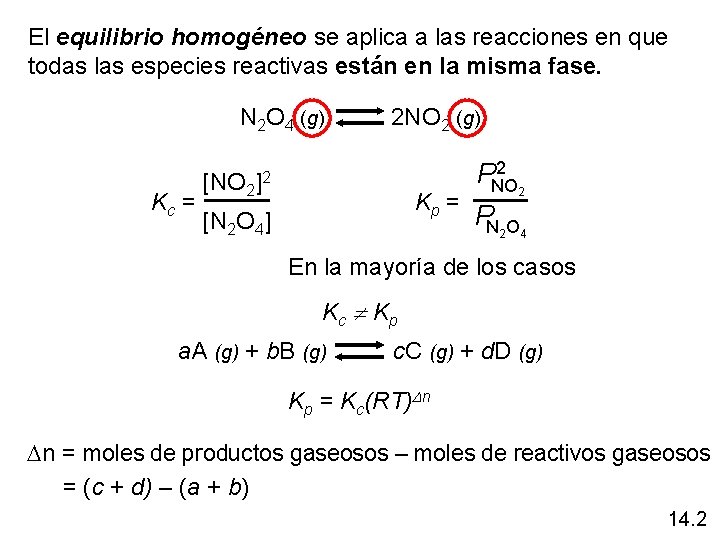
El equilibrio homogéneo se aplica a las reacciones en que todas las especies reactivas están en la misma fase. N 2 O 4 (g) 2 NO 2 (g) Kc = [NO 2 ]2 Kp = [N 2 O 4] 2 PNO 2 PN 2 O 4 En la mayoría de los casos Kc Kp a. A (g) + b. B (g) c. C (g) + d. D (g) Kp = Kc(RT)Dn Dn = moles de productos gaseosos – moles de reactivos gaseosos = (c + d) – (a + b) 14. 2
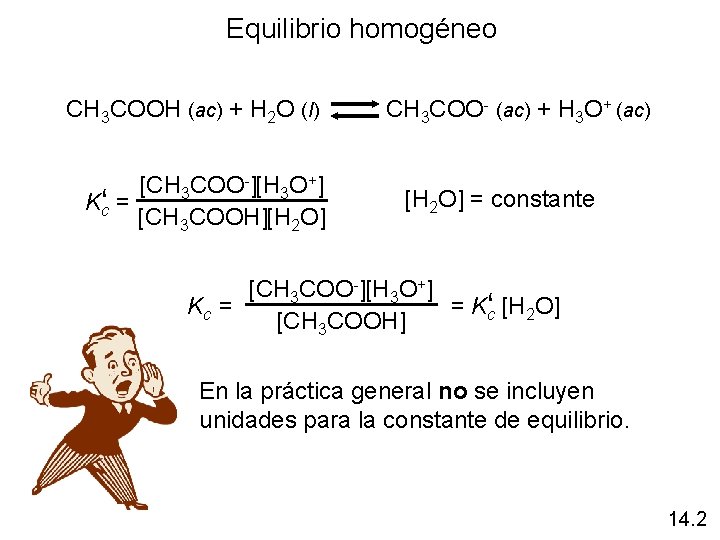
Equilibrio homogéneo CH 3 COOH (ac) + H 2 O (l) CH 3 COO- (ac) + H 3 O+ (ac) [CH 3 COO-][H 3 O+] Kc‘ = [CH 3 COOH][H 2 O] = constante [CH 3 COO-][H 3 O+] = Kc‘ [H 2 O] Kc = [CH 3 COOH] En la práctica general no se incluyen unidades para la constante de equilibrio. 14. 2

Las concentraciones de equilibrio para la reacción entre monóxido de carbono y cloro molecular para formar COCl 2 (g) a 740 C son [CO] = 0. 012 M, [Cl 2] = 0. 054 M, y [COCl 2] = 0. 14 M. Calcule las constantes de equilibrio Kc y K p. CO (g) + Cl 2 (g) COCl 2 (g) [COCl 2] 0. 14 = = 220 Kc = [CO][Cl 2] 0. 012 x 0. 054 Kp = Kc(RT)Dn Dn = 1 – 2 = -1 R = 0. 0821 T = 273 + 74 = 347 K Kp = 220 x (0. 0821 x 347)-1 = 7. 7 14. 2

La constante de equilibrio Kp para la reacción 2 NO 2 (g) 2 NO (g) + O 2 (g) es 158 a 1000 K. ¿Cuál es la presión en el equilibrio de O 2 si las PNO = 0. 400 atm y PNO = 0. 270 atm? 2 Kp = 2 PNO PO 2 2 PNO 2 PO 2 = Kp 2 PNO 2 2 PNO PO 2 = 158 x (0. 400)2/(0. 270)2 = 347 atm 14. 2
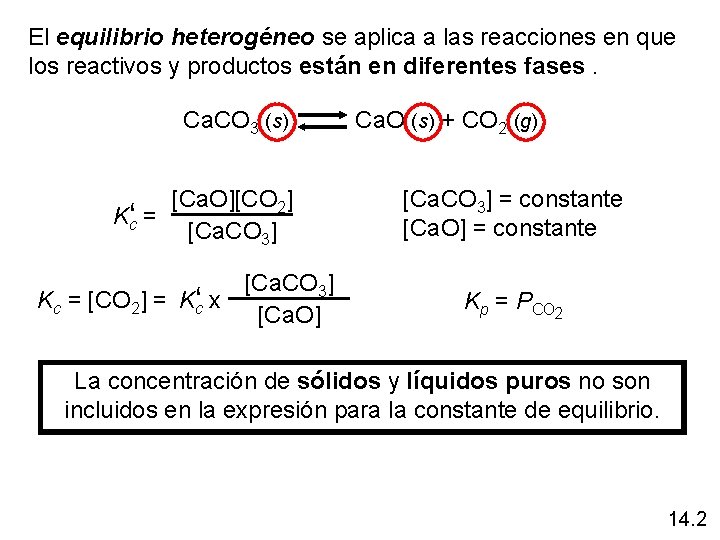
El equilibrio heterogéneo se aplica a las reacciones en que los reactivos y productos están en diferentes fases. Ca. CO 3 (s) Ca. O (s) + CO 2 (g) [Ca. O][CO 2] Kc‘ = [Ca. CO 3] Kc = [CO 2] = Kc‘ x [Ca. O] [Ca. CO 3] = constante [Ca. O] = constante Kp = PCO 2 La concentración de sólidos y líquidos puros no son incluidos en la expresión para la constante de equilibrio. 14. 2
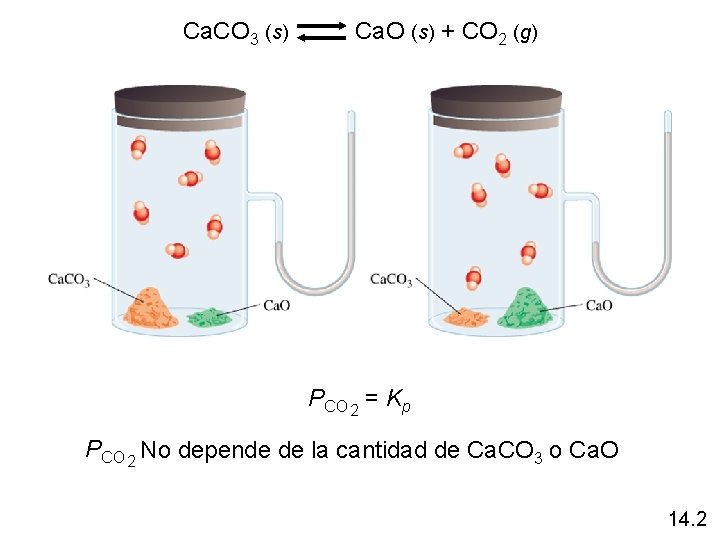
Ca. CO 3 (s) Ca. O (s) + CO 2 (g) PCO 2 = Kp PCO 2 No depende de la cantidad de Ca. CO 3 o Ca. O 14. 2

Considere el equilibrio siguiente en 295 K: NH 4 HS (s) NH 3 (g) + H 2 S (g) La presión parcial de cada gas es 0. 265 atm. ¿Calcule Kp y Kc para la reacción? Kp = PNH PH S = 0. 265 x 0. 265 = 0. 0702 3 2 Kp = Kc(RT)Dn Kc = Kp(RT)-Dn Dn = 2 – 0 = 2 T = 295 K Kc = 0. 0702 x (0. 0821 x 295)-2 = 1. 20 x 10 -4 14. 2
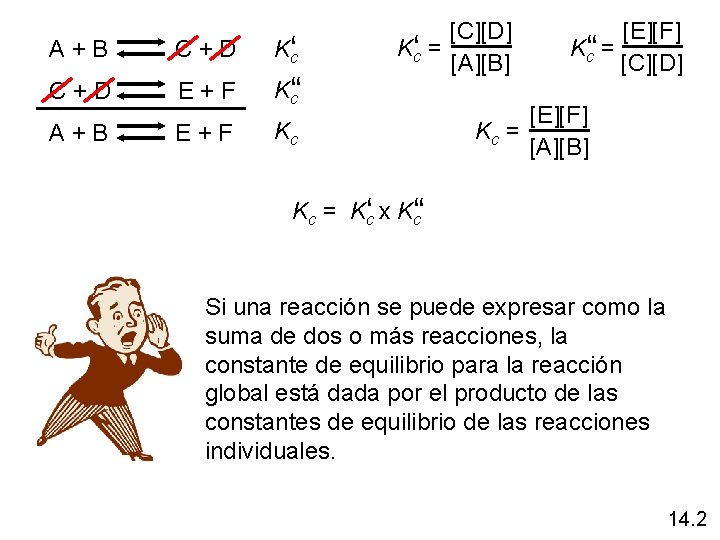
A + B C + D Kc‘ C + D E + F K‘c‘ A + B E + F Kc [C][D] Kc‘ = [A][B] [E][F] Kc‘‘ = [C][D] [E][F] Kc = [A][B] Kc = Kc‘ x K‘c‘ Si una reacción se puede expresar como la suma de dos o más reacciones, la constante de equilibrio para la reacción global está dada por el producto de las constantes de equilibrio de las reacciones individuales. 14. 2
![N 2 O 4 (g) 2 NO 2 (g) K = [NO 2]2 [N N 2 O 4 (g) 2 NO 2 (g) K = [NO 2]2 [N](http://slidetodoc.com/presentation_image/1f1f94a4231bb6898151a60f10fea36f/image-14.jpg)
N 2 O 4 (g) 2 NO 2 (g) K = [NO 2]2 [N 2 O 4] = 4. 63 x 10 -3 2 NO 2 (g) N 2 O 4 (g) [N 2 O 4] 1 ‘ = 216 = K = 2 K [NO 2] Cuando la ecuación para una reacción reversible se escribe en dirección opuesta, la constante de equilibrio se vuelve el inverso de la constante de equilibrio original. 14. 2

Escritura de las expresiones de las constante de equilibrio • Las concentraciones de las especies reactivas en fase condensada se expresan en M. En la fase gaseosa, las concentraciones se pueden expresar en M o en atm. • Las concentraciones de sólidos puros, líquidos puros y solventes no aparecen en las expresiones de constantes de equilibrio. • La constante de equilibrio es una cantidad adimensional. • Citando un valor por la constante de equilibrio, debe especificar la ecuación balanceada y la temperatura. • Si una reacción puede expresarse como una suma de dos o más reacciones, la constante de equilibrio para la reacción global está dada por el producto de las constantes de equilibrio de las reacciones individuales. 14. 2

Química cinética y equilibrio químico kf A + 2 B AB 2 kr velocidadf = kf [A][B]2 velocidadr = kr [AB 2] Equilibrio velocidadf = velocidadr kf [A][B]2 = kr [AB 2] kf [AB 2] = Kc = kr [A][B]2 14. 3
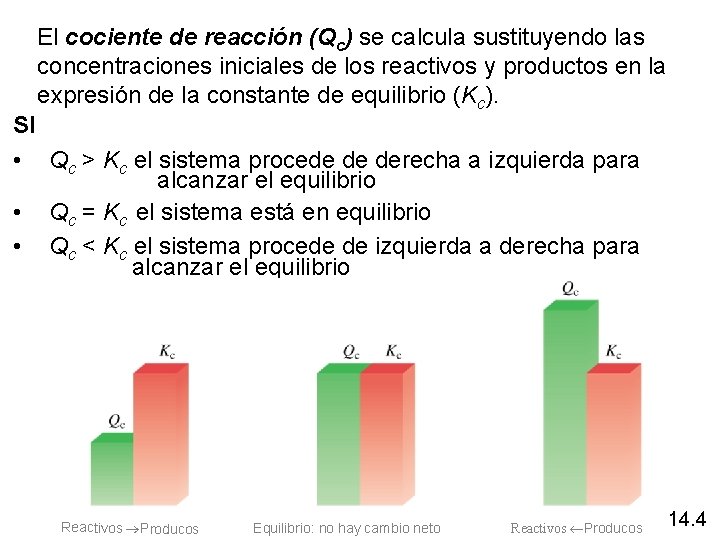
El cociente de reacción (Qc) se calcula sustituyendo las concentraciones iniciales de los reactivos y productos en la expresión de la constante de equilibrio (Kc). SI • Qc > Kc el sistema procede de derecha a izquierda para alcanzar el equilibrio • Qc = Kc el sistema está en equilibrio • Qc < Kc el sistema procede de izquierda a derecha para alcanzar el equilibrio Reactivos Producos Equilibrio: no hay cambio neto Reactivos Producos 14. 4

Cálculo de las concentraciones de equilibrio 1. Exprese las concentraciones de equilibrio de todas las especies en términos de las concentraciones iniciales y una sola variable x que representan el cambio en la concentración. 2. Escriba la expresión de la constante de equilibrio en términos de las concentraciones de equilibrio. Sabiendo el valor de la constante de equilibrio, resuelva para x. 3. Habiendo resuelto para x, calcule las concentraciones de equilibrio de todas las especies. 14. 4

A 12800 C la constante de equilibrio (Kc) para la reacción Br 2 (g) 2 Br (g) Es 1. 1 x 10 -3. Si las concentraciones iniciales son [Br 2] = 0. 063 M y [Br] = 0. 012 M, calcule las concentraciones de estas especies en equilibrio. Sea x el cambio en la concentración de Br 2 (g) 2 Br (g) Inicial (M) 0. 063 0. 012 Cambio (M) -x +2 x Equilibrio(M) 0. 063 - x 0. 012 + 2 x [Br]2 Kc = [Br 2] (0. 012 + 2 x)2 = 1. 1 x 10 -3 Kc = 0. 063 - x Resuelva para x 14. 4

(0. 012 + 2 x)2 = 1. 1 x 10 -3 Kc = 0. 063 - x 4 x 2 + 0. 048 x + 0. 000144 = 0. 0000693 – 0. 0011 x 4 x 2 + 0. 0491 x + 0. 0000747 = 0 -b ± b 2 – 4 ac 2 x = ax + bx + c =0 2 a x = -0. 0105 x = -0. 00178 Br 2 (g) 2 Br (g) Inicial(M) 0. 063 0. 012 Cambio(M) -x +2 x 0. 063 - x 0. 012 + 2 x Equilibrio(M) En equilibrio, [Br] = 0. 012 + 2 x = -0. 009 M o 0. 00844 M En equilibrio, [Br 2] = 0. 062 – x = 0. 0648 M 14. 4
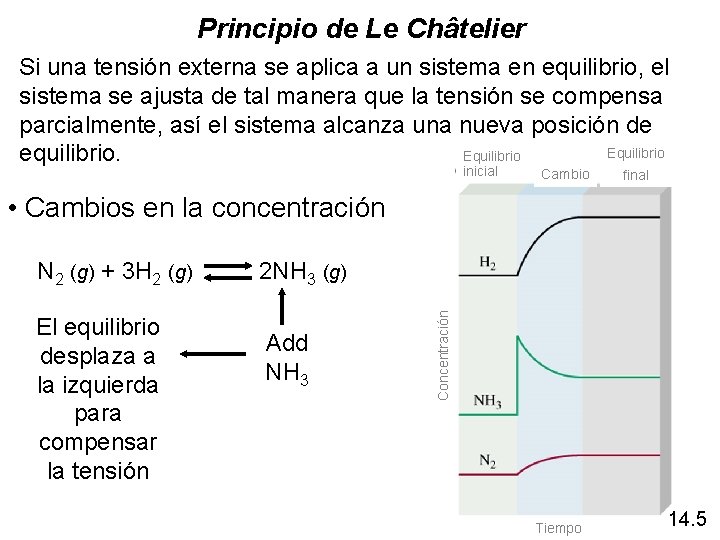
Principio de Le Châtelier Si una tensión externa se aplica a un sistema en equilibrio, el sistema se ajusta de tal manera que la tensión se compensa parcialmente, así el sistema alcanza una nueva posición de Equilibrio equilibrio. inicial Cambio final • Cambios en la concentración El equilibrio desplaza a la izquierda para compensar la tensión Add NH 3 Concentración N 2 (g) + 3 H 2 (g) 2 NH 3 (g) Tiempo 14. 5
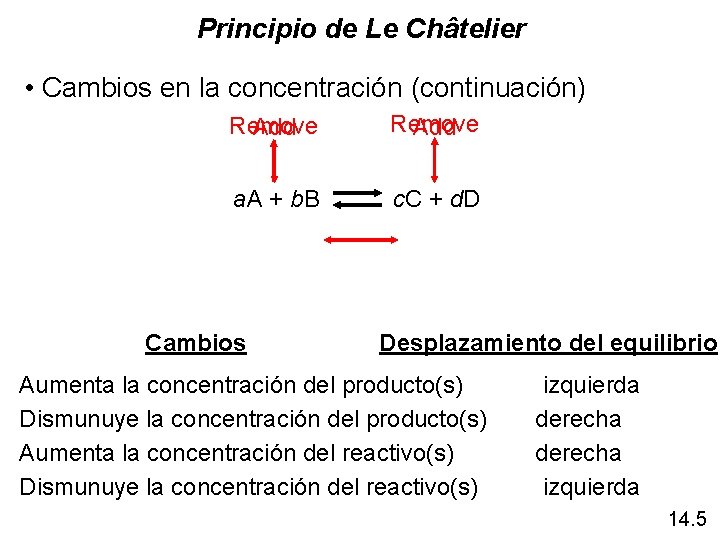
Principio de Le Châtelier • Cambios en la concentración (continuación) Remove Add a. A + b. B c. C + d. D Cambios Desplazamiento del equilibrio Aumenta la concentración del producto(s) Dismunuye la concentración del producto(s) Aumenta la concentración del reactivo(s) Dismunuye la concentración del reactivo(s) izquierda derecha izquierda 14. 5

Principio de Le Châtelier • Cambios en el volumen y presión A (g) + B (g) Cambio Aumenta la presión Disminuye la presión Aumenta el volumen Disminuye el volumen C (g) Desplazamiento del equilibrio Lado con menos moles de gas Lado con más moles de gas Lado con menos moles de gas 14. 5

Principio de Le Châtelier • Cambios en la temperatura Cambio Rx exotérmica Aumenta la temperatura K disminuye Disminuye la temperature K aumenta Rx endotérmica K aumenta K disminuye • Adicionando un catalizador • no cambia K • no desplaza la posición de un sistema en equilibrio • el sistema alcanzará el equilibrio más pronto 14. 5
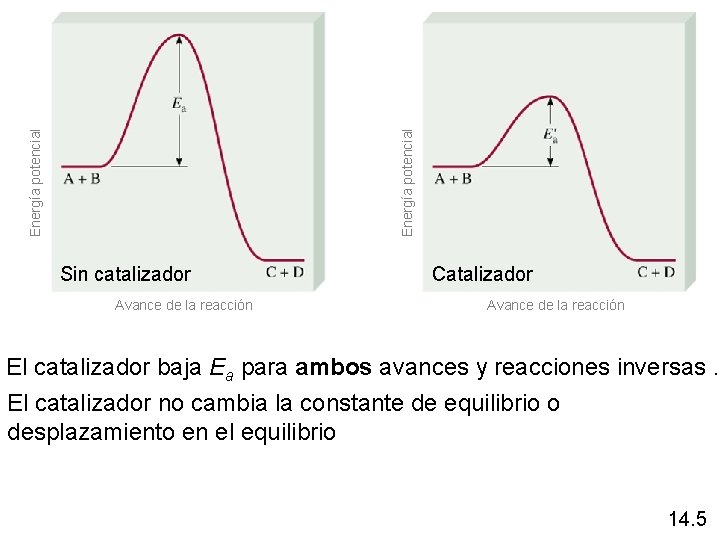
Energía potencial Sin catalizador Avance de la reacción Catalizador Avance de la reacción El catalizador baja Ea para ambos avances y reacciones inversas. El catalizador no cambia la constante de equilibrio o desplazamiento en el equilibrio 14. 5
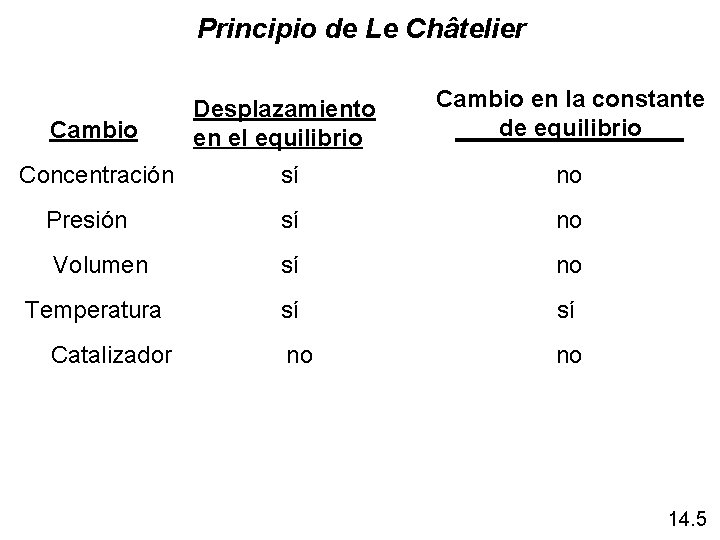
Principio de Le Châtelier Cambio Desplazamiento en el equilibrio Cambio en la constante de equilibrio Concentración sí no Presión sí no Volumen sí no Temperatura sí no no Catalizador 14. 5
- Slides: 26