Equilibrio de Complejos Cualquier especie formada por la

Equilibrio de Complejos "Cualquier especie formada por la asociación de dos o más entes químicos que puede existir libremente en solución. " Símil a una reacción ácido-base de Lewis
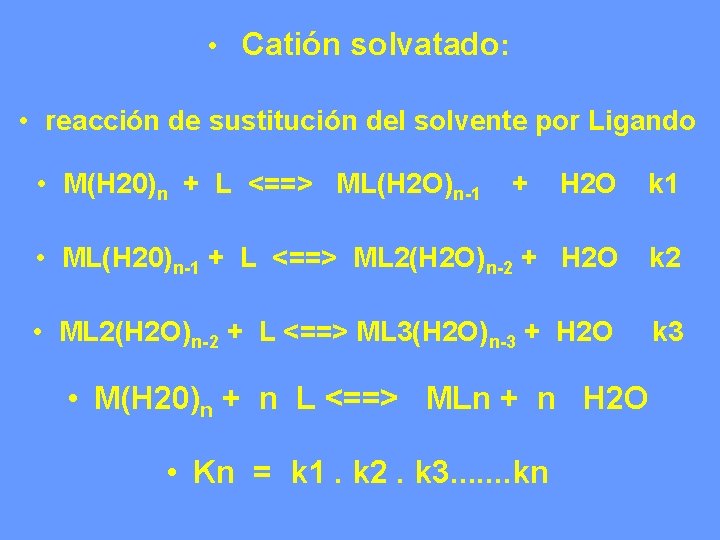
• Catión solvatado: • reacción de sustitución del solvente por Ligando • M(H 20)n + L <==> ML(H 2 O)n-1 + H 2 O k 1 • ML(H 20)n-1 + L <==> ML 2(H 2 O)n-2 + H 2 O k 2 • ML 2(H 2 O)n-2 + L <==> ML 3(H 2 O)n-3 + H 2 O k 3 • M(H 20)n + n L <==> MLn + n H 2 O • Kn = k 1. k 2. k 3. . . . kn

N : es el Nº coordinación máximo de L Depende de: a) nº y disposición espacial de los orbitales desocupados del ión b) tamaño del Metal (M) y Ligando (L) Factores que influyen en la coordinación : a) acidez catión con relación densidad de carga b) basicidad del ligando con electronegatividad c) configuración espacial del complejo

Iones pequeños : alta electropositividad > afinidad con L pequeños F>> Cl > Br > I iones altamente electronegativos (por ej. Hg+2), afinidad es a la inversa • En el estudio de los complejos se debe analizar la pareja M - L • Se debe considerar: • deformabilidad del cation central • polarizabilidad del ligando

L duros: alta electronegatividad (orbitales de alta Evacíos), difíciles de oxidar baja capacidad de donar electrones baja polarizabilidad, ej. F- L blandos a la inversa de lo anterior, ej. CN- ión M blandos ión M duros relación carga /radio (e/r) baja relación e/r alta, electrones externos fácil de excitar Mejor combinación para la formación de complejos es: M duro- L duro o M blando- L blando

Clasificación de Taube : (medidad de la reactividad) a) Estabilidad: tiene relación con la Ea, cambio de Energía libre estabilidad con el de la entropía (aumento del desorden del sistema) b) Reactividad: se relaciona con la VR de la sustitución de un L por otro • Se clasifican en lábil e inerte • Ejemplos: Cu(H 3 N)4++ , es lábil y además es estable. Fe(CN)6 -3 , es inerte e inestable Generalmente los complejos de Cr 3+ y Co 3+ son inertes e inestables

Equilibrios de formación: Estudio se hace sobre complejos lábiles y mononucleares M(H 20)n + L <==> ML(H 2 O)n-1 + H 2 O k 1 ML(H 20)n-1 + L <==> ML 2(H 2 O)n-2 + H 2 O k 2 ML 2(H 2 O)n-2 + L <==> ML(n-1)(H 20) + L <==> ML 3(H 2 O)n-3 + H 2 O MLn + H 2 O k Constante parcial de cada etapa Constante total = [MLn]/[M]. [L] = k 1. k 2. k 3. . . kn k 3 kn
![Constantes condicionales o de Ringbon a = fact. . [ ] fact depende de Constantes condicionales o de Ringbon a = fact. . [ ] fact depende de](http://slidetodoc.com/presentation_image/4554da00ceaa8d0e1694ee0fbf00edd9/image-8.jpg)
Constantes condicionales o de Ringbon a = fact. . [ ] fact depende de (fuerza iónica) (entre 0, 1 y 0, 5 varía poco ) K' = [MLn]'/ [M]'. [L]n ' [M]’ = [M] más todos los compuestos con M no unidos al L principal [L]’ = [L] más todas las especies con L no unidos al M principal Ejemplo : [Y]’ = [Y 4 -] + [YH 3 -] +[YH 22 -]. . +[YZ] [L]’ > o = que [L]
![Función de formación: • n = CL-[L]/CM • Es el número promedio de grupos Función de formación: • n = CL-[L]/CM • Es el número promedio de grupos](http://slidetodoc.com/presentation_image/4554da00ceaa8d0e1694ee0fbf00edd9/image-9.jpg)
Función de formación: • n = CL-[L]/CM • Es el número promedio de grupos coordinados unidos por ión metálico presente a una determinada [L] • para complejos mononucleares, depende sólo de L (pared mononuclear) • complejos polinucleares depende de CL y CM
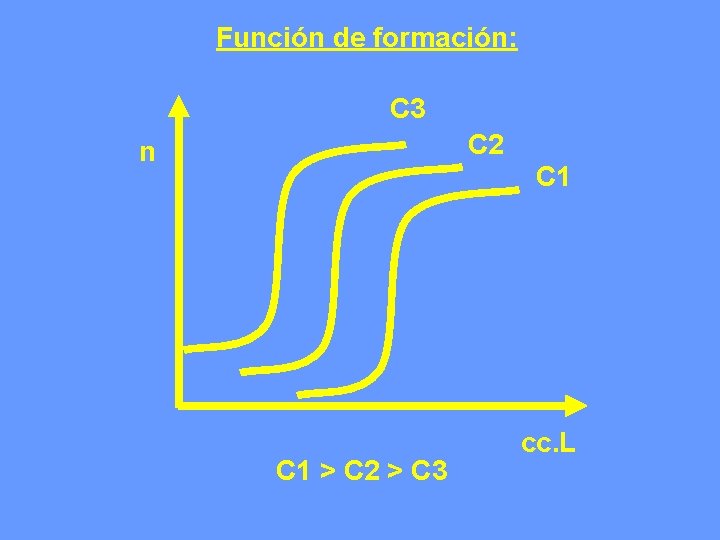
Función de formación: C 3 C 2 n C 1 > C 2 > C 3 C 1 cc. L
![Competencia de Equilibrio Acidez de catión: [Fe(SCN)5] = + 3 (OH)- <====> Fe(OH)3 + Competencia de Equilibrio Acidez de catión: [Fe(SCN)5] = + 3 (OH)- <====> Fe(OH)3 +](http://slidetodoc.com/presentation_image/4554da00ceaa8d0e1694ee0fbf00edd9/image-11.jpg)
Competencia de Equilibrio Acidez de catión: [Fe(SCN)5] = + 3 (OH)- <====> Fe(OH)3 + 5 SCNKi = 4 x 10 -7 ; Kt = Ki/P KPS = 10 -38 ; Kt = 1031 Basicidad del Ligando: [Ag(NH 3)2]+ + 2 H 30+ <======> Ag+ + 2 (NH 4)+ Ki = 4 x 10 -8 Kt = Ki /(Ka 2)2 ; Ka = 5, 5 x 10 -10 ; Kt = 1, 3 x 1011
![Formación de complejo más estable: [Ag(NH 3)2]+ + 2 CN- <==> [Ag(CN)2 ]- + Formación de complejo más estable: [Ag(NH 3)2]+ + 2 CN- <==> [Ag(CN)2 ]- +](http://slidetodoc.com/presentation_image/4554da00ceaa8d0e1694ee0fbf00edd9/image-12.jpg)
Formación de complejo más estable: [Ag(NH 3)2]+ + 2 CN- <==> [Ag(CN)2 ]- + 2 NH 3 Kt = Ki[Ag(NH 3)2]+/Ki[Ag(CN)2 ]Ki [Ag(NH 3)2]+ = 4 x 10 -8 ; Ki [Ag(CN)2 ]- = 10 -20 Kt = 4 x 1012 [Ni(CN)4]= + 2 Ag+ <==> 2 [Ag(NH 3)2]+ + Ni 2+

Enmascaramiento Ocurre cuando a una sustancia se le disminuye su concentración, de manera de impedir el producto de una reacción en forma apreciable Ejemplos a) Titulación de Pb++ en presencia de Ni++ con EDTA Se agrega CN- para complejar el Ni++ β[Ni(CN)4]= = 1030 ; β Ni. Y= = 1018, 6 ; β Pb. Y= = 1018, 3 b) Titulación de Ca++ en presencia de Mg++ con EDTA p. H = 12 ppta Mg(OH)2 y queda Ca++ en solución
![[M]e < [M]L [M]e concentración que deja libre el enmascarante [M]L concentración mínima límite [M]e < [M]L [M]e concentración que deja libre el enmascarante [M]L concentración mínima límite](http://slidetodoc.com/presentation_image/4554da00ceaa8d0e1694ee0fbf00edd9/image-14.jpg)
[M]e < [M]L [M]e concentración que deja libre el enmascarante [M]L concentración mínima límite para que la reacción sea apreciable Grado de enmascaramiento ºE = [Ag]L / [Ag]e debe ser > 1 KPS Ag. Cl = 1, 8 x 10 -10 ==> no precipitación Q < P Ejemplo: como enmascarar la precipitación de Ag. Cl con NH 3 Ki Ag(NH 3)2+ = 6, 3 x 10 -8 ; [Cl] = 1, 8 M; [Ag+] = 0, 1 M Concentración de NH 3 necesaria para enmascarar la precipitación 8 M

Aplicaciones Analíticas de los complejos a) Identificación de Ni con DMG aumento sensibilidad complejo rojo b) Separaciones analíticas Al+++ y Fe+++ ; Con (OH)- [Al(OH)4]- soluble; Fe(OH)3 precipitado Cd++, Cu++, Co++ Con CN- complejos de CNluego + S= precipita Cd. S color amarillo c) Titulación de Pb++ en presencia de Ni++ con EDTA Aumento selectividad enmascarando Ni++ con CNd) Disolución de metales Au 3+ + HNO 3 + 4 HCl ==> Au. Cl 4 - + NO + H 3 O+
![e) Estabilización o modificación de potenciales de oxidación Ecuación de Nerst relación [Oxidado]/[Reducido] f) e) Estabilización o modificación de potenciales de oxidación Ecuación de Nerst relación [Oxidado]/[Reducido] f)](http://slidetodoc.com/presentation_image/4554da00ceaa8d0e1694ee0fbf00edd9/image-16.jpg)
e) Estabilización o modificación de potenciales de oxidación Ecuación de Nerst relación [Oxidado]/[Reducido] f) Titulaciones g) Buffer ión metálico p. M = p. Kest + log [ML]/[L] Se utiliza en medios biológicos donde si los iones metálicos sufren pequeñas alteraciones pueden perjudicar los procesos metabólicos inclusive llevar a la muerte Bibliografía: Burriel Marti(Cualitativa) Kolthoff-Sandell 5º Ed. (Cuantitativa) Enciclopedia Kolthoff Qca. Analítica. Caps. 8 y 14 Underwood Equilibrios Químicos
- Slides: 16