EQUILIBRIO CIDOBASE Caractersticas CIDOS Tienen sabor agrio Son

EQUILIBRIO ÁCIDO-BASE

Características ÁCIDOS: ¡ ¡ ¡ Tienen sabor agrio. Son corrosivos para la piel. Enrojecen ciertos colorantes vegetales. Disuelven sustancias Atacan a los metales desprendiendo H 2. Pierden sus propiedades al reaccionar con bases. BASES: ¡ ¡ ¡ Tiene sabor amargo. Suaves al tacto pero corrosivos con la piel. Dan color azul a ciertos colorantes vegetales. Precipitan sustancias disueltas por ácidos. Disuelven grasas. Pierden sus propiedades al reaccionar con ácidos. 2

Definición de Arrhenius ¡ Publica en 1887 su teoría de “disociación iónica” l Hay sustancias (electrolitos) que en disolución se disocian en cationes y aniones. ÁCIDO: Sustancia que en disolución acuosa disocia cationes H+. ¡ BASE: Sustancia que en disolución acuosa disocia aniones OH–. ¡ 3

Disociación ÁCIDOS: ¡ AH (en disolución acuosa) A– + H+ ¡ Ejemplos: ¡ l l HCl (en disolución acuosa) Cl– + H+ H 2 SO 4 (en disolución acuosa) SO 42– + 2 H+ BASES: ¡ BOH (en disolución acuosa) B ¡ Ejemplo: ¡ l + + OH– Na. OH (en disolución acuosa) Na+ + OH– 4

Neutralización Se produce al reaccionar un ácido con una base por formación de agua: ¡ H+ + OH– — H 2 O ¡ El anión que se disoció del ácido y el catión que se disoció de la base quedan en disolución inalterados (sal disociada): ¡ Na. OH +HCl — H 2 O + Na. Cl (Na+ + Cl–) ¡ 5

Teoría de Brönsted-Lowry. ÁCIDOS: ¡ “Sustancia que en disolución cede H +”. ¡ BASES: ¡ “Sustancia que en disolución acepta H+”. ¡ 6

Par Ácido/base conjugado Siempre que una sustancia se comporta como ácido (cede H+) hay otra que se comporta como base (captura dichos H+). ¡ Cuando un ácido pierde H+ se convierte en su “base conjugada” y cuando una base captura H+ se convierte en su “ácido conjugado”. + ¡ ÁCIDO (HA) BASE (B) –H BASE CONJ. (A–) + H+ + +) ÁC. CONJ. (HB H+H+ – 7
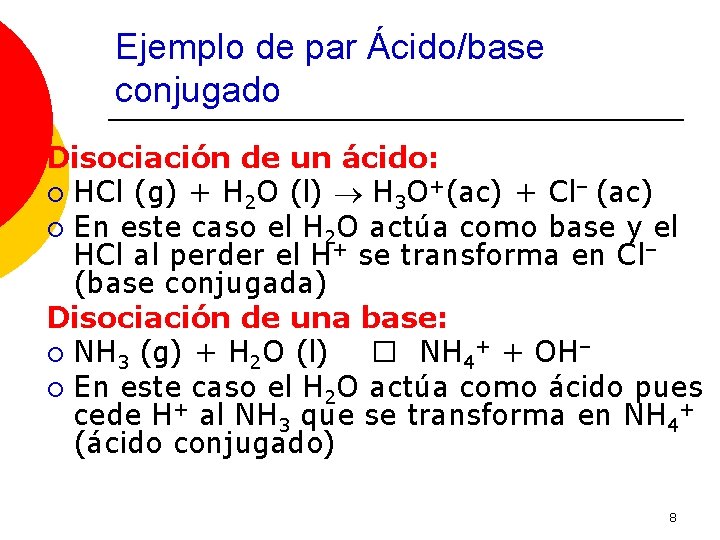
Ejemplo de par Ácido/base conjugado Disociación de un ácido: ¡ HCl (g) + H 2 O (l) H 3 O+(ac) + Cl– (ac) ¡ En este caso el H 2 O actúa como base y el HCl al perder el H+ se transforma en Cl– (base conjugada) Disociación de una base: ¡ NH 3 (g) + H 2 O (l) � NH 4+ + OH– ¡ En este caso el H 2 O actúa como ácido pues cede H+ al NH 3 que se transforma en NH 4+ (ácido conjugado) 8

Teoría de Lewis ÁCIDOS: ¡ “Sustancia que contiene al menos un átomo capaz de aceptar un par de electrones y formar un enlace covalente coordinado”. BASES: ¡ “Sustancia que contiene al menos un átomo capaz de aportar un par de electrones para formar un enlace covalente coordinado”. 9

Teoría de Lewis (Ejemplos) HCl (g) + H 2 O (l) H 3 O+(ac) + Cl– (ac) En este caso el HCl es un ácido porque contiene un átomo (de H) que al disociarse y quedar como H+ va a aceptar un par de electrones del H 2 O formando un enlace covalente coordinado (H 3 O+). ¡ NH 3 (g) + H 2 O (l) �NH 4+ + OH– En este caso el NH 3 es una base porque contiene un átomo (de N) capaz de aportar un par de electrones en la formación del enlace covalente coordinado (NH 4+). ¡ 10

Teoría de Lewis De esta manera, sustancias que no tienen átomos de hidrógeno, como el Al. Cl 3 pueden actuar como ácidos: ¡ Al. Cl 3 + : NH 3 Cl 3 Al: NH 3 ¡ 11
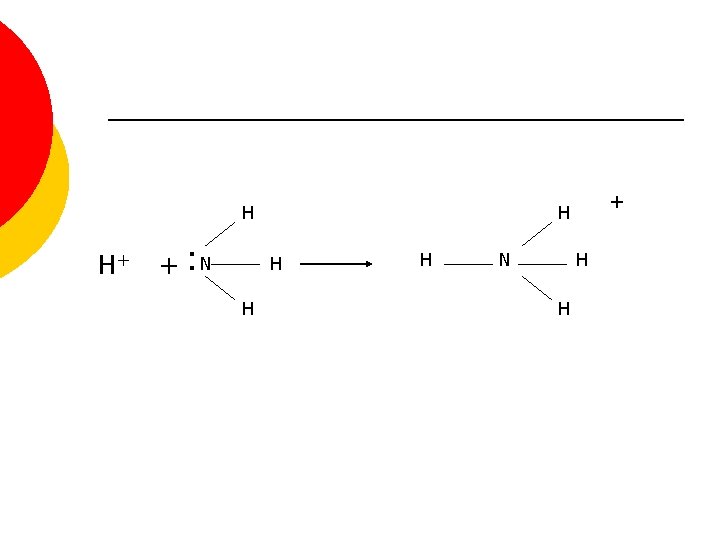
H H+ + : N H H + H H N H H
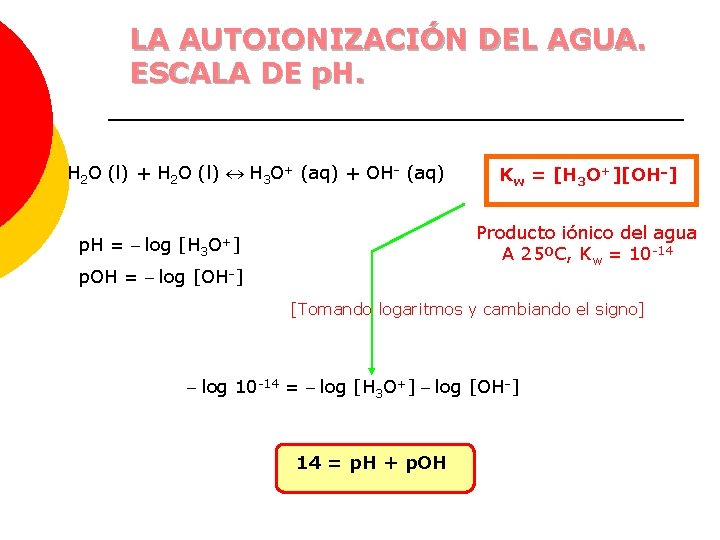
LA AUTOIONIZACIÓN DEL AGUA. ESCALA DE p. H. H 2 O (l) + H 2 O (l) H 3 O+ (aq) + OH- (aq) Kw = [H 3 O+][OH-] Producto iónico del agua A 25ºC, Kw = 10 -14 p. H = - log [H 3 O+] p. OH = - log [OH-] [Tomando logaritmos y cambiando el signo] - log 10 -14 = - log [H 3 O+] - log [OH-] 14 = p. H + p. OH
![Agua pura: [H 3 O+] = [OH-] ; [H 3 O+] = 10 -7 Agua pura: [H 3 O+] = [OH-] ; [H 3 O+] = 10 -7](http://slidetodoc.com/presentation_image_h/ecbc24794d01cf7020730564d3f9d0a7/image-14.jpg)
Agua pura: [H 3 O+] = [OH-] ; [H 3 O+] = 10 -7 Þ p. H = 7 [OH-] = 10 -7 Þ p. OH = 7 DISOLUCIÓN NEUTRA DISOLUCIÓN ÁCIDA DISOLUCIÓN BÁSICA [H 3 O+] = [OH-] p. H = 7 [H 3 O+] > [OH-] p. H < 7 [H 3 O+] < [OH-] p. H > 7 ácida 7 básica p. H

FUERZA DE ÁCIDOS Y BASES. CONSTANTES DE IONIZACIÓN. Fuerza de un ácido o base: mayor o menor tendencia a transferir o aceptar un protón. Medida cuantitativa: constante de equilibrio de su reacción con agua. HA(aq) + H 2 O (l) H 3 O+ (aq) + A- (aq) Constante de acidez (de disociación, de ionización) Mayor fuerza de un ácido: mayor será Ka (menor p. Ka) Caso extremo: ácido fuerte (p. ej. HCl, HNO 3, HCl. O 4, . . . ) se encuentra totalmente disociado (Ka >> 1, Ka ¥)

Análogamente con las bases: B (aq) + H 2 O (l) BH+ (aq) + OH- (aq) Constante de basicidad Mayor fuerza de una base: mayor será Kb (menor p. Kb) Caso extremo: base fuerte (p. ej. Na. OH, KOH, . . . ) se encuentra totalmente disociada (Kb >> 1, Kb ¥) En el caso de un par ácido-base conjugado, Ka y Kb están relacionadas B (aq) + H 2 O (l) BH+ (aq) + OH- (aq) Kw = K a K b

p. H, p. OH y p. Kw p. X= -log. X P ordenador de X, reduce el rango de valores de X. Por lo tanto, se tiene: p. H, p. OH, p. K p. H = -log[H+] p. OH = -log[OH-] p. Kw = -log(Kw)

A 25 ºC: p. Kw = -log(1, 0 x 10 -14) p. Kw = 14, 0 p. Kw = -log([H+] • [OH-]) = -log[H+] -log[OH-] p. Kw = p. H + p. OH = 14. 0 a 25 o. C

Cuantificación de los sistemas de ácidos y bases 1. Acidos y bases fuertes: Ø 100% ionizados Ø HCl ejemplo de ácido fuerte Ø Disuelto en agua, la solución resultante contiene iones Cl-, H+, OH-

Condiciones que se cumplen en este tipo de equilibrio: ¡ ¡ Equilibrio de disociación del agua Balance de masa: l ¡ relaciona especies resultante con la concentración nominal Electroneutralidad: l iones positivos = iones negativos

Equilibrio ionización del agua HCl ácido fuerte, por lo tanto ecuación se reduce a: [H+] = [OH-] + [Cl-]
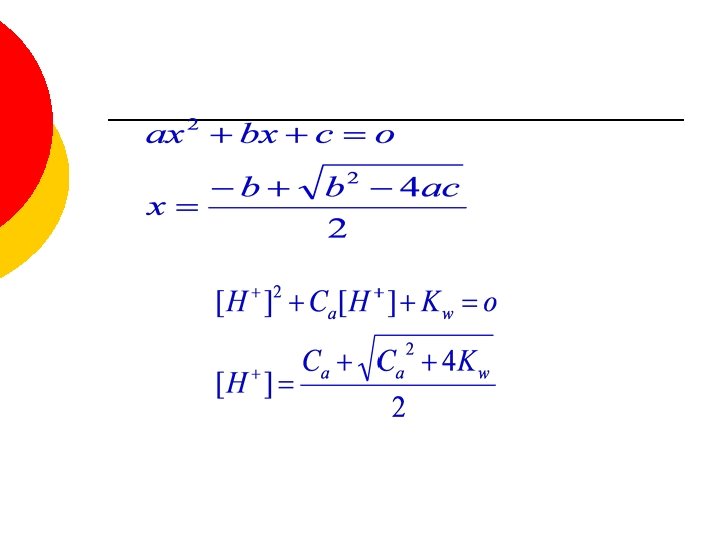

Ácidos débiles HA H+ + A- ALGUNOS ACIDOS DEBILES, SUS CONTANTES DE DISOCIACION Y p. Ka a 25ºC Ácido Fórmula Láctico Acético Cianhídrico Ka p. Ka CH 3 CH(OH)CO 2 H 8. 4 x 10 -4 3. 08 CH 3 CO 2 H 1. 8 x 10 -5 4. 75 4. 9 x 10 -10 9. 31 HCN

Cálculos de p. H Según los datos entregados y las características de las sustancias a medir, existen varias formas. ¡ Se estudiaran 7 de ellas: ¡

1) p. H en forma directa ¡ Calcular el p. H de una solución cuya [H 3 O+] es 0, 0008 M. Indique si es ácido o base.
![2) p. H a partir de Kw. ¡ Se tiene una sustancia cuya [OH-] 2) p. H a partir de Kw. ¡ Se tiene una sustancia cuya [OH-]](http://slidetodoc.com/presentation_image_h/ecbc24794d01cf7020730564d3f9d0a7/image-26.jpg)
2) p. H a partir de Kw. ¡ Se tiene una sustancia cuya [OH-] es 0, 0005 M. calcular su [H 3 O+], p. OH y p. H.

3) p. H a partir del valor de Ka o Kb ¡ Se tiene una sustancia cuya Ka = 1, 2 x 10 – 3 calcular el p. H cuando se tienen 0, 01 M de ésta.

4) p. H en ácidos y bases débiles p. H = p Ka + log [A-] / [HA] ¡ Calcular el p. H de una sustancia cuyo p. Ka = 4, 18 cuando se tienen 0, 02 M de la sustancia y se disocia al 80%.

5) Calculo de p. H en reacciones ácido – base fuertes, sin buffer. Se tienen 10 m. L de HCl al 0, 02 M que reaccionan con Na. OH al 0, 02 M. Calcular p. H cuando: a) Se usan 5 m. L de Na. OH b) Se usan 10 m. L de Na. OH c) Se usan 15 m. L de Na. OH ¡

6) p. H en sales débiles ¡ Se tiene una solución de acetato de sodio al 0, 05 M. si el p. Ka del ácido acético es 5. Calcular el p. H

7) p. H de una solución reguladora, buffer o tampón. ¡ Primero veamos que significa y como funcionan las soluciones reguladoras.

DISOLUCIONES AMORTIGUADORAS. Para muchos procesos, el control del p. H resulta fundamental (p. ej. reacciones bioquímicas) Disoluciones amortiguadoras (o tampón): Disoluciones que mantienen un p. H aproximadamente constante cuando se agregan pequeñas cantidades de ácido o base o cuando se diluyen. Composición Cantidades sustanciales de un ácido débil y de su base conjugada (o una base débil y su ácido conjugado). (p. ej. : CH 3 COOH/CH 3 COONa)

Mecanismo de acción: HA (aq) + H 2 O (l) H 3 O+ (aq) + A- (aq) Si al equilibrio le añado, p. ej. , un ácido, se desplazará a la izquierda, disminuirá el cociente [A-]/[HA] y el p. H bajará. Pero si la cantidad añadida es pequeña comparada con las cantidades (grandes) que hay de A- y HA, el cociente cambiará muy poco y el p. H apenas se modificará. P. ej. : * si añado 0. 001 moles de HCl a un 1 L de agua, el p. H pasa de 7 a 3. * si añado 0. 001 moles de HCl a un 1 L de disolución que contiene 0. 7 moles de acético y 0. 6 moles de acetato sódico, el p. H pasa de 4. 688 a 4. 686.

¿Cómo calcular el p. H de una disolución tampón? ¿Cómo estimar aproximadamente el p. H de una disolución tampón? Exacta Dado que las concentraciones iniciales de ácido y de su base conjugada son grandes, se puede suponer que las cantidades que desaparecerán y que aparecerán mientras se va alcanzando el equilibrio serán pequeñas, comparadas con las iniciales. Por tanto, en la fórmula anterior las concentraciones en el equilibrio se pueden aproximar por las concentraciones iniciales.

Características importantes de una disolución amortiguadora: * Su p. H Þ depende de Ka y de las concentraciones * Su capacidad amortiguadora Capacidad amortiguadora: Cantidad de ácido o base que se puede agregar a un tampón antes de que el p. H comience a cambiar de modo apreciable. ¿De qué depende? * Del número de moles de ácido y base (deben ser altos para que la capacidad también lo sea) * Del cociente [base]/[ácido]. para que la capacidad sea alta, ha de ser próximo a 1. Si es < 0. 1 ó > 10, no será muy eficiente. Mayor eficiencia: cuando p. H = p. Ka)

Ejemplo

INDICADORES. Indicadores: Ácidos o bases débiles cuyas formas ácido/base conjugadas presentan colores diferentes. HInd (aq) + H 2 O (l) H 3 O+ (aq) + Ind- (aq) Color A Color B Cuando a una disolución le añadimos un indicador, estarán presentes las dos especies HInd e Ind-.
![¿Qué color veré? • Si [HInd]/[Ind-] ³ 10 Þ Color A (predomina forma ácida) ¿Qué color veré? • Si [HInd]/[Ind-] ³ 10 Þ Color A (predomina forma ácida)](http://slidetodoc.com/presentation_image_h/ecbc24794d01cf7020730564d3f9d0a7/image-38.jpg)
¿Qué color veré? • Si [HInd]/[Ind-] ³ 10 Þ Color A (predomina forma ácida) • Si [HInd]/[Ind-] £ 0. 1 Þ Color B (predomina forma básica) • Si 0. 1< [HInd]/[Ind-]< 10 Þ Color mezcla de A y B El cociente depende de la Ka y del p. H: • Si [HInd]/[Ind-] ³ 10 Þ [H 3 O+] ³ 10 KInd Þ p. H £ p. KInd – 1 Color A (predomina forma ácida) • Si [HInd]/[Ind-] £ 0. 1 Þ [H 3 O+] £ 0. 1 KInd Þ p. H ³ p. KInd +1 Color B (predomina forma básica) • Si 0. 1< [HInd]/[Ind-]< 10 Þ p. KInd – 1 < p. H < p. KInd +1 Mezcla A y B Intervalo de viraje (2 unidades de p. H)
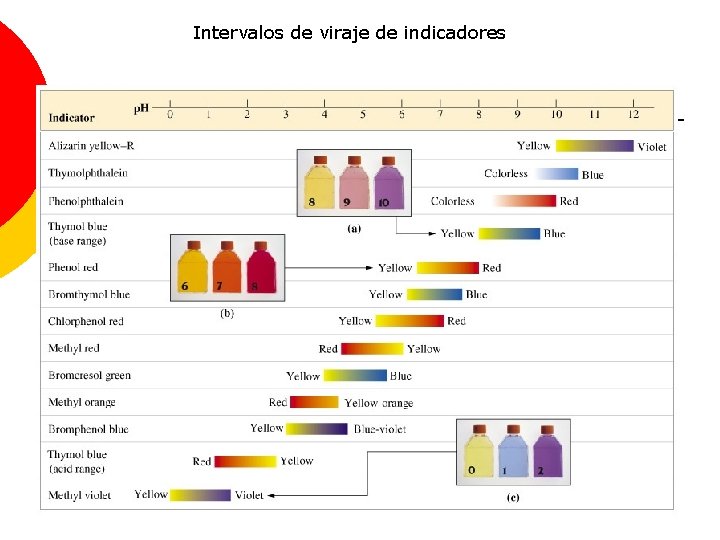
Intervalos de viraje de indicadores

VALORACIONES ÁCIDO-BASE. ¿Cómo podemos determinar la concentración de un ácido o de una base en una disolución? Método más empleado: valoración ácido-base Una disolución que contiene una concentración conocida de base (o ácido) se hace reaccionar con una disolución de ácido (o de base) de concentración desconocida. Medimos el volumen de la disolución de base (o ácido) necesario para que consuma (neutralice) todo el ácido (o base). Cuando se logra la neutralización completa: Punto de equivalencia
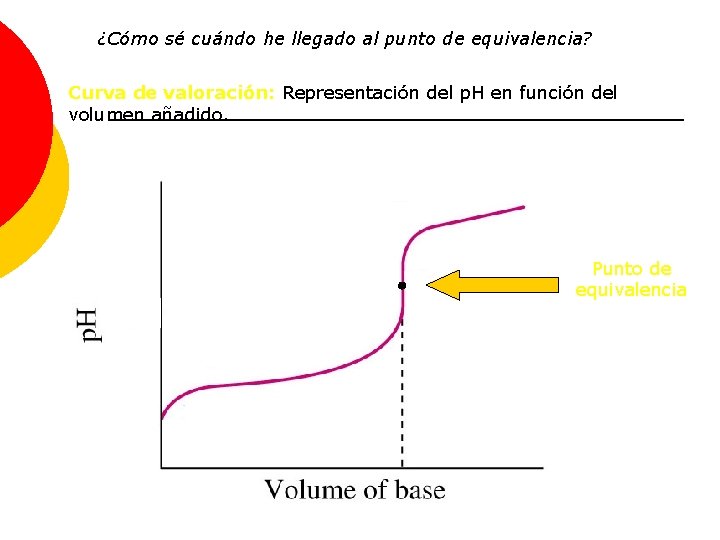
¿Cómo sé cuándo he llegado al punto de equivalencia? Curva de valoración: Representación del p. H en función del volumen añadido. Punto de equivalencia

¿Cuál es el p. H del punto de equivalencia? • Si valoro ácido fuerte con base fuerte (o al revés) Þ p. H = 7 • Si valoro ácido débil con base fuerte Þ p. H > 7 • Si valoro base débil con ácido fuerte Þ p. H < 7 ¿Cómo calcular el p. H de ese punto o de cualquier punto de la curva? Con el tratamiento exacto. ¿Cómo sé que he llegado al punto de equivalencia sin necesidad de representar la curva de valoración entera? Mediante un indicador apropiado Apropiado: que cambie de color justo cuando la reacción llega al punto de equivalencia.
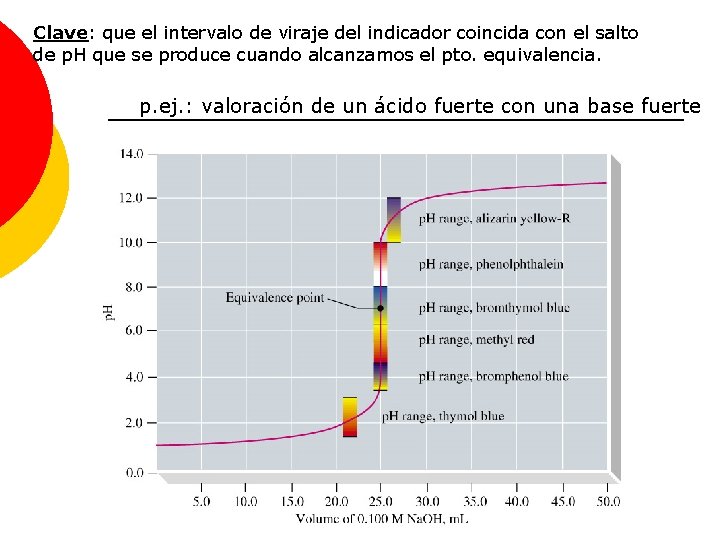
Clave: que el intervalo de viraje del indicador coincida con el salto de p. H que se produce cuando alcanzamos el pto. equivalencia. p. ej. : valoración de un ácido fuerte con una base fuerte
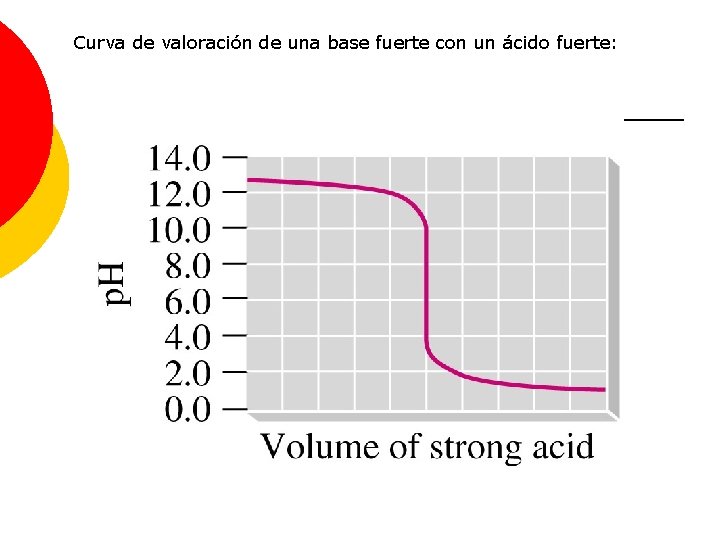
Curva de valoración de una base fuerte con un ácido fuerte:
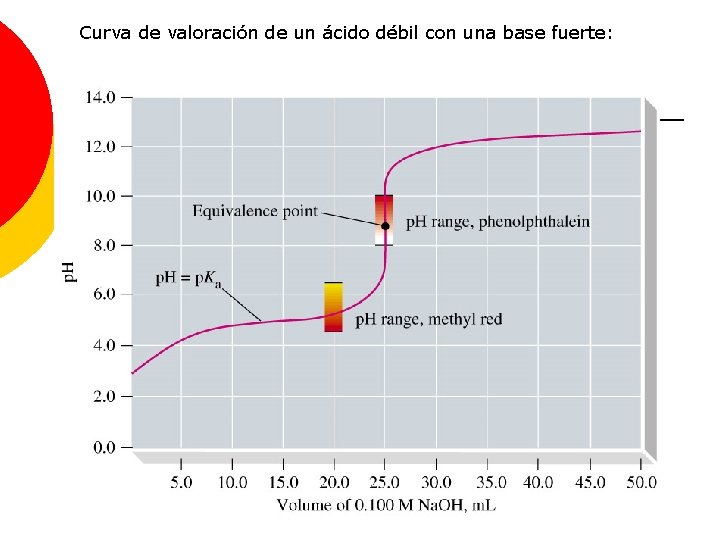
Curva de valoración de un ácido débil con una base fuerte:
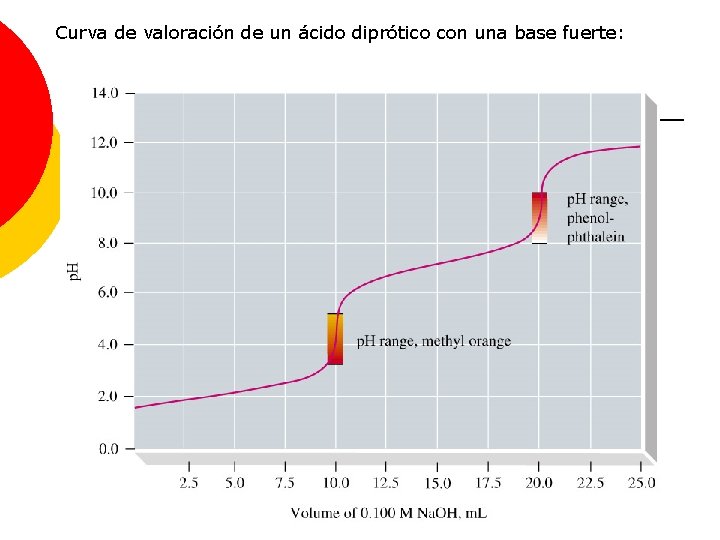
Curva de valoración de un ácido diprótico con una base fuerte:
- Slides: 46