Equilibrio AcidoBase Prof M Pinzani p H H

Equilibrio Acido-Base Prof. M. Pinzani
![p. H [H+] Pa. CO 2 Partial pressure O 2 HCO 3 - Bicarbonate p. H [H+] Pa. CO 2 Partial pressure O 2 HCO 3 - Bicarbonate](http://slidetodoc.com/presentation_image_h2/ec4d4f91149f7fbb5694471107dab04b/image-2.jpg)
p. H [H+] Pa. CO 2 Partial pressure O 2 HCO 3 - Bicarbonate BE Base excess Sa. O 2 Oxygen Saturation

BE - eccesso di basi - esprime la componente metabolica dell’eq. acido/base ed equivale ai mm. Eq di bicarbonato che devo aggiungere a 1 L di sangue di un soggetto con Pa. CO 2 normale per riportare il p. H a 7. 40. n. v. : +/- 2 - al disotto di - 2 si è consumato bicarbonato per causa metabolica, acidosi metabolica. - al disopra di +2 c’è un eccesso di bicarbonati, alcalosi metabolica.

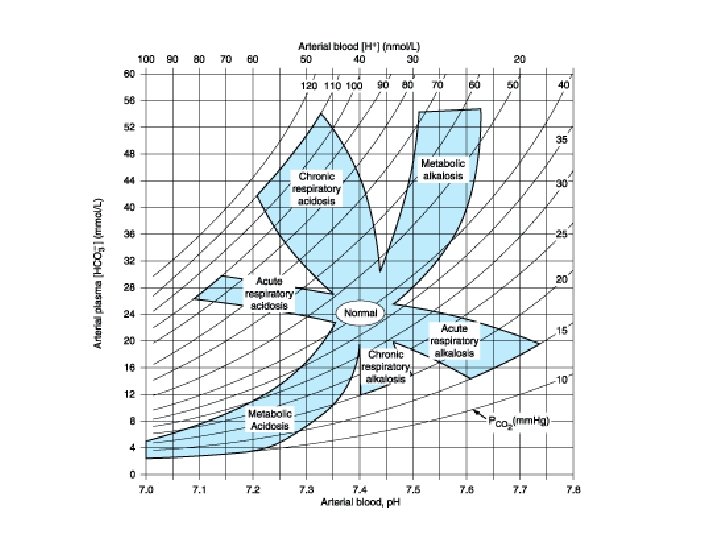
![p. H or [H+] nmol/L p. H 20 25 30 35 40 45 50 p. H or [H+] nmol/L p. H 20 25 30 35 40 45 50](http://slidetodoc.com/presentation_image_h2/ec4d4f91149f7fbb5694471107dab04b/image-5.jpg)
p. H or [H+] nmol/L p. H 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 126 158 7. 70 7. 60 7. 52 7. 45 7. 40 7. 35 7. 30 7. 26 7. 22 7. 19 7. 15 7. 12 7. 10 7. 07 7. 05 7. 02 7. 00 6. 90 6. 80 Reference ranges: [H+]: 35 - 45 nmol/L p. H: 7. 45 - 7. 35
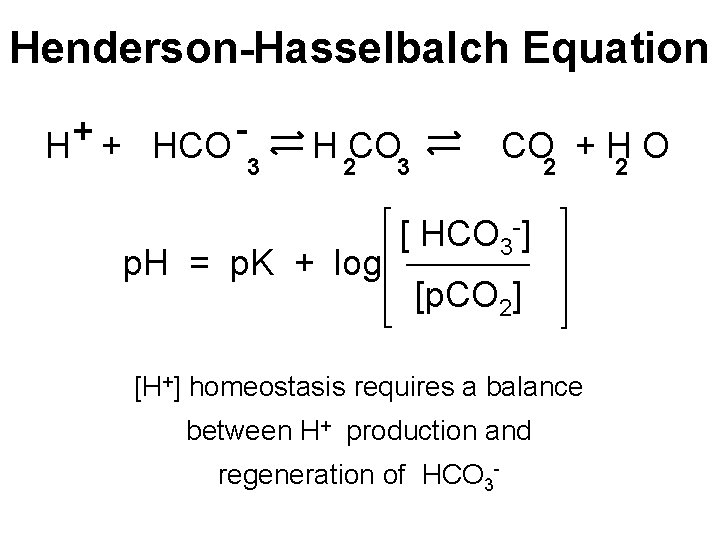
Henderson-Hasselbalch Equation + HCO 3 H 2 CO 3 p. H = p. K + log CO 2 + H 2 O [ HCO 3 -] [p. CO 2] [H+] homeostasis requires a balance between H+ production and regeneration of HCO 3 -
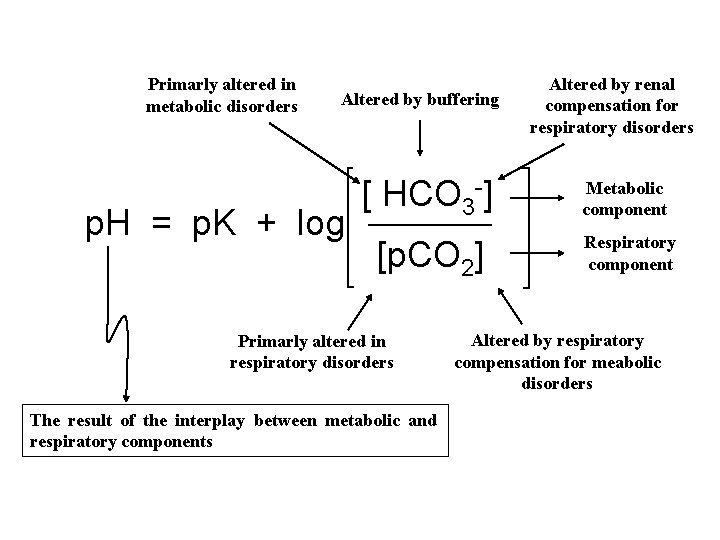
Primarly altered in metabolic disorders Altered by buffering p. H = p. K + log [ HCO 3 -] [p. CO 2] Primarly altered in respiratory disorders The result of the interplay between metabolic and respiratory components Altered by renal compensation for respiratory disorders Metabolic component Respiratory component Altered by respiratory compensation for meabolic disorders
![Acid-Base Homeostasis Metabolism Input Output Maintenance of Normal [H+] Buffers Acid-Base Homeostasis Metabolism Input Output Maintenance of Normal [H+] Buffers](http://slidetodoc.com/presentation_image_h2/ec4d4f91149f7fbb5694471107dab04b/image-8.jpg)
Acid-Base Homeostasis Metabolism Input Output Maintenance of Normal [H+] Buffers
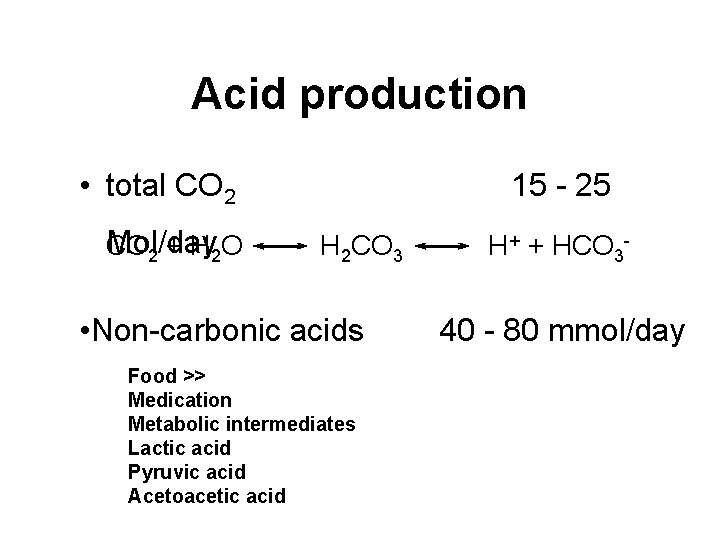
Acid production • total CO 2 Mol/day CO 2 + H 2 O 15 - 25 H 2 CO 3 • Non-carbonic acids Food >> Medication Metabolic intermediates Lactic acid Pyruvic acid Acetoacetic acid H+ + HCO 3 - 40 - 80 mmol/day

Nonvolatile acids are removed instantaneously from body fluids by reaction with buffers. In extracellular fluid, bicarbonate is converted to water and carbon dioxide, which is excreted by the lungs. Although this mechanism minimizes changes in acidity, it destroys bicarbonate and uses up cell buffer capacity.

Buffering Systems – Carbonic Il sistema tampone Acid-Bicarbonate ritenuto di maggiore importanza il sistema acido carbonico– è Haemoglobin bicarbonato , considerato come sistema aperto. – Phosphate Ciò è dovuto al fatto che esistono precisi – Proteins meccanismi fisiologici nella regolazione delle – Ammonia componenti fondamentali (la CO 2 è regolata - dal rene). – respiratorio, Misc organic acids dal sistema l’HCO 3
Sites of Acid-base metabolism Lungs Kidneys GI tract Liver

Respiratory Component Ø function of the lungs Ø Carbonic acid H 2 CO 3 Ø Approximately of CO 2 98% normal metabolites are in the form CO 2 + H 2 O H 2 CO 3 Ø excess CO 2 exhaled by the lungs

Role of the Lungs The normal level of CO 2 in body fluids is fixed around 40 mm. Hg by the lungs. Although CO 2 reacts with water and body buffers during transport from cells to pulmonary alveoli, no net change in body fluid composition results, since CO 2 excreted by the lungs is equal to the CO 2 produced by cells. The principal acid product of metabolism is CO 2, equivalent to potential carbonic acid.

Tissue Gas Exchange CO 2 CO A livello alveolare, l’ossigenazione dell’Hb sposta gli H+ legati ai - formando H CO e quindi + tamponi che si combinano con HCO 3 2 la CO 2 viene eliminata. 2 HCO +H H Hb+O H +Hb. O La riduzione della Pa. O del glomo - 2 (rilevata + dai chemocettori + carotideo) e l’aumento 3 della Pa. CO 2 (rilevata dai chemocettori 2 del centro respiratorio midollare) sono i parametri che nel soggetto normale consentono di mantenere un’ossigenazione adeguata e valori di Pa. CO 2 entro i limiti fisiologici nonostante il notevole carico quotidiana di CO 2. Cl

Metabolic Component Ø Function of the kidneys Ø base bicarbonate Na HCO 3 + into the urine and reabsorbing Process of kidneys excreting H Ø HCO 3 into the blood from the renal tubules 1) active exchange Na+ for H+ between the tubular cells and glomerular filtrate 2) carbonic anhydrase is an enzyme that accelerates hydration/dehydration CO 2 in renal epithelial cells

Role of the Kidney 1) retention of extracellular bicarbonate 2) excretion of protons of nonvolatile acids produced by metabolic processes. Both functions are served by secretion of protons into tubular fluids (Na-H+-ATPasi pump). Protons secreted are derived from carbonic acid (= CO 2), removal of protons generates bicarbonate in the tubular cell. This bicarbonate is reabsorbed with filtered sodium. When secreted protons are buffered by filtered bicarbonate, it is destroyed (not destroyed when protons are buffered by other urinary buffers). The bicarbonate lost in this process is replaced by bicarnonate generated in tubular cells.

Secreted H+ has four possible fates - 1 - about 98% of secreted H+ titrates is filtered HCO 3 - in a reclamation process - 2 - about 1% is buffered by NH 3 to form NH 4 - 3 - about 1% is buffered by other tubular buffers, for the most part HPO 4 --, to form titratable acid - 4 - a minute amount of H+ remains free in the final urine
![Renal Acid Excretion The kidneys regulate plasma [HCO 3 -] and acid-base balance by Renal Acid Excretion The kidneys regulate plasma [HCO 3 -] and acid-base balance by](http://slidetodoc.com/presentation_image_h2/ec4d4f91149f7fbb5694471107dab04b/image-19.jpg)
Renal Acid Excretion The kidneys regulate plasma [HCO 3 -] and acid-base balance by reclaming filtered HCO 3 - and by generating new HCO 3 - to replace that lost internally in titrating metabolic acid and externally from the gastrointestinal tract. Secretion of H+: - to reclaim filtered HCO 3 secretion of H+ that is not needed to reclaim filtered HCO 3 - results in the generation of new HCO 3 -, and formation of NH 4+ and titrable acid. -
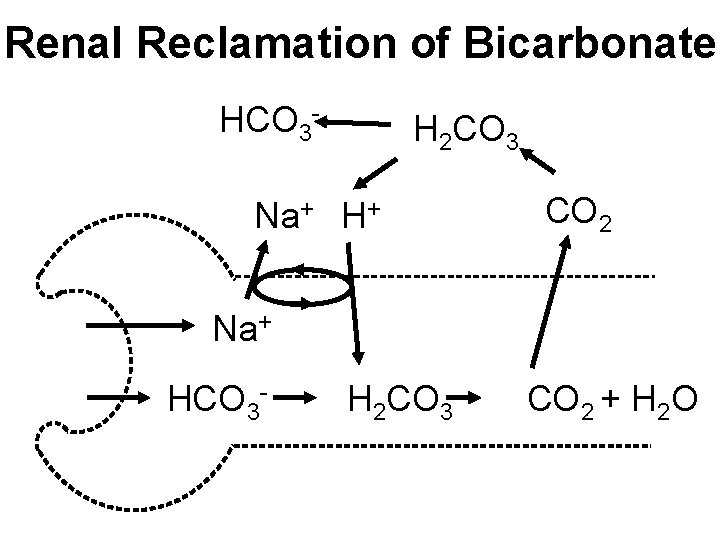
Renal Reclamation of Bicarbonate HCO 3 - H 2 CO 3 Na+ H+ CO 2 Na+ HCO 3 - H 2 CO 3 CO 2 + H 2 O
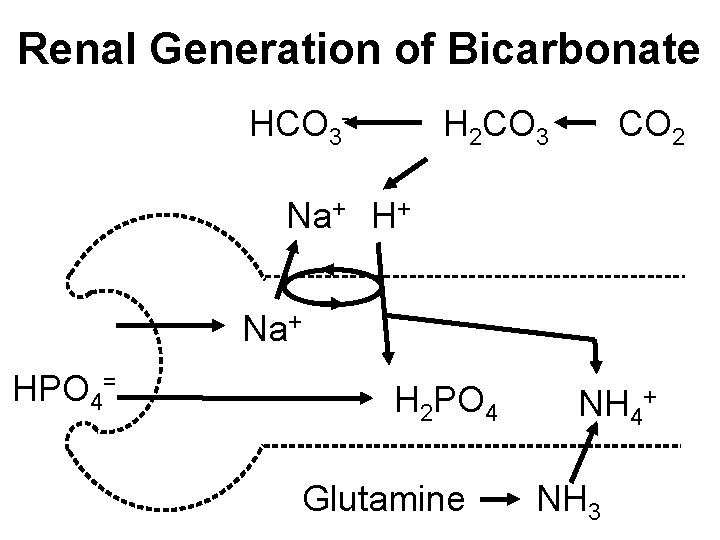
Renal Generation of Bicarbonate HCO 3 - H 2 CO 3 CO 2 Na+ H+ Na+ HPO 4= H 2 PO 4 Glutamine NH 4+ NH 3
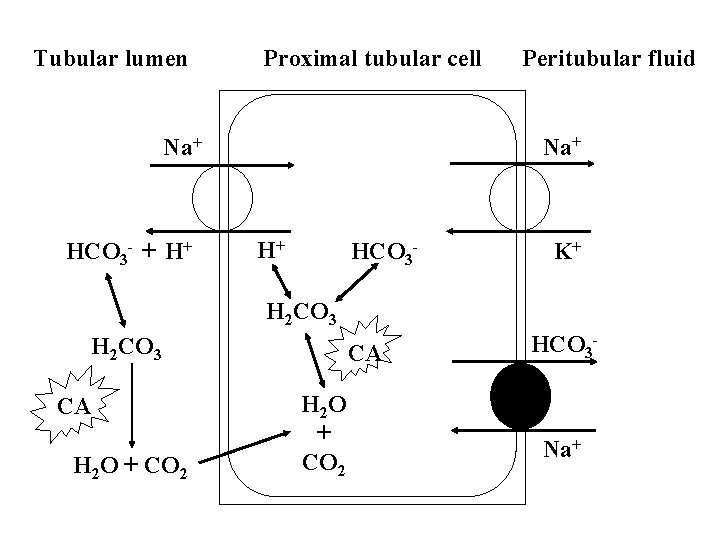
Tubular lumen Proximal tubular cell Na+ HCO 3 - + H+ Peritubular fluid H+ HCO 3 - K+ H 2 CO 3 CA H 2 O + CO 2 HCO 3 - Na+
Mineralo-corticoid Action in the Kidney
Acid-Base in the G-I Tract CO 2 + HCO 3 -

Equilibrio AB: valori normali p. H 7. 35 – 7. 45 (7. 38 - 7. 42) Pa. CO 2 35 – 45 mm. Hg Pa. O 2 80 – 100 mm. Hg HCO 3 22 – 26 mmol/L BE -2 +2 Sa. O 2 >95%

Acid-Base Pathology Acidosis Acidosi: eccesso relativo di radicali acidi nel sangue per Metabolic accumulo oppure perdita di radicali basici. Alkalosis Alcalosi: eccesso relativo di radicali basici nel sangue per accumulo o perdita di radicali acidi. Acidosis Respiratory Alkalosis

Acidosis p. H < 7. 35 Alkalosis p. H > 7. 45 PCO 2 > 45 PCO 2 < 35 HCO 3 < 22 HCO 3 > 26
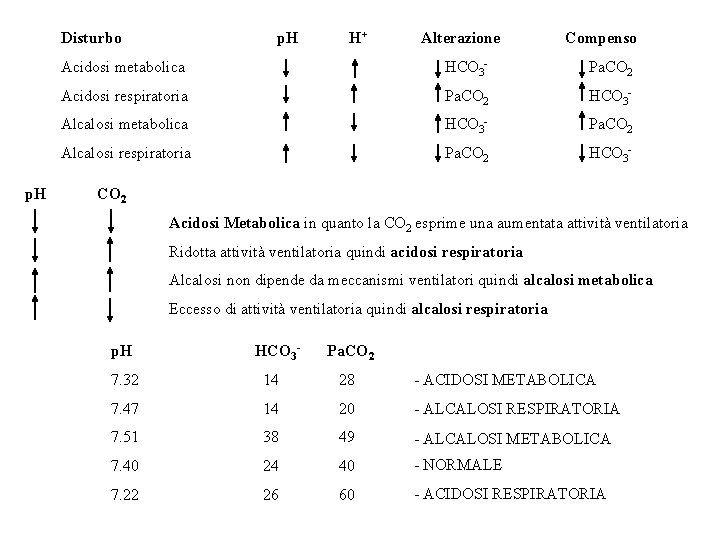
Disturbo p. H H+ Alterazione Compenso Acidosi metabolica HCO 3 - Pa. CO 2 Acidosi respiratoria Pa. CO 2 HCO 3 - Alcalosi metabolica HCO 3 - Pa. CO 2 Alcalosi respiratoria Pa. CO 2 HCO 3 - CO 2 Acidosi Metabolica in quanto la CO 2 esprime una aumentata attività ventilatoria Ridotta attività ventilatoria quindi acidosi respiratoria Alcalosi non dipende da meccanismi ventilatori quindi alcalosi metabolica Eccesso di attività ventilatoria quindi alcalosi respiratoria p. H HCO 3 - Pa. CO 2 7. 32 14 28 - ACIDOSI METABOLICA 7. 47 14 20 - ALCALOSI RESPIRATORIA 7. 51 38 49 - ALCALOSI METABOLICA 7. 40 24 40 - NORMALE 7. 22 26 60 - ACIDOSI RESPIRATORIA

Alterazione primitiva Compenso e sua entità Acidosistabilire Metabolica HCO Diminuzione di 1. 2 mm. Hg della Pa. CO per è Per se l’alterazione acido-base in atto ogni decremento degli HCO di 1 m. Eq/L semplice oppure complessa, è sufficiente conoscere Alcalosi Metabolica HCO compensatoria Aumento della Pa. CO di 0. 7 mm. Hg per ogni l’entità della risposta prevedibile per aumento di 1 m. Eq/L di HCO ogni alterazione primitiva e quindi valutare se l’entità Acidosi Respiratoria Pa. CO corrisponde o meno a quanto del compenso in atto acuta Aumento degli HCO di 1 m. Eq/L per ogni teoricamente previsto. aumento di 10 mm. Hg di Pa. CO , in quanto 3 3 2 3 2 sono solo parzialmente funzionanti i meccanismi renali cronica Aumento degli HCO 3 - di 3. 5 m. Eq/L per ogni aumento di 10 mm. Hg di Pa. CO 2, in quanto i meccanismi renali sono a pieno regime Il compenso atteso si basa sull’osservazione che per Alcalosi Respiratoria Pa. CO una variazione primitiva di PCO o di bicarbonati, acuta Riduzione 2 degli HCO di 2 m. Eq/L per ogni decremento di 10 mm. Hg della Pa. CO esistono delle quote di compenso. 2 3 2 cronica Riduzione degli HCO 3 - di 5 m. Eq/L per ogni decremento di 10 mm. Hg della Pa. CO 2

Esempio: tasso di HCO 3 - di 14 m. Eq/L (cioè ridotto di 10 rispetto al v. n. di 24) ci dovremmo aspettare un decremento della Pa. CO 2 che da 40 mm. Hg dovrebbe passare a 28 mm. Hg (10 X 1. 2) = 12 mm. Hg (cioè 40 -12 = 28). p. H = 7, 32 HCO 3 - = 14 Pa. CO 2 = 28 rappresenta un quadro di acidosi metabolica pura. Se la Pa. CO 2 fosse 35 mm. Hg, sarebbe associata un’alterazione che determina un aumento della Pa. CO 2 e questa alterazione è l’acidosi respiratoria.

Qualora non si riesca ad ottenere un campione di sangue arterioso Ogni 10 mm. Hg di Pa. CO 2 il p. H si sposta di 10 decimali. La differenza Artero-Venosa di CO 2è un parametro fisso (5 mm. Hg), Nel sangue venoso è presente una maggiore quota di bicarbonati, va quindi applicata una correzione di 0. 02. Dunque da un campione di sangue venoso posso ottenere una buona stima del p. H, Pa. CO 2 e BE.

Metabolic Alkalosis p. H 7. 50 Pa. CO 2 45 HCO 3 30

Cause di Alcalosi Metabolica Perdite di H+ Eccesso di HCO 3 Alcalosi da contrazione della volemia Perdite di H+ Eccesso -di. Gastroenteriche HCO 3 - rimozione di secrezioni gastriche tramite vomito o SNG - Trasfusioni diantiacida sangue in particolare con resine a scambio ionico terapia - Somministrazione di Na. HCO diarrea con perdite di cloruri 3 - Sindrome da eccessivo apporto di alcali col latte - Renali diuretici d’ansa o tiazidici Alcalosi da contrazione della volemia eccesso di mineralcorticoidi dopo ipercapnia cronica - Diuretici dell’ansa bassa introduzione di cloruri - Perdite alte gastriche in pazienti con acloridria dosi di carbencillina o di altri derivati della pennicillina - Sudorazione abbondante in pazienti con fibrosi cistica ipercalcemia compresa la Milk-alkali syndrome - Passaggio all’interno delle cellule ipopotassiemia alimentazione dopo digiuno prolungato

L’ipovolemia agisce sia come causa di alcalosi metabolica se i liquidi perduti contengono minime quote di HCO 3 - (alcalosi da contrazione), ma soprattutto come fattore rilevante nel mantenimento dell’alcalosi. Nelle condizioni di ipovolemia (stati edematosi, CHF, cirrosi epatica, vomito, diarrea), l’aumentato riassorbimento di HCO 3 - è legato all’iperaldosteronismo secondario che, aumentando la quota di Na+ riassorbita a livello dei dotti collettori, favorisce la secrezione di H+. La deplezione di cloruri mantiene l’alcalosi metabolica attivando sia la macula densa con produzione di renina ed iperaldosteronismo, si la pompa H+-ATP-asi presente nei tubuli collettori. Anche l’ipo. Kaliemia è un potente stimolo alla secrezione di H+ cui consegue il riassorbimento di HCO 3 -. L’escrezione urinaria di Cl- è inferiore a 15 m. Eq/L nelle forme associate ad ipovolemia (ed ipocloremia). Nell’iperaldosteronismo (eccesso di mineralcorticoidi con ipervolemia) l’escrezione di Cl- è maggiore. Tale regola non vale in presenza di marcata ipo. Kaliemia (< 2 m. Eq/L) perché il rene non riesce a trattenere Cl-.

Sintomi e Segni dell’Alcalosi Metabolica I pazienti possono essere completamente asintomatici o presentare: - sintomi legati all’ipovolemia astenia crampi muscolari capogiri in ortostatismo - sintomi legati all’ipo. Kaliemia poliuria polidipsia debolezza muscolare - sintomi legati all’alcalemia parestesie spasmi carpali-tarsali capogiri L’esame fisico del paziente può far rilevare i segni dell’ipovolemia: - secchezza della cute e delle mucose, bassa pressione venosa giugulare, ipotensione posturale.

Respiratory Alkalosis p. H 7. 50 Pa. CO 2 30 HCO 3 22

Cause dell’Alcalosi Respiratoria Ipossiemia Malattie Polmonari Ipossiemia Stimolazione diretta del centro del respiro - Malattie polmonari - Iperventilazione psicogena o volontaria - Insufficienzapolmoniti epatica - Setticemia da Gram-negativi fibrosi interstiziale - Intossicazione da salicilati embolia - Esiti di correzione di acidosi metabolica - Gravidanza eedema fase luteinica del ciclo mestruale (dovuta al progesterone) - Malattie neurologiche - Scompenso cariaco accidenti cerebrovascolari - Ipotensione o grave anemia tumori pontini Ventilazione Meccanica - Vita ad alta quota

I meccanismi di compenso che si realizzano in questa situazione, sono infatti il passaggio di H+ dalle cellule al settore extracellulare dove si uniscono agli HCO 3 -, riducendone la quota plasmatica e la riduzione dell’escrezione renale di acidi. Il primo meccanismo si attiva pressoché istantaneamente, mentre il secondo meccanismo inizia entro 2 ore ma diviene pienamente efficace nell’arco di 2 -3 giorni. La risposta renale è caratterizzata da bicarbonaturia e ridotta escrezione renale H+ ed è un diretto effetto dell’alcalosi sulle cellule renali.

Sintomi e Segni dell’Alcalosi Respiratoria L’alcalosi respiratoria determina una maggiore eccitabilità di membrana e riduce il flusso ematico cerebrale. I sintomi sono, pertanto, prevalentemente neurologici: - distrazione - alterazione dello stato di coscienza - parestesie alle estremità - crampi - spasmo carpopedale - sincope I sintomi sono più frequenti in caso di alcalosi respiratoria acuta, specialmente se la Pa. CO 2 scende al di sotto dei 25 -30 mm. Hg. N. B. un reperto biochimico interessante è la riduzione del Pi plasmatico (fino a 0. 51. 5 mg/d. L) per aumentato ingresso di fosfati all’interno delle cellule. Talora ipocalcemia.

Metabolic Acidosis p. H 7. 30 Pa. CO 2 40 HCO 3 15

Cause di acidosi Metabolica Ridotta Eliminazione degli H+ Aumento della quota di H+ Perdita di HCO 3 Ridotta eliminazione degli H+ Perdita di HCO A - 3 Ridotta produzione di NH 4+ insufficienza renale A - Perdite Intestinali ipoaldosteronismo diarrea B - Ridotta secrezione di H+ fistole pancreatiche, biliari o intestinali acidosi tubulare distale ureterosigmoidostomia + Aumento della quota di H colestiramina A - Acidosi lattica B - Perdite Renali B - Chetoacidosi C - Intossicazioni acidosi tubulare prossimale Salicilati Metanolo Glicol etilenico Paraldeide Zolfo Toluene Cloruro di NH 4+ D - Rabdomiolisi massiva Formaldeide NPT

Anion Gap Acidosi con elevato gap degli anioni (acidosi normocloremica) La perdita di Accumulo di radicali acidi HCO 3 - che può avvenire attraverso acidosi lattica (lattati) l’intestino o per via (beta-idrossibutirrato) renale, da luogo ad una chetoacidosi particolare forma di acidosi metabolica insufficienza renale (solfati, fosfati, urati) ipercloremica con normale gap anionico. intossicazioni (salicilati, metanolo, ecc. ) Rabdomiolisi imponente Il gap anionico indica la quota di anioni non misurabili e viene Acidosi con normale gap degli anioni (acidosi ipercloremica) espresso dalla formula: Perdite di HCO 3 - intestinali Gap anionico = Na+ plasmatico renali - (Cl plasmatico + HCO 3 plasmatico) [Na+ - (Cl- + Abbondanti assunzioni di HCO 3 -)] =cloruro 140 d’ammonio - (105 +24) = 11 (9 -14 u. n. m. Eq) liquidi per alimentazione parenterale Chetoacidosi in trattamento insulinico con abbondate perdita di chetoacidi nelle urine

L’organismo risponde all’accumulo di acidi con 4 meccanismi di compenso: 1. Tamponamento extracellulare 2. Tamponamento intracellulare 3. Compenso respiratorio 4. Escrezione renale di H+ 1. Ad opera degli HCO 3 - è rapido ed efficiente, tampona il 99% degli H+ in eccesso 2. Tampona il 55 -60% del carico acido ma comporta una immissione di K+ nel compartimento extracellulare. 3. Iperventilazione con aumento del VC (dai normali 5 -6 L/min fino a 30 L/min). Tale meccanismo si rende evidente dopo 1 -2 ore e raggiunge la sua massima espressione dopo 12 -24 ore. 4. Normalmente 50 -100 m. Eq di H+ sotto forma di acidità titolabile (H+ legati ai u. Pi 10 -40 m. Eq/die) ed NH 4+ (H+ legati all’ammoniaca 30 -60 m. Eq/die). Se la quota di H+ da eliminare è maggiore, il rene produce più NH 4+ fino a 250 m. Eq. E’ più difficile, per il rene, aumentare la quota di acidi titolabili (fanno eccezione i chetoanioni in corso di chetoacidosi diabetica)

Sintomi e Segni dell’Acidosi Metabolica L’acidosi metabolica si esprime con sintomi solo se il tasso di HCO 3 - è al di sotto dei 10 m. Eq/L. - Il sintomo più comune è la dispnea do sforzo o a riposo (nei casi più gravi) - Aritmie ventricolari e riduzione della contrattilità miocardica se il p. H è inferiore a 7, 1 -7, 0. - Sintomi Muscoloscheletrici (comuni nell’IRC e nell’RTA) - dovuti al riassoribimento osseo di Ca e Pi secondario al tamponamento osseo degli H+ in eccesso - Sintomi Neurologici (dovuti alla riduzione del p. H liquorale) - possono variare dalla confusione fino al coma N. B. I sintomi neurologici possono dipendere anche dalla diminuzione della perfusione cerebrale in caso di shock, dalla iperosmolarità nella chetoacidosi diabetica e da effetti tossici.

Respiratory Acidosis p. H 7. 30 Pa. CO 2 60 HCO 3 26

Cause di Acidosi Respiratoria Inibizione del centro respiratorio midollare Alterazioni della muscolatura respiratoria e della gabbia toracica Ostruzione delle vie aeree superiori Alterazione degli scambi dei gas attraverso i capillari polmonari Inibizione centro respiratorio midollare Ostruzionedel delle vie aeree superiori acuta -- farmaci (oppiacei, anestetici, acute aspirazione di corpo estraneo sedativi) o vomito -- S. ossigenoterapia nella sonno-apnea di tipoipercapnia ostruttivo cronica -- arresto cardiaco laringospasmo - sindrome tipo centrale Alterazione degli scambi dei gassonno-apnea attraverso idi capillari polmonari cronica -- obesità estremadei (S. una Pickwick) acute esacerbazione patologia polmonare -- lesioni delrespiratoria sistema nervoso centrale sindrome dell’adulto (ARDS) - crisi asmatica grave o polmonite Alterazioni della muscolatura respiratoria e della gabbia toracica - edema polmonare acuto cardiogeno acute - astenia muscolare: crisi miastenica, paralisi periodica, aminoglicosidi, S. - pneumotorace emotorace di Guillan-Barré, o grave ipopotassiemia od ipofosforemia croniche malattiemuscolare: polmonari poliomielite, ostruttive croniche: enfisema - astenia sclerosibronchiti, laterale amiotrofica Ventilazione Meccanica - cifoscoliosi - obesità estrema

L’ipercapnia e l’acidosi vengono inizialmente tamponate dai tamponi intracellulari con generazione di HCO 3 - a seguito della reazione: CO 2 + H 2 O H 2 CO 3 H+ + HCO 3 - (H+ Tamp) + HCO 3 - Nella forma acuta non c’è tempo per l’attivazione del meccanismo renale di escrezione degli H+ che si associa al riassorbimento renale di HCO 3 -. Ne consegue che l’incremento della bicarbonatemia in fase acuta è minore, per analoghi valori di ipercapnia, di quello prevedibile in corso di acidosi respiratoria cronica con compenso renale attivo.

Sintomi e Segni dell’Acidosi Respiratoria Acuta - Fase precoce cefalea visione offuscata agitazione Ac. Respiratoria Cronica stato d’ansia - Fase avanzata tremori Il compenso renale impedisce il realizzarsi di quadri clinici delirio così severi ed in genere i sintomi sono espressione della sonnolenza (carbonarcosi) patologia polmonare di base. In caso di cuore polmonare: La severità del quadro clinico neurologico è legata alla rapidità con cui la CO 2 edemi periferici espressione di una ritenzione renale di Na plasmatica si mette in equilibrio con il liquido cefalorachidiano, determinando riduzione del p. H cerebrale (se p. H < 7. 10 episodi di aritmia, vasodilatazione associata all’ipercapnia. periferica e grave ipotensione). N. B. è spesso presente ipertensione liquorale con papilledema legati all’iperafflusso cerebrale indotto dall’acidemia.

What are the compensations? Respiratory acidosis metabolic alkalosis Respiratory alkalosis metabolic acidosis In respiratory conditions, therefore, the kidneys will attempt to compensate and visa versa. In chronic respiratory acidosis (COPD) the kidneys increase the elimination of H+ and absorb more HCO 3. The ABG will Show NL p. H, CO 2 and HCO 3. Buffers kick in within minutes. Respiratory compensation is rapid and starts within minutes and complete within 24 hours. Kidney compensation takes hours and up to 5 days.

Compensatory Mechanisms • Respiratory • Renal bicarbonate regeneration • Hepatic shift between urea synthesis and ammonia excretion [H+] 40 nmol/L range 36 -44

L’Alcalosi Metabolica è l’unico disordine emogasanalitico che non si compensa mai fino in fondo. Nel caso di una situazione di compenso con Pa. CO 2 > 60 mm. Hg ci troviamo difronte ad una acidosi respiratoria compensata, infatti in corso di compenso per alcalosi metabolica, quando si raggiungono valori di Pa. CO 2 > 60 riprende il drive respiratorio.

How to Analyze an ABG 1. PO 2 NL 1. p. H NL = 7. 35 – 7. 45 Acidotic <7. 35 Alkalotic >7. 45 3. PCO 2 NL = 35 – 45 mm. Hg Acidotic >45 Alkalotic <35 4. HCO 3 NL = 22 – 26 mmol/L Acidotic < 22 Alkalotic > 26 = 80 – 100 mm. Hg

Four-step ABG Interpretation Step 1: Ø Examine Pa. O 2 & Sa. O 2 Ø Determine oxygen status Ø Low Pa. O 2 (<80 mm. Hg) & Sa. O 2 means hypoxia Ø NL/elevated oxygen means adequate oxygenation

Four-step ABG Interpretation Step 2: Ø p. H acidosis alkalosis <7. 35 >7. 45

Four-step ABG Interpretation Step 3: Ø study Pa. CO 2 & HCO 3 Ø respiratory irregularity if Pa. CO 2 abnl & HCO 3 NL Ø metabolic irregularity if HCO 3 abnl & Pa. CO 2 NL

Four-step ABG Interpretation Step 4: Determine if there is a compensatory mechanism working to try to correct the p. H. ie: if have primary respiratory acidosis will have increased Pa. CO 2 and decreased p. H. Compensation occurs when the kidneys retain HCO 3.
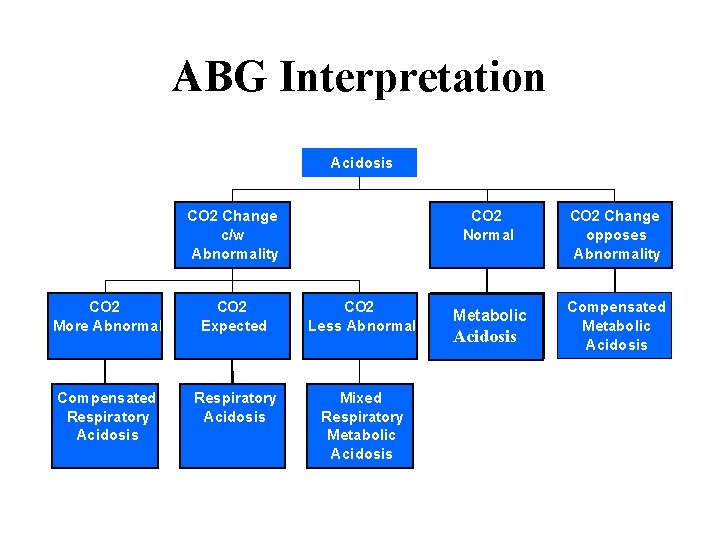
ABG Interpretation Acidosis CO 2 Change c/w Abnormality CO 2 More Abnormal CO 2 Expected CO 2 Less Abnormal Compensated Respiratory Acidosis Mixed Respiratory Metabolic Acidosis CO 2 Normal CO 2 Change opposes Abnormality Metabolic Compensated Metabolic Acidosis
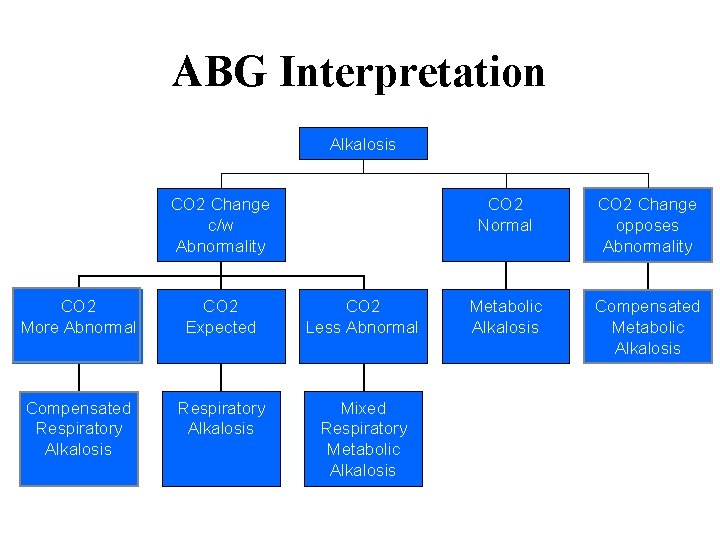
ABG Interpretation Alkalosis CO 2 Change c/w Abnormality CO 2 More Abnormal CO 2 Expected CO 2 Less Abnormal Compensated Respiratory Alkalosis Mixed Respiratory Metabolic Alkalosis CO 2 Normal CO 2 Change opposes Abnormality Metabolic Alkalosis Compensated Metabolic Alkalosis

Practice ABG’s 1. Pa. O 2 90 Sa. O 2 Respiratory 95 p. H 7. 48 Pa. CO 2 32 alkalosis Sa. O 2 90 p. H 7. 32 Pa. CO 2 48 Respiratory acidosis HCO 3 24 HCO 3 18 4. Pa. O 2 87 Sa. O 2 100 p. H 7. 30 Pa. CO 2 40 Metabolic acidosis Sa. O 94 p. H 7. 38 Pa. CO 2 2 48 Compensated respiratory acidosis 5. Pa. O 2 94 Sa. O 2 HCO 3 30 7. Pa. O 2 93 99 p. H 7. 49 Pa. CO 2 40 Metabolic alkalosis Sa. O 91 p. H 7. 35 Pa. CO Compensated respiratory acidosis 2 2 48 Sa. O 97 p. H 7. 45 Pa. CO Compensated metabolic alkalosis 2 2 47 8. Pa. O 2 95 Sa. O 2 38 HCO 3 15 50 HCO 3 24 2. Pa. O 2 60 3. Pa. O 2 95 6. Pa. O 2 62 99 p. H 7. 31 Pa. CO 2 Metabolic acidosis 9. Pa. O 2 65 Sa. O 2 Respiratory 89 p. H 7. 30 Pa. CO 2 alkalosis 10. Pa. O 2 110 Sa. O 2 Metabolic 100 p. H 7. 48 Pa. CO 2 907. 42 p. H 7. 42 Pa. CO Respiratory acidosis 11. Pa. O 2 p. H 2 Pa. O 2 260 ? Sa. O ? Pa. CO Metabolic alkalosis 2 2 59 HCO 3 25 HCO 3 28 HCO 3 27 HCO 3 29 40 HCO 3 30 65 HCO 30 3 18 3

Case study No. 1 56 yo neurologic dz required ventilator support for several weeks. She seemed most comfortable when hyperventilated to Pa. CO 2 28 -30 mm. Hg. She required daily doses of lasix to assure adequate urine output and received 40 mmol/L IV K+ each day. On 10 th day of ICU her ABG on 24% oxygen & VS:

ABG Results p. H PCO 2 PO 2 HCO 3 BE K+ 7. 62 30 mm. Hg 85 mm. Hg 30 mmol/L 10 mmol/L 2. 5 mmol/L BP Pulse RR VT MV 115/80 mm. Hg 88/min 1000 ml 10 L Interpretation: Acute alveolar hyperventilation (resp. alkalosis) and metabolic alkalosis with corrected hypoxemia.

Case study No. 2 27 yo retarded with insulin-dependent DM arrived at ER from the institution where he lived. On room air ABG & VS: p. H PCO 2 PO 2 HCO 3 BE 7. 15 22 mm. Hg 9 mmol/L -30 mmol/L Interpretation: BP Pulse RR VT MV 180/110 mm. Hg 130/min 40/min 800 ml 32 L Partly compensated metabolic acidosis.

Case study No. 3 74 yo with hx chronic renal failure and chronic diuretic therapy was admitted to ICU comatose and severely dehydrated. On 40% oxygen her ABG & VS: p. H PCO 2 PO 2 HCO 3 BE 7. 52 55 mm. Hg 92 mm. Hg 42 mmol/L 17 mmol/L BP Pulse RR VT MV 130/90 mm. Hg 120/min 25/min 150 ml 3. 75 L Interpretation: Partly compensated metabolic alkalosis with corrected hypoxemia.

Case study No. 4 43 yo arrives in ER 20 minutes after a MVA in which he injured his face on the dashboard. He is agitated, has mottled, cold and clammy skin and has obvious partial airway obstruction. An oxygen mask at 10 L is placed on his face. ABG & VS: p. H 7. 10 BP 150/110 mm. Hg PCO 2 60 mm. Hg Pulse 150/min PO 2 125 mm. Hg RR 45/min HCO 3 18 mmol/L VT ? ml BE -15 mmol/L MV ? L. Interpretation: Acute ventilatory failure (resp. acidosis) and acute metabolic acidosis with corrected hypoxemia

Case study No. 5 17 yo, 48 kg with known insulin-dependent DM came to ER with Kussmaul breathing and irregular pulse. Room air ABG & VS: p. H PCO 2 PO 2 HCO 3 BE 7. 05 12 mm. Hg 108 mm. Hg 5 mmol/L -30 mmol/L BP Pulse RR VT MV 140/90 mm. Hg 118/min 40/min 1200 ml 48 L Interpretation: Severe partly compensated metabolic acidosis without hypoxemia.

Case No. 6 cont’d This patient is in diabetic ketoacidosis. IV glucose and insulin were immediately administered. A judgement was made that severe acidemia was adversely affecting CV function and bicarb was elected to restore p. H to 7. 20. Bicarb administration calculation: Base deficit X weight (kg) 4 30 X 48 = 360 mmol/L 4 Admin 1/2 over 15 min & repeat ABG

Case No. 6 cont’d ABG result after bicarb: p. H PCO 2 PO 2 HCO 3 BE 7. 27 25 mm. Hg 92 mm. Hg 11 mmol/L -14 mmol/L BP Pulse RR VT MV 130/80 mm. Hg 100/min 22/min 600 ml 13. 2 L

Case No. 6 cont’d Oxygen was changed to 2 L N/C. 1/2 hour pt. ready to be D/C to floor and ABG & VS: p. H PCO 2 PO 2 HCO 3 BE Sa. O 2 Hb 7. 41 10 mm. Hg 148 mm. Hg 6 mmol/L -17 mmol/L 99% 7 g/d. L BP Pulse RR VT MV 130/90 mm. Hg 95/min, regular 20/min 350 ml 7 L

Case No. 6 cont’d What is going on?

Case No. 6 cont’d If the picture doesn’t fit, repeat ABG!! p. H PCO 2 PO 2 HCO 3 BE Sa. O 2 Hb 7. 45 31 mm. Hg 87 mm. Hg 22 mmol/L -2 mmol/L 96% 13 g/d. L BP Pulse RR VT MV 130/90 mm. Hg 95/min 20/min 350 ml 7 L Technical error was presumed

Case study No. 7 67 yo who had closed reduction of leg fx without incident. Four days later she experienced a sudden onset of severe chest pain and SOB. Room air ABG & VS: p. H PCO 2 PO 2 HCO 3 BE Sa. O 2 7. 36 33 mm. Hg 55 mm. Hg 18 mmol/L -5 mmol/L 88% BP 130/90 mm. Hg Pulse 100/min RR 25/min MV 18 L Interpretation: Compensated metabolic acidosis with moderate hypoxemia. Dx: PE

Case study No. 8 76 yo with documented chronic hypercapnia secondary to severe COPD has been in ICU for 3 days while being tx for pneumonia. She had been stable for past 24 hours and was transferred to general floor. Pt was on 2 L oxygen & ABG &VS: p. H 7. 44 BP 135/95 mm. Hg PCO 2 63 mm. Hg Pulse 110/min PO 2 52 mm. Hg RR 22/min HCO 3 42 mmol/L BE +16 mmol/L MV 10 L Sa. O 2 86%. Interpretation: Chronic ventilatory failure (resp. acidosis) with uncorrected hypoxemia

Case study No. 9 45 yr woman Na+ 135 mmol/L K+ 5. 9 mmol/L Cl 101 mmol/L HCO 3 - 12 mmol/L Urea 42 mmol/L Creat 720 mmol/L 132 -144 3. 5 -5. 5 98 -108 21 -28 <8 <120 Interpretation: Metabolic acidosis

Case study No. 10 70 yr male long Hx epigastric pain & dyspepsia and 7 days vomiting Na+ 127 (135 -145) H+ 26 (36 -44) K+ 2. 2 (3. 5 -5. 5) p. O 2 9. 7 (12 -15) Urea 6. 1) 17. 3 <10 p. CO 2 6. 2 (4. 4 - Creat 250 <150 HCO 3 - 44 (21 -28) Interpretation: metabolic alkalosis

Case study No. 11 55 yr known Ca Bronchus (ectopic ACTH) weakness upper and lower limbs Na+ K+ Cl. HCO 3 - > 40 Creat Cortisol H+ p. O 2 p. CO 2 144 1. 7 85 Cl- Urine : Na+ 25 mmol/L K+ 56 35 50 mmol/L 1750 nmol/L (160 -690) 29 nmol/L (36 -44) 6. 5 k. Pa (12 -15) 5. 6 k. Pa (4. 4 -6. 1) Interpretation: Metabolic alkalosis

Case study No. 12 47 yr old asthmatic smoker brought to A&E breathless with cough and green sputum H+ 83 (36 -44) p. O 2 7. 24 (12 -15) p. CO 2 7. 75 (4. 4 -6. 1) HCO 3 - 21. 5 (21 -28) O 2 saturation 86% Interpretation: Respiratory acidosis

Case study No. 13 16 yr girl asthma acute distress/SOB parasthesiae around mouth and fingers H+ p. O 2 p. CO 2 HCO 3 - 25 nmol/L (36 -44) 17 k. Pa (12 -15) 2. 7 k. Pa (4. 4 -6. 1) 20 mmol/L (21 -28) CO 2 excretion > CO 2 production Interpretation: Respiratory Alkalosis

Case study No. 14 10 yr asthmatic girl admitted in status asthmaticus Na K Cl HCO 3 Urea Creat 135 5. 2 96 (98 -108) 33 (21 -28) 2. 9 4. 3 H+ p. O 2 p. CO 2 135 9. 1 6. 6 (36 -44) (12 -15) (4. 4 -6. 1) Interpretation: Mixed acidosis

Acidosis - unconscious in the garage 19 yr male found with car engine running H+ 50 nmol/L p. O 2 14. 0 k. Pa p. CO 2 2. 0 k. Pa HCO 315 mmol/L anion gap 22 mmol/L lactate 10 mmol/L • what colour was his blood? (0. 9 -1. 7)

Cancer, jaundice and acidosis 56 yrs woman with colon cancer develops weight loss and jaundice H+ 60 (36 -44) glucose 4 p. O 2 14 (12 -15) ketones neg p. CO 2 3. 3 (4. 4 -6. 1) lactate 15 (0. 9 -1. 7) HCO 310 (21 -28) anion gap 27
- Slides: 81