Equilibrio Acido Bsico p H potencial de Hidrgeno

Equilibrio Acido Básico

p. H (potencial de Hidrógeno) Es el resultado de la relación existente en un líquido entre la concentración de ácidos y de bases. Representa el grado de acidez o alcalinidad de una solución. Para el funcionamiento correcto de la célula se requiere un p. H de 7. 35 -7. 45. [p. H] mayor acidez [p. H] mayor alcalinidad

Sistemas Amortiguadores • Los sistemas amortiguadores evitan cambios excesivos en el PH eliminando o liberando iones hidrogeno. Si existe un exceso de iones hidrógenos en los líquidos corporales, los sistemas amortiguadores se combinan con el ion hidrogeno, reduciendo al mínimo el cambio de PH.

El agua es vital para la salud y el correcto funcionamiento celular, y sirve como: • Medios para reacciones metabólicas dentro de las células. • Transportador de nutrientes, productos de desechos y sustancias. • Lubricante. • Aislante y amortiguador. • Medio para regular y mantener la temperatura corporal.

Distribución de Líquidos Corporales El agua del organismo representa del 50 -75% de la masa corporal. Se distribuye en Espacio Extra Celular y Espacio Intra Celular El liquido intra celular (LIC) representa del 3040% del peso (2/3 partes del agua total). El liquido extra celular (LEC) constituye del 2025% del peso (1/3 parte del agua total). Esta formado por: Sangre, linfa, liquido instersticial, peritoneal, pericárdico, pleural, liquido cefalo raquídeo.

Regulación de Líquidos Corporales En una persona sana, el volumen y la composición química de los compartimientos líquidos se encuentran dentro de unos estrechos límites de seguridad. El mecanismo de la sed es el principal regulador de la entrada de líquidos. El centro de la sed esta ubicado en el hipotálamo.
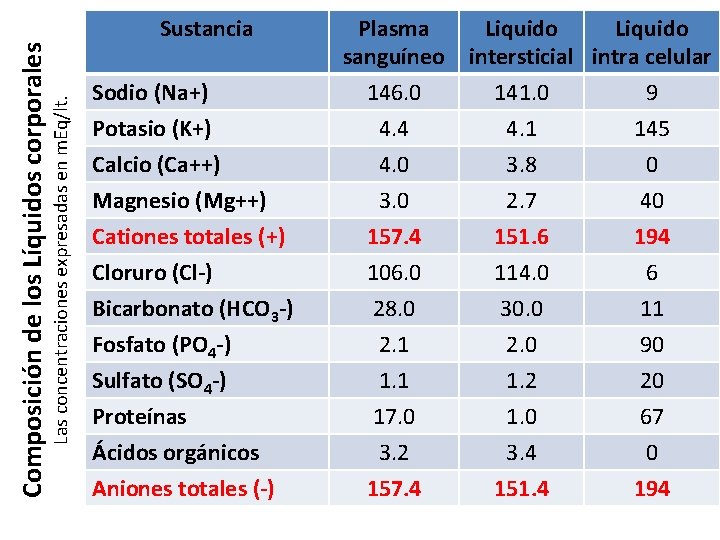
Las concentraciones expresadas en m. Eq/lt. Composición de los Líquidos corporales Sustancia Sodio (Na+) Potasio (K+) Calcio (Ca++) Magnesio (Mg++) Cationes totales (+) Cloruro (Cl-) Bicarbonato (HCO 3 -) Fosfato (PO 4 -) Sulfato (SO 4 -) Proteínas Ácidos orgánicos Aniones totales (-) Plasma Liquido sanguíneo intersticial intra celular 146. 0 141. 0 9 4. 4 4. 1 145 4. 0 3. 0 157. 4 106. 0 28. 0 2. 1 17. 0 3. 2 157. 4 3. 8 2. 7 151. 6 114. 0 30. 0 2. 0 1. 2 1. 0 3. 4 151. 4 0 40 194 6 11 90 20 67 0 194

Salida de Líquidos Las pérdidas de líquidos en el organismo equilibran la entrada diaria promedio de líquidos, de unos 2500 ml, de un adulto. Existen cuatro rutas para la salida de líquidos: • Orina • Perdidas insensibles a través de los pulmones, en forma de vapor de agua en el aire espirado. • Perdidas notorias a través de la piel (sudor). • Perdidas a través del intestino, con las heces.

Intercambio interno de líquidos y electrolitos Difusión: desplazamiento de partículas de mayor a menor concentración. Ósmosis: concentración igual en ambos lados de la membrana según su osmolalidad (osmoles por Kg de agua)/osmolaridad (osmoles/Lt. De solución). Transporte activo: transporte de electrolitos del liquido intracelular al extracelular y viceversa (Ej. Sodio/potasio).

Equilibrio Acido Básico • Una parte importante de la regulación del equilibrio químico u homeostasis de los líquidos corporales es regular su acidez o alcalinidad. • Un acido es una sustancia que libera iones hidrogeno (H*) en solución o sustancias que pierden iones. • Las bases son sustancias capaces de captar iones.
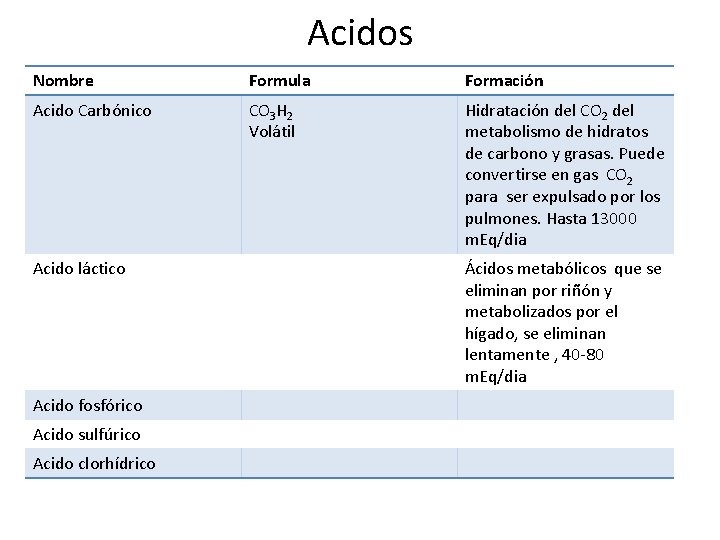
Acidos Nombre Formula Formación Acido Carbónico CO 3 H 2 Volátil Hidratación del CO 2 del metabolismo de hidratos de carbono y grasas. Puede convertirse en gas CO 2 para ser expulsado por los pulmones. Hasta 13000 m. Eq/dia Acido láctico Acido fosfórico Acido sulfúrico Acido clorhídrico Ácidos metabólicos que se eliminan por riñón y metabolizados por el hígado, se eliminan lentamente , 40 -80 m. Eq/dia
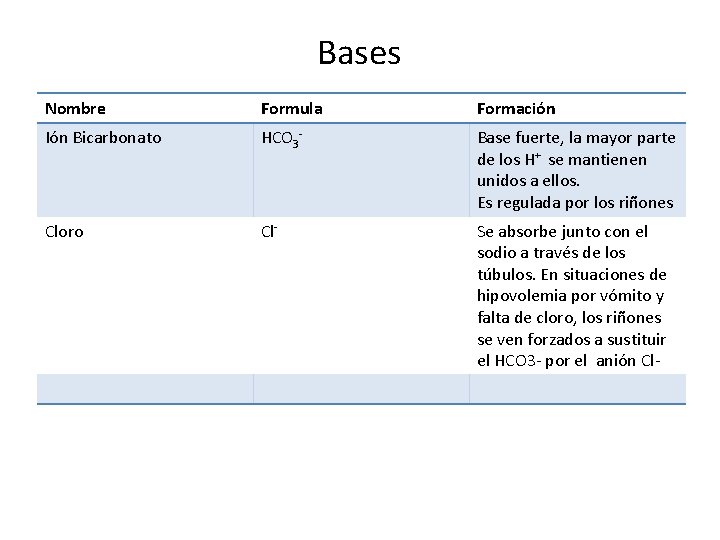
Bases Nombre Formula Formación Ión Bicarbonato HCO 3 - Base fuerte, la mayor parte de los H+ se mantienen unidos a ellos. Es regulada por los riñones Cloro Cl- Se absorbe junto con el sodio a través de los túbulos. En situaciones de hipovolemia por vómito y falta de cloro, los riñones se ven forzados a sustituir el HCO 3 - por el anión Cl-

Regulación Respiratoria • Los pulmones ayudan a regular el equilibrio acido básico eliminando o reteniendo bióxido de carbono (CO 2). • Las frecuencias y la profundidad respiratorias disminuyen, esto hace que se retenga bióxido de carbono y que los niveles de ácidos carbónicos se eleven, y que se neutralicen el exceso de

Regulación Renal • Responden a los cambios de forma más lenta, ya que precisan hora o días para corregir los equilibrios pero su respuesta es más permanente y selectiva que la de los otros sistemas, los riñones mantienen el equilibrio acido básico eliminando o conservando iones bicarbonato e hidrogeno de forma selectiva.

Factores que afectan al equilibrio Hidroeléctrico y Acido • • Edad Género y tamaño corporal Temperatura ambiental Ritmo de vida

Desequilibrio de Líquidos Hay dos tipos de desequilibrio de líquidos: isotónicos y osmolares. q Déficit de volumen de líquidos: El déficit de volumen de líquidos (DVL) isotónico se produce cuando el organismo pierde agua y electrolitos del LEC (Líquidos Electrolíticos Corporales).

En general el DVL se produce como resultado de: ü Perdidas anormales a través de la piel, tracto gastrointestinal o riñón. ü Reducción de la entrada de líquidos. ü Sangrado ü Desplazamiento de líquidos hacia el tercer espacio. (perdida de liquido extracelular en un espacio que no contribuye al equilibrio entre este y el EIC) Manifestaciones clínicas ü Debilidad y sed. ü Pérdida de peso. ü Disminución de la turgencia de los tejidos. ü Sequedad de la mucosa, globos oculares hundidos, disminución de la formación de lágrimas. ü Temperatura por debajo de lo normal. ü Pulso débil y rápido. ü Hipotensión.

Exceso de volumen de líquidos (EVL) Se produce cuando el organismo retiene agua y sodio. Es lo que se denomina hipervolemia (aumento del volumen sanguíneo). Causas especificas de exceso de volumen de líquidos: ü Ingestión excesiva de cloruro de sodio ü Administración demasiado rápida de perfusiones que contienen sodio. ü Afecciones que alteran los mecanismos reguladores, como insuficiencia cardíaca, insuficiencia renal y cirrosis hepática.

Desequilibrio Electrolíticos Sodio(Na₊) Hiponatremia (déficit de sodio) ü Perdida de sodio ü Aporte excesivo de agua ü Síndrome de secreción inadecuada de la hormona anti diurética Hipernatremia(exceso de sodio) ü Perdida de líquidos
Potasio (K+) Hipopotasemia (déficit de potasio) ü Perdida de potasio ü Uso de fármacos que inducen a la perdida de potasio como los diuréticos. Hiperpotasemia ü Disminución de la eliminación de potasio ü Elevado aporte de potasio
Calcio (Ca++) Hipocalcemia (déficit de calcio) ü Extirpación de las glándulas paratiroides por ingestión inadecuada de vitamina D ü Abuso de alcohol Hipercalcemia (exceso de calcio) Afecciones como: ü Hipoparatiroidismo ü Tumores óseos malignos
Magnesio (Mg++) Hipomagnesemia (déficit de magnesio) ü Perdidas por el tracto gastrointestinal (diarrea, aspiración naso gástrica) ü Uso prolongado de ciertos fármacos como diuréticos. Hipermagnesemia (exceso) Retención anormal de magnesio ü Insuficiencia renal ü Insuficiencia suprarrenal ü Tratamiento con sales de magnesio.

Fosfato (PO 4 -) Hipofosfatemia: ü Hiperparatiroidismo ü cuando es persistente se asocia con Anorexia, vértigos, dolor óseo, debilidad muscular, marcha tambaleante) Hiperfosfatemia: ü Insuficiencia renal ü Hipoparatiroidismo
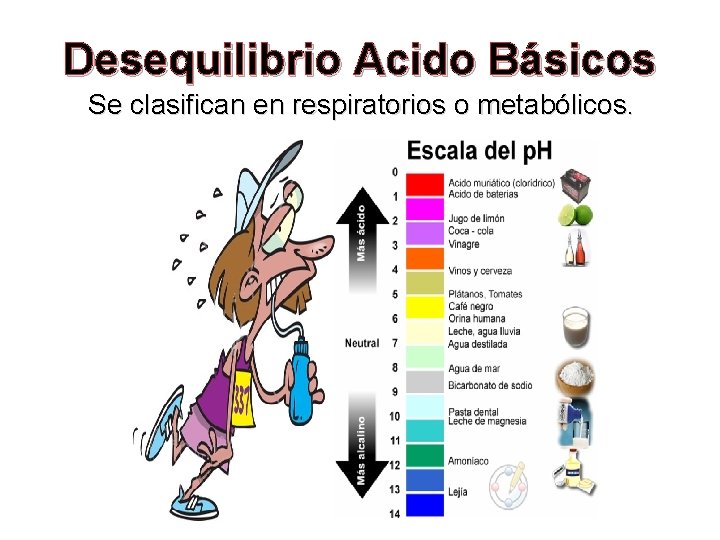
Desequilibrio Acido Básicos Se clasifican en respiratorios o metabólicos.

Bicarbonato (HCO 3 -) Deficit = Acidosis metabólica Asociado a: ü Cetosis diabética ü Insuficiencia renal ü Inanición ü Diarrea grave ü Ingestión de ciertos venenos (alcohol metílico, etilenglicol, paraldehido y salicilato). Signos y síntomas: ü Estupor ü Respiración profunda y rápida (kussmaul) ü Debilidad ü Perdida del conocimiento. 35 ü p. H en orina < de 6. 0 ü Bicarbonato en plasma < 25 meq/lt. ü p. H plasmático < de 7. 35 ü Presión parcial de PCO 2 en sangre baja. Inferior a 30 mm Hg.

Bicarbonato (HCO 3 -) Exceso = Alcalosis metabólica Asociado a: ü Pérdida del Ion Hidrogeno ü Vómito o aspiración de jugo gástrico ü Ingestión excesiva de bicarbonato de sodio Signos y síntomas: ü Hipertonicidad muscular ü Tetania ü Depresión respiratoria ü p. H en orina de 7. 0 ü Bicarbonato plasmático superior a 29 meq/lt. ü p. H plasmático > de 7. 45 ü K+ en plasma < a 4 meq/lt. ü Presion parcial de bioxido de carbono PCO 2 elevada de 44 -48 mm Hg.

Déficit de Dióxido de Carbono Alcalosis Respiratoria Asociada a: ü Aumento de p. H en sangre ü Falta de oxigeno ü Fiebre ü Ansiedad ü Respiración intensa deliberada ü Al inicio de la intoxicación por salicilato Signos y Síntomas ü Tetania ü Convulsiones ü Perdida del conocimiento ü p. H en orina >7. 0 ü PCO 2 < 35 mm Hg. ü p. H en plasma > 7. 45 ü Bicarbonato en plasma ligeramente menor de 25 meq/lt.

Exceso de Dióxido de Carbono Acidosis Respiratoria Asociado a: ü Enfisema ü Obstrucción de las vías respiratorias ü Después de exceso de morfina, barbitúricos o sedantes ü Respiración excesiva de bióxido de carbono. Signos y síntomas ü Cefalea ü Desorientación ü Debilidad y letargia ü p. H en orina < 6. 0 ü p. H en plasma < 7. 35 ü PCO 2 > 45 mm. Hg
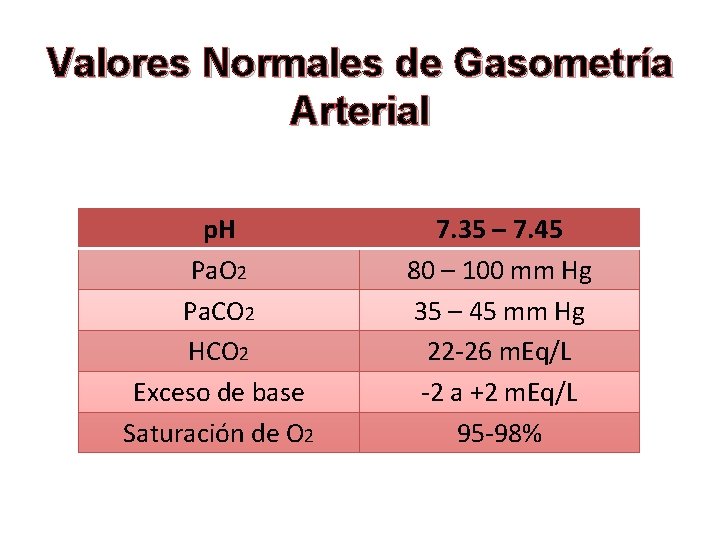
Valores Normales de Gasometría Arterial p. H Pa. O 2 Pa. CO 2 HCO 2 Exceso de base Saturación de O 2 7. 35 – 7. 45 80 – 100 mm Hg 35 – 45 mm Hg 22 -26 m. Eq/L -2 a +2 m. Eq/L 95 -98%

Diagnóstico • • • Déficit del volumen de líquidos Exceso de volumen de líquidos Riesgo de desequilibrio de volumen de líquidos • Riesgo de déficit de volumen de líquidos • Deterioro del cambio gaseoso

Para la valoración de la función respiratoria los cuatro parámetros fundamentales en sangre arterial son los siguientes: • p. H: Mide la resultante global de la situación del equilibrio ácidobase. • Pa. CO 2: Mide la presión parcial de dióxido de carbono en sangre arterial. Se trata de un parámetro de gran importancia diagnóstica, pues tiene estrecha relación con una parte de la respiración: la ventilación (relación directa con la eliminación de CO 2). Así, cuando existe una Pa. CO 2 baja significa que existe una hiperventilación, y al contrario, cuando existe una Pa. CO 2 elevada significa una hipo ventilación.

Para la valoración de la función respiratoria los cuatro parámetros fundamentales en sangre arterial son los siguientes: • Pa. O 2: Mide la presión parcial de oxígeno en sangre arterial. Parámetro, así mismo, de gran utilidad, ya que evalúa la otra parte de la respiración: la oxigenación (captación de oxígeno del aire atmosférico). Una Pa. O 2 baja significa que existe hipoxemia y una Pa. O 2 elevada, una hiperoxia. • HCO 3: Mide la saturación del componente básico del equilibrio acido-base. El exceso o déficit de base es una medición del exceso o déficit del HCO 3, Un exceso de base indica alcalosis metabólica y la deficiencia de base indica acidosis metabólica.
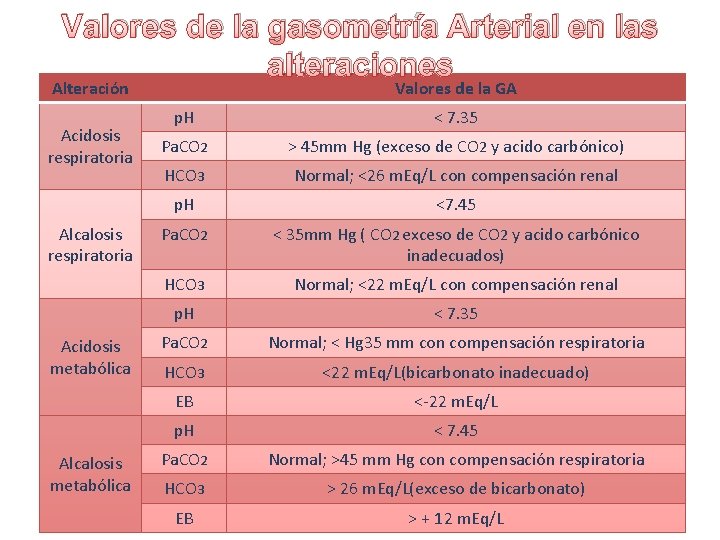
Valores de la gasometría Arterial en las alteraciones Alteración Acidosis respiratoria Alcalosis respiratoria Acidosis metabólica Alcalosis metabólica Valores de la GA p. H < 7. 35 Pa. CO 2 > 45 mm Hg (exceso de CO 2 y acido carbónico) HCO 3 Normal; <26 m. Eq/L con compensación renal p. H <7. 45 Pa. CO 2 < 35 mm Hg ( CO 2 exceso de CO 2 y acido carbónico inadecuados) HCO 3 Normal; <22 m. Eq/L con compensación renal p. H < 7. 35 Pa. CO 2 Normal; < Hg 35 mm con compensación respiratoria HCO 3 <22 m. Eq/L(bicarbonato inadecuado) EB <-22 m. Eq/L p. H < 7. 45 Pa. CO 2 Normal; >45 mm Hg con compensación respiratoria HCO 3 > 26 m. Eq/L(exceso de bicarbonato) EB > + 12 m. Eq/L

Ejemplo de Soluciones Intravenosas Soluciones Isotónicas • Na. Cl al 0. 9% (salino normal) • Ringer lactato (una solución electrolítica equilibrada) • Dextrosa al 5% en agua Soluciones Hipotónicas • Na. Cl al 0. 45% (mitad de salino normal) • Na. Cl al 0. 33% (un tercio de salino normal)

Soluciones Hipertónicas • Dextrosa al 5% en suero salino normal (D 5 SN) • Dextrosa al 5% en Na. CI al 0. 45% (D 5 ½ SN) • Dextrosa al 5% en Ringer Lactato (D 5 RL)
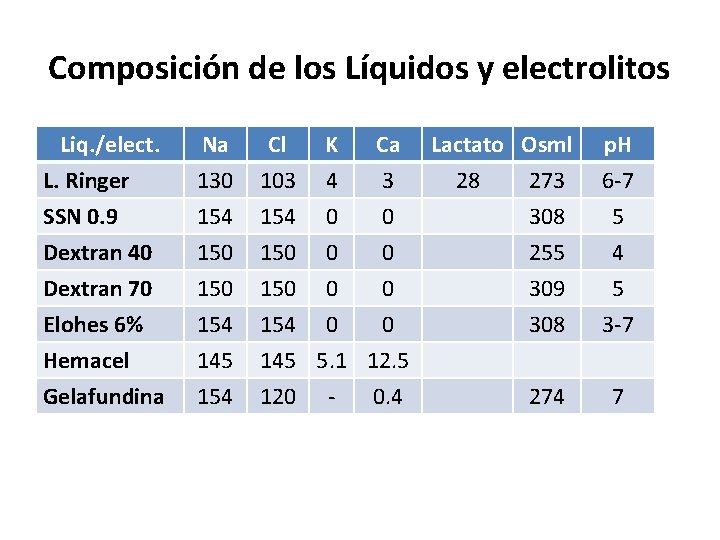
Composición de los Líquidos y electrolitos Liq. /elect. L. Ringer SSN 0. 9 Dextran 40 Na 130 154 150 Cl 103 154 150 K 4 0 0 Ca 3 0 0 Dextran 70 Elohes 6% Hemacel Gelafundina 150 154 145 154 150 0 0 154 0 0 145 5. 1 12. 5 120 0. 4 Lactato Osml 28 273 308 255 p. H 6 -7 5 4 309 308 5 3 -7 274 7
- Slides: 36