Equilibre acidobasique 2 TROUBLES DE LEQUILIBRE ACIDOBASIQUE Gnralits

Equilibre acido-basique 2. TROUBLES DE L’EQUILIBRE ACIDO-BASIQUE Généralités Diagramme de Davenport Troubles d’origine respiratoire Troubles d’origine métabolique Thierry PETITCLERC Biophysique du milieu intérieur PCEM 1 – Université Paris 6

Troubles acido-basiques Définition : anomalie de la concentration en acides fixes et/ou volatil : trouble respiratoire : anomalie de la concentration [CO 2 dissous] (= a PCO 2) en acide volatil : - excès (PCO 2 > 42 mm. Hg) : acidose respiratoire - défaut (PCO 2 < 36 mm. Hg) : alcalose respiratoire trouble métabolique : anomalie de la concentration en acides fixes : - excès : acidose métabolique - défaut : alcalose métabolique NB : la conc. en acides fixes n’est pas mesurable. Seule la variation (excès ou défaut) est mesurable par le laboratoire.

Troubles acido-basiques : définitions acidémie : p. H < 7, 38 alcalémie : p. H > 7, 42 trouble pur : l’anomalie de la concentration ne porte que sur une seule classe d’acides (soit fixes, soit volatil) trouble compensé : la variation de la concentration d’une classe d’acides est compensée par une variation dans le sens opposé de l’autre classe. La compensation est totale si elle permet d’obtenir un p. H normal (compensation partielle sinon). trouble mixte : les concentrations deux classes d’acides ont varié dans le même sens (et aggravent donc leur effet sur le p. H). trouble aigu : début brutal (duré généralement peu de temps) trouble chronique : dure longtemps (début souvent progressif)

Diagramme de Davenport Henderson-Hasselbach : Diagramme utilisable pour toute solution contenant le tampon HCO 3 - / CO 2 ouvert. Le point N (p. H normal et bicarbonate normal donc PCO 2 normale) représente l'équilibre acido-basique normal. Tous les autres points correspondent à un trouble de l'équilibre acidobasique. [HCO 3 -] mmol/L Pour se déplacer sur ce diagramme, il faut faire varier la concentration des acides fixes et/ou volatils. 24 N + 7, 40 p. H
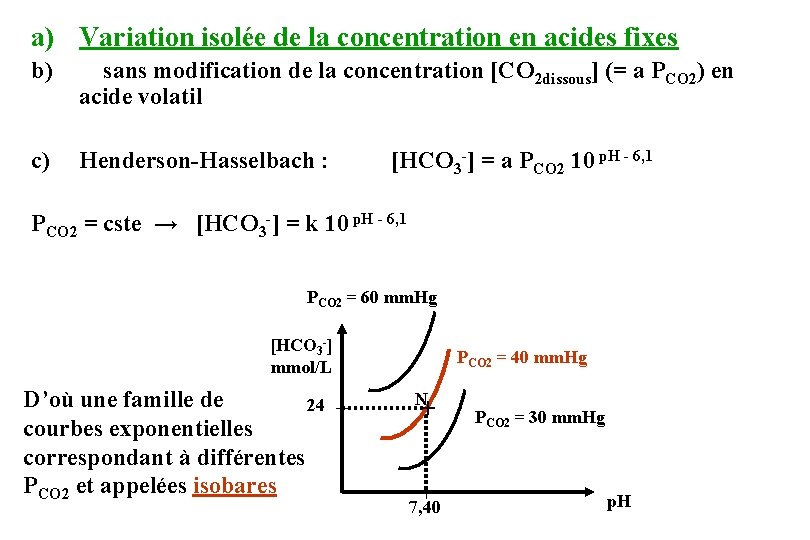
a) Variation isolée de la concentration en acides fixes b) sans modification de la concentration [CO 2 dissous] (= a PCO 2) en acide volatil c) Henderson-Hasselbach : [HCO 3 -] = a PCO 2 10 p. H - 6, 1 PCO 2 = cste → [HCO 3 -] = k 10 p. H - 6, 1 PCO 2 = 60 mm. Hg [HCO 3 -] mmol/L D’où une famille de 24 courbes exponentielles correspondant à différentes PCO 2 et appelées isobares PCO 2 = 40 mm. Hg N + 7, 40 PCO 2 = 30 mm. Hg p. H
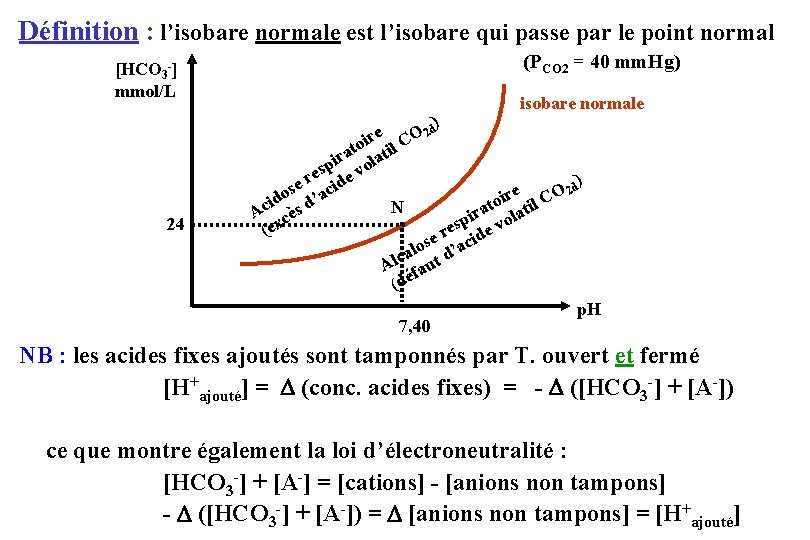
Définition : l’isobare normale est l’isobare qui passe par le point normal [HCO 3 -] mmol/L 24 (PCO 2 = 40 mm. Hg) isobare normale ) d 2 e ir l CO o t i ira olat p es e v r ) d se acid 2 e O o id s d’ oir til C t c N a A cè ir ola p x s e de v (e r ose d’aci l a Alc faut (dé p. H 7, 40 NB : les acides fixes ajoutés sont tamponnés par T. ouvert et fermé [H+ajouté] = (conc. acides fixes) = - ([HCO 3 -] + [A-]) ce que montre également la loi d’électroneutralité : [HCO 3 -] + [A-] = [cations] - [anions non tampons] - ([HCO 3 -] + [A-]) = [anions non tampons] = [H+ajouté]
![b) Variation isolée de la concentration [CO 2 d] en acide volatil sans modification b) Variation isolée de la concentration [CO 2 d] en acide volatil sans modification](http://slidetodoc.com/presentation_image_h/9a523ca02711b1e7a11178ac4f135fb8/image-7.jpg)
b) Variation isolée de la concentration [CO 2 d] en acide volatil sans modification de la concentration en acides fixes - L’acide volatil CO 2 d est tamponné uniquement par les tampons fermés. CO 2 dissous → HCO 3 - + H+ et H+ + A- → AH - On se déplace sur la courbe de titration des tampons fermés. p. H courbe de titration 7, 8 6, 8 7, 8 zoom sur la zone tampon 6, 8 [H+]ajouté = [HCO 3 -]
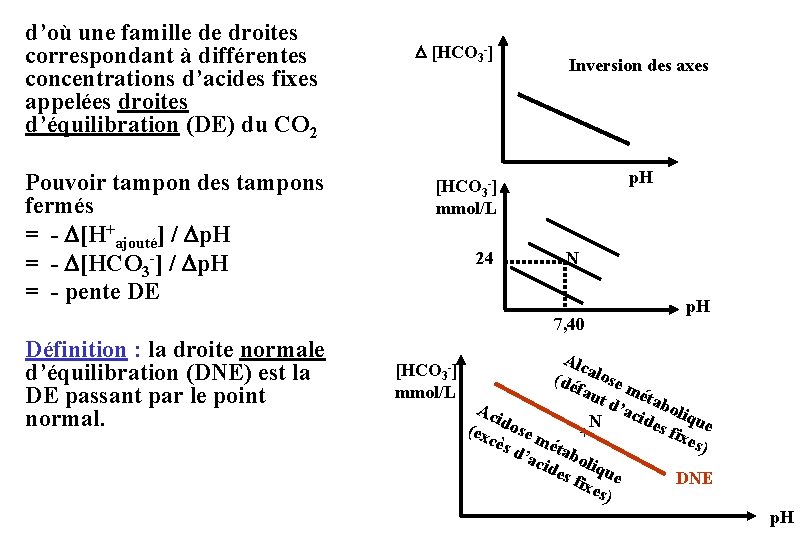
d’où une famille de droites correspondant à différentes concentrations d’acides fixes appelées droites d’équilibration (DE) du CO 2 Pouvoir tampon des tampons fermés = - [H+ajouté] / p. H = - [HCO 3 -] / p. H = - pente DE [HCO 3 -] Inversion des axes p. H [HCO 3 -] mmol/L 24 N 7, 40 Définition : la droite normale d’équilibration (DNE) est la DE passant par le point normal. [HCO 3 -] mmol/L p. H Alc (dé alose fau mét t d’ abo Ac a c ide lique ido N s fi (ex s xes cès e mét + ) d’a abo cid l es f ique DNE ixe s) p. H

Remarques : 1) pente DE = - pouvoir tampon des tampons fermés. anémie → pente diminuée 2) En l’absence de tampons fermés, pente DE = 0 → [HCO 3 -] = constante dans le domaine étudié de variation En effet : CO 2 → HCO 3 - + H+ H+ n’est pas tamponné → reste libre Lorsque le p. H varie de 7, 4 à 6, 8, [H+] augmente de 40 à 160 nmol/L donc [HCO 3 -] augmente aussi de 120 nmol/L et varie alors de 24 à 24, 00012 mmol/L ! 3) En présence de tampons fermés, la quantité de H+ajouté qui reste libre (et est ainsi responsable de la variation de p. H) est négligeable devant la quantité prise en charge par les tampons fermés.
![Troubles respiratoires La PCO 2 (et donc [CO 2 dissous]) s’ajustent de manière que Troubles respiratoires La PCO 2 (et donc [CO 2 dissous]) s’ajustent de manière que](http://slidetodoc.com/presentation_image_h/9a523ca02711b1e7a11178ac4f135fb8/image-10.jpg)
Troubles respiratoires La PCO 2 (et donc [CO 2 dissous]) s’ajustent de manière que le bilan du CO 2 reste équilibré. Variation de la production de CO 2 : → variation négligeable de la PCO 2 (qui reste dans les limites physiologiques → pas de trouble acido-basique). Variation de l’élimination de CO 2 (hypoventilation ou hyperventilation) : → variation importante de la PCO 2 → trouble acido-basique respiratoire : a) HYPOVENTILATION → augmentation de PCO 2 → augmentation de la concentration [CO 2 dissous] en acide volatil → acidose respiratoire b) HYPERVENTILATION → diminution de PCO 2 → diminution de la concentration [CO 2 dissous] en acide volatil → alcalose respiratoire

Troubles respiratoires : étiologies a) Acidoses respiratoires (hypoventilation) - Acidose respiratoire aiguë : - obstructive : obstacle, crise d’asthme - neurologique : médicaments (morphine) - Acidose respiratoire chronique : - obstructive : bronchite chronique - restrictive : fibrose pulmonaire - neurologique : poliomyélite b) Alcaloses respiratoires (hyperventilation) - Hyperventilation primitive (souvent aiguë) : - Psychogène : émotion - Organique : encéphalopathies - Iatrogène : ventilation assistée - Hyperventilation secondaire à l’hypoxie (souvent chronique) : - Hypoxémie (séjour en altitude, fibrose pulmonaire) - Hypoxie tissulaire (anémie, diminution du débit cardiaque)
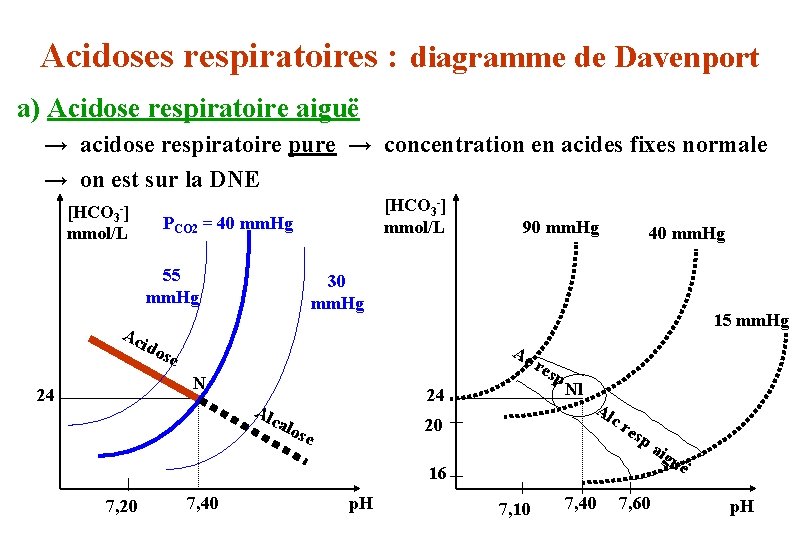
Acidoses respiratoires : diagramme de Davenport a) Acidose respiratoire aiguë → acidose respiratoire pure → concentration en acides fixes normale → on est sur la DNE [HCO 3 -] mmol/L PCO 2 = 40 mm. Hg 55 mm. Hg 15 mm. Hg Ac N 24 Alc alo se res p Nl Al cr 20 16 7, 20 7, 40 40 mm. Hg 30 mm. Hg Ac ido se 24 90 mm. Hg p. H 7, 10 7, 40 esp aig uë 7, 60 p. H
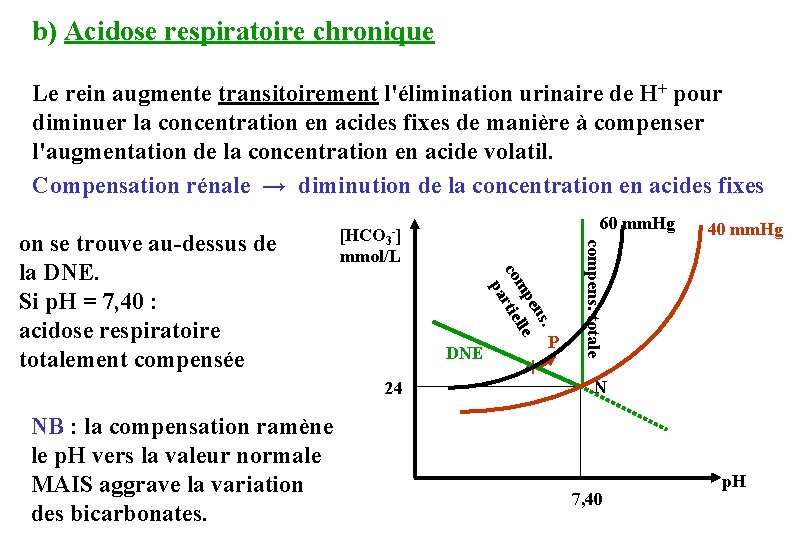
b) Acidose respiratoire chronique Le rein augmente transitoirement l'élimination urinaire de H+ pour diminuer la concentration en acides fixes de manière à compenser l'augmentation de la concentration en acide volatil. Compensation rénale → diminution de la concentration en acides fixes DNE 24 NB : la compensation ramène le p. H vers la valeur normale MAIS aggrave la variation des bicarbonates. P + 40 mm. Hg compens. totale s. en mp lle co rtie pa on se trouve au-dessus de la DNE. Si p. H = 7, 40 : acidose respiratoire totalement compensée 60 mm. Hg [HCO 3 -] mmol/L N 7, 40 p. H

Troubles métaboliques : étiologies a) Acidoses métaboliques - Charge acide excessive (réponse rénale adaptée) : - exogène : médicaments (aspirine), toxiques (antigel) - endogène : synthèse accrue (acidocétose diabétique) défaut de métabolisation (acidose lactique) - perte digestive de base : diarrhées aiguës - Défaut d’élimination rénale (réponse rénale inadaptée) : b) Alcaloses métaboliques - Perte digestive d’acides fixes : vomissements répétés - Excès d’apports de bases : pansements gastriques
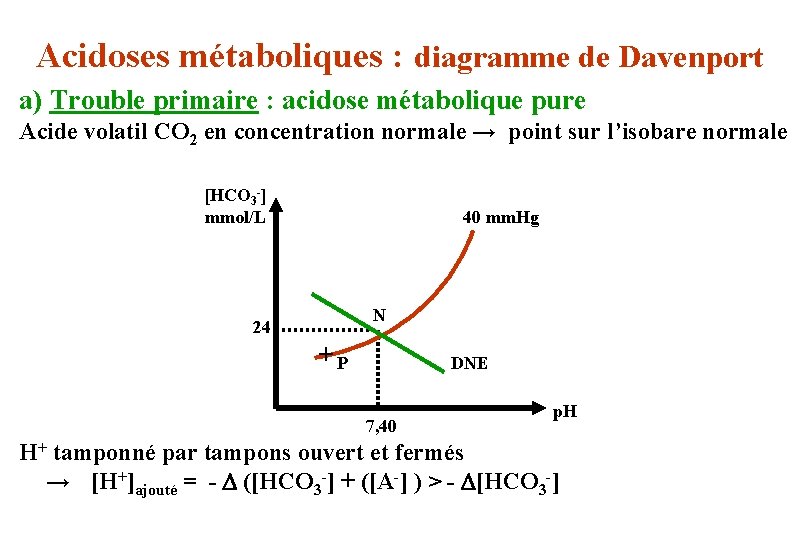
Acidoses métaboliques : diagramme de Davenport a) Trouble primaire : acidose métabolique pure Acide volatil CO 2 en concentration normale → point sur l’isobare normale [HCO 3 -] mmol/L 40 mm. Hg N 24 +P DNE 7, 40 p. H H+ tamponné par tampons ouvert et fermés → [H+]ajouté = - ([HCO 3 -] + ([A-] ) > - [HCO 3 -]
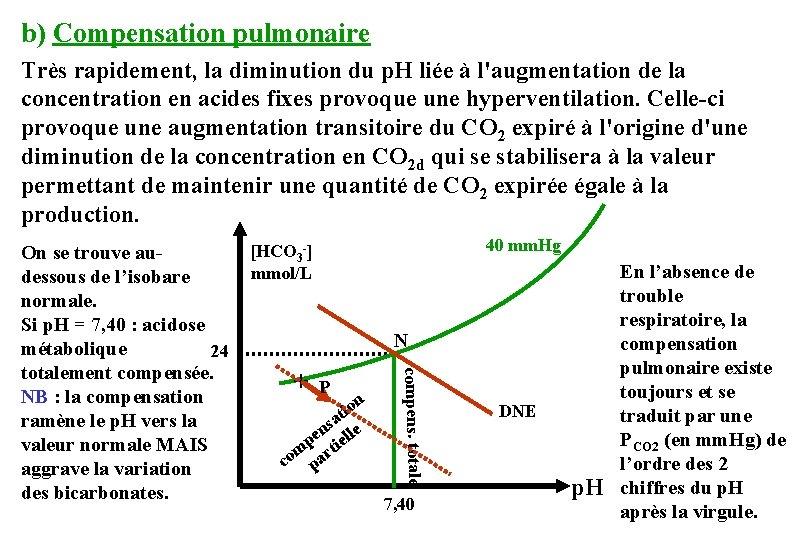
b) Compensation pulmonaire Très rapidement, la diminution du p. H liée à l'augmentation de la concentration en acides fixes provoque une hyperventilation. Celle-ci provoque une augmentation transitoire du CO 2 expiré à l'origine d'une diminution de la concentration en CO 2 d qui se stabilisera à la valeur permettant de maintenir une quantité de CO 2 expirée égale à la production. 40 mm. Hg [HCO 3 -] mmol/L N + P ion t sa e n pe tiell m co par compens. totale On se trouve audessous de l’isobare normale. Si p. H = 7, 40 : acidose métabolique 24 totalement compensée. NB : la compensation ramène le p. H vers la valeur normale MAIS aggrave la variation des bicarbonates. 7, 40 DNE p. H En l’absence de trouble respiratoire, la compensation pulmonaire existe toujours et se traduit par une PCO 2 (en mm. Hg) de l’ordre des 2 chiffres du p. H après la virgule.
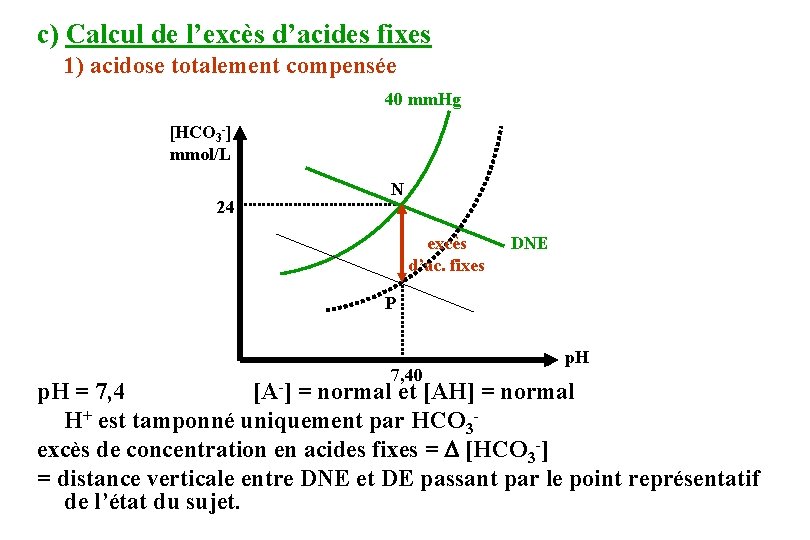
c) Calcul de l’excès d’acides fixes 1) acidose totalement compensée 40 mm. Hg [HCO 3 -] mmol/L N 24 excès d’ac. fixes DNE P [A-] 7, 40 p. H = 7, 4 = normal et [AH] = normal H+ est tamponné uniquement par HCO 3 excès de concentration en acides fixes = [HCO 3 -] = distance verticale entre DNE et DE passant par le point représentatif de l’état du sujet.
![2) Cas général 40 mm. Hg [HCO 3 -] mmol/L N 24 + P 2) Cas général 40 mm. Hg [HCO 3 -] mmol/L N 24 + P](http://slidetodoc.com/presentation_image_h/9a523ca02711b1e7a11178ac4f135fb8/image-18.jpg)
2) Cas général 40 mm. Hg [HCO 3 -] mmol/L N 24 + P excès d’ac. fixes DNE M 7, 40 p. H excès de concentration en acides fixes en P = excès de concentration en acides fixes en M = distance verticale entre DNE et DE passant par P NB : 1) La détermination de l’excès de concentration en acides fixes nécessite détermination de la pente de la DE. 2) La pente DE mesurée in vitro est pente in vivo → La mesure in vitro de l’excès de concentration en acides fixes n’a pas de signfication quantitative précise.
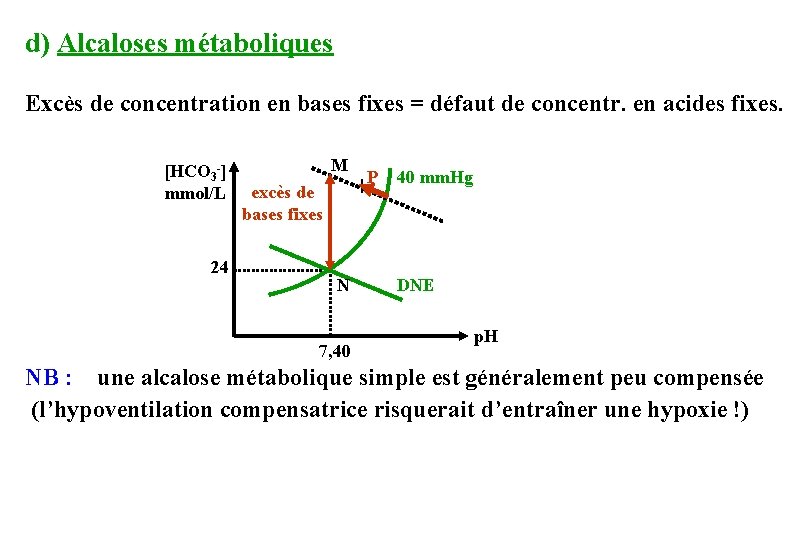
d) Alcaloses métaboliques Excès de concentration en bases fixes = défaut de concentr. en acides fixes. [HCO 3 -] mmol/L 24 M excès de bases fixes N 7, 40 +P 40 mm. Hg DNE p. H NB : une alcalose métabolique simple est généralement peu compensée (l’hypoventilation compensatrice risquerait d’entraîner une hypoxie !)
![En Résumé : diagramme de Davenport [HCO 3 -] mmol/L 40 mm. Hg Alc. En Résumé : diagramme de Davenport [HCO 3 -] mmol/L 40 mm. Hg Alc.](http://slidetodoc.com/presentation_image_h/9a523ca02711b1e7a11178ac4f135fb8/image-20.jpg)
En Résumé : diagramme de Davenport [HCO 3 -] mmol/L 40 mm. Hg Alc. métab. Ac. resp. Alcalose mixte Ac. mixte N Ac. métab. Alc. resp. 7, 40 DNE p. H
- Slides: 20