EQUILBRIO QUMICO Reversibilidade de reaes n Velocidade de

EQUILÍBRIO QUÍMICO Reversibilidade de reações n Velocidade de reação n Conceito de equilíbrio químico n Análise gráfica n
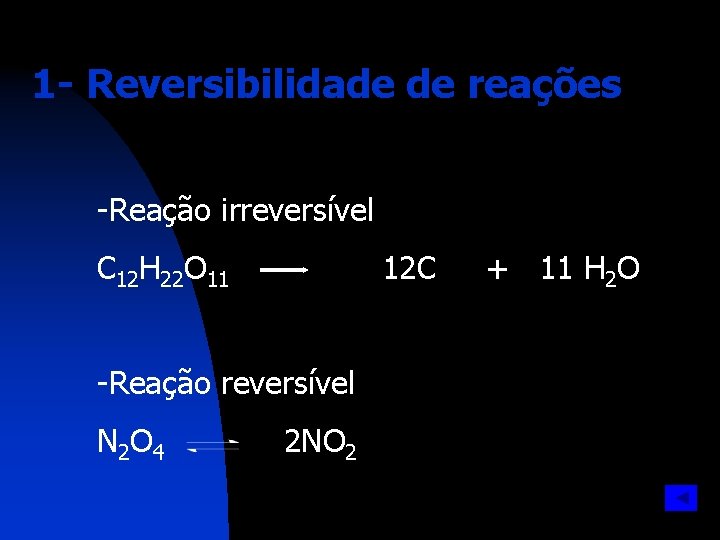
1 - Reversibilidade de reações -Reação irreversível C 12 H 22 O 11 12 C -Reação reversível N 2 O 4 2 NO 2 + 11 H 2 O
![2 - Velocidade de reação química v = [ ] / t, onde: v 2 - Velocidade de reação química v = [ ] / t, onde: v](http://slidetodoc.com/presentation_image_h2/42af0d8f06ede53af08ca9f1da888651/image-3.jpg)
2 - Velocidade de reação química v = [ ] / t, onde: v = velocidade da reação (em mol/L·seg); [ ] = conc. (em mol/L); t = tempo (em seg. )

2. 1 - Dependência da velocidade em função da concentração Na reação: 2 H 2 + 2 NO [H 2] (mol/L) [NO] (mol/L) N 2 + 2 H 2 O, temos: vinicial (mol/L·h) 1 · 10 -3 3 · 10 -5 2 · 10 -3 1 · 10 -3 6 · 10 -5 2 · 10 -3 24 · 10 -5
![n v ~ [ ], logo: v=k·[ ] n Para o exemplo anterior, temos n v ~ [ ], logo: v=k·[ ] n Para o exemplo anterior, temos](http://slidetodoc.com/presentation_image_h2/42af0d8f06ede53af08ca9f1da888651/image-5.jpg)
n v ~ [ ], logo: v=k·[ ] n Para o exemplo anterior, temos a seguinte expressão da velocidade: v = k · [H 2] · [NO]2

2. 2 - Lei cinética de uma reação a. X + b. Y produtos v = k · [X]m · [Y]n, onde: v = velocidade da reação; k = constante de velocidade; [X] e [Y] = concentração dos reagentes; m e n = expoentes determinados experimentalmente

3 - O que é Equilíbrio Químico? É dada a reação: Se v 1 = v 2 dizemos que o sistema se encontra em equilíbrio químico, ou seja:

Equilíbrio Químico: situação na qual as concentrações dos participantes da reação não se alteram, pois as velocidades direta e inversa se processam na mesma velocidade.

O EQUILÍBRIO É DIN MICO!

4 - Análise Gráfica Veremos algumas situações no quadro-branco.
- Slides: 10