EQUILBRIO CIDO BSICO SISTEMAS TAMPES sistemas que tendem

EQUILÍBRIO ÁCIDO BÁSICO

SISTEMAS TAMPÕES § sistemas que tendem a se opor à mudanças de p. H § mantém a homeostase Equilíbrio ácido - básico

SISTEMAS ATUANTES TAMPÕES PLASMÁTICOS • o efeito de ácidos ou bases adicionados nos líquidos corporais • atuação imediata SISTEMA PULMONAR • elimina ou retém CO 2 • atuação em minutos a horas SISTEMA RENAL • excreção de urina ácida ou básica • atuação em horas a dias

p. H ? 2 H 2 O H 3 O+ + OHH 2 O H+ + OHQuantidades iguais de H+ + OH- = 1 x 10 -7 SORENSEN (1909) p. H (H 2 O) [H+] = 1 x 10 -7 p. H = 7, 0 p. H = - log [H+] p. H (sangue) [H+] = 40 x 10 -9 p. H = 7, 4

ÁCIDO ? BASE ? SOLUÇÃO AQUOSA H+ OHÁCIDO FRACO : ligeira tendência em ceder prótons para a H 2 O FORTE: transfere facilmente prótons TEORIA DA DISSOCIAÇÃO ELETROLÍTICA Eletrólise: as moléculas sofrem um maior ou menor grau de dissociação em íons + ou – propriedades e reações próprias

LEI DAS AÇÕES DAS MASSAS a velocidade de uma reação química é proporcional ao produto das massas ativas (concentrações) das substâncias reagentes AH + H 2 O H+ + A- 1 - H+ + A- AH + H 2 O K 1 = [ H+ ] [ A- ] 2 - AH + H 2 O H+ + A- K 2 = [AH ] [ H 2 O ] K 1 / K 2 = K = [ H+ ] [ A- ] [AH ]
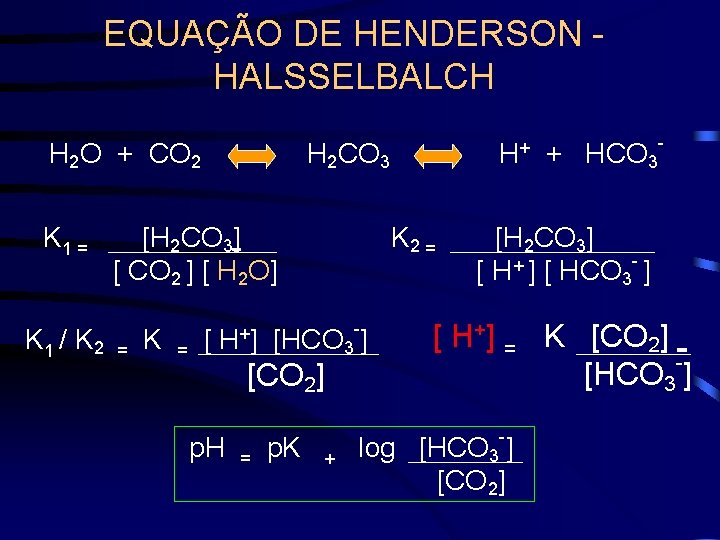
EQUAÇÃO DE HENDERSON - HALSSELBALCH H 2 O + CO 2 H 2 CO 3 K 1 = [H 2 CO 3] [ CO 2 ] [ H 2 O] + K 1 / K 2 = K = [ H ] [HCO 3 ] [CO 2] H+ + HCO 3 K 2 = [H 2 CO 3] - + [ H ] [ HCO 3 ] [ H+] = K [CO 2] . [HCO 3 ] - p. H = p. K + log [HCO 3 ] [CO 2]
![p. H = p. K + log [HCO 3 -] [CO 2] Relação p. H = p. K + log [HCO 3 -] [CO 2] Relação](http://slidetodoc.com/presentation_image_h/bf887e5497813601dac83a0030351210/image-8.jpg)
p. H = p. K + log [HCO 3 -] [CO 2] Relação no sangue: 7, 4 = 6, 1 + 1, 3 20: 1 7, 0 7, 4 7, 8 acidose alcalose
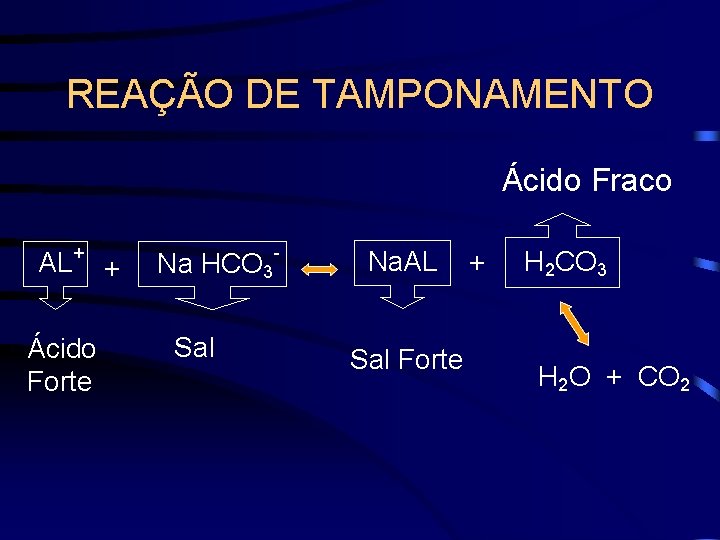
REAÇÃO DE TAMPONAMENTO Ácido Fraco AL + + Ácido Forte Na HCO 3 Sal - Na. AL Sal Forte + H 2 CO 3 H 2 O + CO 2

TAMPÕES PLASMÁTICOS Ø FOSFATO MONOSSÓDICO – FOSFATO DISSÓDICO HCL + Na 2 HPO 4 Na. Cl + Na. H 2 PO 4 Na. OH + Na. H 2 PO 4 H 2 O + Na 2 HPO 4 POUCO SIGNIFICATIVO BAIXA CONCENTRAÇÃO
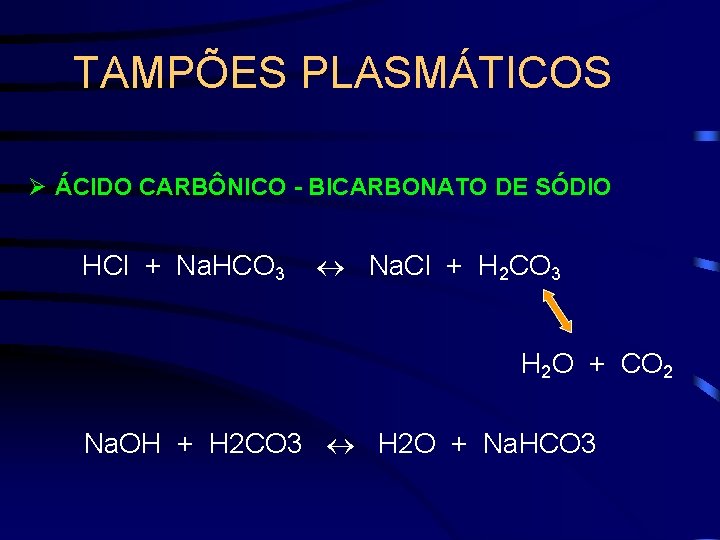
TAMPÕES PLASMÁTICOS Ø ÁCIDO CARBÔNICO - BICARBONATO DE SÓDIO HCl + Na. HCO 3 Na. Cl + H 2 CO 3 H 2 O + CO 2 Na. OH + H 2 CO 3 H 2 O + Na. HCO 3

TAMPÕES PLASMÁTICOS Ø PROTEÍNAS H+ + PROT HPROT + H + Hb. O 2 HHb + O 2 MAIS IMPORTANTE TAMPÃO DO SANGUE 15 g de Hb 3, 85 g de proteínas

BASE TAMPÃO é a soma das duas bases no sangue: 1 - Hb = 17 m. Eq/l 2 - Bicarbonato = 25 m. Eq/l 1 + 2 = 42 m. Eq/l H+ + HCO 3 - H 2 CO 3 H 2 O + CO 2 + H + PROT HPROT PERTUBAÇÕES: • Respiratória (CO 2) NÃO ALTERA BASE TAMPÃO + • Metabólica (H ) ALTERA BT

EXCESSO DE BASE EB = Base Tampão - Base Tampão Normal BT - BTN BT BTN ACIDOSE METABÓLICA BT BTN ALCALOSE METABÓLICA PCO 2 RESPIRATÓRIA EB METABÓLICA
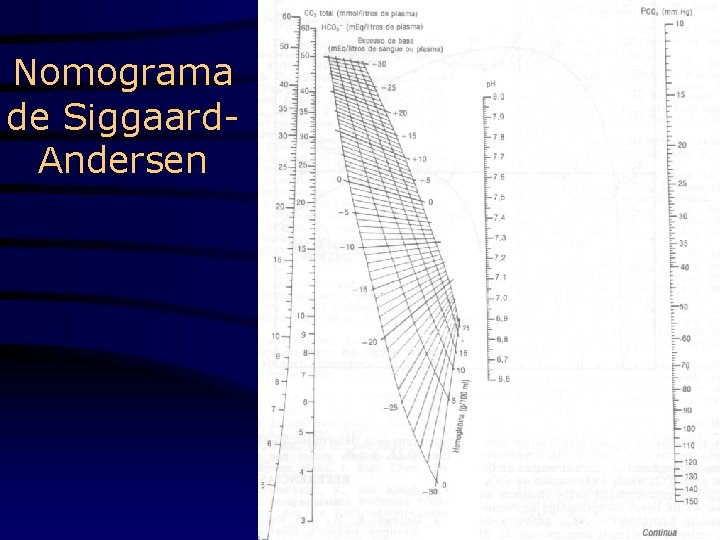
Nomograma de Siggaard. Andersen
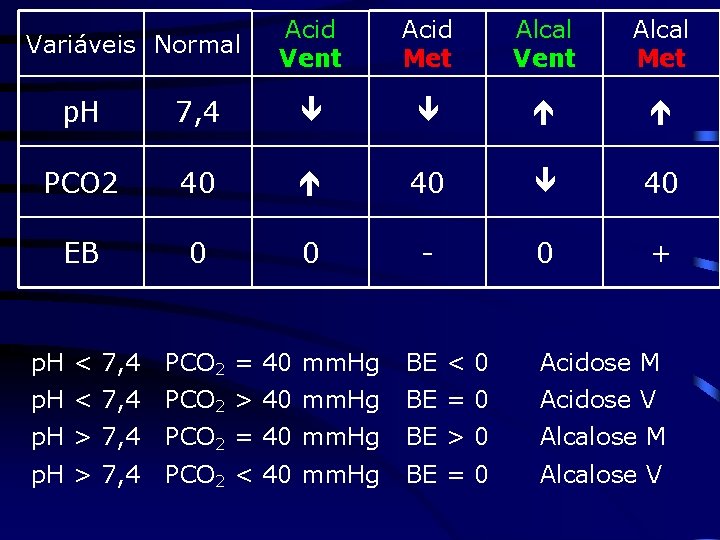
Variáveis Normal Acid Vent Acid Met Alcal Vent Alcal Met p. H 7, 4 PCO 2 40 40 40 EB 0 0 - 0 + p. H < 7, 4 PCO 2 = 40 mm. Hg BE < 0 Acidose M p. H < 7, 4 PCO 2 > 40 mm. Hg BE = 0 Acidose V p. H > 7, 4 PCO 2 = 40 mm. Hg BE > 0 Alcalose M p. H > 7, 4 PCO 2 < 40 mm. Hg BE = 0 Alcalose V

p. H = 7, 29 BE = 0 PCO 2 = 60 mm. Hg acidose V sem compensação p. H = 7, 31 PCO 2 = 70 mm. Hg BE = + 5 acidose V sendo compensada por alcalose M p. H = 7, 51 PCO 2 = 40 mm. Hg BE = + 8 alcalose M sem compensação p. H = 7, 4 PCO 2 = 20 mm. Hg BE = - 10 p. H = 7, 2 PCO 2 = 50 mm. Hg BE = - 9, 5 alcalose V compensada por acidose M acidose V somada a acidose M p. H = 7, 35 PCO 2 = 30 mm. Hg BE = - 8 acidose M sendo compensada por alcalose V
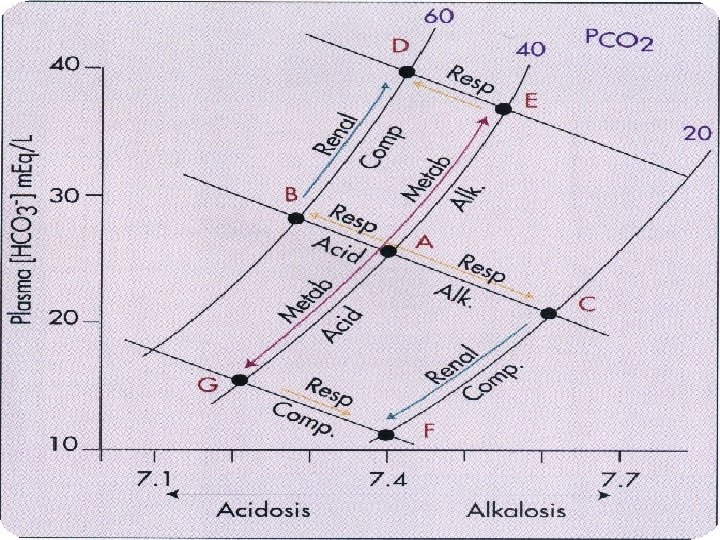
Diagrama de Devenport
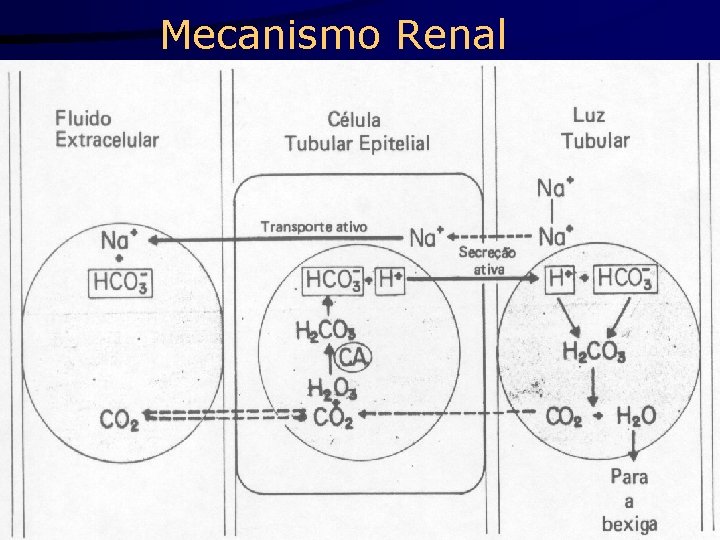
Mecanismo Renal
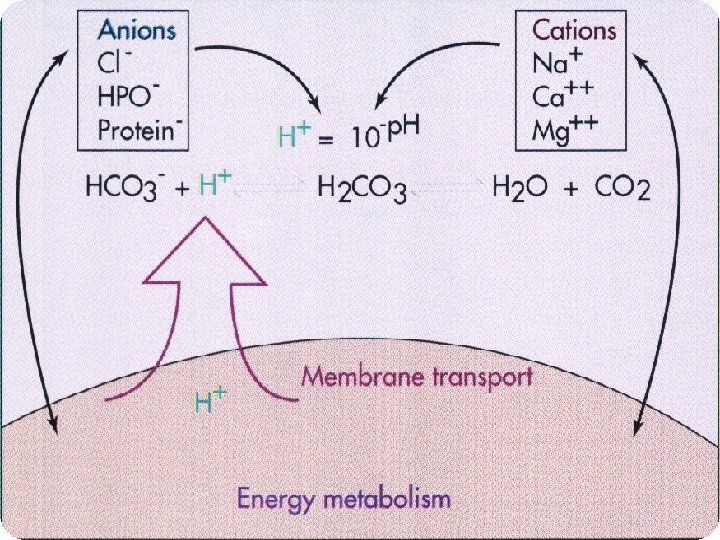
Modelo de Stewart
- Slides: 20