Equao de Onda de Schrdinger Em 1926 Schrdinger









![Configurações Electrónicas dos Catiões e Aniões de Elementos Representativos Na: [Ne]3 s 1 Na+: Configurações Electrónicas dos Catiões e Aniões de Elementos Representativos Na: [Ne]3 s 1 Na+:](https://slidetodoc.com/presentation_image_h2/a8440bd53fcd8b71ef4880b6cfd24b6f/image-26.jpg)































- Slides: 94

Equação de Onda de Schrödinger Em 1926, Schrödinger escreveu uma equação que descrevia simulteamente a natureza ondulatória e corpuscular do electrão. A função de onda (psi) descreve: 1. Energia de e– com uma dada 2. Probabilidade de encontrar e– num dado volume do espaço. A equação de Schrödinger apenas pode ser resolvida com exactidão para o átomo de hidrógénio. 7. 5

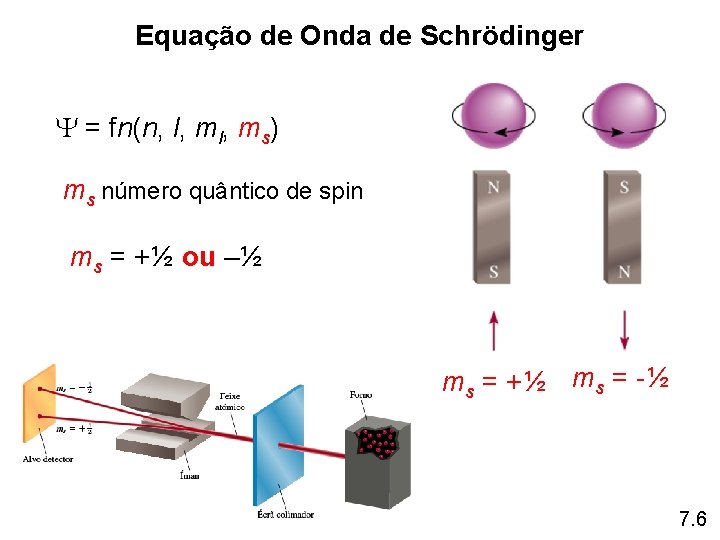
Equação de Onda de Schrodinger fn(n, l, ms) n = número quântico principal n = 1, 2, 3, 4, …. distância de e– a partir do núcleo n=1 n=2 n=3 7. 6

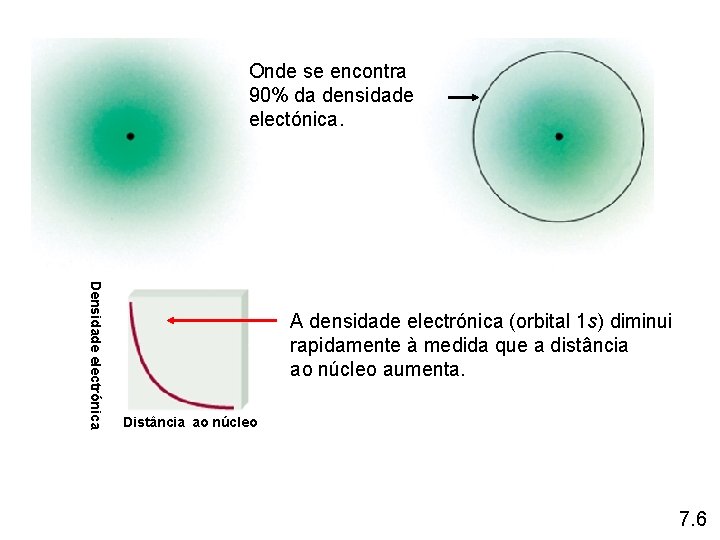
Onde se encontra 90% da densidade electónica. Densidade electrónica A densidade electrónica (orbital 1 s) diminui rapidamente à medida que a distância ao núcleo aumenta. Distância ao núcleo 7. 6

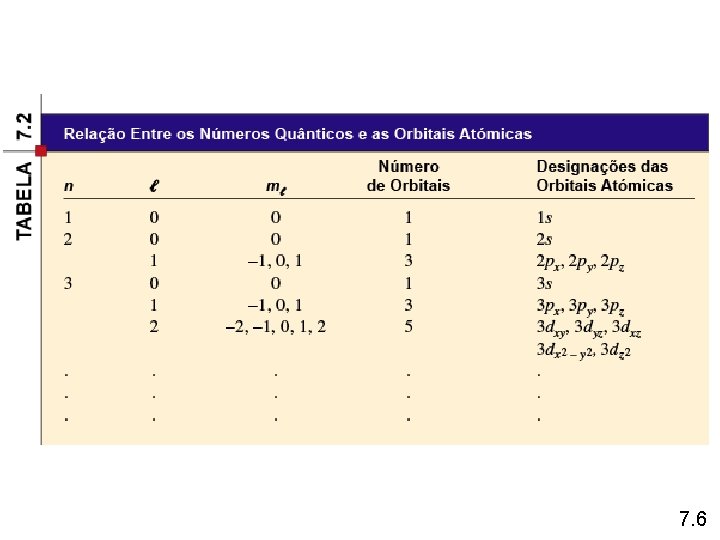
Equação de Onda de Schrodinger = fn(n, l, ms) l número quântico de momento angular para um dado valor de n, l = 0, 1, 2, 3, …, n – 1 n = 1, l = 0 n = 2, l = 0 ou 1 n = 3, l = 0, 1 ou 2 l=0 l=1 l=2 l=3 orbital s orbital p orbital d orbital f Dão forma ao «volume» de espaço que o e– ocupa 7. 6

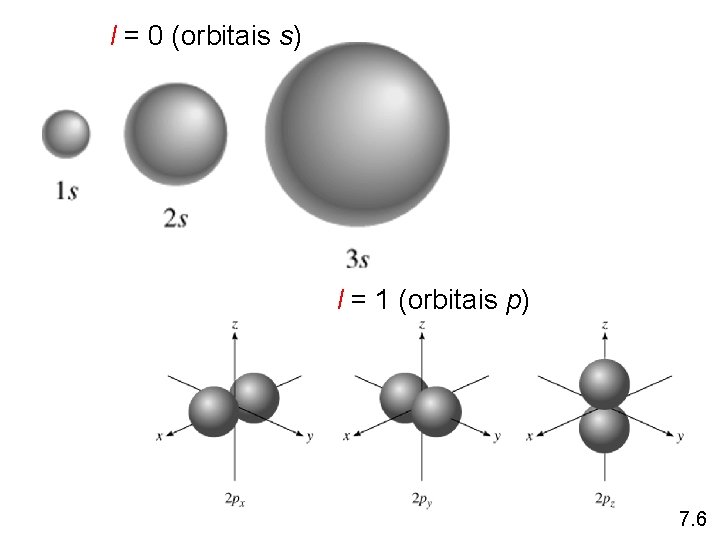
l = 0 (orbitais s) l = 1 (orbitais p) 7. 6

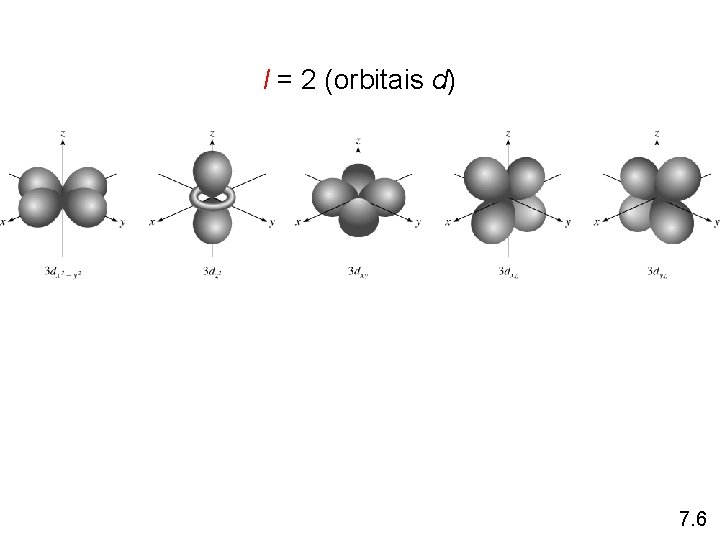
l = 2 (orbitais d) 7. 6

Equação de Onda de Schrodinger = fn(n, l, ms) ml número quântico magnético para um dado valor de l ml = –l, …. , 0, …. + l se l = 1 (orbital p), ml = – 1, 0 ou 1 se l = 2 (orbital d), ml = – 2, – 1, 0, 1 ou 2 orientação da orbital no espaço 7. 6

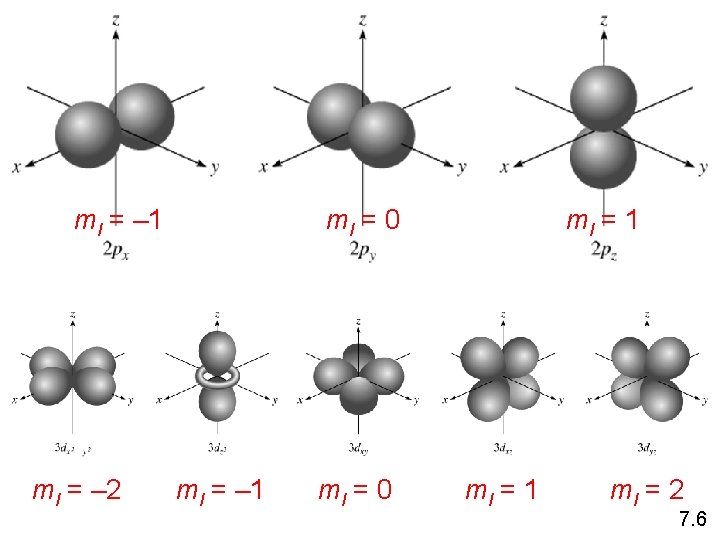
ml = – 1 ml = – 2 ml = 0 ml = – 1 ml = 0 ml = 1 ml = 2 7. 6

Equação de Onda de Schrödinger = fn(n, l, ms) ms número quântico de spin ms = +½ ou –½ ms = +½ ms = -½ 7. 6

Equação de Onda de Schrodinger = fn(n, l, ms) A existência (e a energia) de um electrão num átomo pode apenas ser descrita por uma única função de onda . Princípio de exclusão de Pauli — nenhum par de electrões num átomo pode ter os quatro números quânticos iguais. Cada lugar tem uma idêntificação única (E, R 12, S 8). Cada lugar pode apenas ser ocupado por um indivíduo ao mesmo tempo. 7. 6

7. 6

Equação de Onda de Schrodinger = fn(n, l, ms) Camada — electrões com o mesmo valor de n Subcamada — electrões com os mesmos valores de n e l Orbital — electrões com os mesmos valores de n, l e ml Quantos electrões se podem alojar numa orbital? SE n, l e ml são fixos, então ms = ½ ou –½ = (n, l, ml, ½) ou = (n, l, ml, –½) Uma orbital pode alojar 2 electrões 7. 6

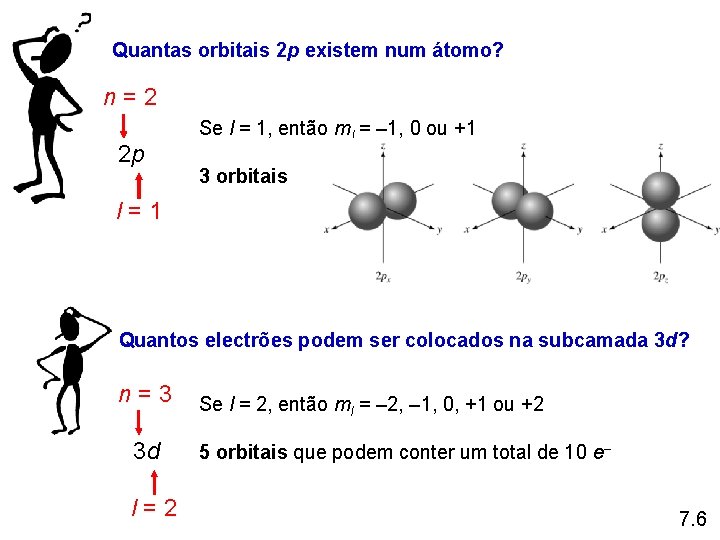
Quantas orbitais 2 p existem num átomo? n=2 2 p Se l = 1, então ml = – 1, 0 ou +1 3 orbitais l=1 Quantos electrões podem ser colocados na subcamada 3 d? n=3 3 d l=2 Se l = 2, então ml = – 2, – 1, 0, +1 ou +2 5 orbitais que podem conter um total de 10 e– 7. 6

Energia das orbitais num átomo com um único electrão A energia apenas depende do número quântico principal n n=3 n=2 En = –RH( 1 n 2 ) n=1 7. 7

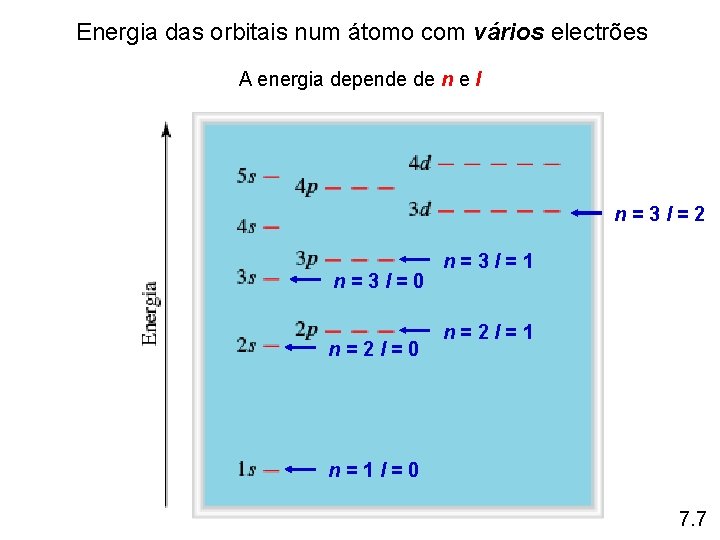
Energia das orbitais num átomo com vários electrões A energia depende de n e l n=3 l=2 n=3 l=0 n=2 l=0 n=3 l=1 n=2 l=1 n=1 l=0 7. 7

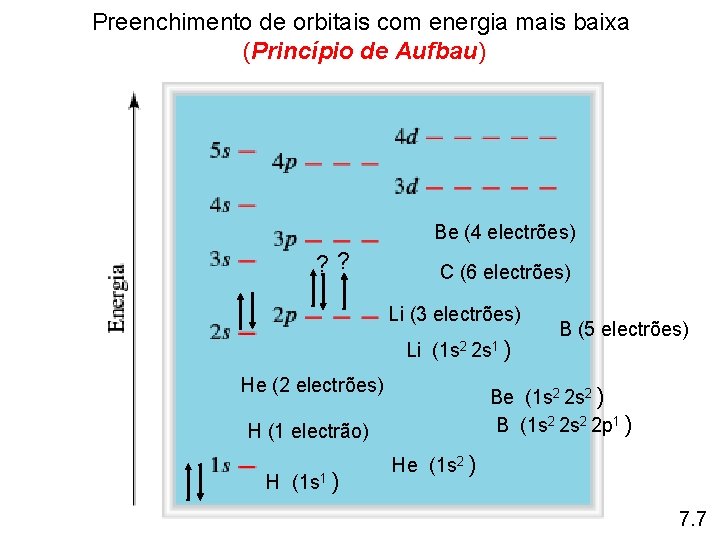
Preenchimento de orbitais com energia mais baixa (Princípio de Aufbau) Be (4 electrões) ? ? C (6 electrões) Li (3 electrões) Li (1 s 2 2 s 1 ) He (2 electrões) Be (1 s 2 2 s 2 ) B (1 s 2 2 p 1 ) H (1 electrão) H (1 s 1 ) B (5 electrões) He (1 s 2 ) 7. 7

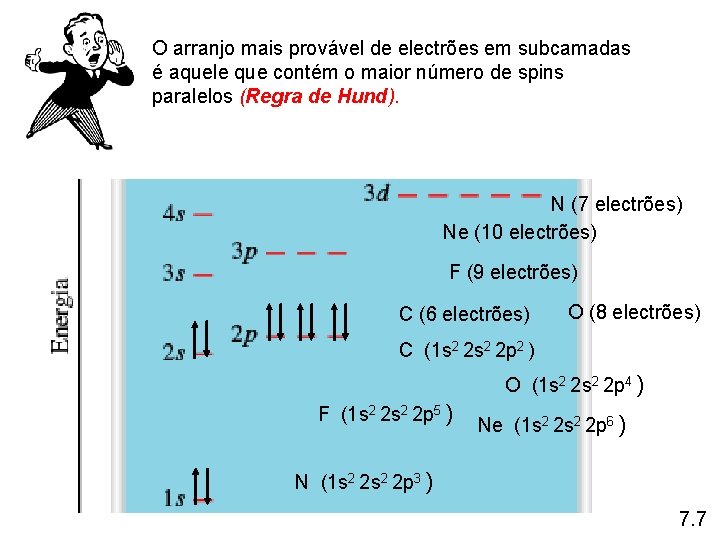
O arranjo mais provável de electrões em subcamadas é aquele que contém o maior número de spins paralelos (Regra de Hund). N (7 electrões) Ne (10 electrões) F (9 electrões) C (6 electrões) O (8 electrões) C (1 s 2 2 p 2 ) O (1 s 2 2 p 4 ) F (1 s 2 2 p 5 ) Ne (1 s 2 2 p 6 ) N (1 s 2 2 p 3 ) 7. 7

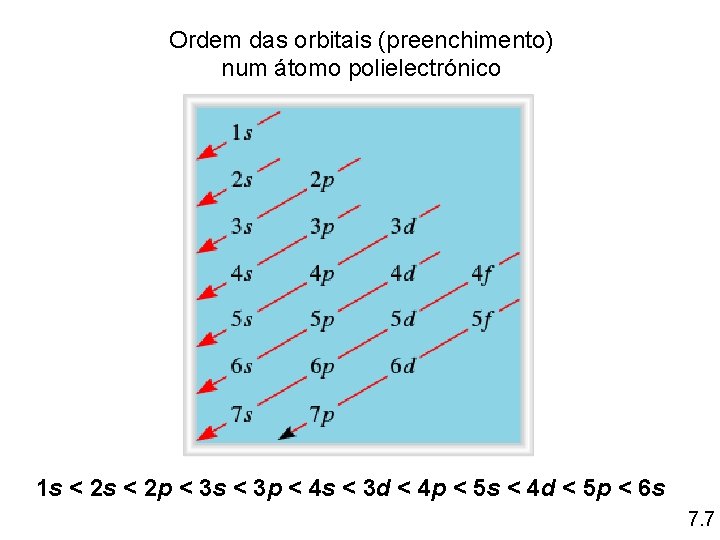
Ordem das orbitais (preenchimento) num átomo polielectrónico 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s 7. 7

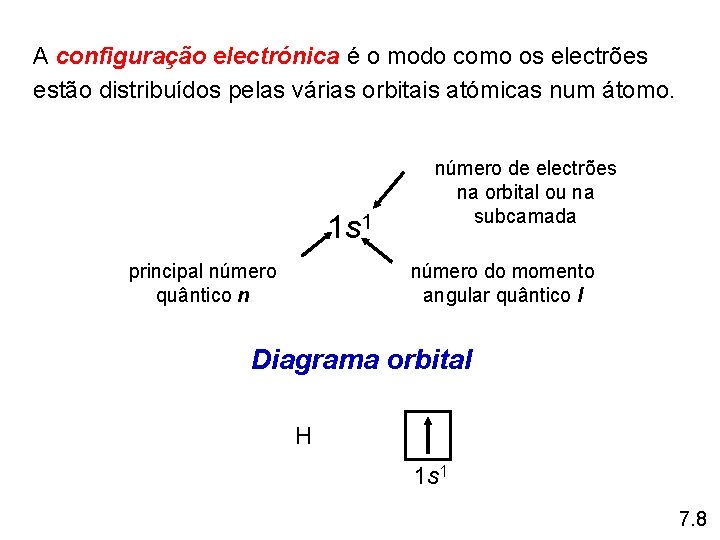
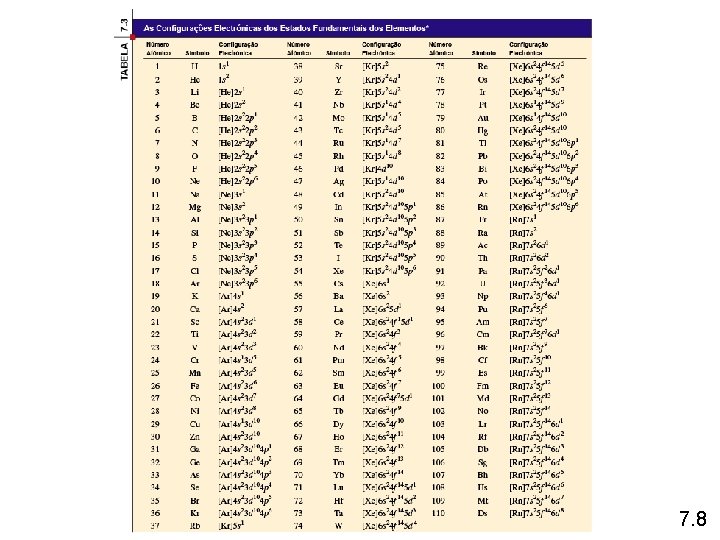
A configuração electrónica é o modo como os electrões estão distribuídos pelas várias orbitais atómicas num átomo. 1 s 1 principal número quântico n número de electrões na orbital ou na subcamada número do momento angular quântico l Diagrama orbital H 1 s 1 7. 8

Qual é a configuração electrónica do Mg? Mg 12 electrões 1 s < 2 p < 3 s < 3 p < 4 s 1 s 2 2 p 6 3 s 2 2 + 6 + 2 = 12 electrões Abreviado [Ne]3 s 2 Quais são os números quânticos possíveis para o último electrão (mais afastado do centro) no Cl? Cl 17 electrões 1 s < 2 p < 3 s < 3 p < 4 s 1 s 2 2 p 6 3 s 2 3 p 5 2 + 6 + 2 + 5 = 17 electrões O último electrão é adicionado à orbital 3 p n=3 l=1 ml = – 1, 0 ou +1 ms = ½ ou –½ 7. 8

7. 8

Capítulo 8 Relações Periódicas Entre Elementos • Desenvolvimento da Tabela Periódica • Classificação Periódica dos Elementos • Variação Periódica das Propriedades Físicas • Energia de Ionização • Afinidade Electrónica • Variação das Propriedades Químicas dos Elementos Representativos Copyright © Mc. Graw-Interamericana de España. Autorização necessária para reprodução ou utilização

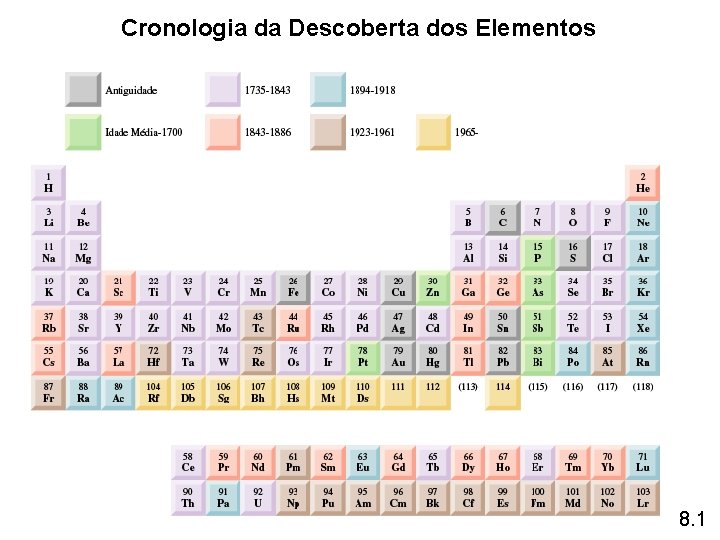
Cronologia da Descoberta dos Elementos 8. 1

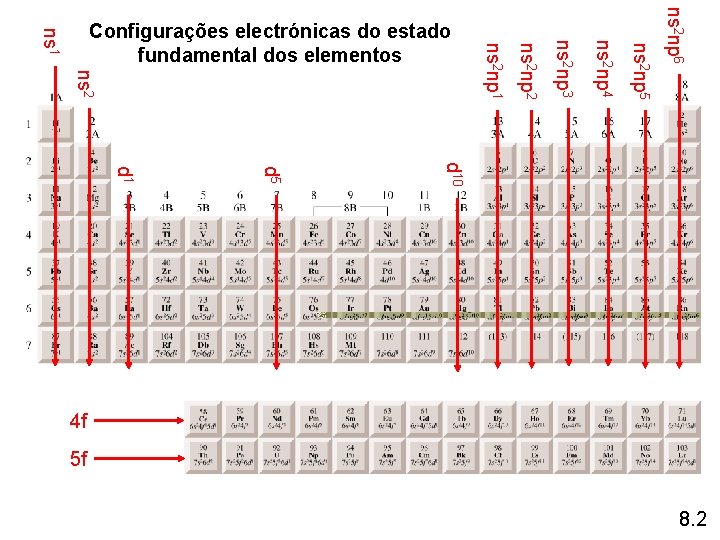
ns 2 np 6 ns 2 np 5 ns 2 np 4 ns 2 np 3 ns 2 np 2 ns 2 np 1 ns 1 Configurações electrónicas do estado fundamental dos elementos d 10 d 5 d 1 4 f 5 f 8. 2

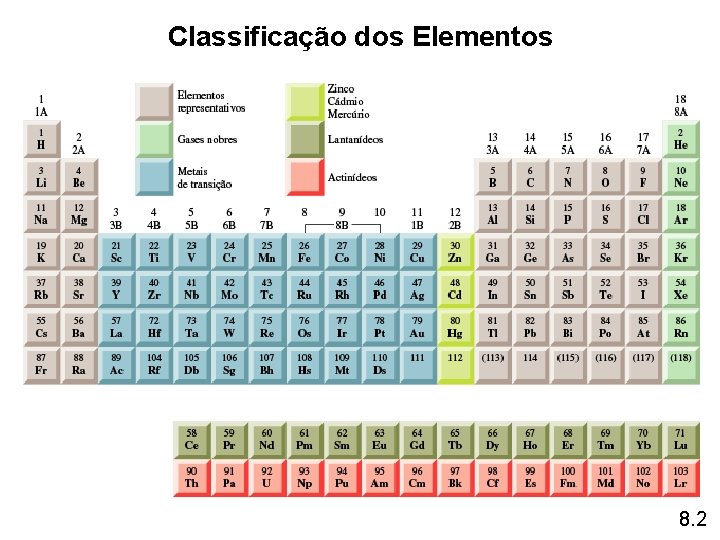
Classificação dos Elementos 8. 2
![Configurações Electrónicas dos Catiões e Aniões de Elementos Representativos Na Ne3 s 1 Na Configurações Electrónicas dos Catiões e Aniões de Elementos Representativos Na: [Ne]3 s 1 Na+:](https://slidetodoc.com/presentation_image_h2/a8440bd53fcd8b71ef4880b6cfd24b6f/image-26.jpg)
Configurações Electrónicas dos Catiões e Aniões de Elementos Representativos Na: [Ne]3 s 1 Na+: [Ne] Ca: [Ar]4 s 2 Ca 2+: [Ar] Al: [Ne]3 s 23 p 1 Al 3+: [Ne] H: 1 s 1 Ganho de electrões ― os aniões têm a configuração de gás nobre. Perda de electrões ― os catiões têm a configuração electrónica de gás nobre. H–: 1 s 2 ou [He] F: 1 s 22 p 5 F–: 1 s 22 p 6 ou [Ne] O: 1 s 22 p 4 O 2–: 1 s 22 p 6 ou [Ne] N: 1 s 22 p 3 N 3–: 1 s 22 p 6 ou [Ne] 8. 2

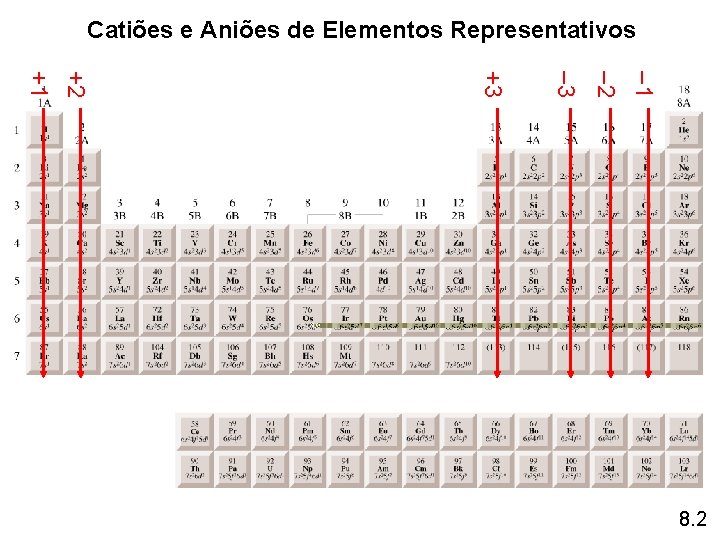
Catiões e Aniões de Elementos Representativos – 1 – 2 – 3 +3 +2 +1 8. 2

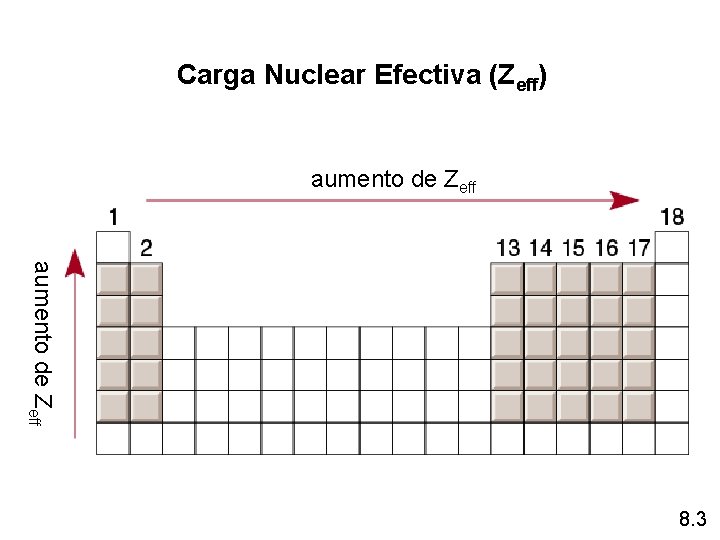
Carga Nuclear Efectiva (Zeff) aumento de Zeff 8. 3

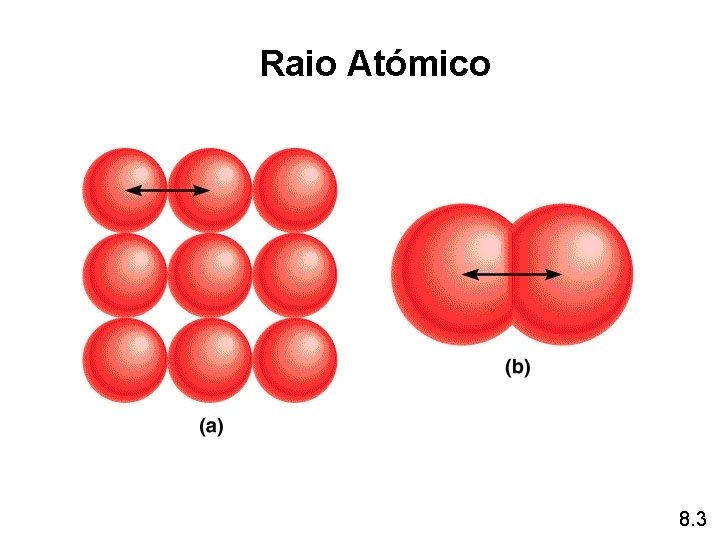
Raio Atómico 8. 3

8. 3

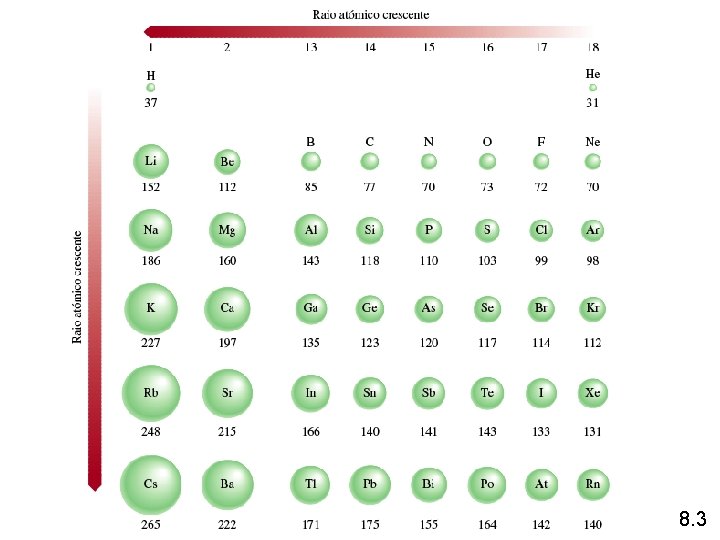
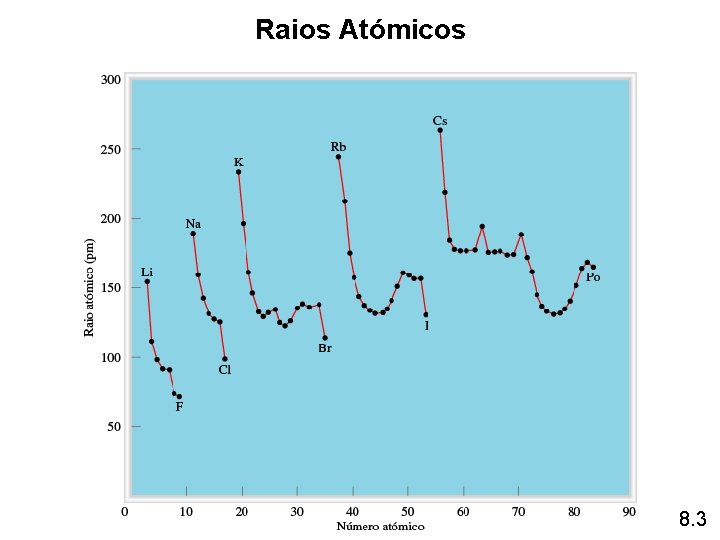
Raios Atómicos 8. 3

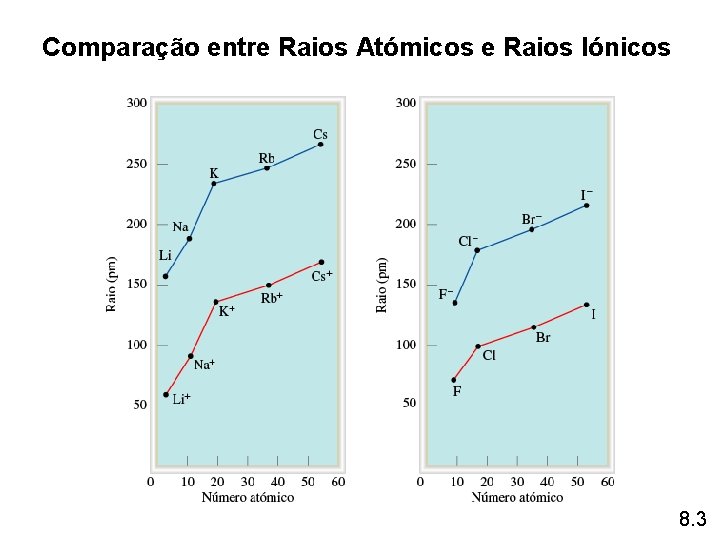
Comparação entre Raios Atómicos e Raios Iónicos 8. 3

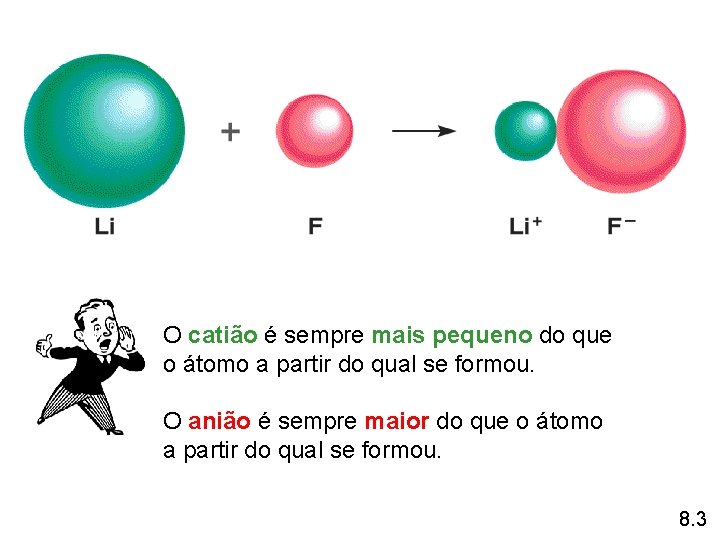
O catião é sempre mais pequeno do que o átomo a partir do qual se formou. O anião é sempre maior do que o átomo a partir do qual se formou. 8. 3

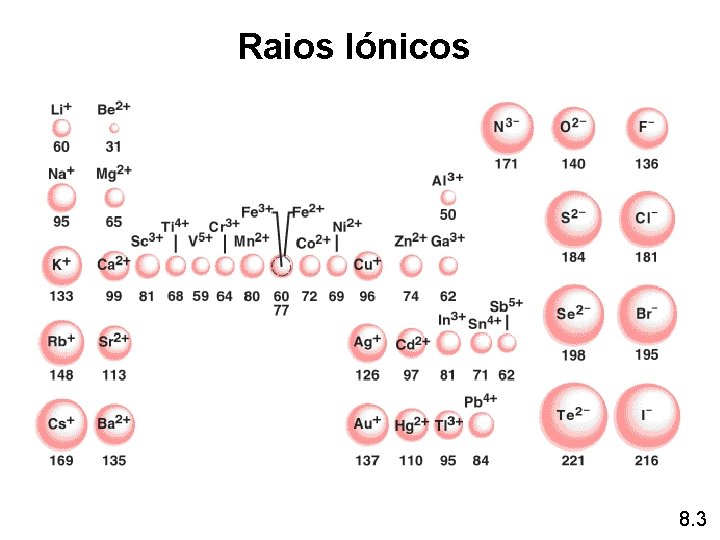
Raios Iónicos 8. 3

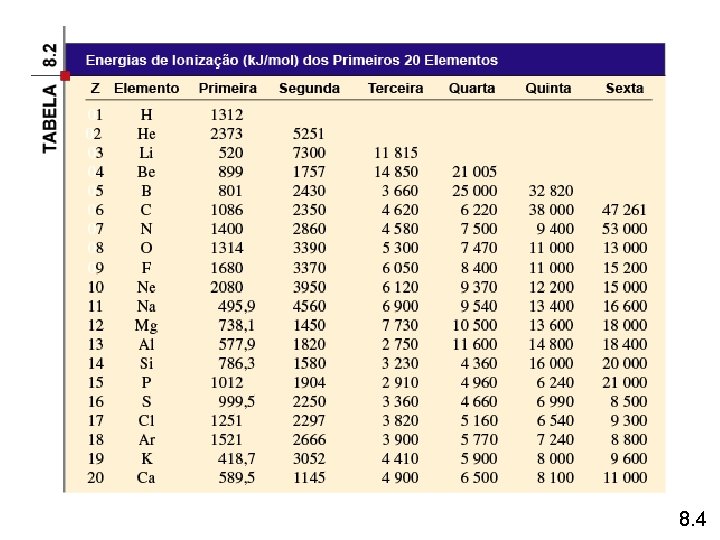
Energia de ionização ― energia mínima necessária (em k. J/mol) para remover um electrão de um átomo no estado gasoso e no seu estado fundamental. I 1 + X (g) I 2 + X+(g) I 3 + X 2+(g) X+(g) + e– X 2+(g) + e– X 3+(g) + e– I 1 primeira energia de ionização I 2 segunda energia de ionização I 3 terceira energia de ionização I 1 < I 2 < I 3 8. 4

8. 4

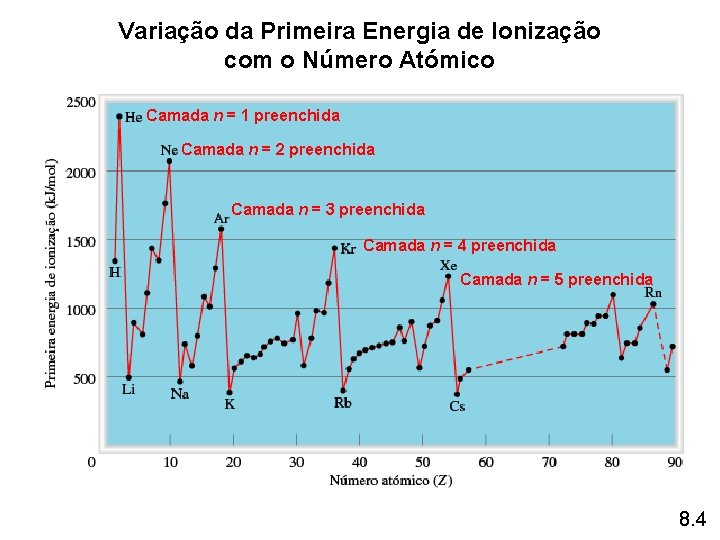
Variação da Primeira Energia de Ionização com o Número Atómico Camada n = 1 preenchida Camada n = 2 preenchida Camada n = 3 preenchida Camada n = 4 preenchida Camada n = 5 preenchida 8. 4

Variação da Primeira Energia de Ionização Aumento da Primeira Energia de Ionização 8. 4

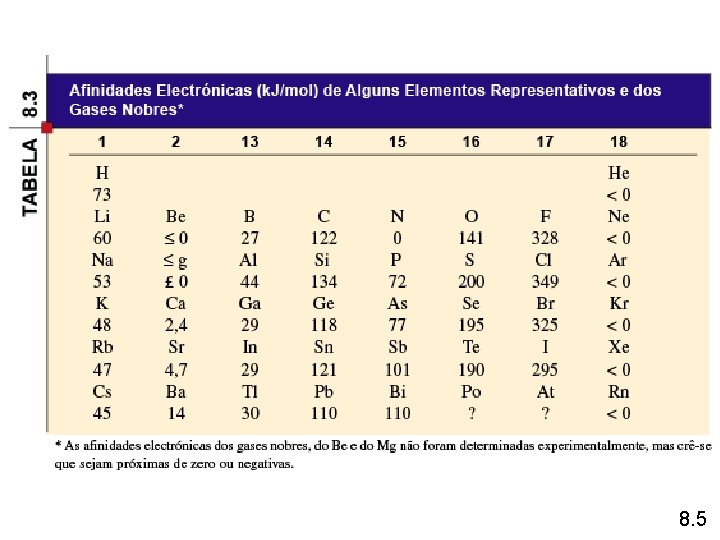
Afinidade electrónica ― o negativo da variação de energia que ocorre quando um electrão é aceite por um átomo no estado gasoso para originar um anião. X (g) + e– X–(g) F (g) + e– X–(g) H = – 328 k. J/mol EA = +328 k. J/mol O (g) + e– O–(g) H = – 141 k. J/mol EA = +141 k. J/mol 8. 5

8. 5

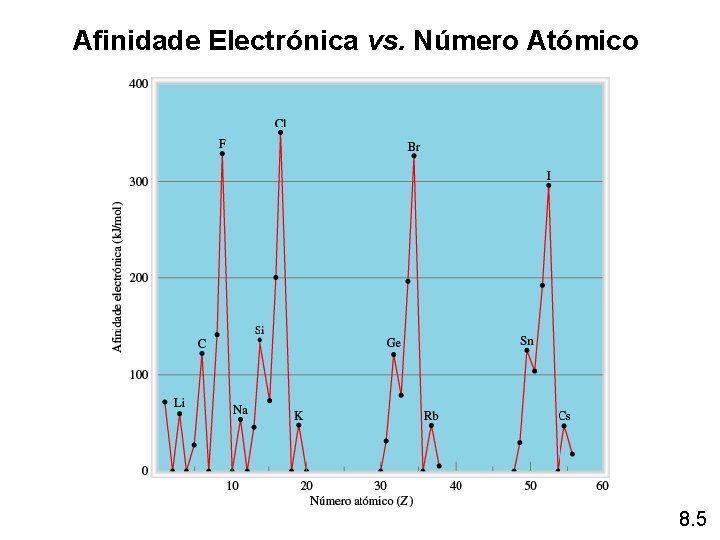
Afinidade Electrónica vs. Número Atómico 8. 5

Capítulo 9 Ligação Química I: Conceitos Básicos • Símbolos de Lewis • Ligação Iónica • Energia de Rede de Compostos Iónicos • Ligação Covalente • Electronegatividade • Escrita de Estruturas de Lewis • Carga Formal e Estruturas de Lewis • Conceito de Ressonância • Excepções à Regra do Octeto • Energia de Ligação Copyright © Mc. Graw-Interamericana de España. Autorização necessária para reprodução ou utilização

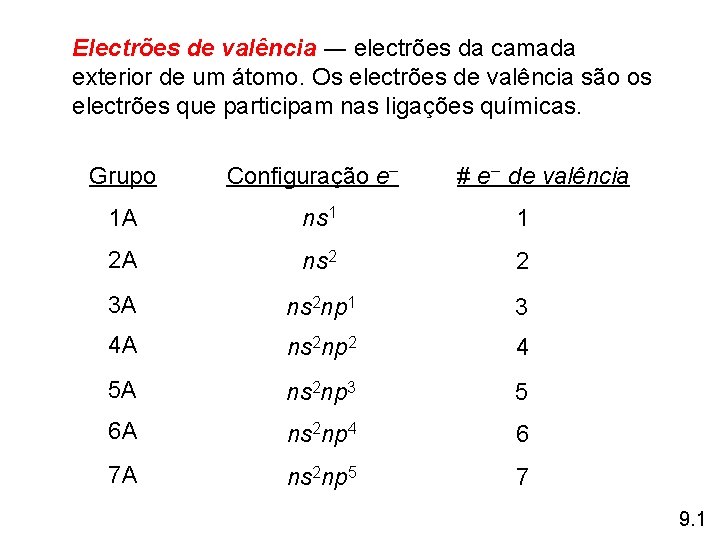
Electrões de valência ― electrões da camada exterior de um átomo. Os electrões de valência são os electrões que participam nas ligações químicas. Grupo Configuração e– # e– de valência 1 A ns 1 1 2 A ns 2 2 3 A ns 2 np 1 3 4 A ns 2 np 2 4 5 A ns 2 np 3 5 6 A ns 2 np 4 6 7 A ns 2 np 5 7 9. 1

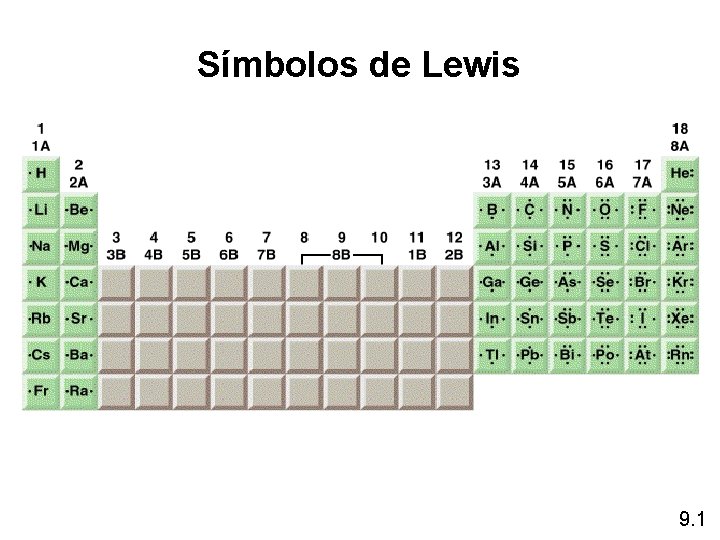
Símbolos de Lewis 9. 1

Ligação Iónica Li 1 s 22 s 1 + F 1 s 22 p 5 Li+ F – 1 s 22 s 22 p 6 Li Li+ + e– e– + F F – Li+ + F – Li+ F – 9. 2

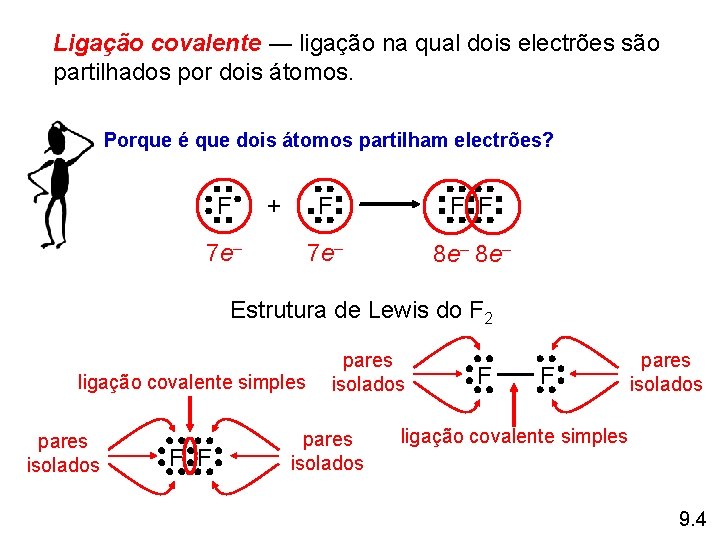
Ligação covalente ― ligação na qual dois electrões são partilhados por dois átomos. Porque é que dois átomos partilham electrões? F + 7 e– F F F 7 e– 8 e– Estrutura de Lewis do F 2 ligação covalente simples pares isolados F F pares isolados ligação covalente simples 9. 4

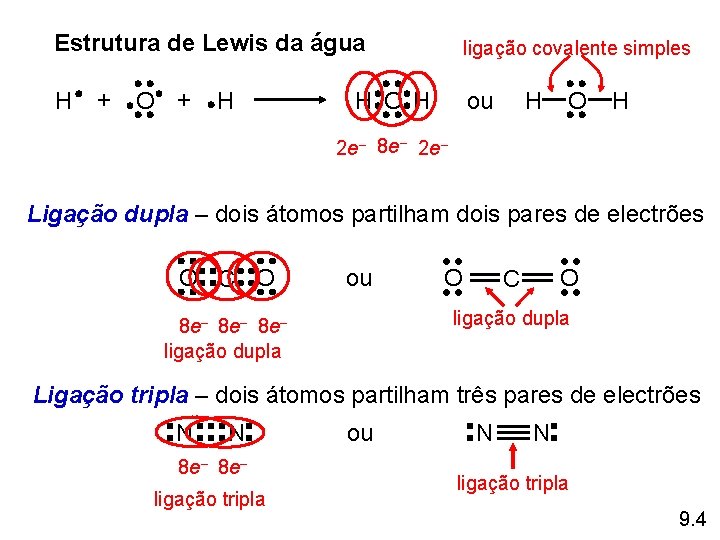
Estrutura de Lewis da água H + O + H ligação covalente simples H O H ou H O H 2 e– 8 e– 2 e– Ligação dupla – dois átomos partilham dois pares de electrões O C O ou O O C ligação dupla 8 e– 8 e– ligação dupla Ligação tripla – dois átomos partilham três pares de electrões N N 8 e– ligação tripla ou N N ligação tripla 9. 4

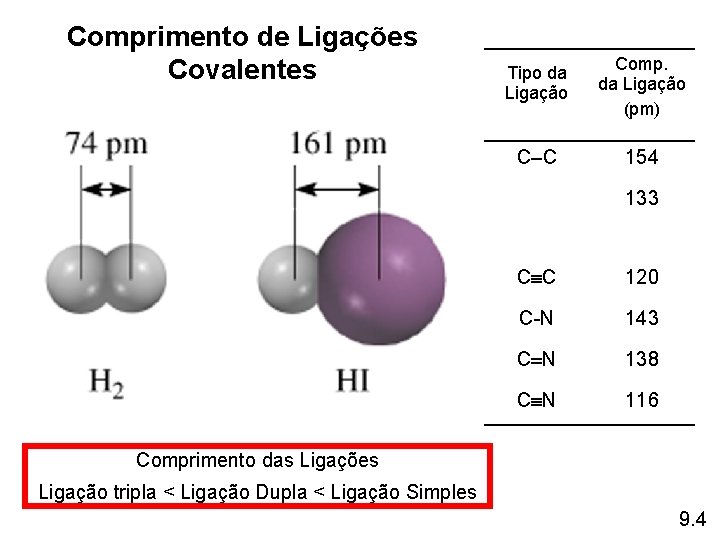
Comprimento de Ligações Covalentes Tipo da Ligação Comp. da Ligação (pm) C–C 154 133 C C 120 C-N 143 C N 138 C N 116 Comprimento das Ligações Ligação tripla < Ligação Dupla < Ligação Simples 9. 4

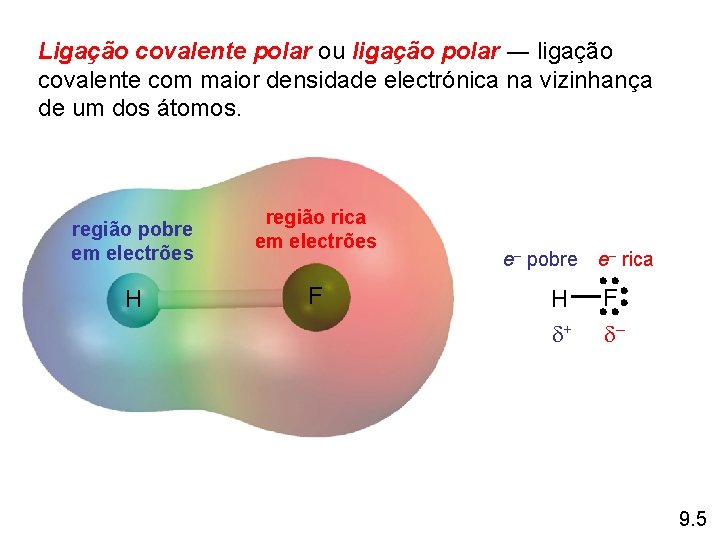
Ligação covalente polar ou ligação polar ― ligação covalente com maior densidade electrónica na vizinhança de um dos átomos. região pobre em electrões H região rica em electrões F e– pobre H + e– rica F – 9. 5

Electronegatividade ― tendência de um átomo para atrair a si os electrões numa ligação. Afinidade electrónica — mensurável, Cl é mais elevada X (g) + e– X–(g) Electronegatividade — relativa, F é mais elevada 9. 5

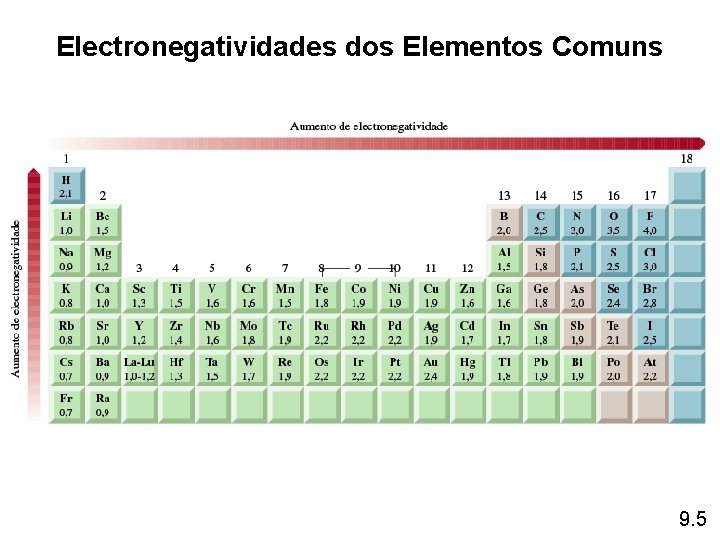
Electronegatividades dos Elementos Comuns 9. 5

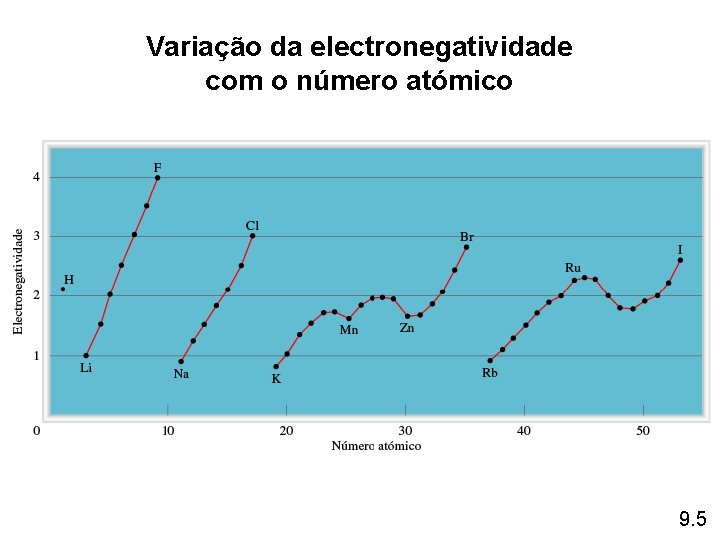
Variação da electronegatividade com o número atómico 9. 5

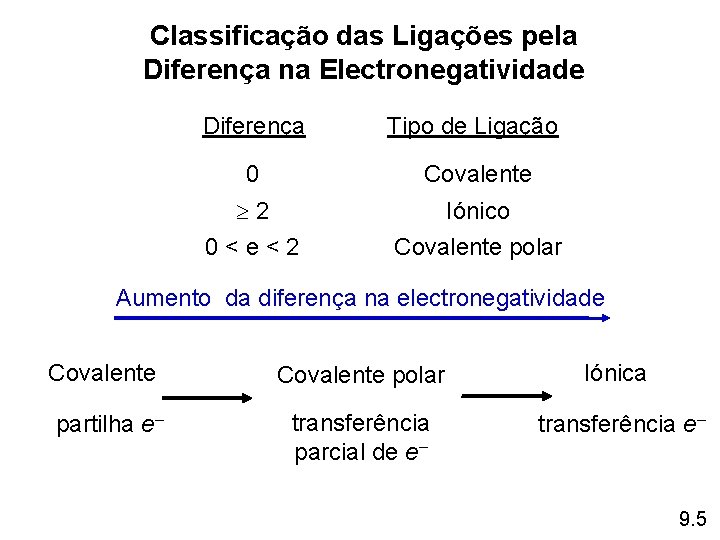
Classificação das Ligações pela Diferença na Electronegatividade Diferença Tipo de Ligação 0 Covalente 2 0<e<2 Iónico Covalente polar Aumento da diferença na electronegatividade Covalente partilha e– Covalente polar Iónica transferência parcial de e– transferência e– 9. 5

Classifique as seguintes ligações como iónicas, covalentes polares ou covalente: a ligação em Cs. Cl; a ligação em H 2 S e a ligação NN em H 2 NNH 2. Cs – 0, 7 Cl – 3, 0 – 0, 7 = 2, 3 Iónica H – 2, 1 S – 2, 5 – 2, 1 = 0, 4 Covalente polar N – 3, 0 – 3, 0 = 0 Covalente 9. 5

Capítulo 3 Relações Mássicas em Reacções Químicas • Massa Atómica • N. º de Avogadro e Massa Molar • Massa Molecular • Espectrómetro de Massa • Composição Percentual dos Compostos • Determinação Experimental de Fórmulas Químicas • Reacções Químicas e Equações Químicas • Quantidades de Reagentes e Produtos • Reagentes Limitantes • Rendimento da Reacção Copyright © Mc. Graw-Interamericana de España. Autorização necessária para reprodução ou utilização

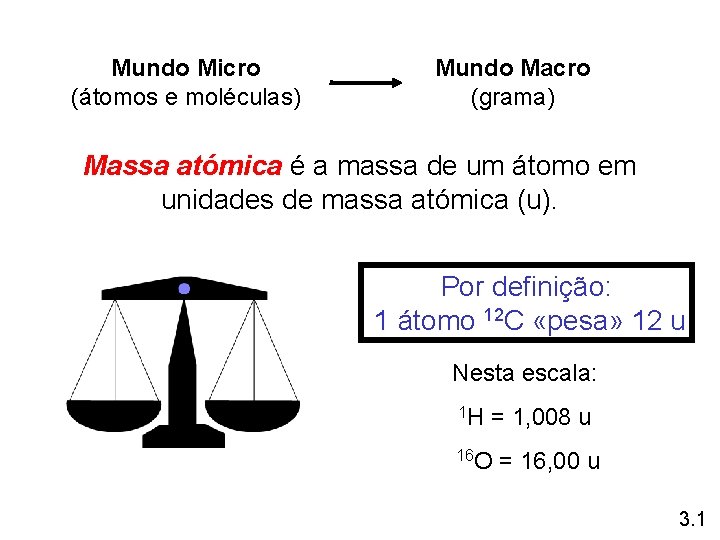
Mundo Micro (átomos e moléculas) Mundo Macro (grama) Massa atómica é a massa de um átomo em unidades de massa atómica (u). Por definição: 1 átomo 12 C «pesa» 12 u Nesta escala: 1 H = 1, 008 u 16 O = 16, 00 u 3. 1

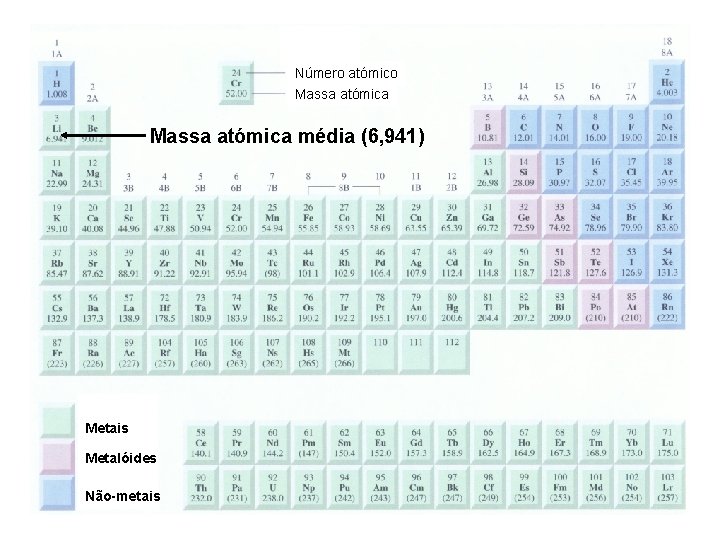
Lítio é: 7, 42% 6 Li (6, 015 u) 92, 58% 7 Li (7, 016 u) Massa atómica média do lítio: 7, 42 × 6, 015 + 92, 58 × 7, 016 = 6, 941 u 100 3. 1

Número atómico Massa atómica média (6, 941) Metais Metalóides Não-metais

Um mole (mol) é a quantidade de substância que contém tantas entidades elementares (átomos, moléculas ou outras partículas) quantas existem em, exactamente, 12 g (ou 0, 012 kg) de 12 C. 1 mol = NA = 6, 0221367 × 1023 Número de Avogadro (NA) 3. 2

Massa molar é a massa de 1 mole de ovos sapatos em berlindes átomos grama 1 mole 12 C átomos = 6, 022 × 1023 átomos = 12, 00 g 1 12 C átomos = 12, 00 u 1 mole 12 C átomos = 12, 00 g 12 C 1 mole átomos de lítio = 6, 941 g de Li Para qualquer elemento massa atómica (u) = massa molar (gramas) 3. 2

Um mole de… S C Hg Cu Fe 3. 2

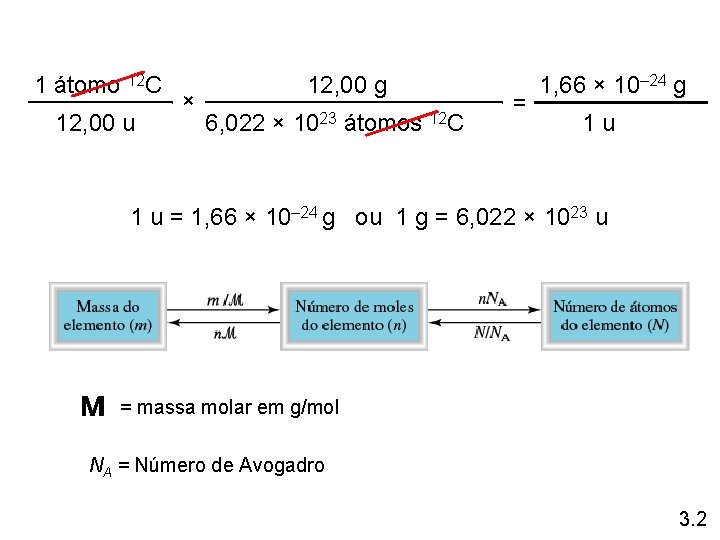
1 átomo 12 C 12, 00 u × 12, 00 g 6, 022 × 1023 átomos 12 C = 1, 66 × 10– 24 g 1 u 1 u = 1, 66 × 10– 24 g ou 1 g = 6, 022 × 1023 u = massa molar em g/mol NA = Número de Avogadro 3. 2

Compreende a Massa Molar? Quantos átomos existem em 0, 551 g de potássio (K)? 1 mol K = 39, 10 g K 1 mol K = 6, 022 × 1023 átomos K 0, 551 g K × 1 mol K 39, 10 g K × 6, 022 × 1023 átomos K 1 mol K = = 8, 49 × 1021 átomos K 3. 2

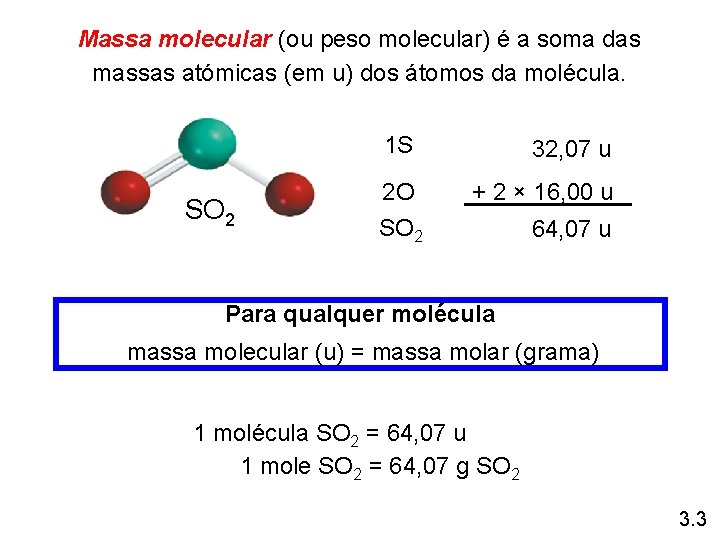
Massa molecular (ou peso molecular) é a soma das massas atómicas (em u) dos átomos da molécula. 1 S SO 2 2 O SO 2 32, 07 u + 2 × 16, 00 u 64, 07 u Para qualquer molécula massa molecular (u) = massa molar (grama) 1 molécula SO 2 = 64, 07 u 1 mole SO 2 = 64, 07 g SO 2 3. 3

Compreende a Massa Molecular? Quantos átomos H existem em 72, 5 g de C 3 H 8 O ? 1 mol C 3 H 8 O = (3 × 12) + (8 × 1) + 16 = 60 g C 3 H 8 O 1 mol C 3 H 8 O moléculas = 8 mol átomos H 1 mol H = 6, 022 × 1023 átomos H 72, 5 g C 3 H 8 O × 1 mol C 3 H 8 O 60 g C 3 H 8 O × 8 mol átomos H 1 mol C 3 H 8 O × 6, 022 × 1023 átomos H 1 mol átomos H = = 5, 82 × 1024 átomos H 3. 3

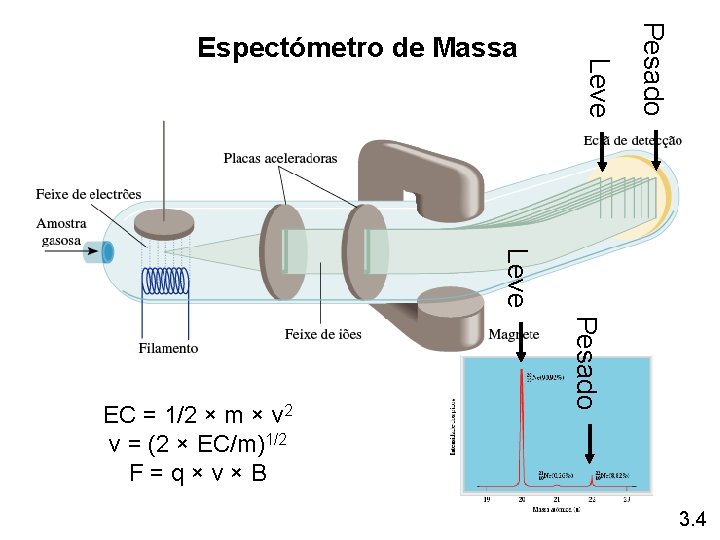
Pesado Leve Espectómetro de Massa Leve Pesado EC = 1/2 × m × v 2 v = (2 × EC/m)1/2 F=q×v×B 3. 4

% composição percentual de um elemento num composto = n × massa molar do elemento massa molar do composto × 100% n é o número de moles do elemento em 1 mole do composto 2 × (12, 01 g) %C = 46, 07 g 6 × (1, 008 g) %H = 46, 07 g 1 × (16, 00 g) %O = 46, 07 g C 2 H 6 O × 100% = 52, 14% × 100% = 13, 13% × 100% = 34, 73% 52, 14% + 13, 13% + 34, 73% = 100, 0% 3. 5

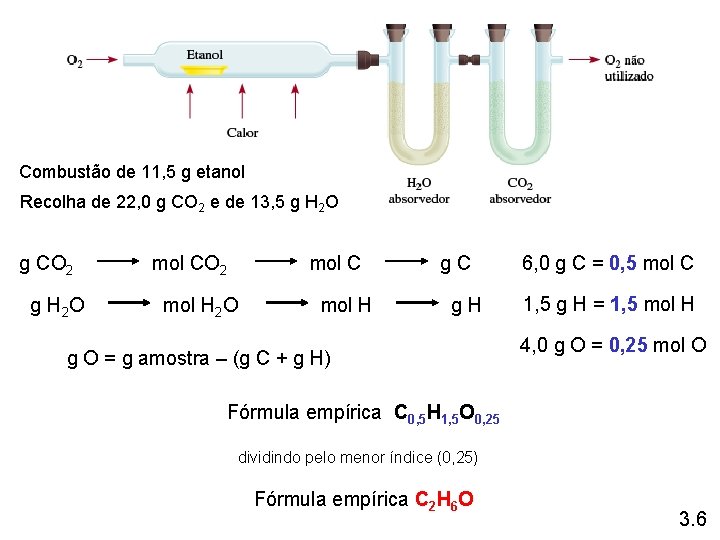
Combustão de 11, 5 g etanol Recolha de 22, 0 g CO 2 e de 13, 5 g H 2 O g CO 2 g H 2 O mol CO 2 mol H 2 O mol H g. C g. H g O = g amostra – (g C + g H) 6, 0 g C = 0, 5 mol C 1, 5 g H = 1, 5 mol H 4, 0 g O = 0, 25 mol O Fórmula empírica C 0, 5 H 1, 5 O 0, 25 dividindo pelo menor índice (0, 25) Fórmula empírica C 2 H 6 O 3. 6

Um processo no qual uma substância (ou substâncias) se transforma numa ou mais novas substância é uma reacção química. Uma equação química usa símbolos químicos para mostrar o que acontece durante uma reacção. 3 maneiras de representar a reacção de H 2 com O 2 para formar H 2 O reagentes produtos 3. 7

Como «Ler» Equações Químicas 2 Mg + O 2 2 Mg. O 2 átomos Mg + 1 molécula O 2 para dar 2 moléculas Mg. O 2 mole Mg + 1 mole O 2 para dar 2 mole Mg. O 48, 6 grama Mg + 32, 0 grama O 2 para dar 80, 6 g Mg. O NÃO É 2 g Mg + 1 g O 2 para dar 2 g Mg. O 3. 7

Acertar Equações Químicas 1. Escreva a fórmula(s) correcta dos reagentes no lado esquerdo e a fórmula(s) correcta do produto(s) no lado direito da equação. O etano reage com oxigénio para formar dióxido de carbono e água C 2 H 6 + O 2 CO 2 + H 2 O 1. Altere os números das fórmulas (coeficientes) para que o número de átomos de cada elemento seja igual em ambos os lados da equação. Não altere os índices. 2 C 2 H 6 NÃO C 4 H 12 3. 7

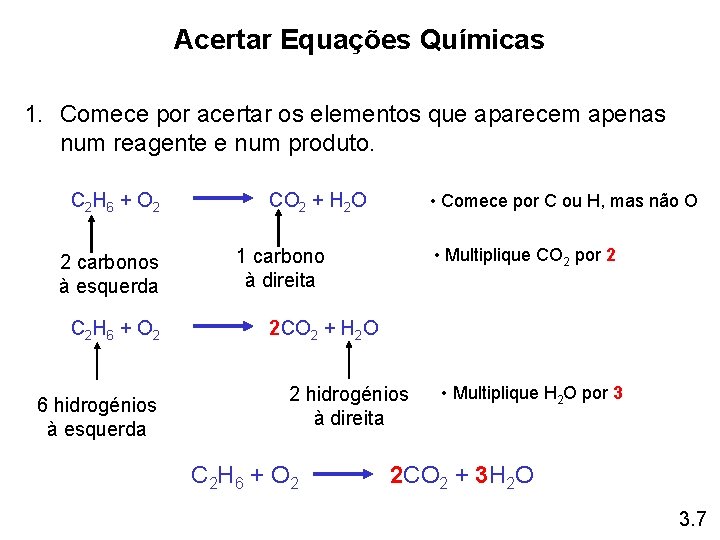
Acertar Equações Químicas 1. Comece por acertar os elementos que aparecem apenas num reagente e num produto. C 2 H 6 + O 2 2 carbonos à esquerda C 2 H 6 + O 2 6 hidrogénios à esquerda CO 2 + H 2 O • Comece por C ou H, mas não O • Multiplique CO 2 por 2 1 carbono à direita 2 CO 2 + H 2 O 2 hidrogénios à direita C 2 H 6 + O 2 • Multiplique H 2 O por 3 2 CO 2 + 3 H 2 O 3. 7

Acertar Equações Químicas 1. Acerte os elementos que aparecem em dois ou mais reagentes ou produtos. C 2 H 6 + O 2 2 CO 2 + 3 H 2 O 2 oxigénios à esquerda C 2 H 6 + 7 O 2 2 2 C 2 H 6 + 7 O 2 • Multiplique O 2 por 7 2 4 oxigénios + 3 oxigénios = 7 oxigénio à direita (3× 1) (2× 2) 2 CO 2 + 3 H 2 O • Remova a fracção multiplicando ambos os lados por 2 4 CO 2 + 6 H 2 O 3. 7

Acertar Equações Químicas 1. Assegure-se de que tem o mesmo número de cada tipo de átomo em ambos os lados da equação. 2 C 2 H 6 + 7 O 2 4 CO 2 + 6 H 2 O 4 C (2 × 2) 4 C 12 H (2 × 6) 12 H (6 × 2) 14 O (7 × 2) 14 O (4 × 2 + 6) Reagentes Produtos 4 C 4 C 12 H 14 O 3. 7

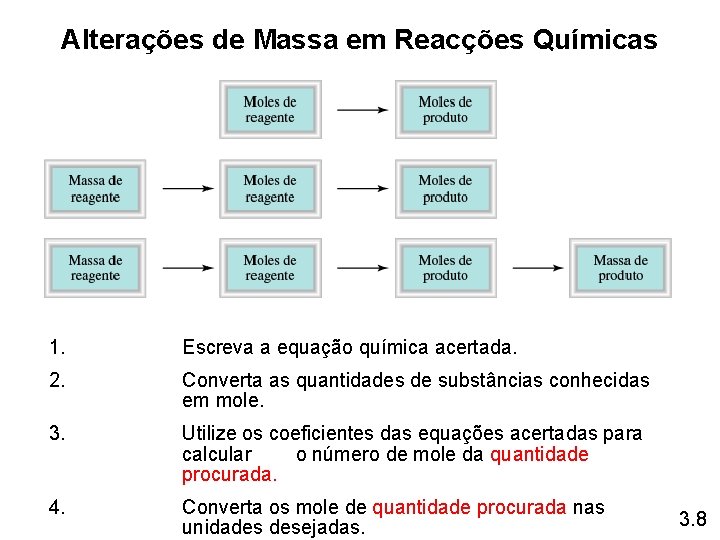
Alterações de Massa em Reacções Químicas 1. Escreva a equação química acertada. 2. Converta as quantidades de substâncias conhecidas em mole. 3. Utilize os coeficientes das equações acertadas para calcular o número de mole da quantidade procurada. 4. Converta os mole de quantidade procurada nas unidades desejadas. 3. 8

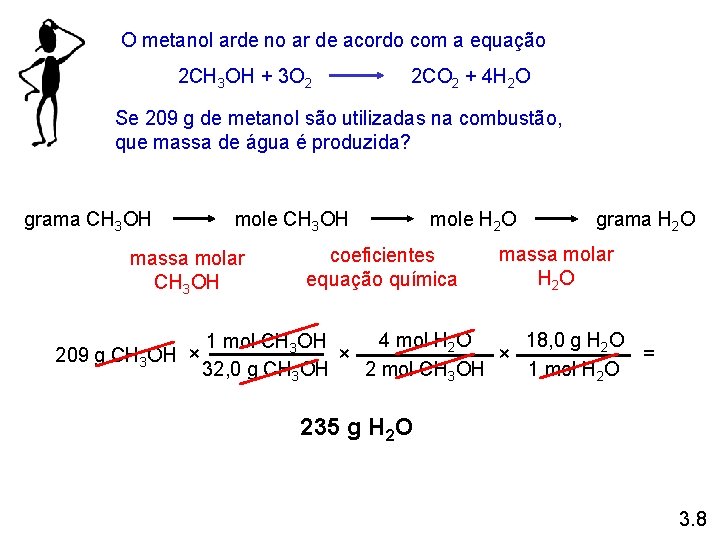
O metanol arde no ar de acordo com a equação 2 CH 3 OH + 3 O 2 2 CO 2 + 4 H 2 O Se 209 g de metanol são utilizadas na combustão, que massa de água é produzida? grama CH 3 OH mole CH 3 OH massa molar CH 3 OH mole H 2 O coeficientes equação química grama H 2 O massa molar H 2 O 4 mol H 2 O 18, 0 g H 2 O 1 mol CH 3 OH = × × 209 g CH 3 OH × 32, 0 g CH 3 OH 1 mol H 2 O 2 mol CH 3 OH 235 g H 2 O 3. 8

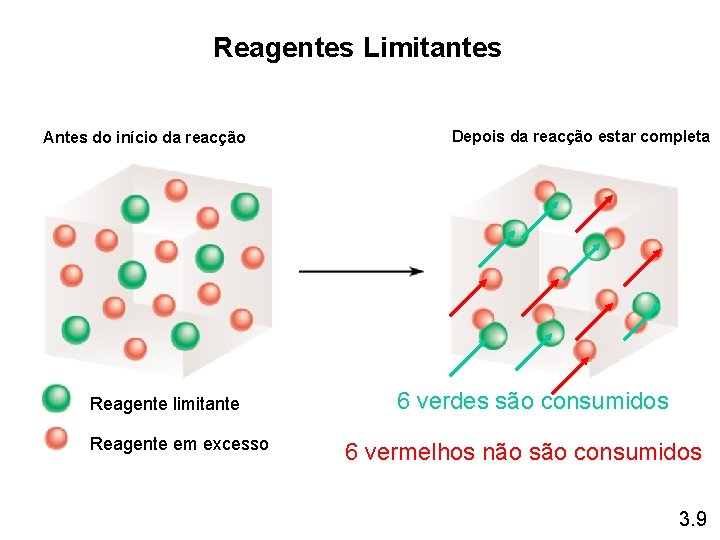
Reagentes Limitantes Antes do início da reacção Reagente limitante Reagente em excesso Depois da reacção estar completa 6 verdes são consumidos 6 vermelhos não são consumidos 3. 9

Compreende os Reagentes Limitantes? Num processo, 124 g de Al reagem com 601 g de Fe 2 O 3 2 Al + Fe 2 O 3 Al 2 O 3 + 2 Fe Calcule a massa de Al 2 O 3 formada. g Al mol Fe 2 O 3 necessárias mol Al g Fe 2 O 3 124 g Al × mol Fe 2 O 3 1 mol Al 27, 0 g Al × Início 124 g Al mol Al necessárias 1 mol Fe 2 O 3 2 mol Al × 160 g Fe 2 O 3 1 mol Fe 2 O 3 g Fe 2 O 3 necessárias g Al necessárias = 367 g Fe 2 O 3 necessárias Como temos mais de Fe 2 O 3 (601 g), o Al é o reagente limitante 3. 9

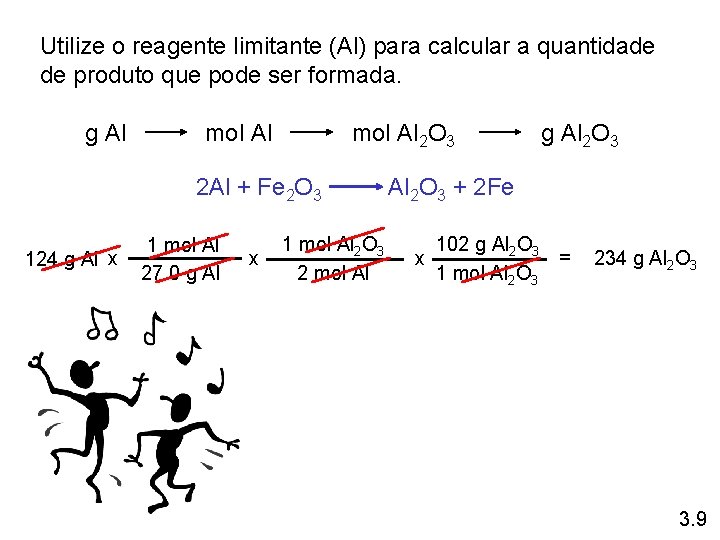
Utilize o reagente limitante (Al) para calcular a quantidade de produto que pode ser formada. g Al mol Al 2 O 3 2 Al + Fe 2 O 3 124 g Al x 1 mol Al 27. 0 g Al x 1 mol Al 2 O 3 2 mol Al g Al 2 O 3 + 2 Fe 102 g Al 2 O 3 = x 1 mol Al 2 O 3 234 g Al 2 O 3 3. 9

Rendimento teórico é a quantidade de produto que se forma se todo o reagente limitante for consumido durante a reacção. Rendimento real é a quantidade de produto obtido na reacção química. % rendimento = Rendimento real Rendimento teórico × 100 3. 10

Concentração de soluções

Solução Estequiométrica A concentração de uma solução é a quantidade de soluto presente numa dada quantidade de solvente ou solução. M = molaridade = mole de soluto litros de solução Que massa de KI é necessária para formar 500 m. L de uma solução 2, 80 M KI? volume KI 500 m. L x M KI 1 L 1000 m. L moles KI x 2, 80 mol KI 1 L M KI x gramas KI 166 g KI 1 mol KI = 232 g KI 4. 5

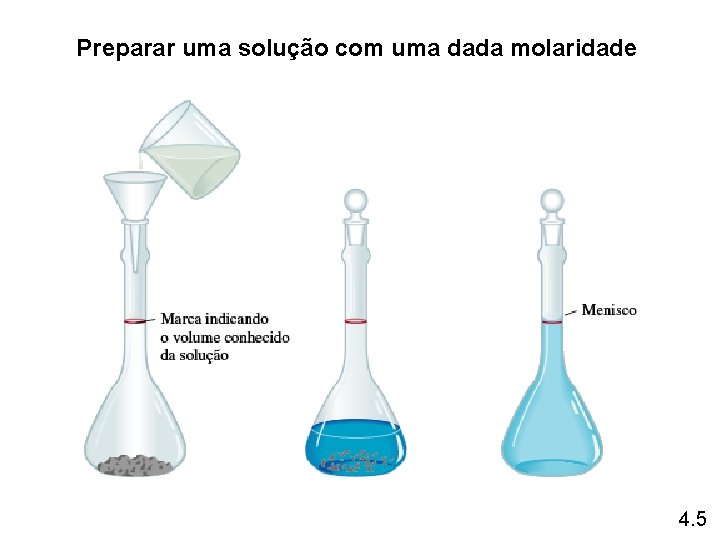
Preparar uma solução com uma dada molaridade 4. 5

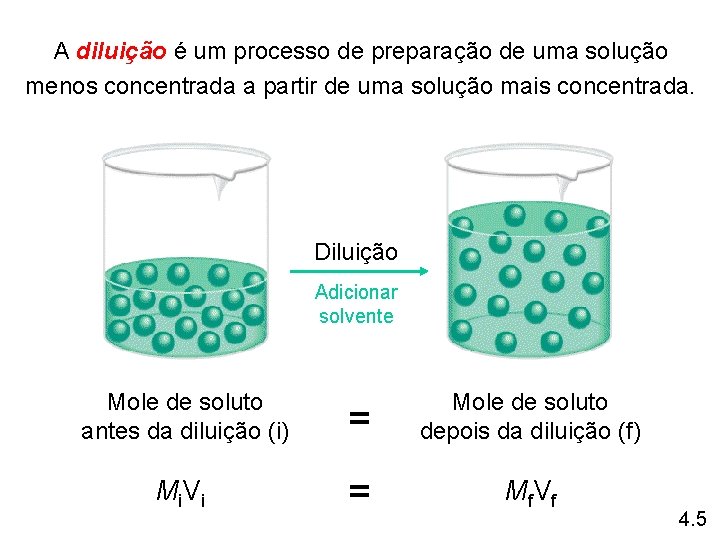
A diluição é um processo de preparação de uma solução menos concentrada a partir de uma solução mais concentrada. Diluição Adicionar solvente Mole de soluto antes da diluição (i) = Mole de soluto depois da diluição (f) Mi V i = Mf V f 4. 5

Como prepararia 60, 0 m. L de uma solução 0, 2 M HNO 3 a partir de uma solução de 4, 00 M HNO 3? Mi V i = Mf V f Mi = 4, 00 Vi = Mf = 0, 200 Mf V f Mi Vf = 0, 06 L Vi = ? L 0, 200 × 0, 06 = = 0, 003 L = 3 m. L 4, 00 3 m. L de ácido + 57 m. L de água = 60 m. L de solução 4. 5

Capítulo 5 Gases • Substâncias que Existem como Gases • Pressão de um Gás • Leis dos Gases • Equação do Gás Ideal • Estequiometria com Gases • Lei de Dalton das Pressões Parciais • Teoria Cinética Molecular dos Gases • Desvios ao Comportamento Ideal Copyright © Mc. Graw-Interamericana de España. Autorização necessária para reprodução ou utilização

Equação do Gás Ideal 1 Lei de Boyle: V (com n e T constantes) P Lei de Charles: V T (com n e P constantes) Lei de Avogadro: V n (com P e T constantes) n. T V P n. T V = constante × =R P P R é a constante dos gases PV = n. RT 5. 4

As condições 0ºC e 1 atm chamam-se condições de pressão e temperatura padrão (PTP). Experiências demonstram que a PTP, 1 mole de um gás ideal ocupa 22, 414 L. PV = n. RT (1 atm)(22, 414 L) PV R= = n. T (1 mol)(273, 15 K) R = 0, 082057 L • atm/(mol • K) 5. 4

Qual é o volume (em litros) ocupado por 49, 8 g de HCl a PTP? T = 0 0 C = 273, 15 K PV = n. RT V= P = 1 atm 1 mol HCl n = 49, 8 g × = 1, 37 mol 36, 45 g HCl L • atm 1, 37 mol × 0, 0821 mol × 273, 15 K • K 1 atm V = 30, 6 L 5. 4

O árgon é um gás inerte usado no interior das lâmpadas para retardar a vaporização do filamento. Uma lâmpada contendo árgon a 1, 20 atm a 18 0 C foi aquecida a 850 C, a volume constante. Qual é a pressão final do árgon no interior da lâmpada (em atm)? PV = n. RT n. R P = T V P 1 T 1 P 2 = P 1 × = n, V e R são constantes = constante P 1 = 1, 20 atm P 2 = ? T 1 = 291 K T 2 = 358 K P 2 T 2 T 1 = 1, 20 atm × 358 K 291 K = 1, 48 atm 5. 4

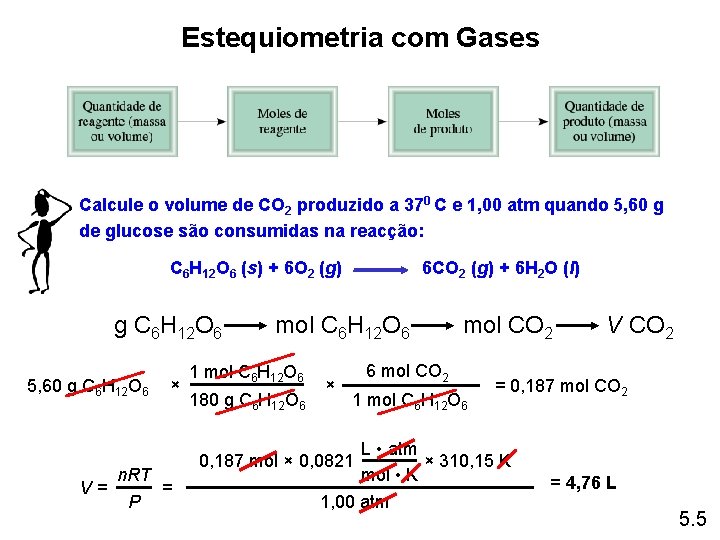
Estequiometria com Gases Calcule o volume de CO 2 produzido a 370 C e 1, 00 atm quando 5, 60 g de glucose são consumidas na reacção: C 6 H 12 O 6 (s) + 6 O 2 (g) g C 6 H 12 O 6 5, 60 g C 6 H 12 O 6 V= n. RT P × 6 CO 2 (g) + 6 H 2 O (l) mol C 6 H 12 O 6 180 g C 6 H 12 O 6 × mol CO 2 6 mol CO 2 1 mol C 6 H 12 O 6 V CO 2 = 0, 187 mol CO 2 L • atm × 310, 15 K mol • K 1, 00 atm 0, 187 mol × 0, 0821 = = 4, 76 L 5. 5

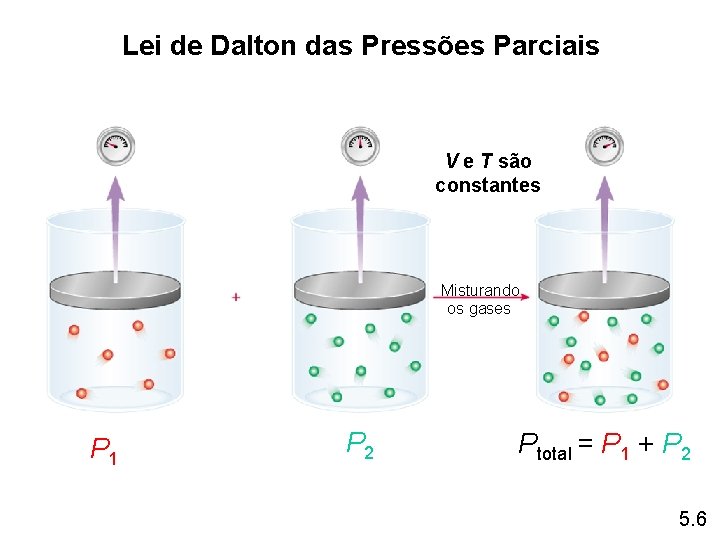
Lei de Dalton das Pressões Parciais V e T são constantes Misturando os gases P 1 P 2 Ptotal = P 1 + P 2 5. 6

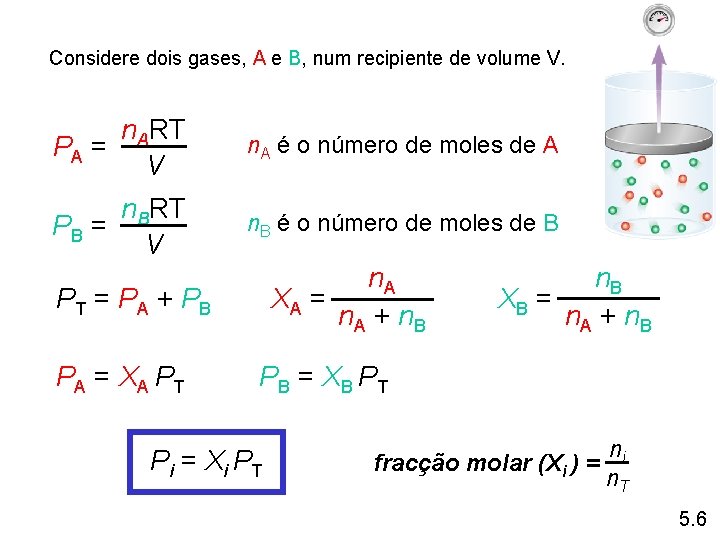
Considere dois gases, A e B, num recipiente de volume V. n. ART PA = V n. A é o número de moles de A n. BRT PB = V n. B é o número de moles de B n. A XA = n. A + n. B PT = PA + PB PA = XA PT n. B XB = n. A + n. B PB = XB PT Pi = Xi PT fracção molar (Xi ) = ni n. T 5. 6

Uma amostra de gás natural contém 8, 24 moles de CH 4, 0, 421 moles de C 2 H 6 e 0, 116 moles de C 3 H 8. Se a pressão total dos gases for 1, 37 atm, qual é a pressão parcial do propano (C 3 H 8)? Pi = Xi PT PT = 1, 37 atm 0, 116 Xpropano = 8, 24 + 0, 421 + 0, 116 = 0, 0132 Ppropano = 0, 0132 × 1, 37 atm = 0, 0181 atm 5. 6