Epigenetika evolucija Biljana Stojkovi Katedra za genetiku i

“Epigenetička” evolucija Biljana Stojković Katedra za genetiku i evoluciju Biološki fakultet, Beograd

Šta je to? • Osnova svake evolucione ideje je nasleđivanje: – Darvin: pangeneza – Moderna sinteza: geni – Evo-devo: geni + epigenetika • Svako otkriće u mehanizmima nasleđivanja utiče na sagledavanje procesa evolucije.
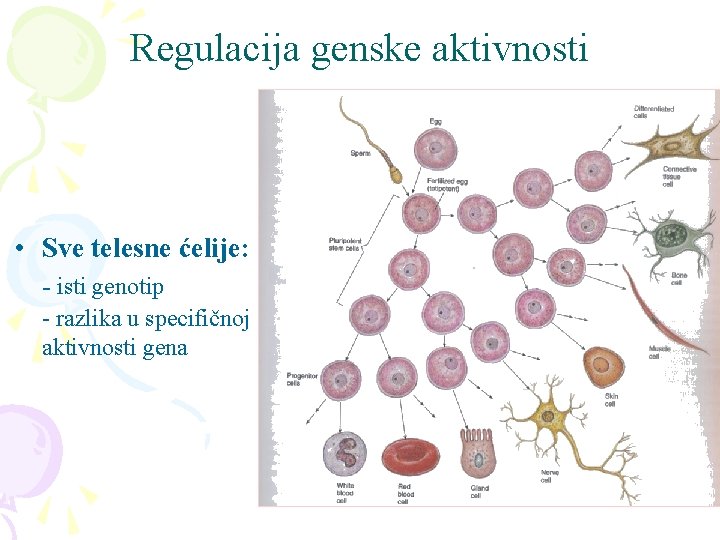
Regulacija genske aktivnosti • Sve telesne ćelije: - isti genotip - razlika u specifičnoj aktivnosti gena
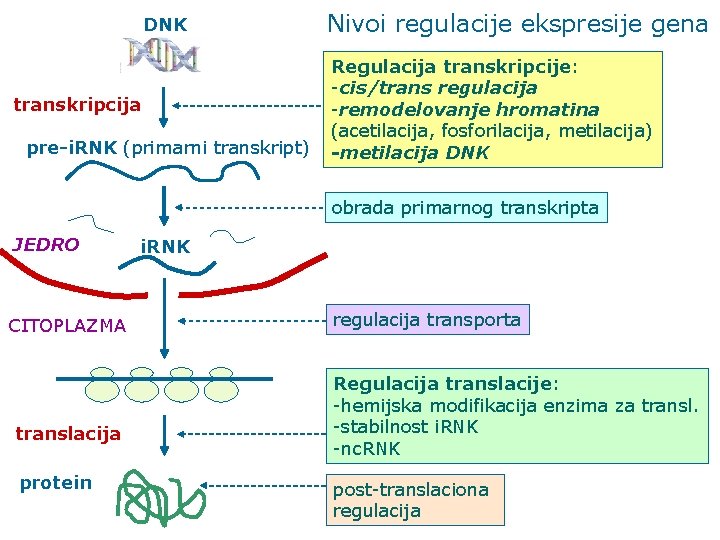
DNK transkripcija pre-i. RNK (primarni transkript) Nivoi regulacije ekspresije gena Regulacija transkripcije: -cis/trans regulacija -remodelovanje hromatina (acetilacija, fosforilacija, metilacija) -metilacija DNK obrada primarnog transkripta JEDRO CITOPLAZMA translacija protein i. RNK regulacija transporta Regulacija translacije: -hemijska modifikacija enzima za transl. -stabilnost i. RNK -nc. RNK post-translaciona regulacija

Epigenetika Izučavanje modifikacija u ekspresiji gena, koje ne obuhvataju promene u nizovima nukleotida DNK. Proučavanje naslednih, potencijalno reverzibilnih, promena u ekspresiji gena zbog DNK metilacije i/ili promena strukture hromatina. Nasledne promene = evolucioni značaj Može li životna sredina uticati na ekspresiju gena? Može li se izmenjen obrazac ekspresije preneti na potomstvo? Kako to menja naše razumevanje evolucije?
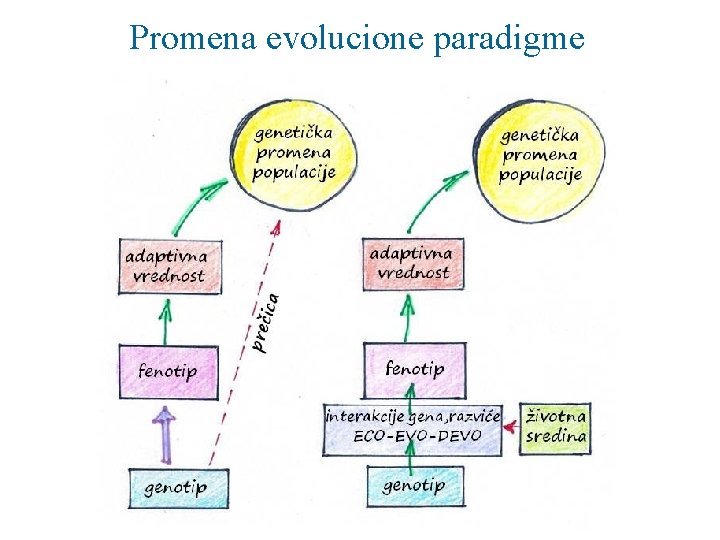
Promena evolucione paradigme
“Meko” nasleđivanje • Mitoza (deoba telesnih ćelija): – Tokom razvića, ćelije postaju specijalizovane i prenose obrazac ekpresije gena na ćerke ćelije – transkripciona memorija mora preživeti mitozu. • Mejoza (deoba polnih ćelija)

Epigenetičko nasleđivanje kroz mejozu - problemi • Epigenetička informacija morala bi biti ograničena na samo jednu generaciju zato što: – Totipotentnost jajne ćelije je neophodno početno stanje za sve buduće ćelijske linije • Masovno brisanje epigenetičkih markera tokom gametogeneze i rane embriogeneze (posebno kod sisara) – U primordijalnim germinativnim ćelijama gubi se metilacija DNK– u muškim oko 60%, u ženskim oko 70% – Nakon oplođenja (pre implantacije) – reprogramiranje roditeljskih genoma
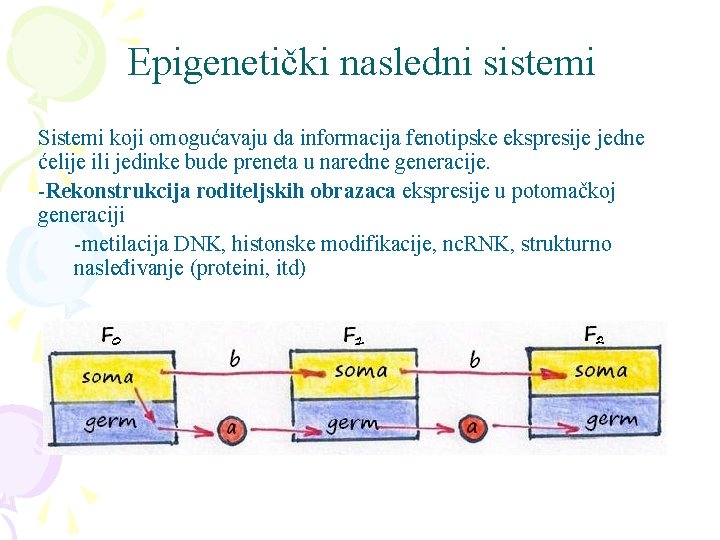
Epigenetički nasledni sistemi Sistemi koji omogućavaju da informacija fenotipske ekspresije jedne ćelije ili jedinke bude preneta u naredne generacije. -Rekonstrukcija roditeljskih obrazaca ekspresije u potomačkoj generaciji -metilacija DNK, histonske modifikacije, nc. RNK, strukturno nasleđivanje (proteini, itd)

Soma → soma nasleđivanje • Epigenetičko nasleđivanje u širem smislu (kod višećelijskih organizama): – Uslovljeno prenošenjem informacija usled inter- i intra-individualnih interakcija - između simbionata, parazit-domaćin, efekti materinskog ponašanja na fiziologiju i ponašanje potomstva, socijalno učenje i komunikacija ishrana: radilice (polen i nektar) matice (matični mleč - rojalaktin, fenil butirat) → sazrevanje ovarijuma i modifikacija ponašanja brižne majke pacova → endokrini odgovor potomstva → povećana metilacija gena za glukokortikoidni receptor u hipokampusu → povećana otpornost na stres, učenje, memorija. . . nebrižne majke → povećana metilacija gena za estrogenski receptor (ERα) → ranija polna zrelost, nediskriminativno sex. ponašanje, veća otpornost na infekcije i gladovanje

Soma→germ nasleđivanje (životinje) • Caenorhabditis elegans: ishrana bakterijama (sa DNK nizom za ds. RNK → gen ceh-13) → si. RNK iz somatskih ćelija ka gametima → “zdepasti“ fenotip (40 generacija) – modifikacija hromatina (hrde-1 gen) • Miševi – Aguti gen – veći broj alela (boja krzna) i metastabilni epialel Avy (viable yellow) – Avy/a genotip – žuti, debeli miševi (osim ukoliko je Avy metilovan) – Majke u ranoj trudnoći na dijeti sa donorima metil grupe → potomstvo braonkasto i sitnije – Stabilan braon fenotip nasleđen do F 2, a mršav fenotip do F 3 generacije – Zaštićenost demetilacije tokom reprogramiranja – Rekonstrukcija metilacionog obrasca posredstvom si. RNK Axin gen

Ljudi - začeće tokom zime gladi u Holandiji (1944 -1945) -potomstvo niži stepen metilacije IGF 2 gena → povećana gojaznost dijabetes i kardiovaskularne bolesti - glad muških tinejdžera u Švedskoj u 19. veku → produžen život muških unuka (manja incidenca dijabetesa) -analiza epigenoma na leukocitima dece iz seoskih krajeva Gambije (Waterland et al. 2010): -deca začeta u kišnom i sušnom periodu -ishrana majke – manje ili više zelene hrane (folna kiselina) → različite grupe gena sa izmenjenim metilacionim statusom

Soma (germ) → germ (paralelni efekti) • Istovremena epigenetička indukcija i soma i germ – Ephestia kuehniella (larve): temperatura, električno polje → supresija Sa mutacije (normalne antene i reprodukcija) → 5 generacija (modifikacija hromatina) – Hormonski status: • Kod spermatozoida - 8 hormonskih i 16 receptora za citokine • Kod oocita – receptori za hormone (estrogen i β 2 -androreceptor, hormon rasta), neurotransmitere (serotonin), Notch 1 i 2
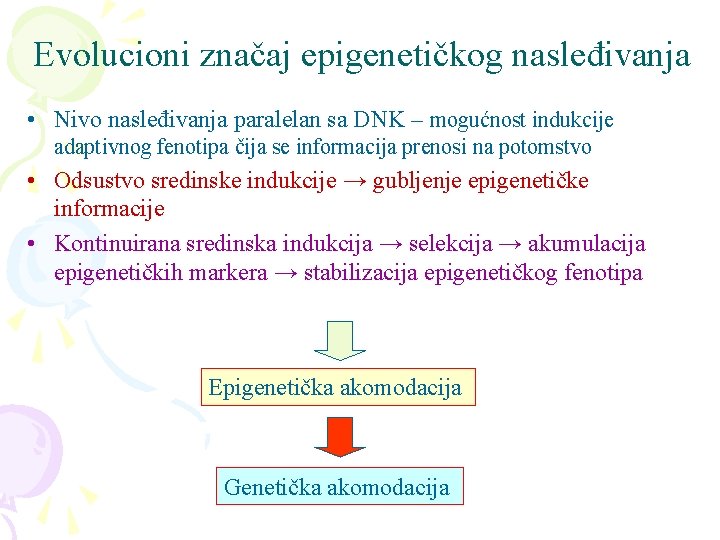
Evolucioni značaj epigenetičkog nasleđivanja • Nivo nasleđivanja paralelan sa DNK – mogućnost indukcije adaptivnog fenotipa čija se informacija prenosi na potomstvo • Odsustvo sredinske indukcije → gubljenje epigenetičke informacije • Kontinuirana sredinska indukcija → selekcija → akumulacija epigenetičkih markera → stabilizacija epigenetičkog fenotipa Epigenetička akomodacija Genetička akomodacija
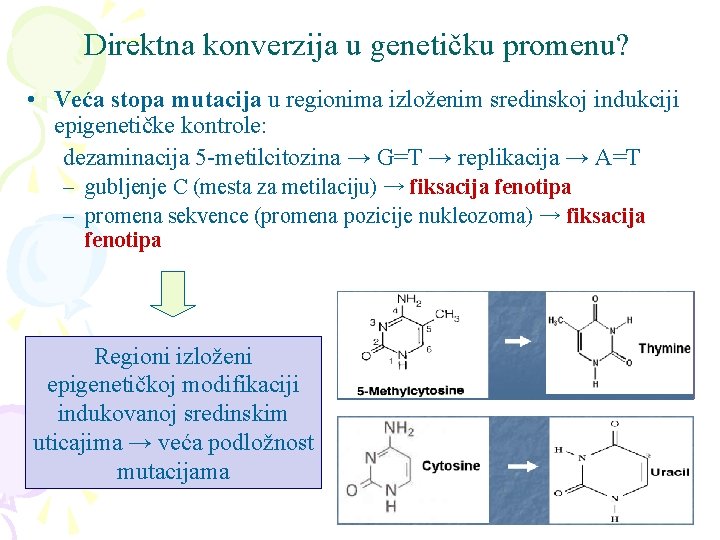
Direktna konverzija u genetičku promenu? • Veća stopa mutacija u regionima izloženim sredinskoj indukciji epigenetičke kontrole: dezaminacija 5 -metilcitozina → G=T → replikacija → A=T – gubljenje C (mesta za metilaciju) → fiksacija fenotipa – promena sekvence (promena pozicije nukleozoma) → fiksacija fenotipa Regioni izloženi epigenetičkoj modifikaciji indukovanoj sredinskim uticajima → veća podložnost mutacijama
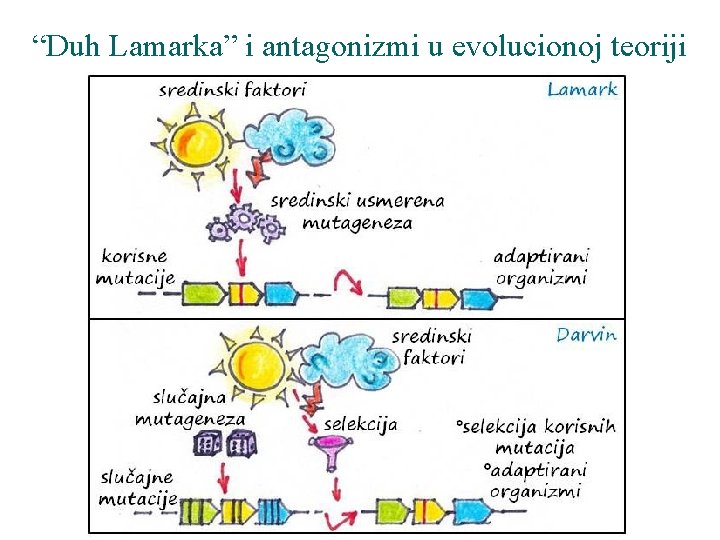
“Duh Lamarka” i antagonizmi u evolucionoj teoriji
- Slides: 16