Epidmiologie des maladies infectieuses et cologie Apport des





- Slides: 10

Epidémiologie des maladies infectieuses et écologie Apport des modélisations déterministe et stochastique

Comprendre les mécanismes de propagation des parasites afin d’identifier les processus de sélection Dynamique des populations du réservoir/vectrices Traits d’histoire de vie des individus Suivis à long terme de populations naturelles Modélisation dynamique Analyses statistiques paramétrage

1 - Un modèle de maladie émergente: la néphropathie épidémique (NE) Ardennes (région étudiée) NE endémique Chletrionomys glareolus NE sporadique Pas de NE ? Hantavirus Puumala Quel est le mécanisme qui permet de comprendre la géographie de la propagation du virus ?

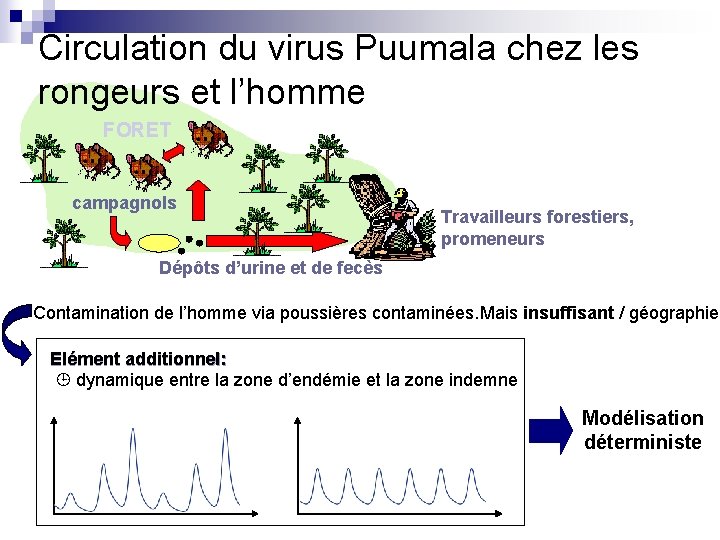
Circulation du virus Puumala chez les rongeurs et l’homme FORET campagnols Travailleurs forestiers, promeneurs Dépôts d’urine et de fecès Contamination de l’homme via poussières contaminées. Mais insuffisant / géographie Elément additionnel: dynamique entre la zone d’endémie et la zone indemne Modélisation déterministe

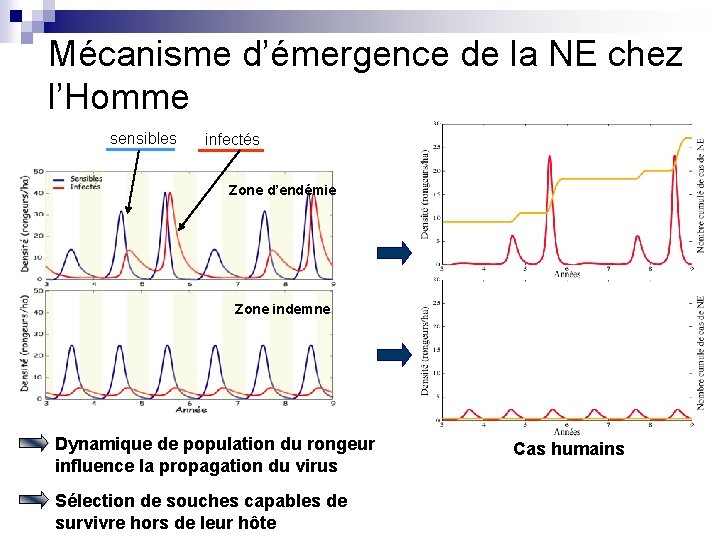
Mécanisme d’émergence de la NE chez l’Homme sensibles infectés Zone d’endémie Zone indemne Dynamique de population du rongeur influence la propagation du virus Sélection de souches capables de survivre hors de leur hôte Cas humains

2 - Mode de transmission du VIF ■ verticalement (placenta, lait) mode de transmission naturel ■ sexuellement (sperme) expérimentalement ■ par morsure (salive) Petites populations (60 -300 hôtes), prévalence VIF = 15 – 30% Mâles dominants = « core-group » pourquoi ce mode de transmission ? simple conséquence ou processus de sélection ? Modélisation stochastique

Patron de persistance du VIF en milieu rural Modèle stochastique SI en population fermée structurée par âge, sexe, comportement (dominant vs subordonnés) probabilité d’extinction 70% après 10 ans probabilité 1000 simulations du réseau de Petri sur 30 ans années prévalence

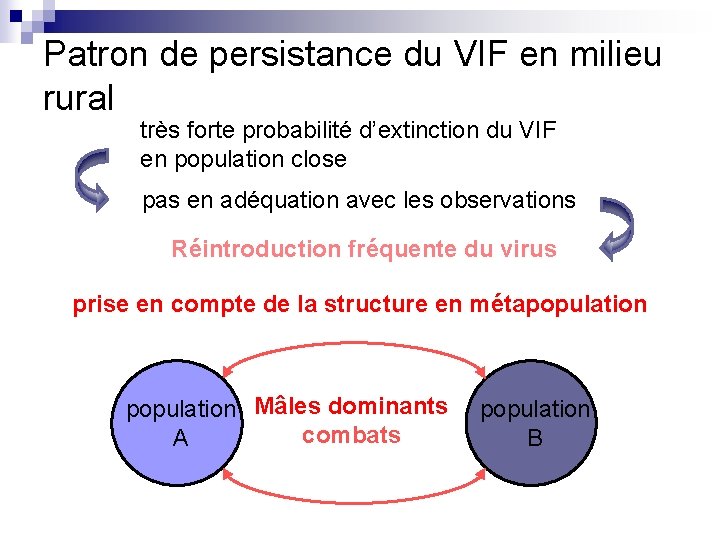
Patron de persistance du VIF en milieu rural très forte probabilité d’extinction du VIF en population close pas en adéquation avec les observations Réintroduction fréquente du virus prise en compte de la structure en métapopulation Mâles dominants combats A population B

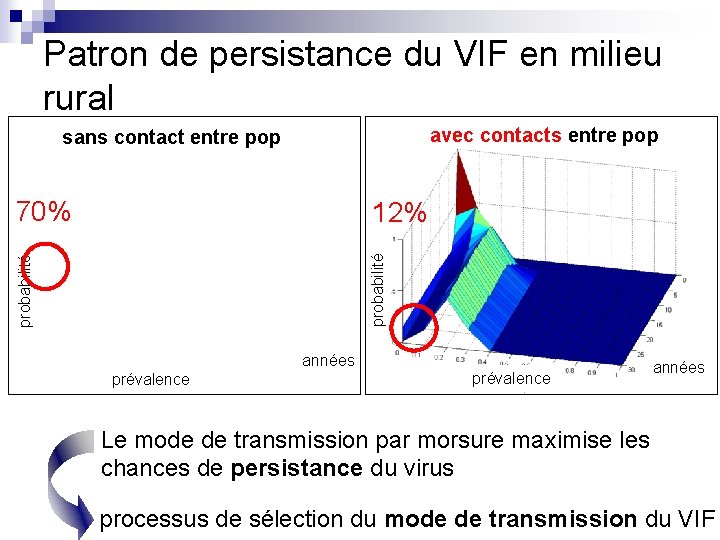
Patron de persistance du VIF en milieu rural sans contact entre pop 70% avec contacts entre pop probabilité 12% années prévalence années Le mode de transmission par morsure maximise les chances de persistance du virus processus de sélection du mode de transmission du VIF

Perspectives Fonctionnement des populations hôtes Facteurs de sélection des pathogènes Généralisation de l’approche à plusieurs parasites Programme Santé-environnement et Santé-travail Pathocénoses et émergence des maladies transmissibles : un concept unificateur mis à l’épreuve sur des pathologies exemplaires (coord. D. Pontier)