Epidemiologia e strategie di prevenzione della varicella Prevalenza





















- Slides: 52

Epidemiologia e strategie di prevenzione della varicella

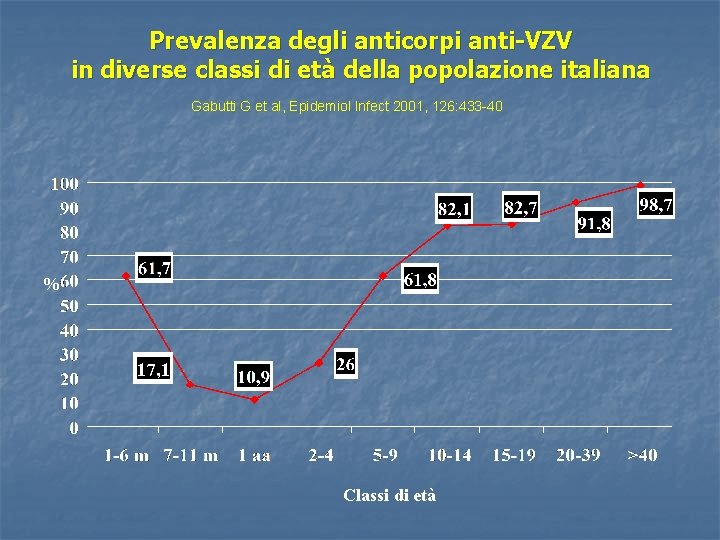
Prevalenza degli anticorpi anti-VZV in diverse classi di età della popolazione italiana Gabutti G et al, Epidemiol Infect 2001, 126: 433 -40 % Classi di età

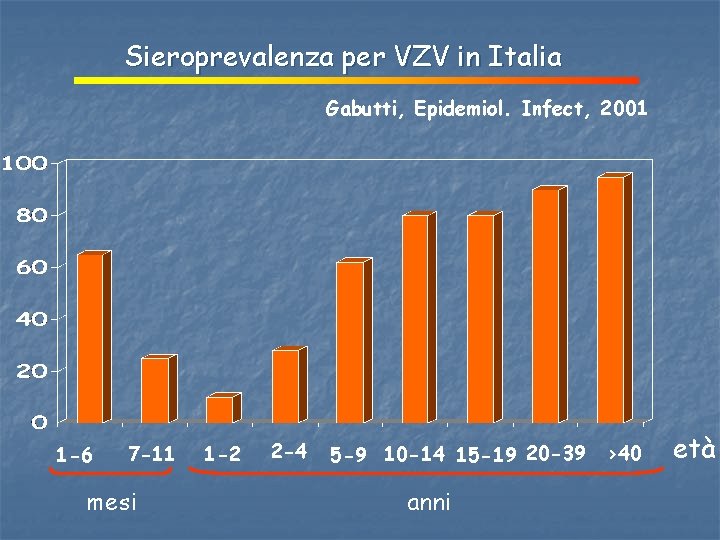
Sieroprevalenza per VZV in Italia Gabutti, Epidemiol. Infect, 2001 1 -6 7 -11 mesi 1 -2 2 -4 5 -9 10 -14 15 -19 20 -39 >40 anni età

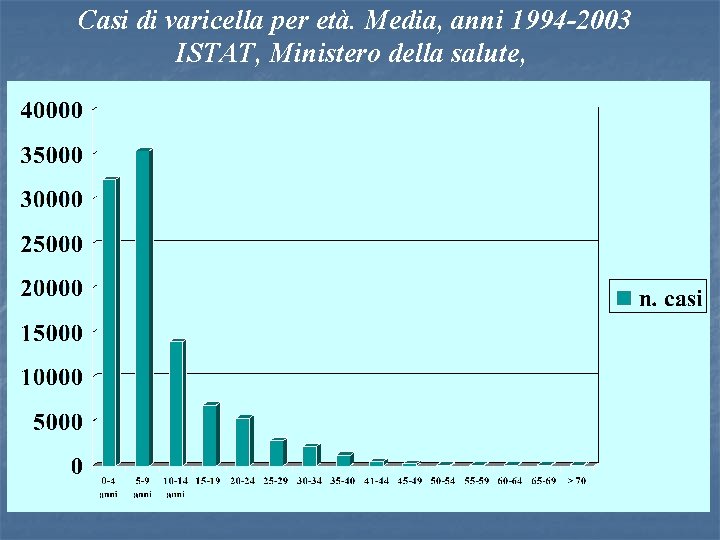
Casi di varicella per età. Media, anni 1994 -2003 ISTAT, Ministero della salute,

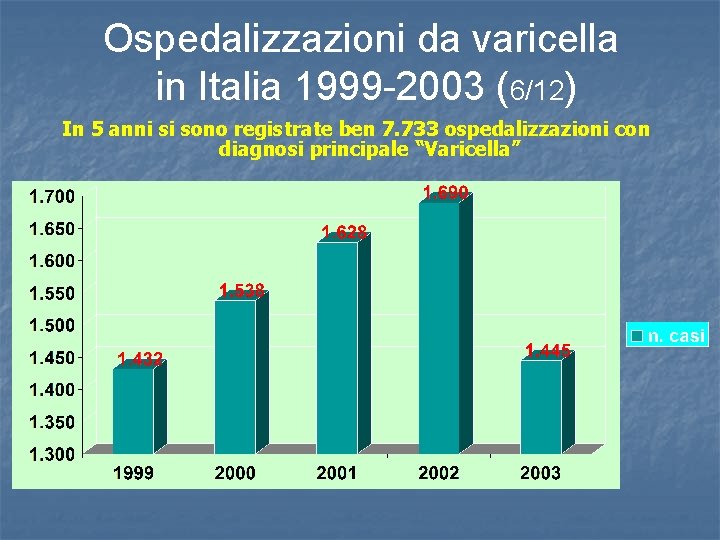
Ospedalizzazioni da varicella in Italia 1999 -2003 (6/12) In 5 anni si sono registrate ben 7. 733 ospedalizzazioni con diagnosi principale “Varicella”

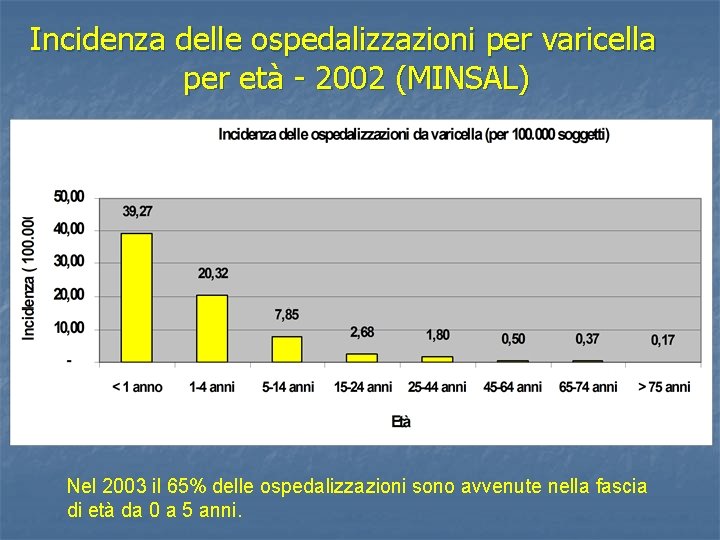
Incidenza delle ospedalizzazioni per varicella per età - 2002 (MINSAL) Nel 2003 il 65% delle ospedalizzazioni sono avvenute nella fascia di età da 0 a 5 anni.

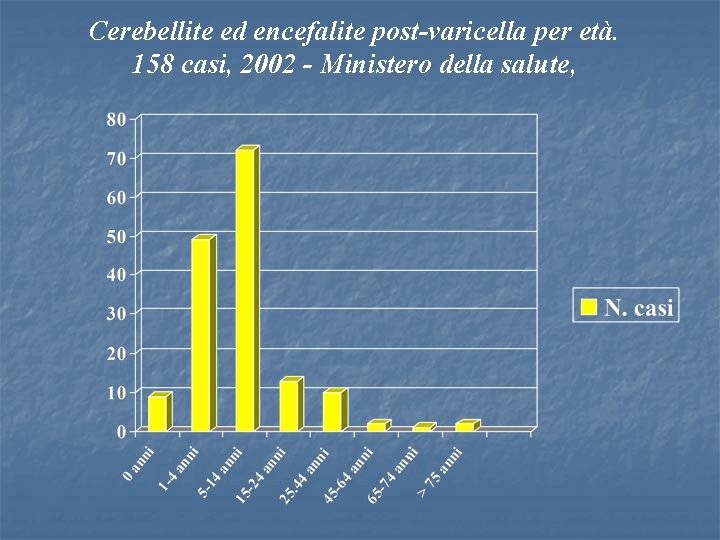
Cerebellite ed encefalite post-varicella per età. 158 casi, 2002 - Ministero della salute,

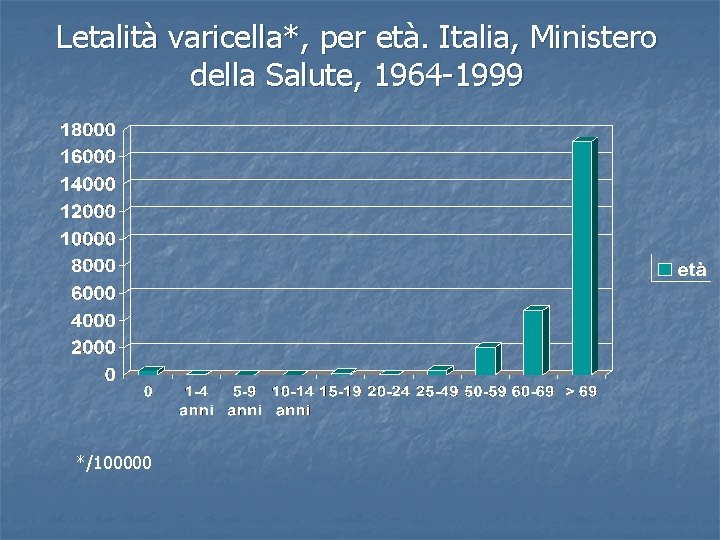
Letalità varicella*, per età. Italia, Ministero della Salute, 1964 -1999 */100000

Giugno 2009

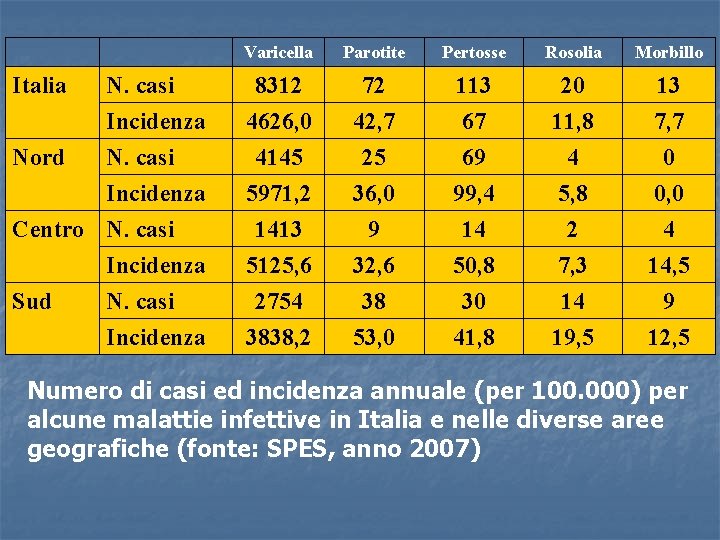
Varicella Parotite Pertosse Rosolia Morbillo Italia N. casi Incidenza N. casi 8312 4626, 0 4145 72 42, 7 25 113 67 69 20 11, 8 4 13 7, 7 0 Incidenza Centro N. casi Incidenza Sud N. casi 5971, 2 1413 5125, 6 2754 36, 0 9 32, 6 38 99, 4 14 50, 8 30 5, 8 2 7, 3 14 0, 0 4 14, 5 9 Incidenza 3838, 2 53, 0 41, 8 19, 5 12, 5 Nord Numero di casi ed incidenza annuale (per 100. 000) per alcune malattie infettive in Italia e nelle diverse aree geografiche (fonte: SPES, anno 2007)

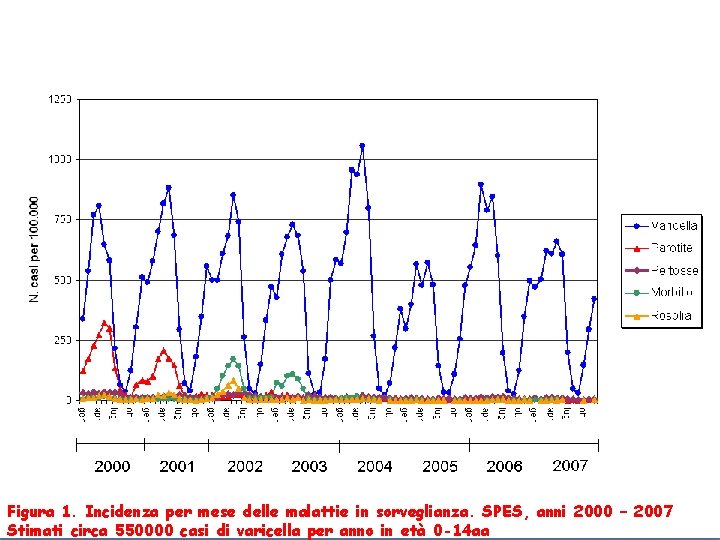
Figura 1. Incidenza per mese delle malattie in sorveglianza. SPES, anni 2000 – 2007 Stimati circa 550000 casi di varicella per anno in età 0 -14 aa

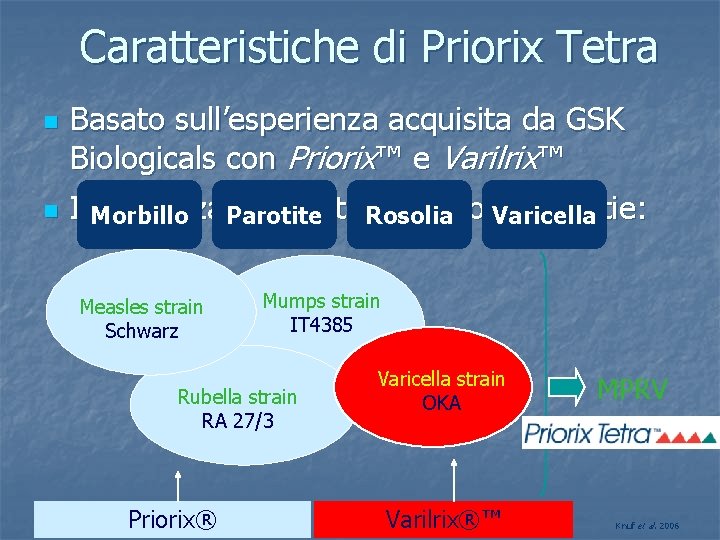
Caratteristiche di Priorix Tetra n n Basato sull’esperienza acquisita da GSK Biologicals con Priorix™ e Varilrix™ Immunizzazione attiva contro Varicella 4 malattie: Morbillo Parotite Rosolia Measles strain Schwarz Mumps strain IT 4385 Rubella strain RA 27/3 Knuf et al. 2006 Priorix® Varicella strain OKA Varilrix®™ MPRV Knuf et al. 2006

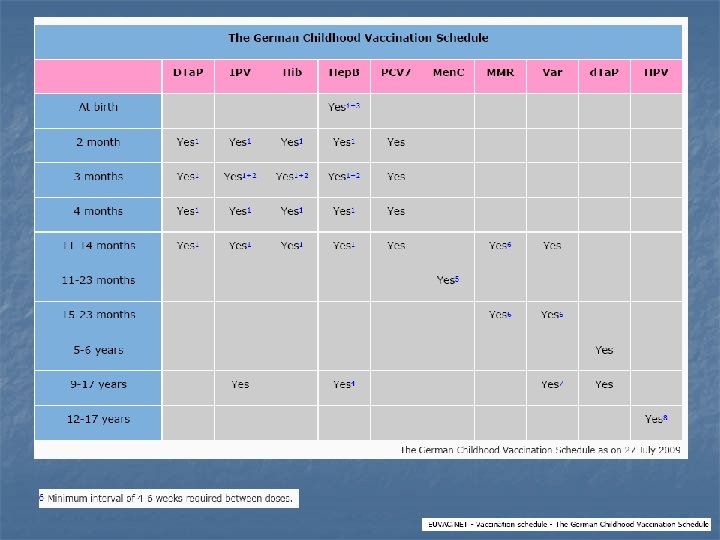
profilo registrativo n n n Priorix Tetra è stato registrato in Germania nel 2006 Nel 2007 autorizzato in 24 Paesi EU tramite procedura di Mutuo riconoscimento Registrato anche in Australia e Canada





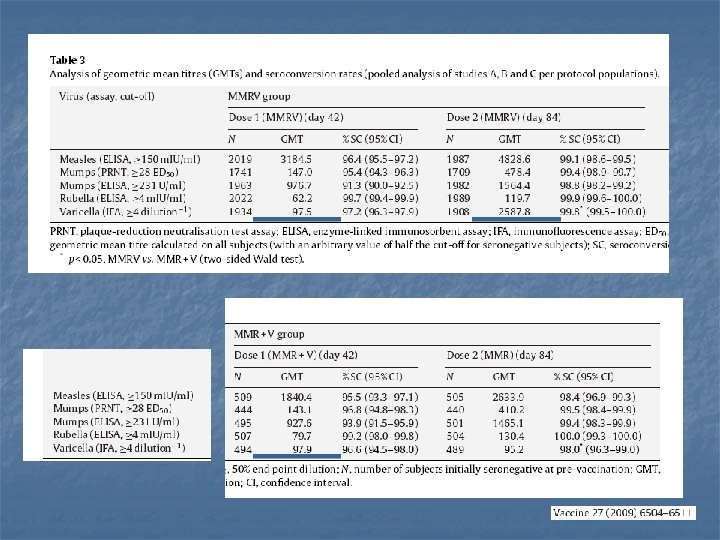
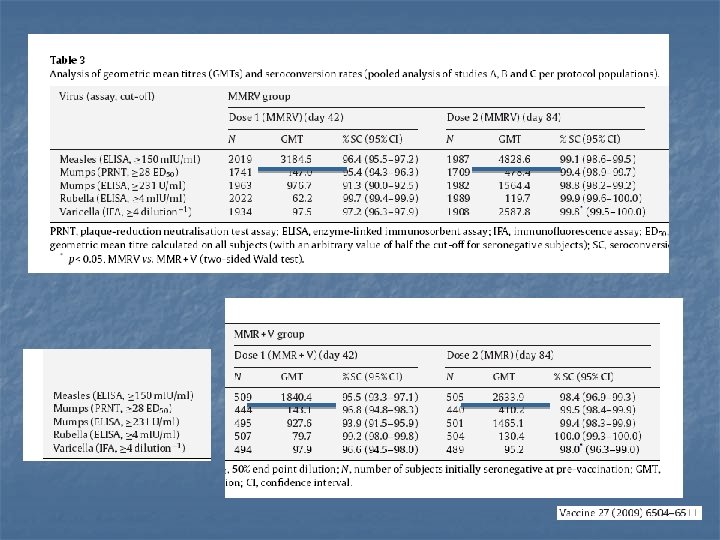
immunogenicità - sc n n n sieroconversione dopo 2 dosi circa 100% per tutte le 4 componenti sia come MMRV che MMR+V sieroconversione per M, M, R equivalente tra MMRV e MMR+V; aumento della percentuale di sc per V in MMRV 2° dose rispetto a MMR



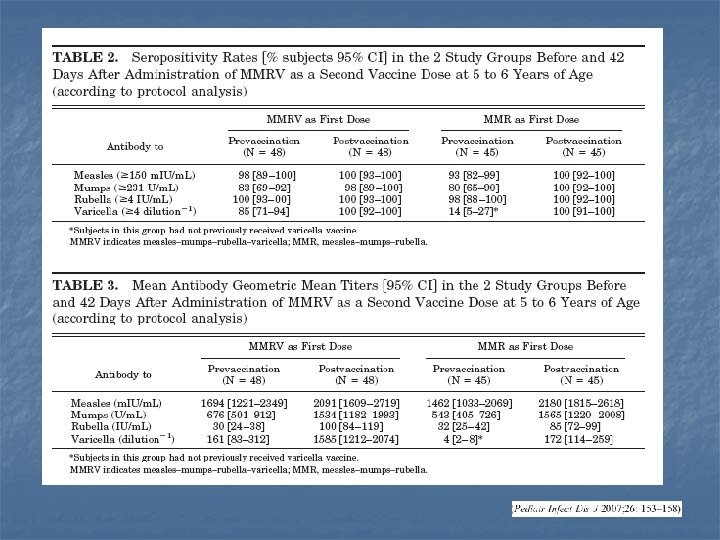
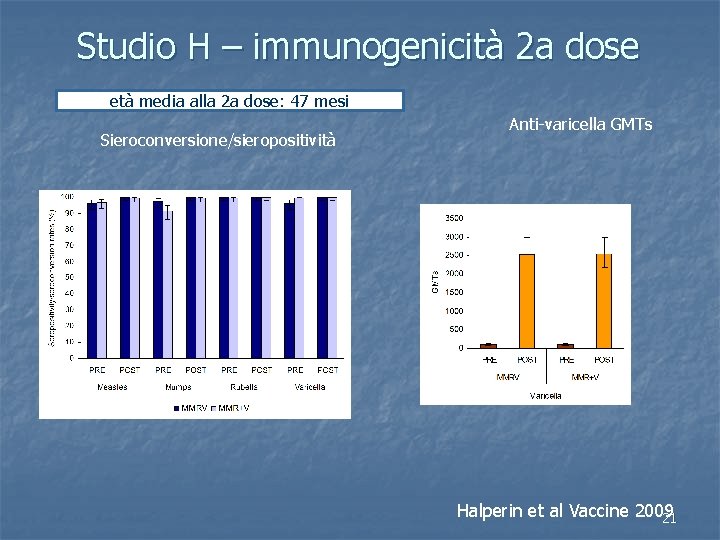
Studio H – immunogenicità 2 a dose età media alla 2 a dose: 47 mesi Sieroconversione/sieropositività Anti-varicella GMTs Halperin et al Vaccine 2009 21

immunogenicità - GMT n n n incremento di 26 volte delle GMT di V dopo la 2° dose (97. 5 ->2587. 8) nessun incremento nel controllo GMT del morbillo maggiori nel gruppo MMRV di 1. 7 (1° dose) e 1. 8 (2° dose) volte



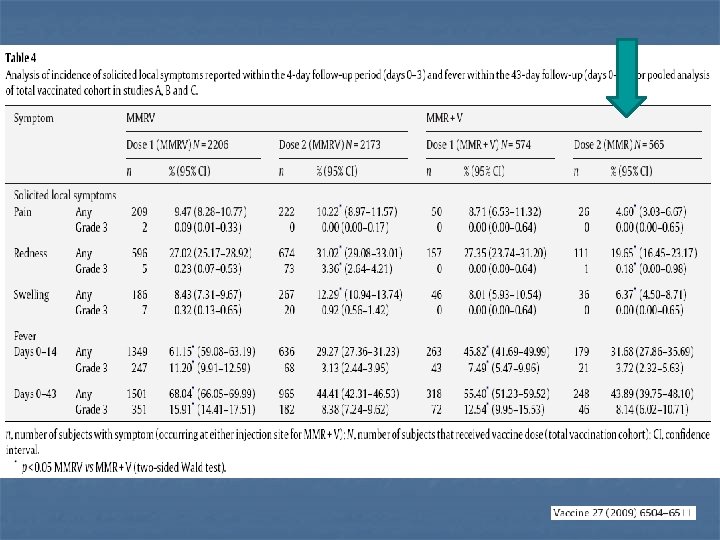
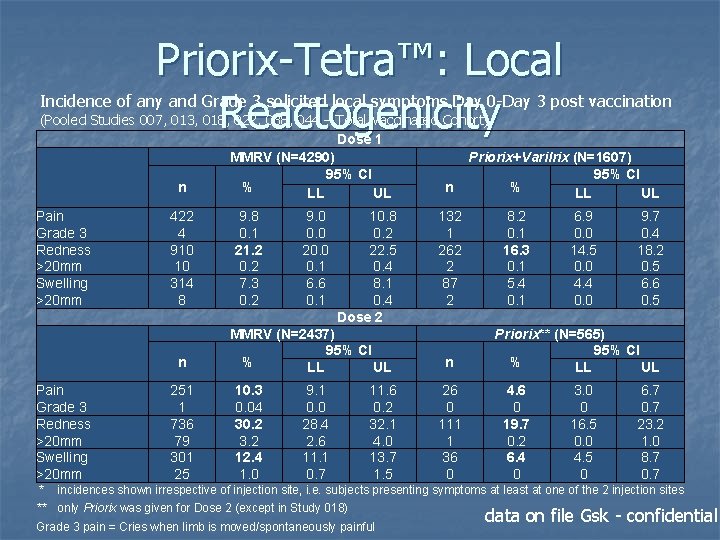
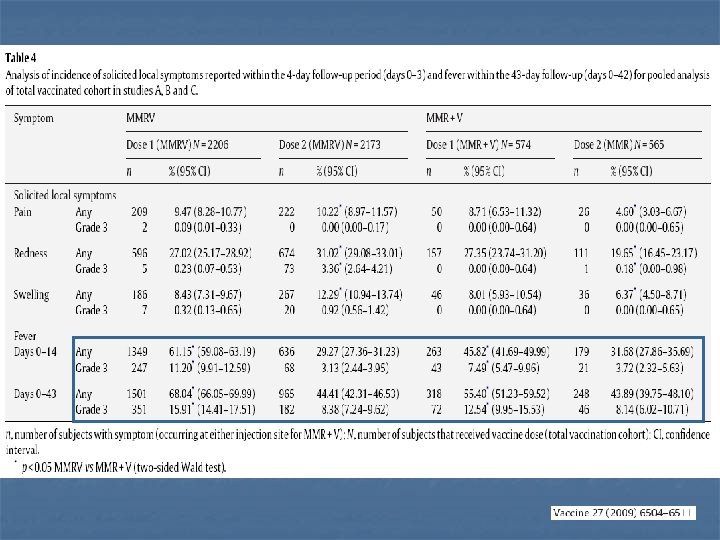
Reattogenicità e sicurezza n n nessuna differenza dopo la 1° dose tra MMRV e MMR+V per dolore, rossore (più frequente, 27%)e gonfiore maggiore frequenza in MMRV dopo la 2° dose per dolore, rossore e gonfiore rispetto a MMR (no V) reazioni di grado 3 sono state riscontrate raramente in entrambi i gruppi i rash si sono verificati con maggiore frequenza dopo la 2° dose in entrambi i gruppi

Priorix-Tetra™: Local Reactogenicity Incidence of any and Grade 3 solicited local symptoms Day 0 -Day 3 post vaccination (Pooled Studies 007, 013, 018, 022, 038, 044 – Total Vaccinated Cohort) Dose 1 MMRV (N=4290) Priorix+Varilrix (N=1607) 95% CI n % LL UL Pain Grade 3 Redness >20 mm Swelling >20 mm 422 4 910 10 314 8 n Pain Grade 3 Redness >20 mm Swelling >20 mm * 251 1 736 79 301 25 9. 8 0. 1 21. 2 0. 2 7. 3 0. 2 9. 0 0. 0 20. 0 0. 1 6. 6 0. 1 10. 8 0. 2 22. 5 0. 4 8. 1 0. 4 Dose 2 MMRV (N=2437) 95% CI % LL UL 10. 3 0. 04 30. 2 3. 2 12. 4 1. 0 9. 1 0. 0 28. 4 2. 6 11. 1 0. 7 11. 6 0. 2 32. 1 4. 0 13. 7 1. 5 132 1 262 2 87 2 n 26 0 111 1 36 0 8. 2 0. 1 16. 3 0. 1 5. 4 0. 1 6. 9 0. 0 14. 5 0. 0 4. 4 0. 0 9. 7 0. 4 18. 2 0. 5 6. 6 0. 5 Priorix** (N=565) 95% CI % LL UL 4. 6 0 19. 7 0. 2 6. 4 0 3. 0 0 16. 5 0. 0 4. 5 0 6. 7 0. 7 23. 2 1. 0 8. 7 0. 7 incidences shown irrespective of injection site, i. e. subjects presenting symptoms at least at one of the 2 injection sites ** only Priorix was given for Dose 2 (except in Study 018) Grade 3 pain = Cries when limb is moved/spontaneously painful data on file Gsk - confidential

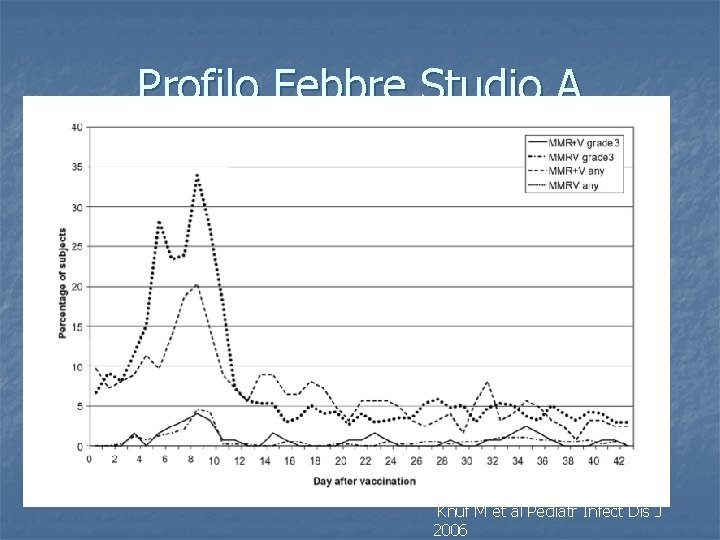
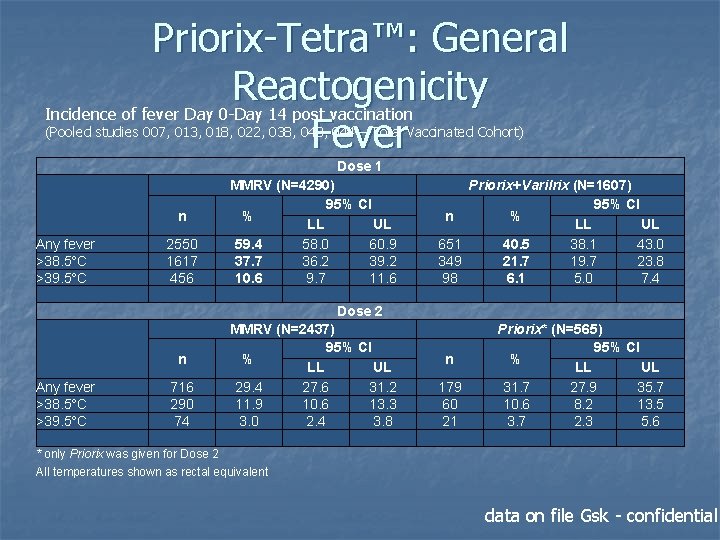
febbre n n la febbre si è manifestata con maggiore frequenza nelle 2 settimane dopo la somministrazione grado 3 sovrapponibile nei due gruppi di trattamento

Profilo Febbre Studio A Knuf M et al Pediatr Infect Dis J 2006

Incidenza di febbre studio C Schuster V et al. . Int J Infect Dis


Priorix-Tetra™: General Reactogenicity Incidence of fever Day 0 -Day 14 post vaccination Fever (Pooled studies 007, 013, 018, 022, 038, 043, 044 – Total Vaccinated Cohort) Dose 1 n Any fever >38. 5°C >39. 5°C 2550 1617 456 MMRV (N=4290) 95% CI % LL UL 59. 4 58. 0 60. 9 37. 7 36. 2 39. 2 10. 6 9. 7 11. 6 Priorix+Varilrix (N=1607) 95% CI n % LL UL 651 40. 5 38. 1 43. 0 349 21. 7 19. 7 23. 8 98 6. 1 5. 0 7. 4 Dose 2 n Any fever >38. 5°C >39. 5°C 716 290 74 MMRV (N=2437) 95% CI % LL UL 29. 4 27. 6 31. 2 11. 9 10. 6 13. 3 3. 0 2. 4 3. 8 n 179 60 21 Priorix* (N=565) 95% CI % LL UL 31. 7 27. 9 35. 7 10. 6 8. 2 13. 5 3. 7 2. 3 5. 6 * only Priorix was given for Dose 2 All temperatures shown as rectal equivalent data on file Gsk - confidential

eventi avversi gravi (SAE) n solo 4 eventi avversi gravi correlabili a vaccino nei 3 studi, tutti nel gruppo MMRV (1° dose 2206 soggetti , 2° dose 2173 soggetti): 1) convulsioni febbrili 8 gg dopo la 2° dose (A) n 2)reazione allergica (orticaria) (B) n 3) febbre prolungata (B) n 4) tonsillite convulsione febbrile 9 gg dopo 1° dose (C) n n tutti gli eventi risolti senza sequele

Priorix-Tetra™: Safety Serious Adverse Events SAEs considered related by the investigator MMRV (N=4811)* Comparator (N=2706)* 58 1. 16% 32 1. 18% 4 • Acute tonsillitis + febrile convulsion • Febrile convulsion • Pyrexia • Hypersensitivity reaction * Full database, incl. Study 006 1 • Fever & convulsions associated with pharyngitis data on file GSK - confidential

Persistenza dell'immunità - studi di follow up 1 anno 2 anni 3 anni MMRV morbillo parotite rosolia varicella 296 100 90 100 99 273 100 95 100 97 225 99 97 100 99 MMR+V morbillo parotite rosolia varicella 105 100 96 100 101 100 92 100 91 79 100 94 100 97

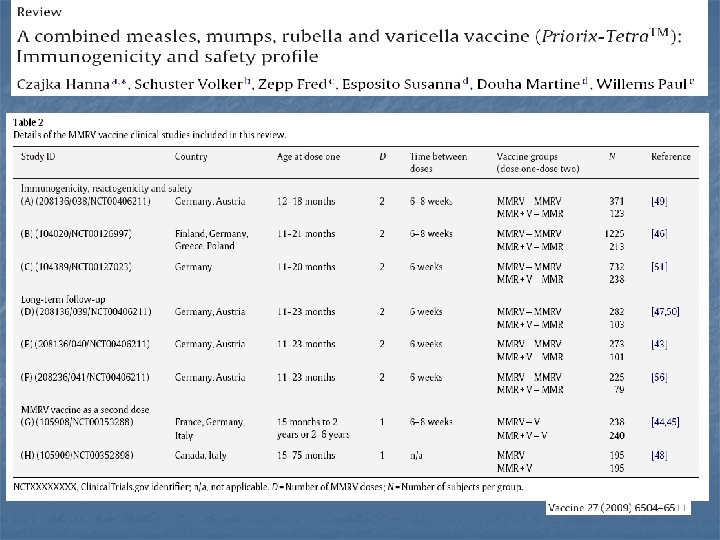
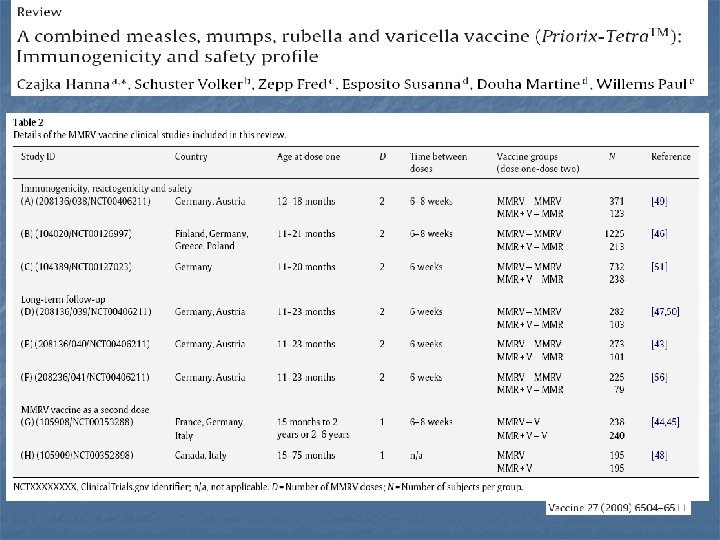
Priorix Tetra come 2° dose n n n n 3 studi disponibili 2 studi parte dell’analisi di Czajka (condotti anche in Italia) 2° dose a 6 -8 settimane (2 studi) o a 4 -5 anni (1 studio) di distanza range di età dei soggetti: 15 mesi – 6 anni prima dose : MMR o MMR+V o MMRV sieropositività (MMR) e sieroconversione (V) confermate in tutti gli studi profilo di sicurezza e tollerabilità sovrapponibile ai controlli (febbre uguale nei due gruppi di trattamento)

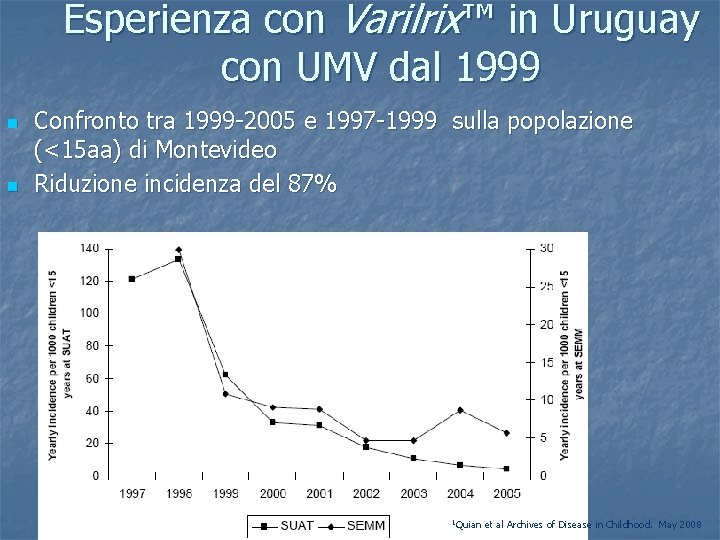
Esperienza con Varilrix™ in Uruguay con UMV dal 1999 n n Confronto tra 1999 -2005 e 1997 -1999 sulla popolazione (<15 aa) di Montevideo Riduzione incidenza del 87% 1 Quian et al Archives of Disease in Childhood. May 2008

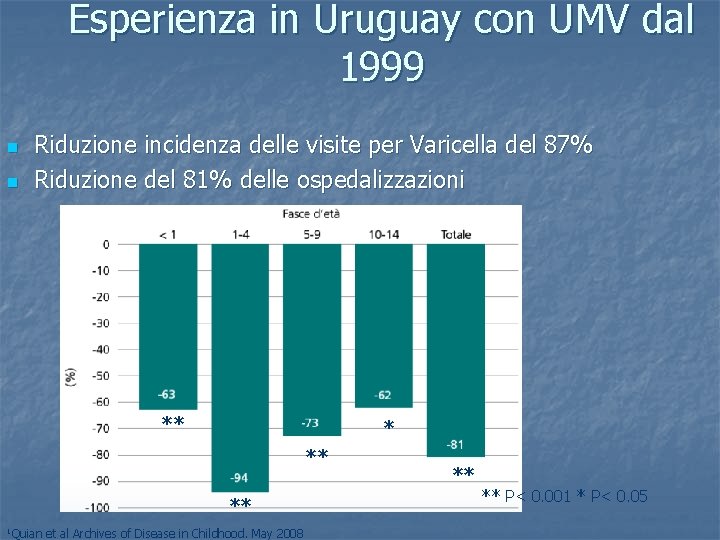
Esperienza in Uruguay con UMV dal 1999 n n Riduzione incidenza delle visite per Varicella del 87% Riduzione del 81% delle ospedalizzazioni ** ** 1 Quian et al Archives of Disease in Childhood. May 2008 ** ** P< 0. 001 * P< 0. 05

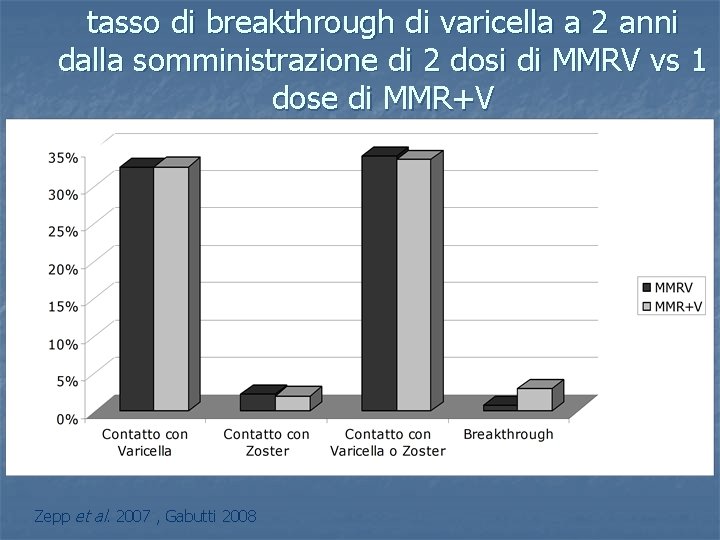
tasso di breakthrough di varicella a 2 anni dalla somministrazione di 2 dosi di MMRV vs 1 dose di MMR+V Zepp et al. 2007 , Gabutti 2008

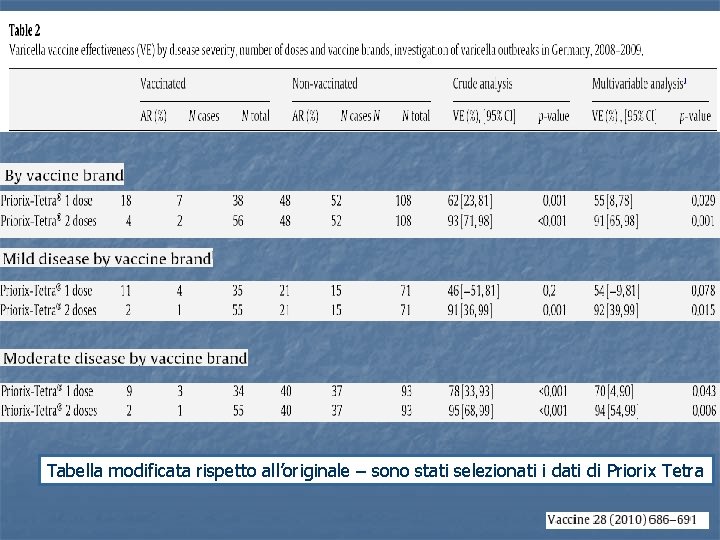
Tabella modificata rispetto all’originale – sono stati selezionati i dati di Priorix Tetra




CDC post-licensure observational study Increased risk of febrile seizure 7 -10 days after vaccination – Pro. Quad – 9 per 10, 000 vaccinations – MMR + V vaccines – 4 per 10, 000


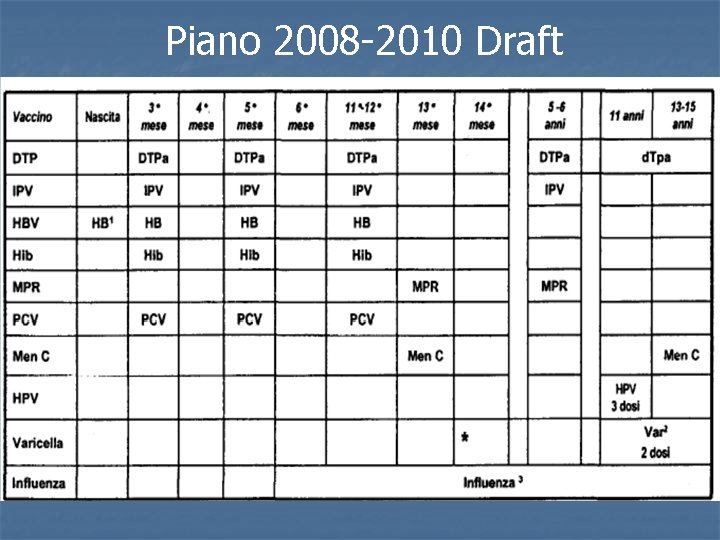
Piano 2008 -2010 Draft

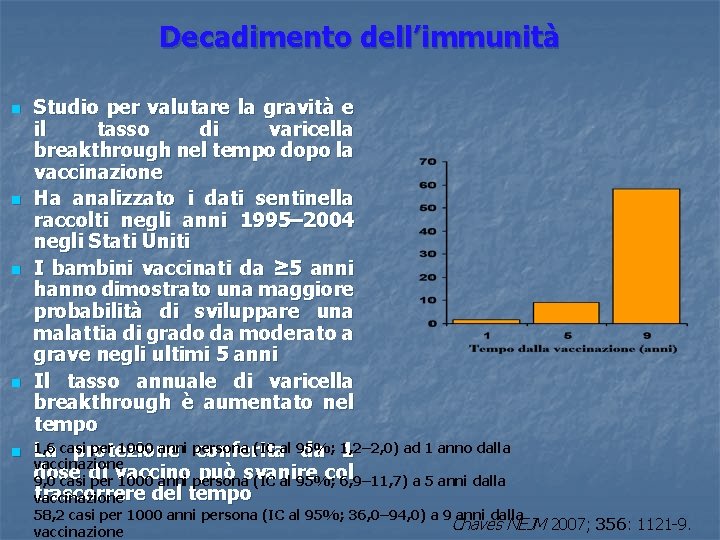
Decadimento dell’immunità n n n Studio per valutare la gravità e il tasso di varicella breakthrough nel tempo dopo la vaccinazione Ha analizzato i dati sentinella raccolti negli anni 1995– 2004 negli Stati Uniti I bambini vaccinati da ≥ 5 anni hanno dimostrato una maggiore probabilità di sviluppare una malattia di grado da moderato a grave negli ultimi 5 anni Il tasso annuale di varicella breakthrough è aumentato nel tempo 1, 6 per 1000 anni persona (IC al 95%; ad 1 anno dalla La casi protezione conferita da 1, 2– 2, 0) 1 vaccinazione dose di vaccino può svanire col 9, 0 casi per 1000 anni persona (IC al 95%; 6, 9– 11, 7) a 5 anni dalla trascorrere del tempo vaccinazione 58, 2 casi per 1000 anni persona (IC al 95%; 36, 0– 94, 0) a 9 anni dalla Chaves NEJM 2007; 356: 1121 -9. vaccinazione






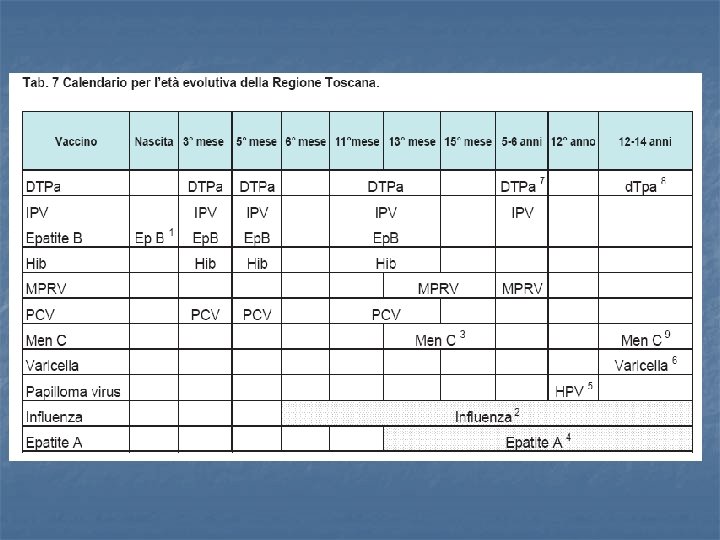
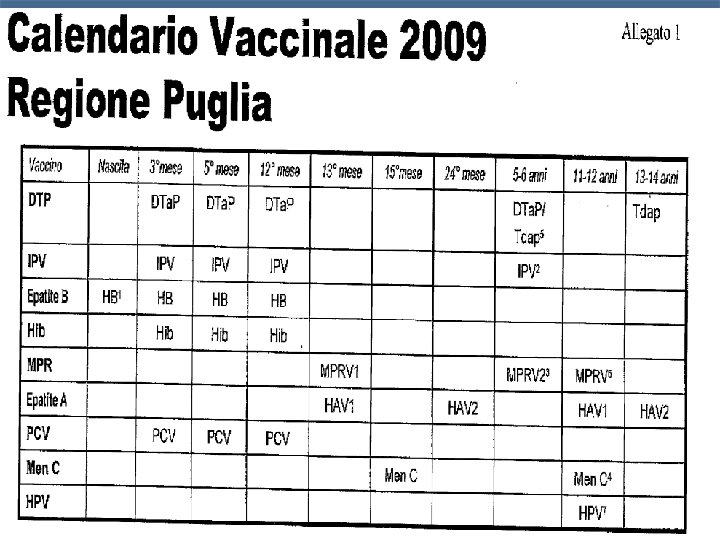
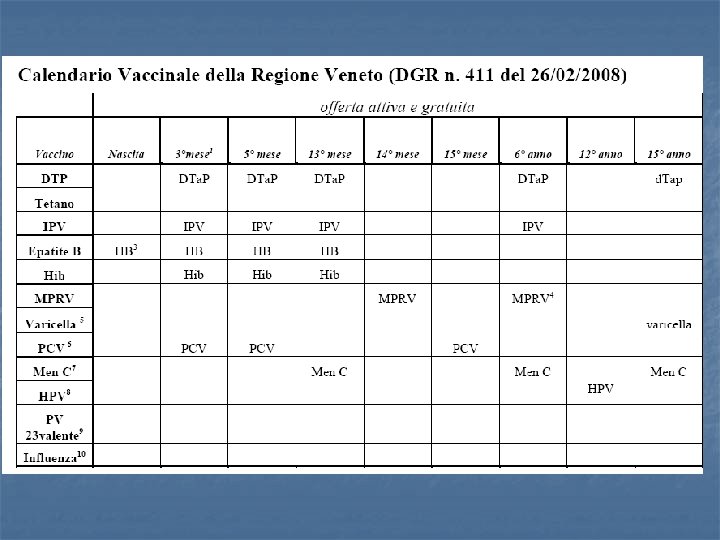
conclusioni n n n Il profilo immunologico, di sicurezza e tollerabilità di Priorix tetra è sovrapponibile a quello di Priorix e Varilrix co-somministrati L’insorgenza di febbre risulta essere più frequente per la 1 dose di MPRV rispetto a MPR + V L’efficacia clinica del vaccino MPRV è documentata e sovrapponibile al vaccino V singolo Le società scientifiche italiane raccomandano la vaccinazione anti-varicella con il vaccino MPRV Alcune Regioni italiane hanno già inserito il vaccino MPRV nel loro calendario