EPGENETK Do Dr Sercan ERGN Tbbi Biyoloji ABD

+ EPİGENETİK Doç. Dr. Sercan ERGÜN Tıbbi Biyoloji ABD

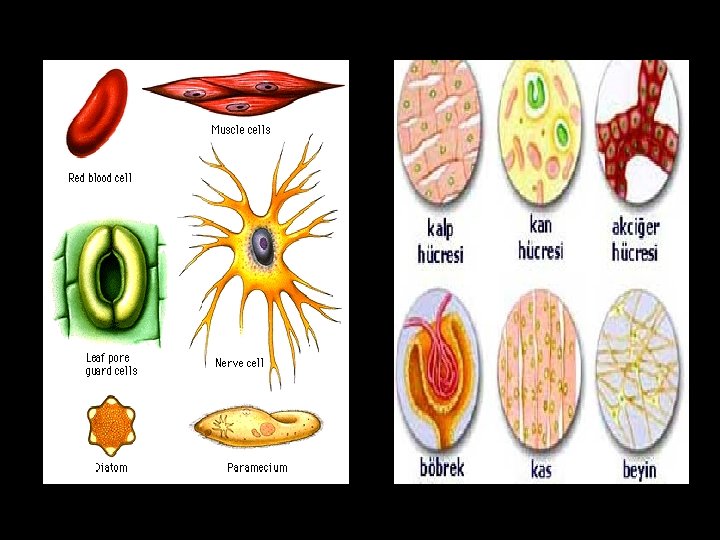
Çok hücreli bir organizmada; bir karaciğer hücresi ile bir sinir hücresi, aynı genotipe sahipken, nasıl olur da, birbirinden çok farklı hücre fonksiyonlarına ve gen ifade profillerine sahip olabilmektedirler?

Agouti “İkiz” Kardeşler

Bu soru yıllar boyunca bilim adamlarının kafasını yormuş ve bu konuda çok araştırma yapılmasına neden olmuştur. Tüm bu çalışmalar neticesinde elde edilen verilere göre belli genlerin aktivasyonunun ne zaman ve nasıl olacağının belirlenmesi epigenetik mekanizmalar dediğimiz sistem tarafından kontrol edildiği ortaya çıkmıştır.

Epigenetik Nedir? q. Epigenetik, genotipik değişikliklerden kaynaklanmayan, ama aynı zamanda kalıtımsal olan, gen ekspresyonundaki farklılıkları inceleyen bilim dalıdır. q. Gen ekspresyonuna dayanan kalıtsal bilgi epigenetik olarak sınıflandırılır. Bu, genetik bilginin aksine gen dizisi ile ilişkili değildir.

§ Yani fenotipik farklılıklardaki, kalıtımsal olup genetik olmayan mekanizmaları incelemektedir. Bu olayın moleküler temeli karmaşık bir olaydır ve belli genlerin aktivasyonunun ne zaman ve nasıl olacağını belirler. §Epigenetik değişimler genlerin sessizleşmesine (silencing) neden olurlar. Bu da geni inaktive edici bir mutasyon veya delesyon gibi genetik bir mekanizmayla eşdeğerdir.

İyi bir müzik dinletisinin ortaya çıkması için, doğru zamanda doğru enstrümanların çalmasını sağlayan bir orkestra şefine benzetilebilir.
• Bu süreç içerisinde erişkinlerde hücre yenilenmesi, X kromozom inaktivasyonu gibi olaylar gerçekleşmektedir. • Eğer bu süreç bozulursa kanser, otoimmun hastalıklar ve nörolojik hastalıkların ortaya çıkması söz konusudur.

• Ancak epigenetik değişimler geri dönüşümlü oluşları ve • DNA’nın baz dizisinde bir değişime neden olmamaları gibi özellikleriyle genetik değişimlerden ayrılırlar. • Sonraki kuşaklara aktarılabilmektedir.
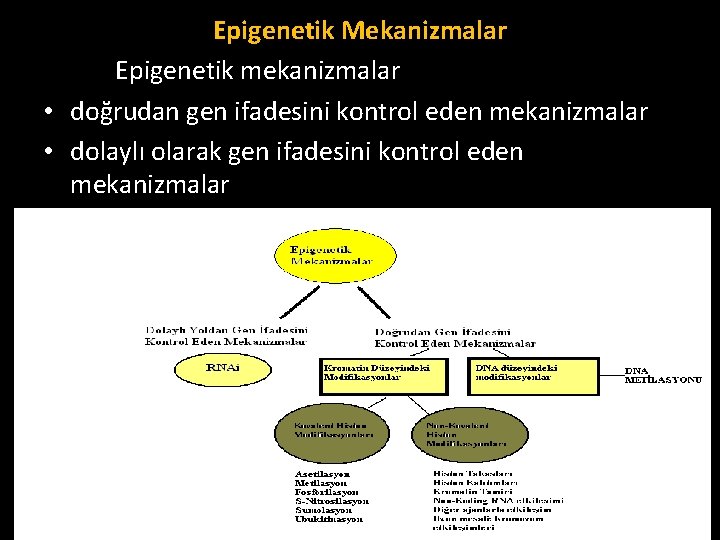
Epigenetik Mekanizmalar Epigenetik mekanizmalar • doğrudan gen ifadesini kontrol eden mekanizmalar • dolaylı olarak gen ifadesini kontrol eden mekanizmalar

Doğrudan Gen İfadesini Kontrol Eden Mekanizmalar • Kromatin düzeyindeki modifikasyonlar • DNA düzeyindeki modifikasyonlar

Kromatin Düzeyindeki Modifikasyonlar • Bu modifikasyonlar hem kovalent hem de nonkovalent olabilirler. • Genlerin sessizleşmesine neden olurlar. Bu da geni inaktive edici bir mutasyon veya delesyon gibi genetik bir mekanizmayla eşdeğerdir.

A. Kovalent Histon Modifikasyonları • • • Asetilasyon, Metilasyon, Fosforilasyon, S-nitrosilasyon, Ubikitinasyon Sumolasyon Genin transkripsiyon aşamasının düzenlenmesini sağlayan faktörlerdir.

EPİGENETİK MODİFİKASYONLAR

• Asetilasyon: Histon proteinlerinin lizin rezidüsüne asetil gruplarının bağlanması olarak tanımlanabilir. Asetilasyonu taklit edebilecek mutasyonların oluşması posttranslasyonel modifikasyonları ve deasetilaz aktiviteyi etkilemektedir. Histon asetilaz enzimi Histon deasetilaz enzimi
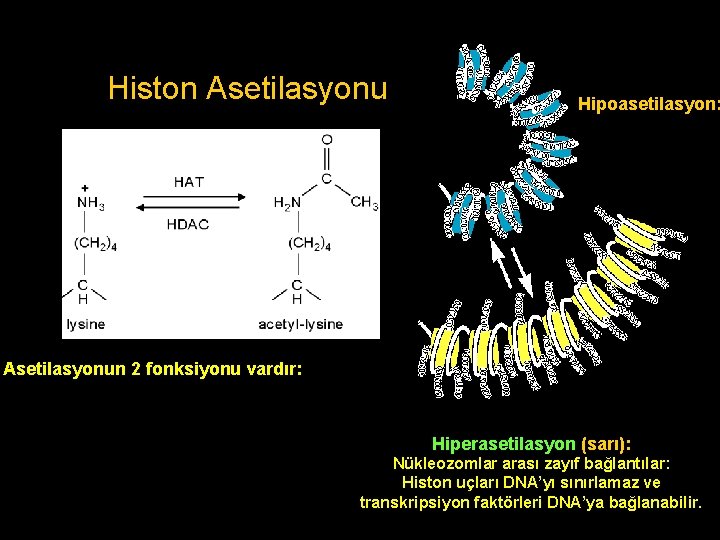
Histon Asetilasyonu Hipoasetilasyon: Nükleozomlar arası güçlü bağlantılar Histone deacetylase Asetilasyonun 2 fonksiyonu vardır: 1. Pozitif yüklü lizin rezidülerini nötralize eder. 2. Histon uçları ile yapısal proteinler arasındaki bağlantıları destabilize eder. Hiperasetilasyon (sarı): Nükleozomlar arası zayıf bağlantılar: Histon uçları DNA’yı sınırlamaz ve transkripsiyon faktörleri DNA’ya bağlanabilir.

• Metilasyon: Histon metiltransferaz enzimleri tarafından histon proteinlerinde bulunan amino asitlere 1, 2 veya 3 tane metil grubu (tri metilasyon) eklenmesi olayıdır. Bir genin ifade edilip edilmeyeceğini o geni açık veya kapalı konuma (switch on- switch off) getiren olay, bu ve benzeri modifikasyonlardır. Açık/Kapalı gen setleri bulunduğu hücre tipine göre farklılık gösterir.

• Fosforilasyon: Histon deasetilazlara geri dönüşümlü olarak fosfat gruplarının bağlanmasıdır. Fosfatlar histon deasetilazlara serin, treonin ve tirozin rezidülerinden bağlanır. Fosforilasyon protein kinazlar (PK) ve protein fosfatazlar (PP) tarafından gerçekleştirilen bir reaksiyondur.

• S-nitrasilasyon: Histon deasetilazlara sistein rezidüsünden nitrosil (NO) grubunun eklenmesi olayıdır. Bu olay katalitik aktiviteyi etkiler ve bunun neticesinde kromatinden korepresörlerin ayrılamamasına neden olur.

• Ubukitinasyon: Ubukitin (Ub) lizin rezidüsü ile bağlanabilen küçük bir proteindir. Üç aşamalı bir enzimatik reaksiyonun oluşumuna neden olur. Bu reaksiyonlar, E 1, E 2, E 3 enzimleri tarafından gerçekleştirilir. Ubukitinasyon neticesinde, proteinlerin yıkılma yolu olan proteosom yolağına proteinlerin girmesine ve degrade olmasına neden olur.

• Sumolasyon: SUMO (small ubuquitin-like modifier) 1, 2, 3 proteinlerinin ubukitin ile birleşmesi olayıdır. Ubukutine benzer bir protein olan SUMO proteinleri lizin rezidülerinden proteinlere bağlanır ve bu olay neticesinde protein degradasyonu engellenir.
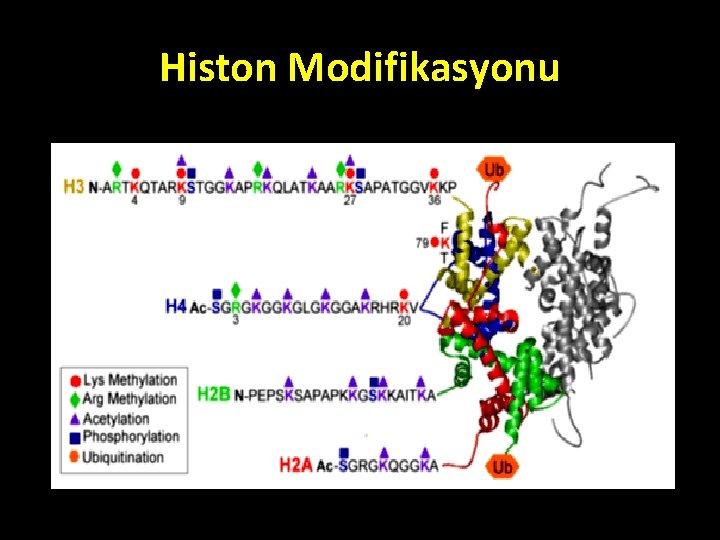
Histon Modifikasyonu

B. Nonkovalent Histon Modifikasyonlar • Histon takasları, histon kalıtımları, kromatin tamiri, nonkoding RNA ile etkileşim, diğer ajanlarla etkileşim (virüsler, farklı protein grupları) uzun-mesafe kromozom etkileşimleri (hem kromozom-içi hem kromozomlar-arası) nonkovalent histon modifikasyonları olarak sayılabilir.
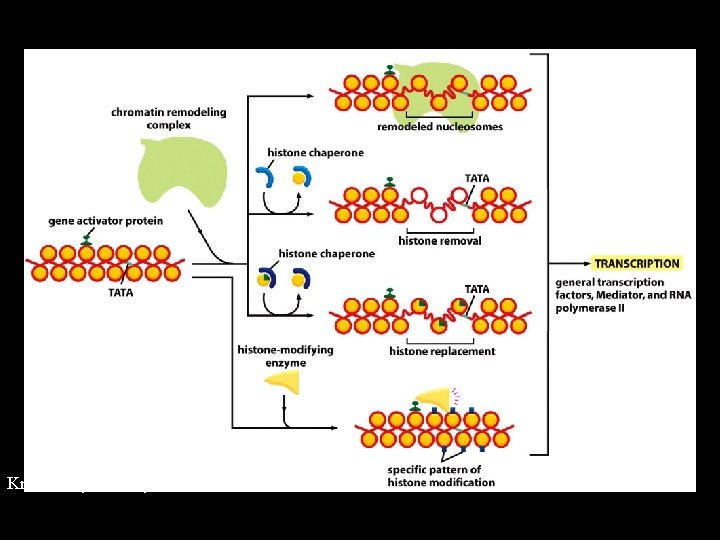
Kromatin yeniden şekillenmesi

Tüm bu mekanizmalar, kromatin yapısında değişiklikler oluşturarak transkripsiyonu düzenleyici komplekslerin DNA’ya ulaşabilirliğini etkilerler. Ayrıca birçok histon modifikasyonu geri dönüşümlüdür ve modifikasyon seviyesi ile transkripsiyon seviyesi sıkı ilişki içerisindedir.

II. DNA düzeyindeki modifikasyonların en bilinen ve en işlevsel olanı DNA metilasyonudur. DNA metilasyonu, DNA'nın bir kimyasal değişimidir, kalıtsal olup sonradan ilk dizi geri gelecek şekilde çıkartılabilir. Bu özelliği nedeniyle epigenetik koda aittir ve en iyi karakterize edilmiş epigenetik mekanizmadır.
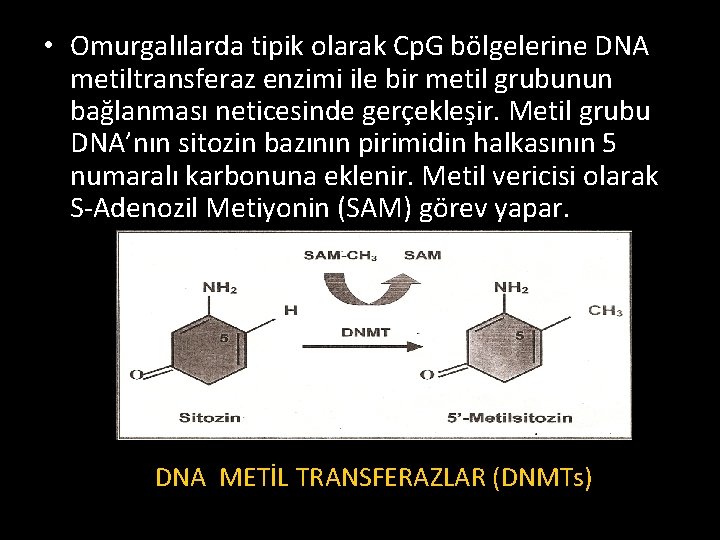
• Omurgalılarda tipik olarak Cp. G bölgelerine DNA metiltransferaz enzimi ile bir metil grubunun bağlanması neticesinde gerçekleşir. Metil grubu DNA’nın sitozin bazının pirimidin halkasının 5 numaralı karbonuna eklenir. Metil vericisi olarak S-Adenozil Metiyonin (SAM) görev yapar. DNA METİL TRANSFERAZLAR (DNMTs)

DNA metilasyonu • DNA metilasyonu epigenetik değişikliklerden biridir. • Cp. G dizisindeki sitozinin 5. karbonuna DNA metil transferazların katalizlemesiyle bir metil grubunun eklenmesiyle meydana gelen biyokimyasal bir işlemdir. • DNA metilasyon değişimleri hipo veya hipermetilasyon şeklinde oluşabilir. • Hipometilasyon transkripsiyonu ve genin etkinliğini artırırken hipermetilasyon transkripsiyonu baskılamaktadır. • İnsan DNA’ sındaki tüm Cp. G alanlarının % 70 -80’ i metillenmiştir.
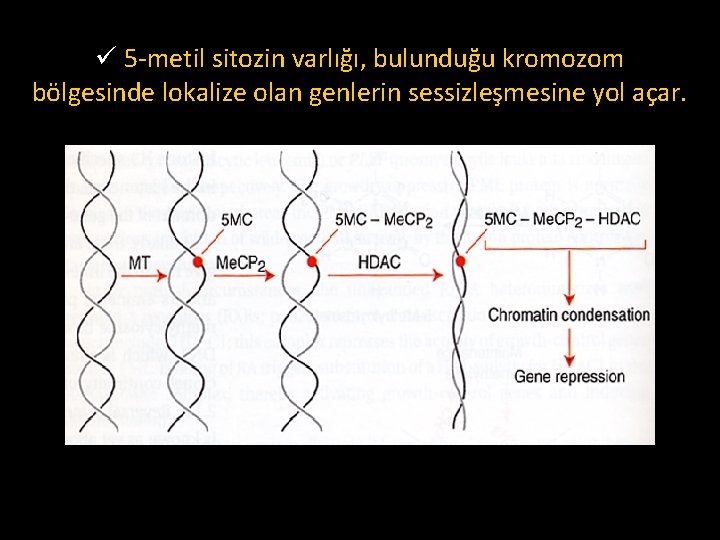
ü 5 -metil sitozin varlığı, bulunduğu kromozom bölgesinde lokalize olan genlerin sessizleşmesine yol açar.

• Metilasyon DNA’nın inaktive olmasına neden olarak protein ekspresyonunu engelleyen bir sistemdir. • Erişkin somatik dokularda DNA metilasyonu tipik olarak Cp. G dinükleotit dizilerinde meydana gelir. • Cp. G dışı metilasyon embriyonik kök hücrelerde hâkimdir.

Cp. G NEDİR ? • Cp. G, Sitozin fosfo Guanin anlamına gelir. • İnsanlarda Cp. G dinükleotidi sıklığının ölçüsü çok azdır, bu CG baskılanması olarak bahsedilen bir olaydır.

GC Baskılanması • İnsan genomunun başından sonuna kadar 3003000 bç uzunluğundaki küçük alanlar haricinde, çok belirgindir. • Bu alanlara Cp. G adacıkları denilmektedir ve genomun %1 kadarında bulunduğu düşünülmektedir.

Cp. G ADACIKLARI • Cp. G adalarının öncelikli olarak, ifade olan genlerin 5’ bölgesinde bulundukları gözlenmiştir ve insan promotorlarının % 60’ından fazlası bu Cp. G adalarını içermektedir.

Cp. G ADACIKLARI • Promotorlardaki Cp. G adaları metillendikleri zaman gen sürekli sessiz hale gelir ve bu sessizlik mitoz bölünmeler boyunca aktarılır. • Bu sebeple Cp. G adacıklarının metilasyonu epigenetik bir modifikasyonu temsil eder.
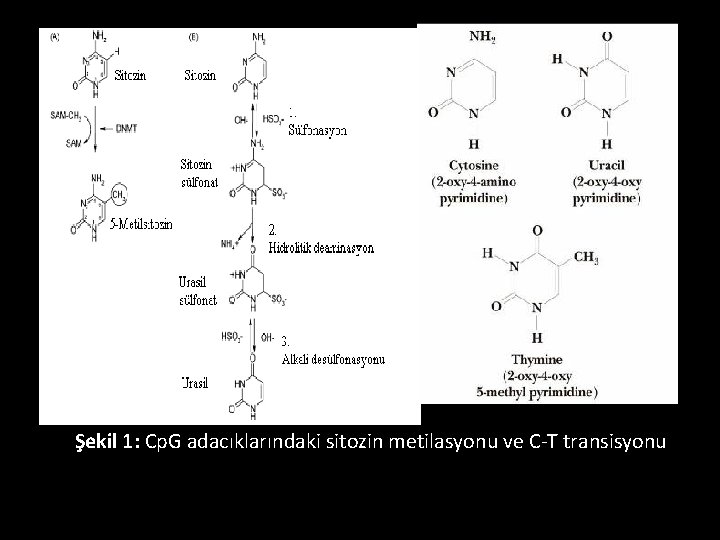
Şekil 1: Cp. G adacıklarındaki sitozin metilasyonu ve C-T transisyonu

DNA METİLASYONU • DNA metilasyonunun en önemli görevi gen regülasyonu’dur.

DNA metilasyonu • Genomu transpozonlardan koruma • Transkripsiyonel susturma • Genomik imprinting • X inaktivasyonu • Doku spesifik gen anlatımı

Bir genin metillenme derecesi neyi ifade eder ? • Bir genin metillenme derecesi ile ifade edilme derecesi arasında ters bir ilişki vardır. • Metillenme oranı gen ifadesi oranı

Bir genin metillenme derecesi neyi ifade eder ? • Metillenme dokuya özgüdür ve bir kere gerçekleşince o hücrelerine aktarılır. dokunun bütün

DNA metilasyonu gen ifadesini nasıl kontrol eder ? 1 - Metillenmiş promotor bölgelerine bağlanabilen proteinlerin hedef dizilere (sekanslara) bağlanarak, esas bağlanması gereken faktörlerinin buralara bağlanmasını engelleyerek, 2 - Transkripsiyon engelleyerek, faktörlerinin metillenmiş sitozine transkripsiyon bağlanmasını 3 - Kromatin yapısını değiştirerek transkripsiyon miktarında bir değişim gerçekleştirerek.

DNA metilasyonu kanserin oluşum sürecini etkiler. DNA tamiri Karsinojen Metabolizması Hormonal Regulasyon DNA Metilasyonu Farklılaşma Hücre Siklusu Apoptoz
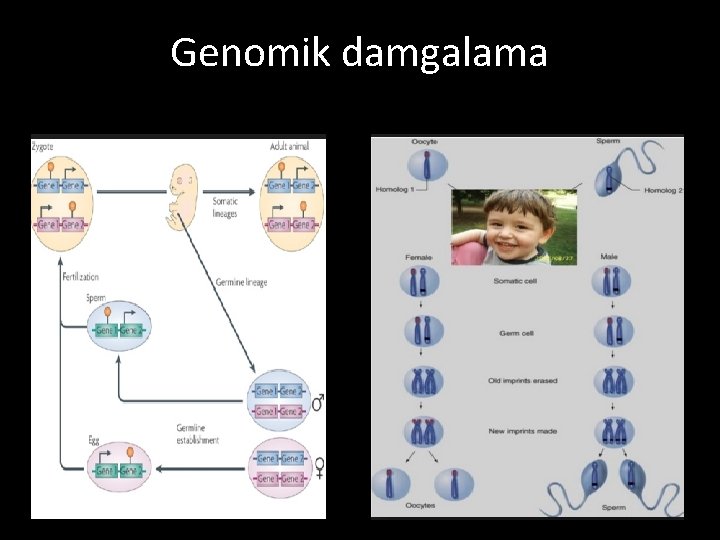
Genomik damgalama

§ İnsan kanserlerinde DNA metilasyon değişimlerinin 2 genel tipi gözlenmektedir: 1. Genomik Hipermetilasyon 2. Genomik Hipometilasyon
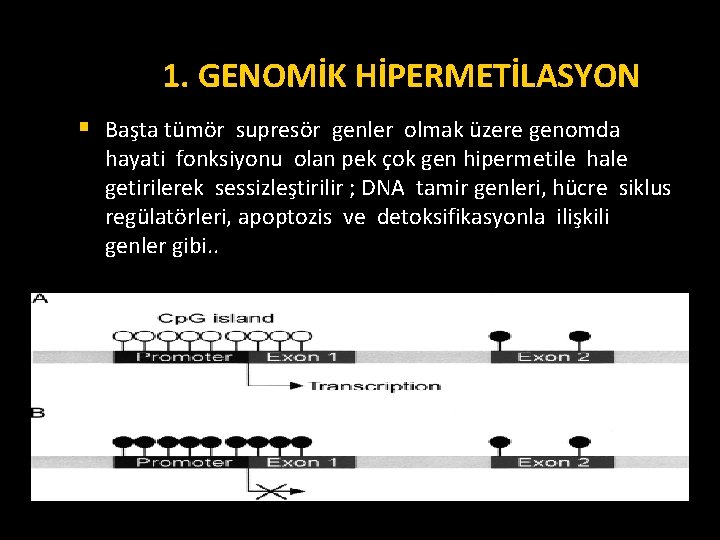
1. GENOMİK HİPERMETİLASYON § Başta tümör supresör genler olmak üzere genomda hayati fonksiyonu olan pek çok gen hipermetile hale getirilerek sessizleştirilir ; DNA tamir genleri, hücre siklus regülatörleri, apoptozis ve detoksifikasyonla ilişkili genler gibi. .

2. GENOMİK HİPOMETİLASYON § Cp. G adaları hipermetile olduklarında, kanser hücre genomları da göze çarpar bir şekilde global hipometilasyona uğrarlar. Bu hipo metile bölgeler, yüksek ya da orta derece de tekrar dizileri içeren DNA bölgeleridir; örneğin: heterokromatik DNA tekrar bölgeleri, serpiştirilmiş retrotranspozonlar ve endojen retroviral elementler. § Habis bir hücre normal halinden %20 -60 daha az genomik 5 metil sitozin içerebilir. Bu metil grubu kaybı, kodlayıcı alanlar ile intronların hipometilasyonu ve tekrarlayıcı dizilerin demetilasyonu sebebiyle gerçekleşir.
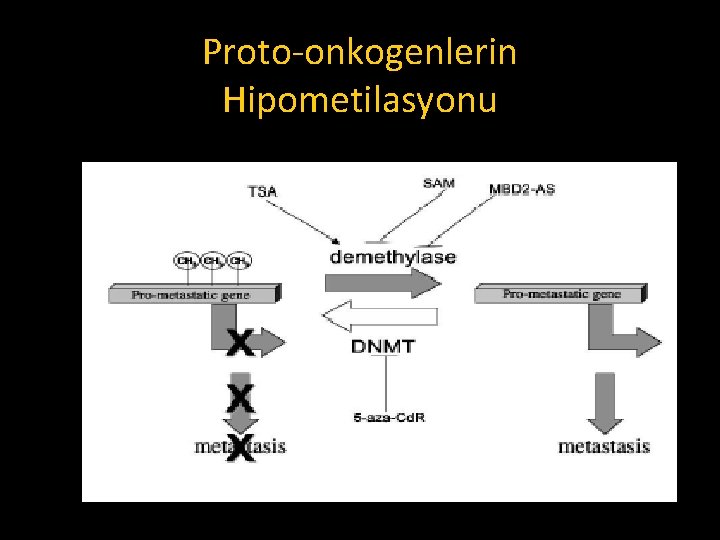
Proto-onkogenlerin Hipometilasyonu

Dolaylı Yoldan Gen İfadesini Kontrol Eden Mekanizmalar POST-TRANSKRİPSİYONEL MEKANİZMALAR ü RNA İNTERFERENCE (RNAi)
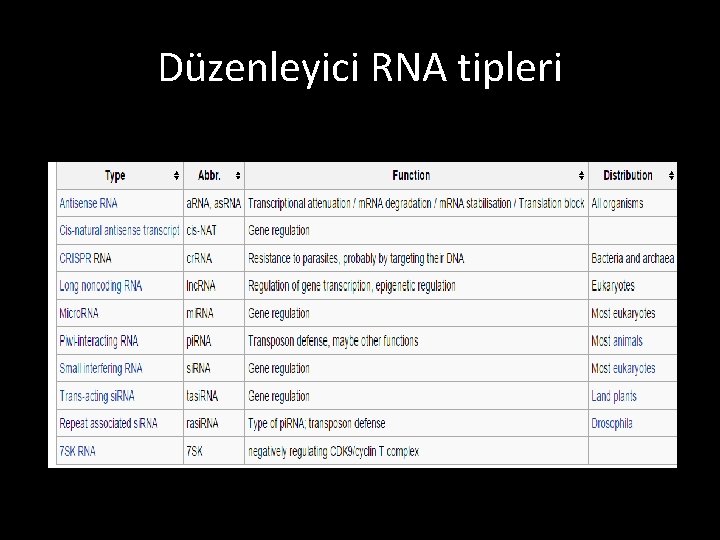
Düzenleyici RNA tipleri
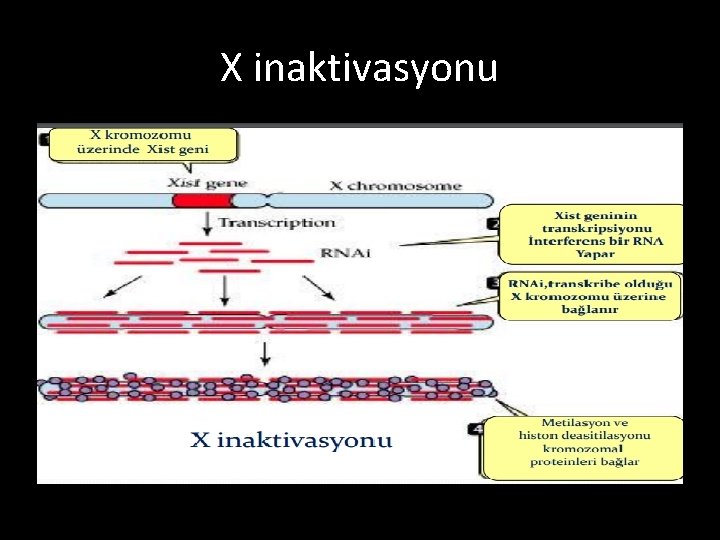
X inaktivasyonu
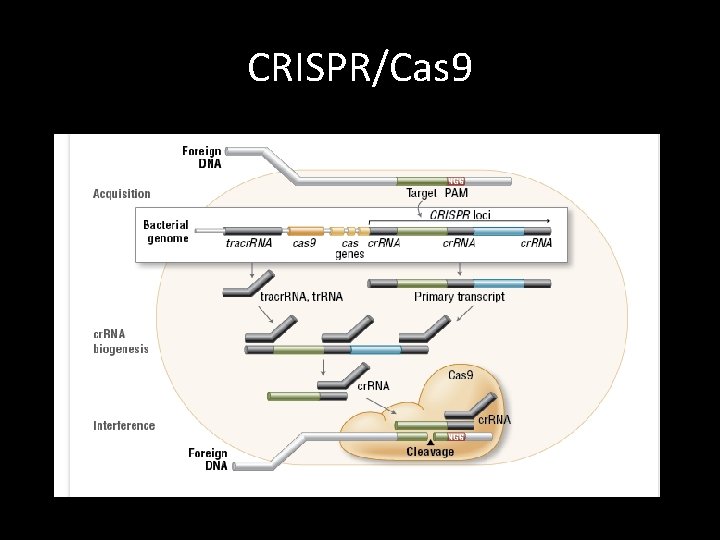
CRISPR/Cas 9
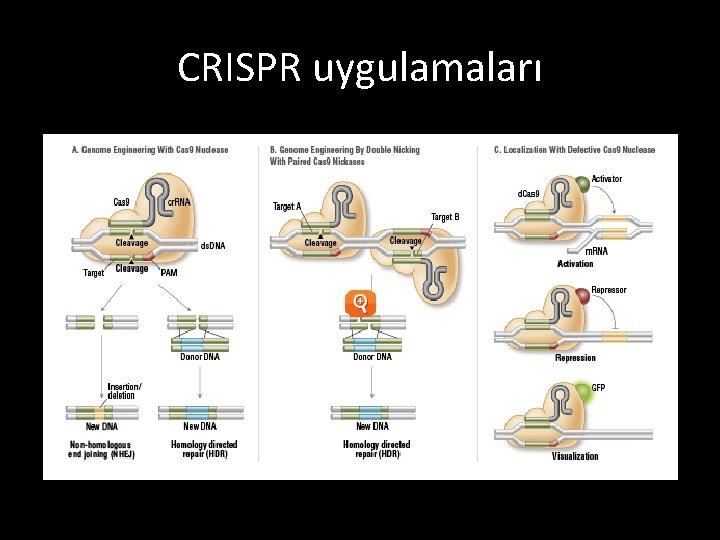
CRISPR uygulamaları

Post-transkripsiyonel (transkripsiyon sonrası, yani ana DNA molekülünden RNA molekülü elde edildikten sonra) mekanizmaları özellikle de nonkoding RNA’nın (RNAi vb. ) kodlayıcı RNA (m. RNA)’yı etkileyerek protein sentezini engellemesini içerir.
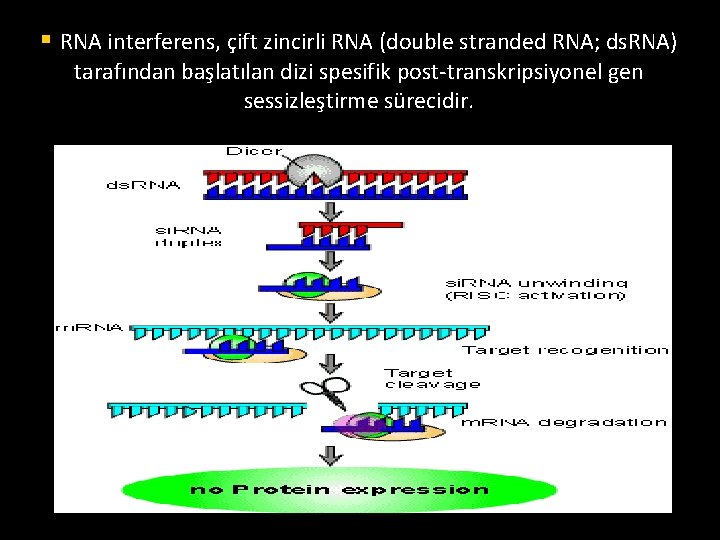
§ RNA interferens, çift zincirli RNA (double stranded RNA; ds. RNA) tarafından başlatılan dizi spesifik post-transkripsiyonel gen sessizleştirme sürecidir.

Terapötik si. RNA’lar si. RNA hedef geni p 53 mutant K-Ras BCR-ABL MDR 1 C-RAF Bcl-2 VEGF PKC- Β-Catenin Hastalık KANSER

§ mi. RNA genlerinin %50’den fazlası kanserle ilişkili genomik alanlarda veya frajil sitelerde lokalizedir. • Bunların tümör supresör gibi davranarak onkogenleri inhibe ettikleri veya tam tersi olarak onkogen gibi hareket ederek tümör supresörleri inhibe ettikleri gösterilmiştir.
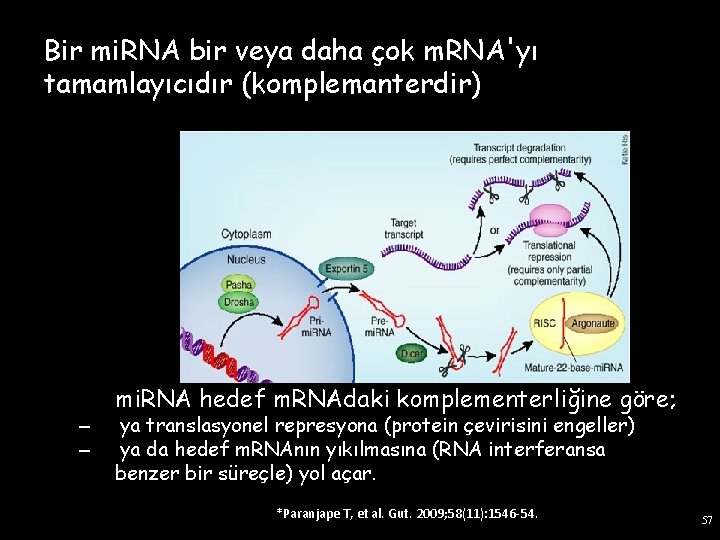
Bir mi. RNA bir veya daha çok m. RNA'yı tamamlayıcıdır (komplemanterdir) – – mi. RNA hedef m. RNAdaki komplementerliğine göre; ya translasyonel represyona (protein çevirisini engeller) ya da hedef m. RNAnın yıkılmasına (RNA interferansa benzer bir süreçle) yol açar. *Paranjape T, et al. Gut. 2009; 58(11): 1546 -54. 57
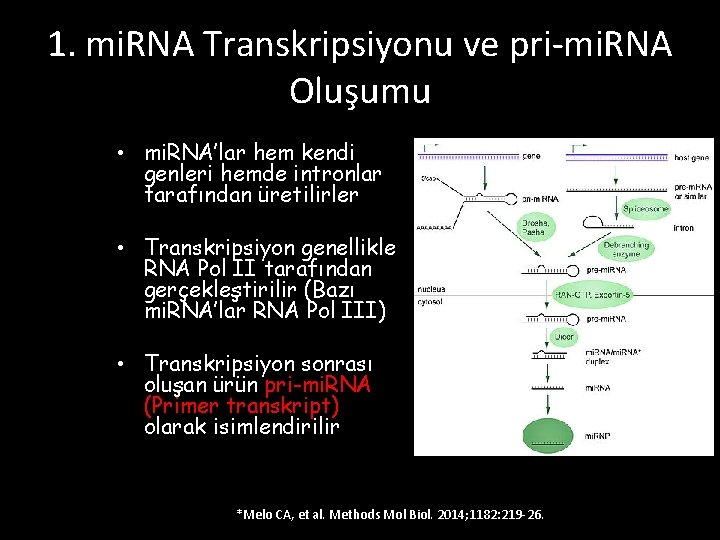
1. mi. RNA Transkripsiyonu ve pri-mi. RNA Oluşumu • mi. RNA’lar hem kendi genleri hemde intronlar tarafından üretilirler • Transkripsiyon genellikle RNA Pol II tarafından gerçekleştirilir (Bazı mi. RNA’lar RNA Pol III) • Transkripsiyon sonrası oluşan ürün pri-mi. RNA (Primer transkript) olarak isimlendirilir *Melo CA, et al. Methods Mol Biol. 2014; 1182: 219 -26.
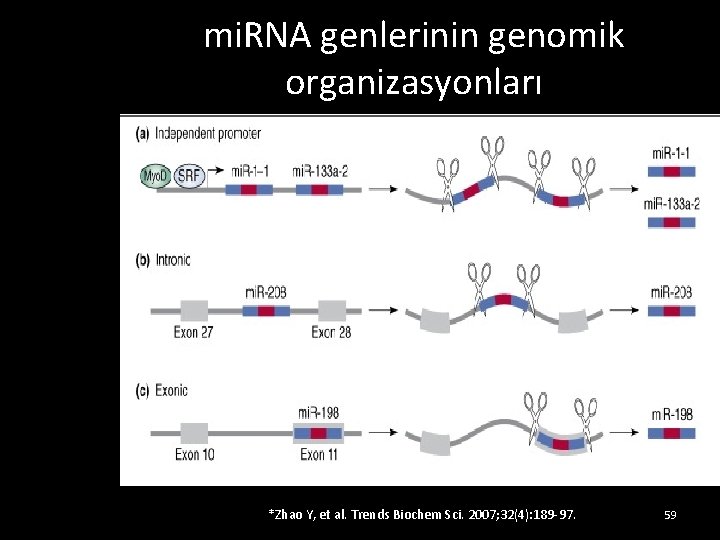
mi. RNA genlerinin genomik organizasyonları *Zhao Y, et al. Trends Biochem Sci. 2007; 32(4): 189 -97. 59
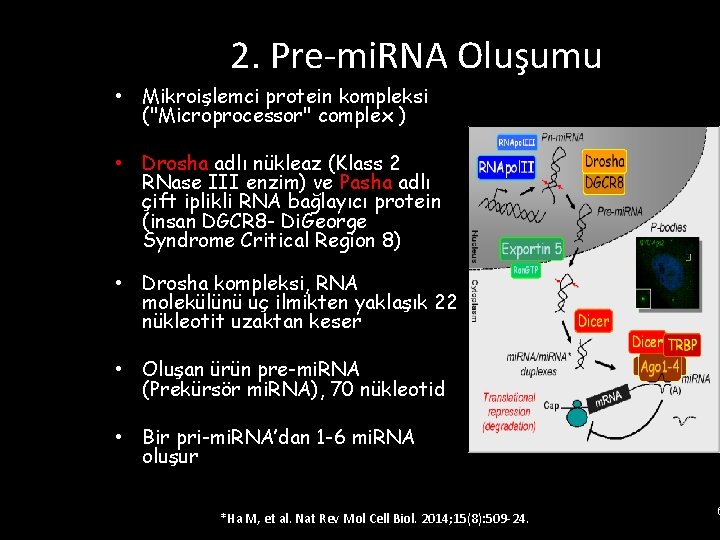
2. Pre-mi. RNA Oluşumu • Mikroişlemci protein kompleksi ("Microprocessor" complex ) • Drosha adlı nükleaz (Klass 2 RNase III enzim) ve Pasha adlı çift iplikli RNA bağlayıcı protein (insan DGCR 8 - Di. George Syndrome Critical Region 8) • Drosha kompleksi, RNA molekülünü uç ilmikten yaklaşık 22 nükleotit uzaktan keser • Oluşan ürün pre-mi. RNA (Prekürsör mi. RNA), 70 nükleotid • Bir pri-mi. RNA’dan 1 -6 mi. RNA oluşur *Ha M, et al. Nat Rev Mol Cell Biol. 2014; 15(8): 509 -24. 6
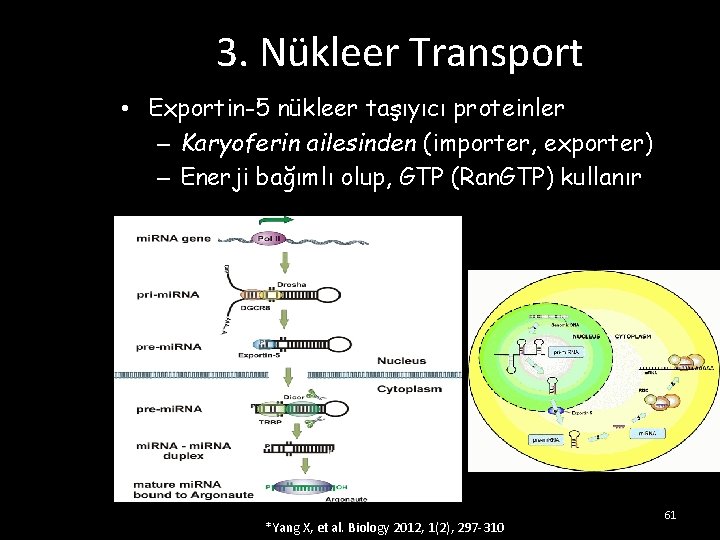
3. Nükleer Transport • Exportin-5 nükleer taşıyıcı proteinler – Karyoferin ailesinden (importer, exporter) – Enerji bağımlı olup, GTP (Ran. GTP) kullanır *Yang X, et al. Biology 2012, 1(2), 297 -310 61

4. mi. RNA oluşumu • Sitoplazmaya transfer edilen mi. RNA Dicer ve partner protein ile (Drosophila R 2 D 2, insan TRBP) saç tokası yapısını keser ve iki ipliği açar. *Ha M, et al. Nat Rev Mol Cell Biol. 2014; 15(8): 509 -24. 62
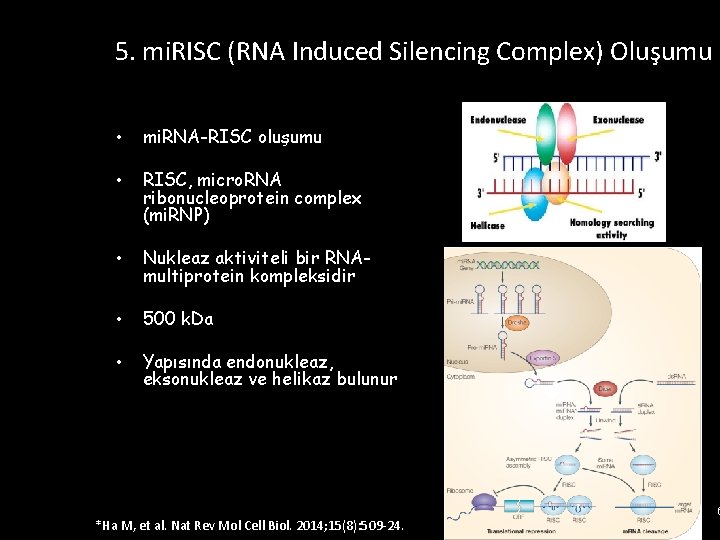
5. mi. RISC (RNA Induced Silencing Complex) Oluşumu • mi. RNA-RISC oluşumu • RISC, micro. RNA ribonucleoprotein complex (mi. RNP) • Nukleaz aktiviteli bir RNAmultiprotein kompleksidir • 500 k. Da • Yapısında endonukleaz, eksonukleaz ve helikaz bulunur *Ha M, et al. Nat Rev Mol Cell Biol. 2014; 15(8): 509 -24. 6
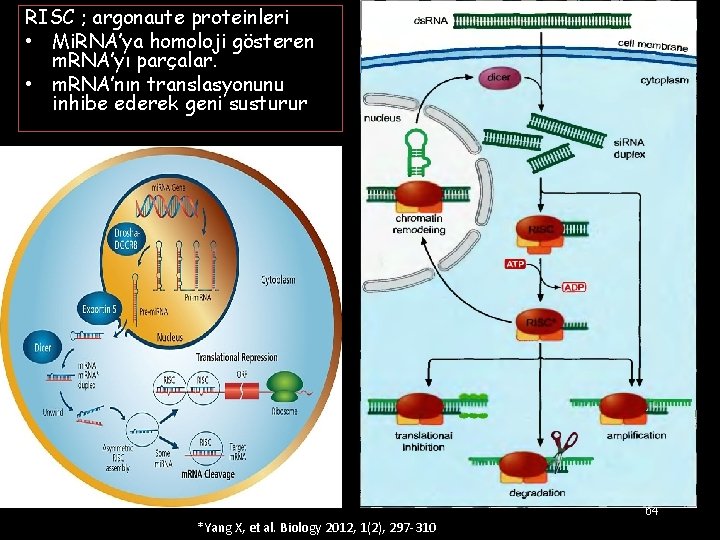
RISC ; argonaute proteinleri • Mi. RNA’ya homoloji gösteren m. RNA’yı parçalar. • m. RNA’nın translasyonunu inhibe ederek geni susturur 64 *Yang X, et al. Biology 2012, 1(2), 297 -310
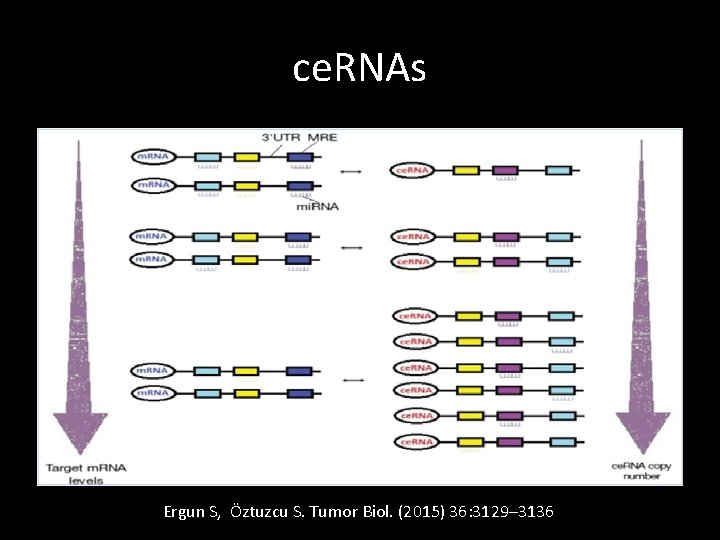
ce. RNAs Ergun S, Öztuzcu S. Tumor Biol. (2015) 36: 3129– 3136

5 q- myelodysplastic syndrome Arancio W. Oncoscience 2015, Vol. 2, No. 10

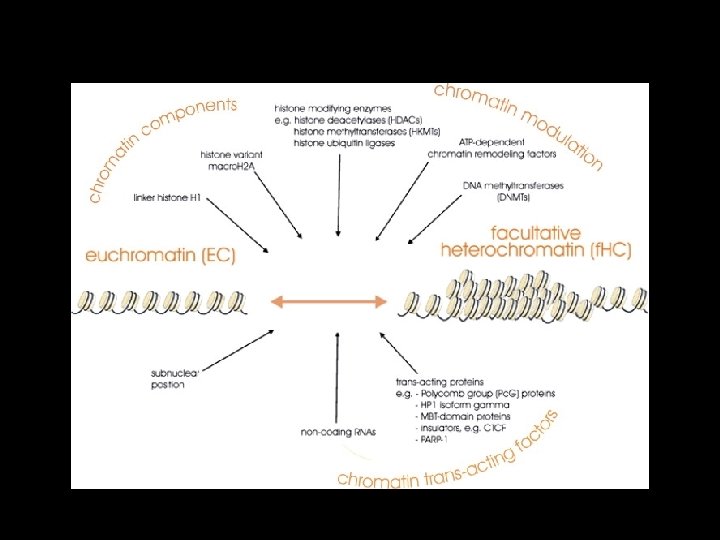
KROMATİN POZİSYON ETKİSİ (CPE) • DNA+diziler arasındaki etkileşimler+proteinler Kromatin • • Paketlenme düzeyi Topolojik konumu Nüklezomları yerleşimi ve sıklığı Histon kodu Histon varyantlarının varlığı Non-histon bağlanma fartörlerinin kompozisyonu Nukleoplazma içerisindeki yerleşim Hücre döngüsü dinamikleri

• Ökromatin • Heterokromatin – Hipoasetile – H 3 K 4 unmetilasyonu – DNA metilasyonunca zengin – H 3 K 9 di ve tri-metilasyonunca zengin – H 3 K 27 ve H 4 K 20 metilasyonu – HP 1 bağlanma

Genler, düzenleyici bölgeler ve tekrar dizleri mozaik • Pozisyon etkisi (PEV) – Genetik materyalin lokasyonunda bir değişik olmasıyla bir genin ya da genetik bölgenin fenotipik değişikliğe uğraması • Kromatin pozisyon etkisi (CPE) – Telomere uzaklık [Telomeric position effect, (TPE)] – cis-düzenleyiciler – insülatörler

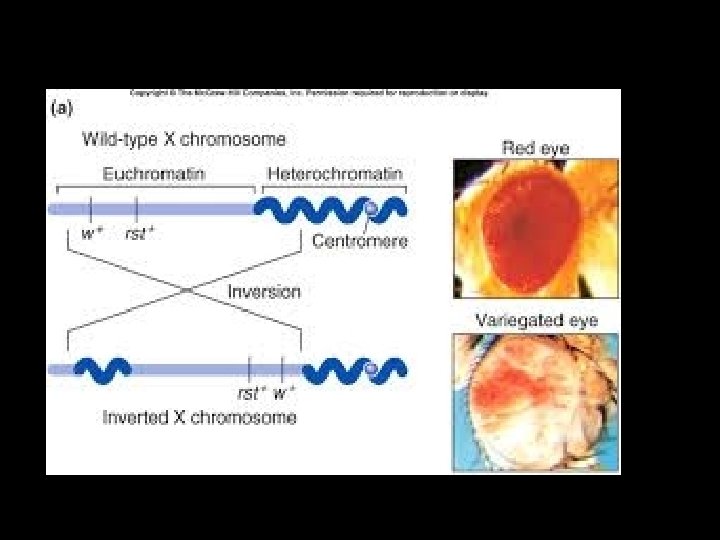
Pozisyon etkisi (PEV) • Sturtevant, 1920 – Drosophila -göz rengi – Kırmızı göz renginin, kırmızı-beyaza dönüşmesi • Muller – X chromosomu inversiyonu – Beyaz göz rengi ile ilişkili gen perisentromerik bölgede lokalize • Heterokromatik bölgelerde lokalize bir gen
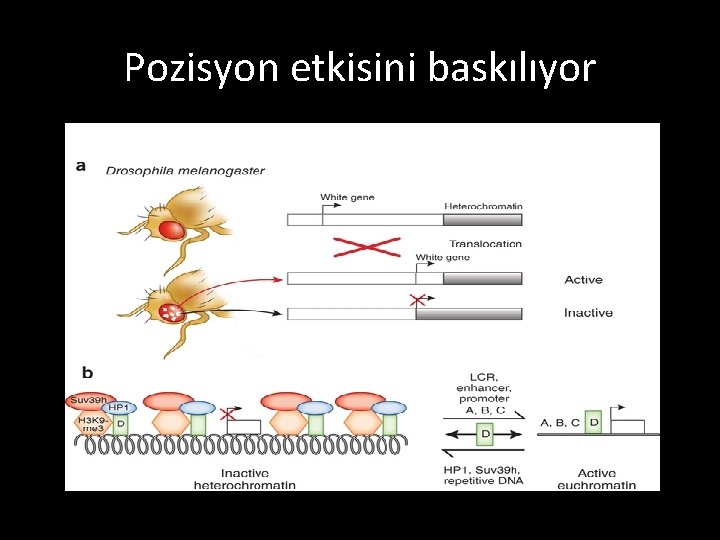
Pozisyon etkisini baskılıyor

PEV • Drosophila’da 50 -150 locusta gözleniyor – Heterokromatin, histonları modifiye eden enzimler, non-histon proteinleri ve çekirdek proteinleri

Telomeric position effect, (TPE) • Saccharomyces cerevisiae’dan Homo sapiens genlerin büyük çoğunluğu susturulur

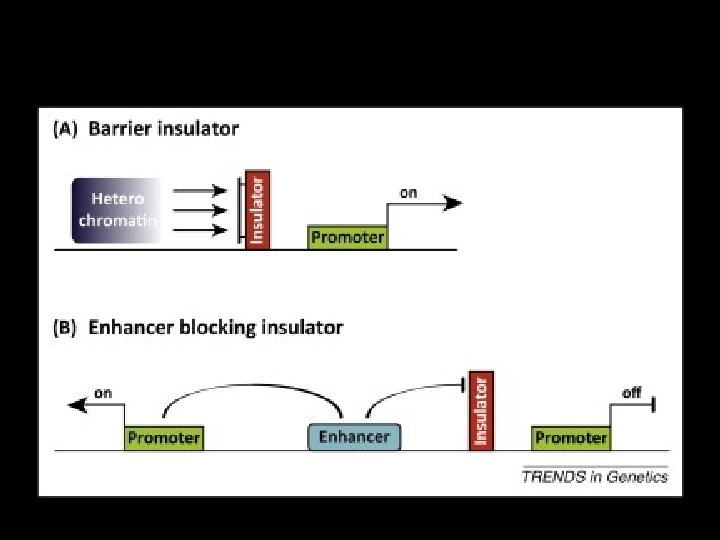
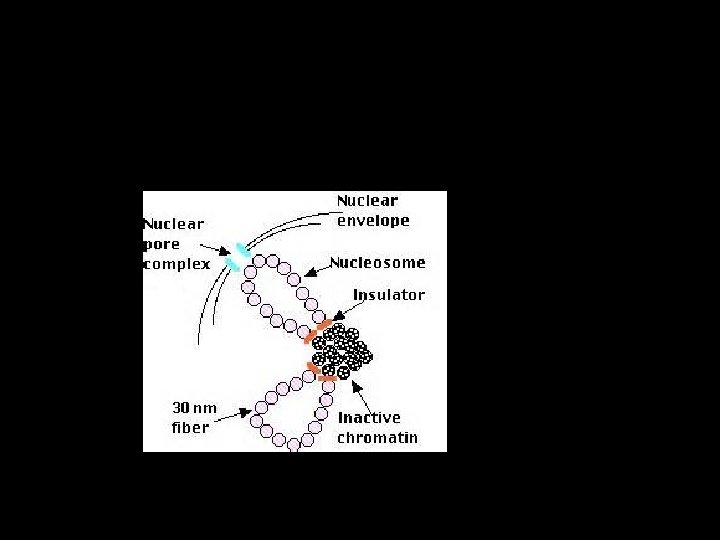
• Aktif ve inaktif kromatin bölgeleri birbirini takip etmektedir • İlk insulator elemanları, scs ve scs’, Udvardy ve arkadaşları tarafından ısı şok lokusunda Drosophila’da 1985’te tanımlanmıştır – Enhencer-blocking insulatörleri – Barrier insulatörleri

Enhencer-blocking insulatörleri • Promotor ve cis-regulator eleman arasına yerleştirildiği zaman iletişlimi keser

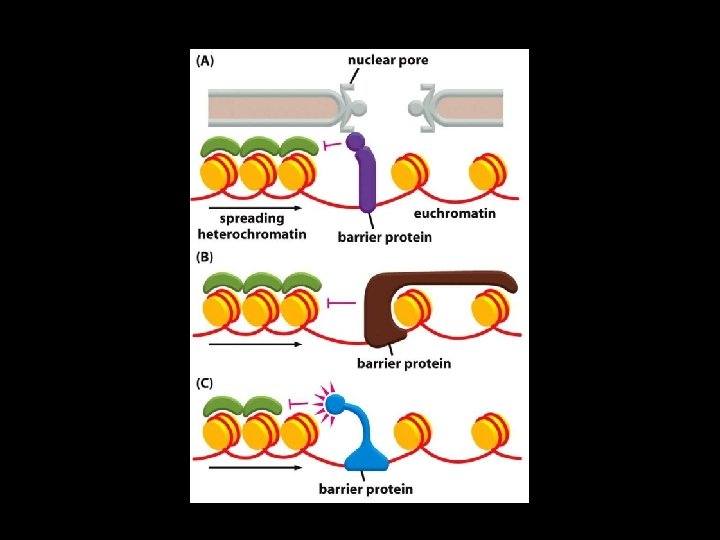
Barrier insulatörleri • Heterokromatin etkisinin genlere yayılmasını engeller
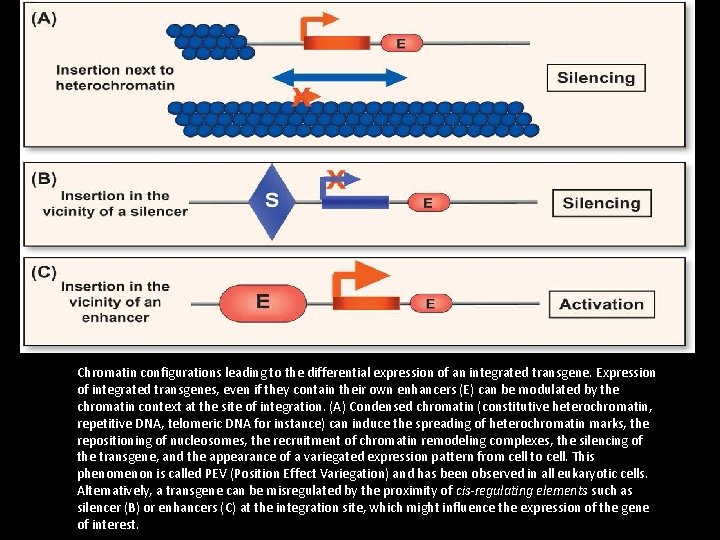
Chromatin configurations leading to the differential expression of an integrated transgene. Expression of integrated transgenes, even if they contain their own enhancers (E) can be modulated by the chromatin context at the site of integration. (A) Condensed chromatin (constitutive heterochromatin, repetitive DNA, telomeric DNA for instance) can induce the spreading of heterochromatin marks, the repositioning of nucleosomes, the recruitment of chromatin remodeling complexes, the silencing of the transgene, and the appearance of a variegated expression pattern from cell to cell. This phenomenon is called PEV (Position Effect Variegation) and has been observed in all eukaryotic cells. Alternatively, a transgene can be misregulated by the proximity of cis-regulating elements such as silencer (B) or enhancers (C) at the integration site, which might influence the expression of the gene of interest.
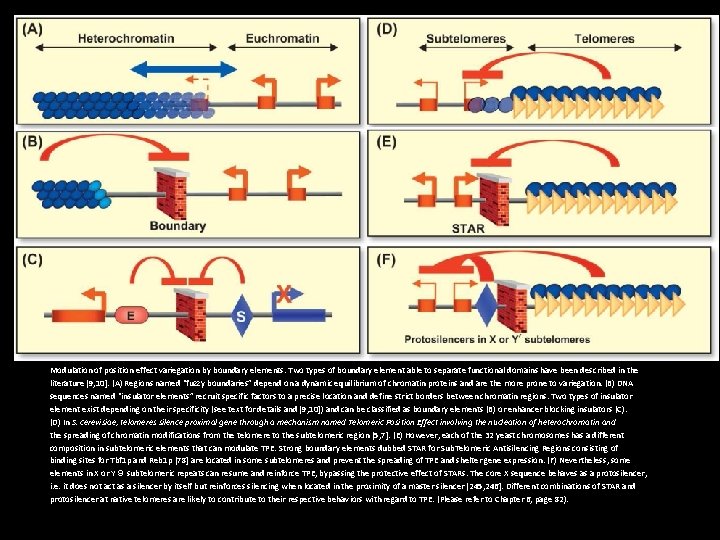
Modulation of position effect variegation by boundary elements. Two types of boundary element able to separate functional domains have been described in the literature [9, 10]. (A) Regions named “fuzzy boundaries” depend on a dynamic equilibrium of chromatin proteins and are the more prone to variegation. (B) DNA sequences named “insulator elements” recruit specific factors to a precise location and define strict borders between chromatin regions. Two types of insulator element exist depending on their specificity (see text for details and [9, 10]) and can be classified as boundary elements (B) or enhancer blocking insulators (C). (D) In S. cerevisiae, telomeres silence proximal gene through a mechanism named Telomeric Position Effect involving the nucleation of heterochromatin and the spreading of chromatin modifications from the telomere to the subtelomeric region [5, 7]. (E) However, each of the 32 yeast chromosomes has a different composition in subtelomeric elements that can modulate TPE. Strong boundary elements dubbed STAR for Sub. Telomeric Antisilencing Regions consisting of binding sites for Tbf 1 p and Reb 1 p [78] are located in some subtelomeres and prevent the spreading of TPE and shelter gene expression. (F) Nevertheless, some elements in X or Y9 subtelomeric repeats can resume and reinforce TPE, bypassing the protective effect of STARs. The core X sequence behaves as a protosilencer, i. e. it does not act as a silencer by itself but reinforces silencing when located in the proximity of a master silencer [245, 246]. Different combinations of STAR and protosilencer at native telomeres are likely to contribute to their respective behaviors with regard to TPE. (Please refer to Chapter 6, page 82).

Üçlü tekrar hastalıları – Kodlamayan tekrar hastalıkları • Epigenetik değişiklikler ve heterokromatin oluşumu • Friederick ataxia • FXG genin azalan ifadesi – FXS • 5’ translasyona uğramayan bölgede • Tekrar bölgesi ve çevresinde hipermetilasyon • FMR 1 genin susturulması

Telomerik pozisyon etkisi • Subtelorik bölgelerde rekombinasyon fazla • Telomerlerden gelen susturma işlemini hızlandırabilir • İdiyopatik MR – 22 qter delesyon sendromu – Cri-du-cat delesyon sendromu
- Slides: 85