ENZYMY ecky en zme v kvasnicch Biokatalyztory katalyzuj

ENZYMY řecky en zýme = v kvasnicích Biokatalyzátory katalyzují reakce v živých organismech
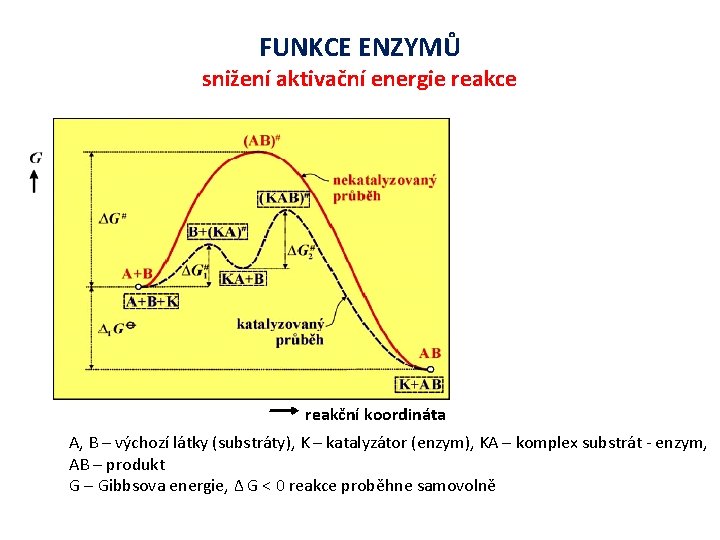
FUNKCE ENZYMŮ snižení aktivační energie reakce reakční koordináta A, B – výchozí látky (substráty), K – katalyzátor (enzym), KA – komplex substrát - enzym, AB – produkt G – Gibbsova energie, Δ G < 0 reakce proběhne samovolně

Faktory ovlivňující rychlost enzymově katalyzované reakce • • Koncentrace substrátu Množství enzymu Fyzikálně – chemické vlastnosti prostředí (teplota, p. H, …. . ) Přítomnost modifikátorů (efektorů) - aktivátory (zvyšují aktivitu enzymu) - inhibitory (snižují aktivitu enzymu)

ENZYMY JAKO KATALYZÁTORY ( porovnání s chemickými katalyzátory) 1. Rychlost – o několik řádů vyšší v porovnání s chem. katalyzátory 2. Mírné podmínky vnitřního prostředí organismu (teploty kolem 40 °C, normální tlak a většina enzymů má p. H-optimum 5 - 7. 3. Vysoká specifita jak co do struktury přeměňovaných molekul substrátů (substrátová specifita), tak co do typu katalyzované reakce (funkční specifita). 4. Regulace na několika úrovních
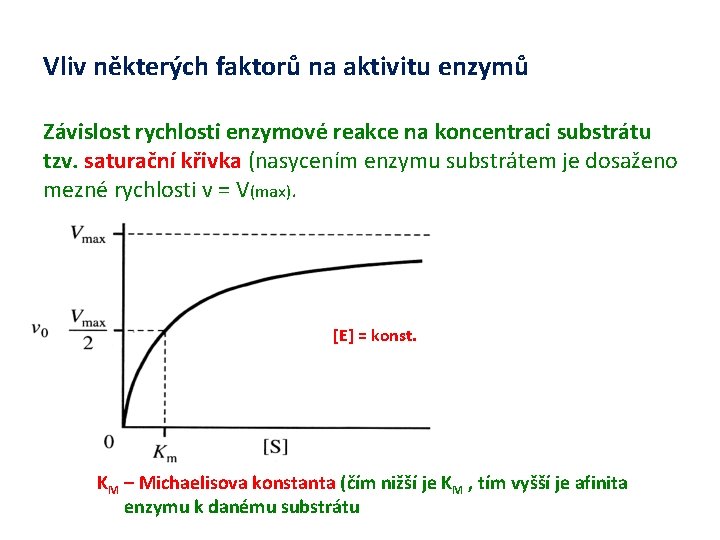
Vliv některých faktorů na aktivitu enzymů Závislost rychlosti enzymové reakce na koncentraci substrátu tzv. saturační křivka (nasycením enzymu substrátem je dosaženo mezné rychlosti v = V(max). [E] = konst. KM – Michaelisova konstanta (čím nižší je KM , tím vyšší je afinita enzymu k danému substrátu
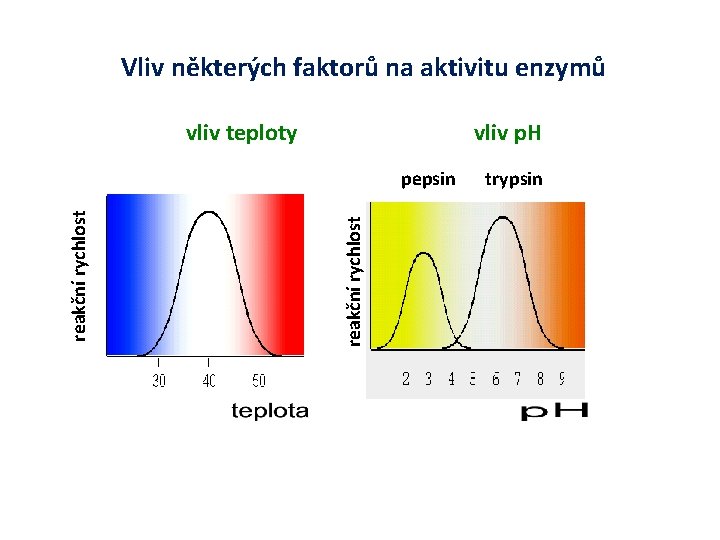
Vliv některých faktorů na aktivitu enzymů vliv teploty vliv p. H reakční rychlost pepsin trypsin

Pokus: Katalasa v bramboru Princip: Jako katalasy označujeme enzymy, které jsou schopny katalyzovat společně s peroxidasami disproporcionaci peroxidu vodíku na vodu a kyslík. Hodnota aktivační energie EA potřebná na rozklad peroxidu vodíku podle druhu použitého katalyzátoru. Rozklad H 202 EA (k. J/mol) bez katalýzy 75, 4 jodid 54, 4 Pt 48, 6 katalasa 23 katalasa

Pokus: Katalasa v bramboru • Pomůcky: brambory, tyčinka nebo kapátko • Chemikálie: 30% a 3% roztok peroxidu vodíku • Postup: Z omyté bramborové hlízy odřízneme dva plátky o síle asi 1 cm. Na řeznou plochu jednoho plátku kápneme 2 -3 kapky 30% peroxidu vodíku a pozorujeme průběh reakce. Na řeznou plochu druhého plátku kápneme ve stejnou dobu stejné množství 3% peroxidu vodíku. • Chemická rovnice: • Pozorování: • Závěr:

SLOŽENÍ A STRUKTURA ENZYMU bílkovinný charakter, většina enzymů (až 70 %) má povahu složených bílkovin tvar globulární část bílkovinou – apoenzym holoenzym nebílkovinou – kofaktor koenzym prostetická skupina pevně vázána na apoenzym kovalentní vazbou, např. hem vázán na apoenzym slabě a snadno se uvolňuje, vystupuje jako 2. substrát (kosubstrát)

STRUKTURA ENZYMU KOFAKTOR APOENZYM • určuje substrátovou specifitu • určuje reakční specifitu, typ reakce, které bude substrát podléhat • má ve své molekule aktivní centrum (hydrogenace, dehydratace atd. ) na které se substrát váže • zaujímá malou část povrchu enzymu, je • váže se také na aktivní centrum tvořeno několika aminokyselinami vazebné místo
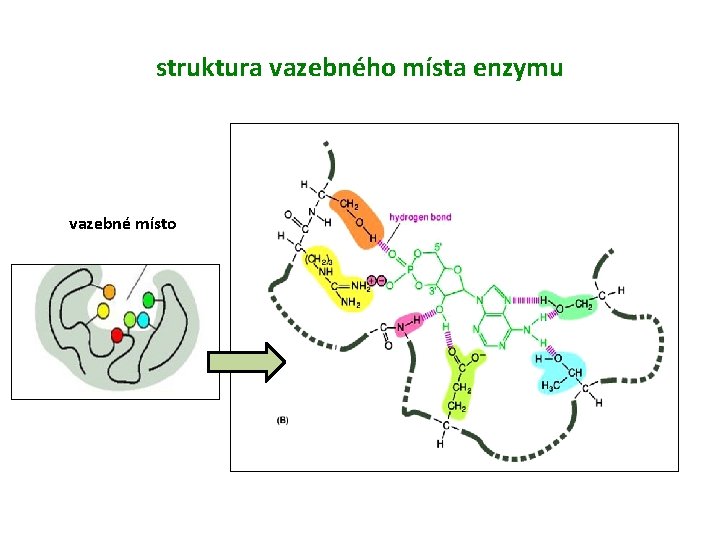
struktura vazebného místa enzymu vazebné místo
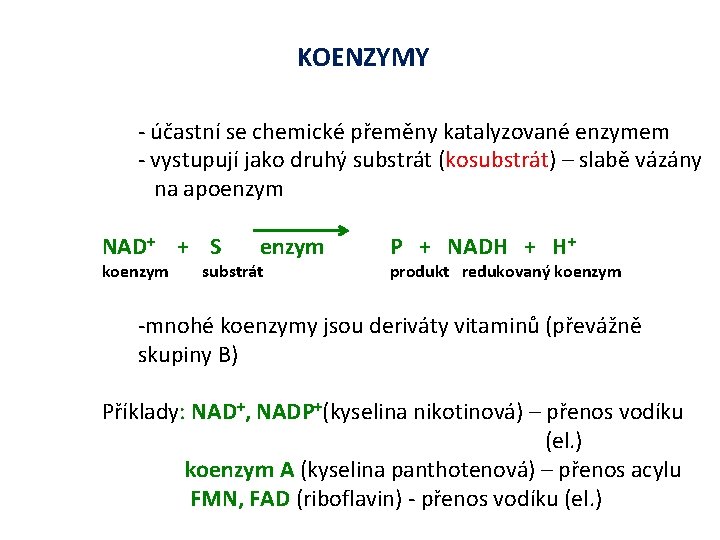
KOENZYMY - účastní se chemické přeměny katalyzované enzymem - vystupují jako druhý substrát (kosubstrát) – slabě vázány na apoenzym NAD+ + S koenzym substrát P + NADH + H+ produkt redukovaný koenzym -mnohé koenzymy jsou deriváty vitaminů (převážně skupiny B) Příklady: NAD+, NADP+(kyselina nikotinová) – přenos vodíku (el. ) koenzym A (kyselina panthotenová) – přenos acylu FMN, FAD (riboflavin) - přenos vodíku (el. )
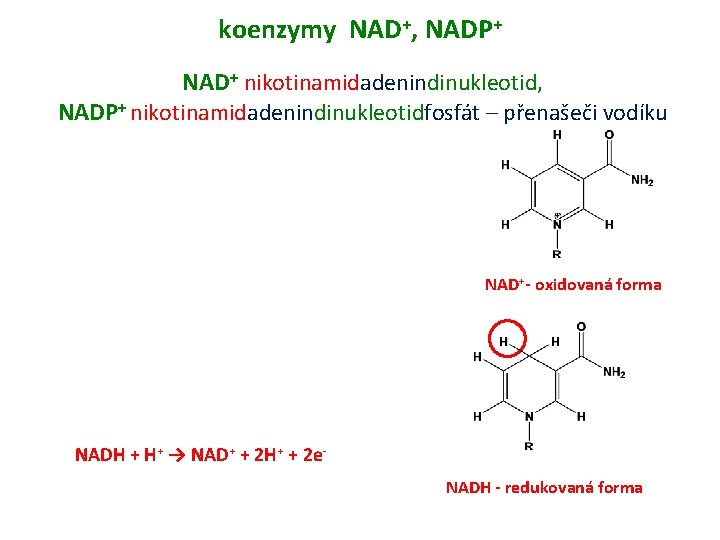
koenzymy NAD+, NADP+ NAD+ nikotinamidadenindinukleotid, NADP+ nikotinamidadenindinukleotidfosfát – přenašeči vodíku NAD+- oxidovaná forma NADH + H+ → NAD+ + 2 H+ + 2 e. NADH - redukovaná forma
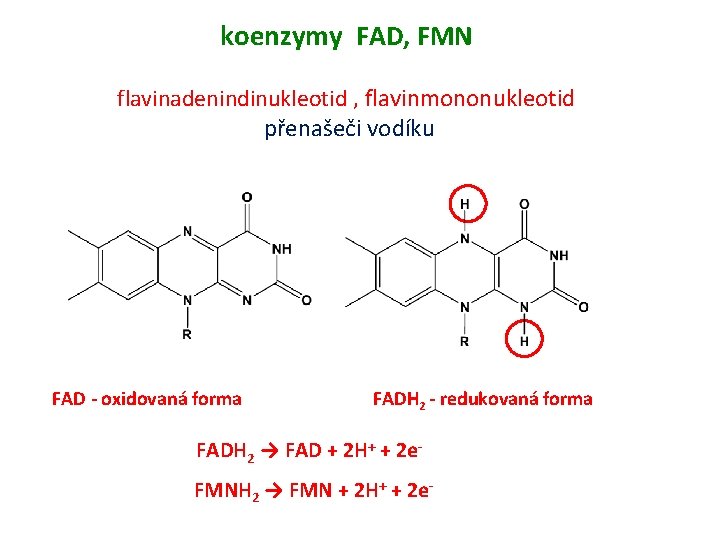
koenzymy FAD, FMN flavinadenindinukleotid , flavinmononukleotid přenašeči vodíku FAD - oxidovaná forma FADH 2 - redukovaná forma FADH 2 → FAD + 2 H+ + 2 e. FMNH 2 → FMN + 2 H+ + 2 e-

koenzym Q ubichinon - přenašeč vodíku cytochromy přenašeči elektronů oxidovaná forma koenzym A přenašeč acylu redukovaná forma

PŮSOBENÍ ENZYMU 1. Teorie zámku a klíče (lock& key, teorie komplementarity) Substrát zapadá svou strukturou přesně do aktivního centra.
Teorie zámku a klíče Enzym
Teorie zámku a klíče Enzym

Teorie zámku a klíče Enzym
Teorie zámku a klíče Enzym

Teorie zámku a klíče Enzym
Teorie zámku a klíče Enzym
Teorie zámku a klíče Enzym

PŮSOBENÍ ENZYMU 2. Teorie indukovaného přizpůsobení (induced fit) Aktivní centrum se svou strukturou přizpůsobí substrátu. ( po otevření stiskněte „go“)
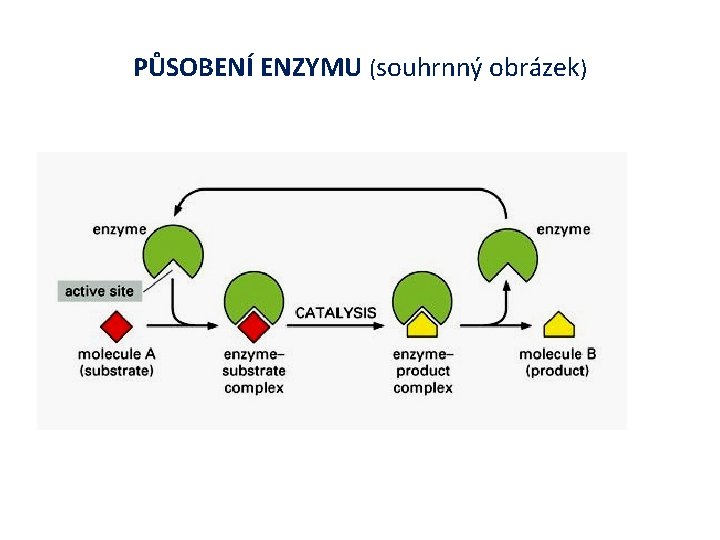
PŮSOBENÍ ENZYMU (souhrnný obrázek)

NÁZVOSLOVÍ ENZYMŮ • nejstarší názvy: koncovka - in (trypsis, pepsin …. ) • postupně: substrát + - asa (amylasa, lipasa, …. ) reakce + - asa (hydrolasa, isomerasa …. ) • systematické názvosloví: substrát + reakce + - asa ( pyruvátdekarboxylasa, laktátdehydrogenasa …. . )
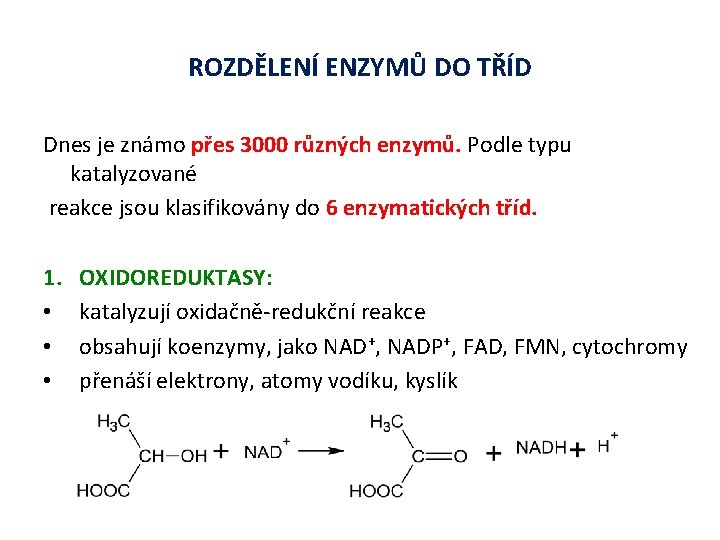
ROZDĚLENÍ ENZYMŮ DO TŘÍD Dnes je známo přes 3000 různých enzymů. Podle typu katalyzované reakce jsou klasifikovány do 6 enzymatických tříd. 1. • • • OXIDOREDUKTASY: katalyzují oxidačně-redukční reakce obsahují koenzymy, jako NAD+, NADP+, FAD, FMN, cytochromy přenáší elektrony, atomy vodíku, kyslík
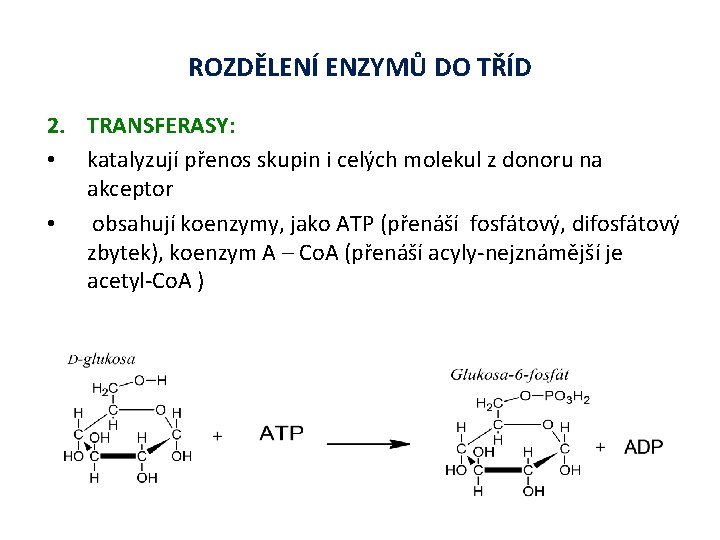
ROZDĚLENÍ ENZYMŮ DO TŘÍD 2. TRANSFERASY: • katalyzují přenos skupin i celých molekul z donoru na akceptor • obsahují koenzymy, jako ATP (přenáší fosfátový, difosfátový zbytek), koenzym A – Co. A (přenáší acyly-nejznámější je acetyl-Co. A )
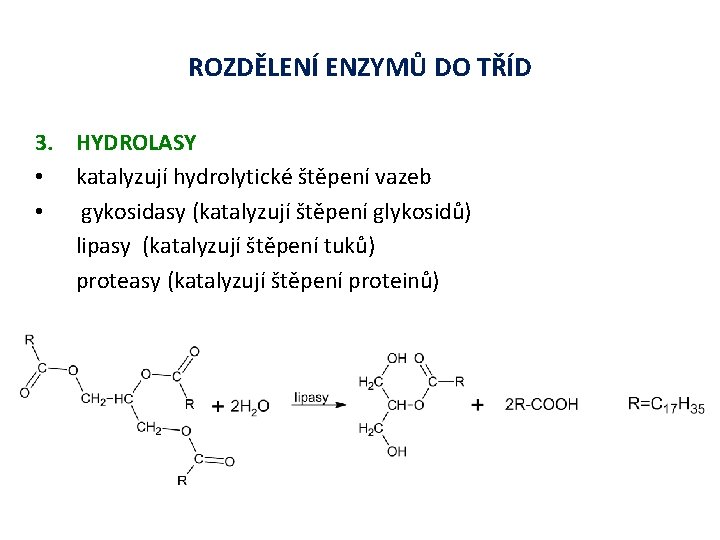
ROZDĚLENÍ ENZYMŮ DO TŘÍD 3. HYDROLASY • katalyzují hydrolytické štěpení vazeb • gykosidasy (katalyzují štěpení glykosidů) lipasy (katalyzují štěpení tuků) proteasy (katalyzují štěpení proteinů)
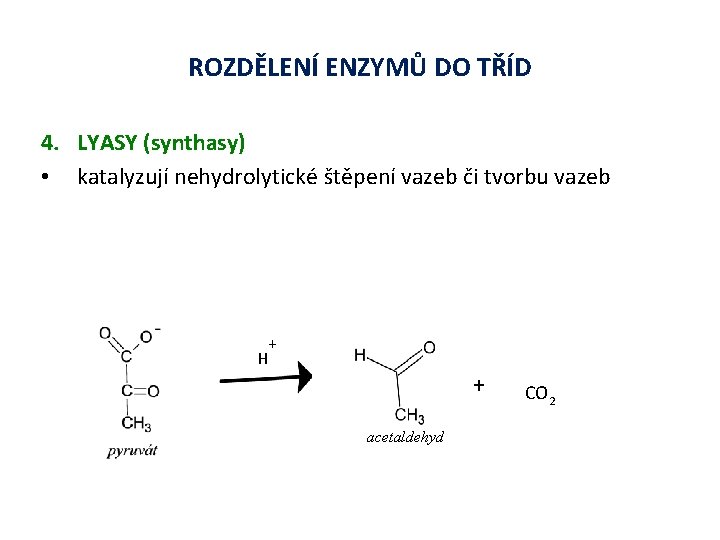
ROZDĚLENÍ ENZYMŮ DO TŘÍD 4. LYASY (synthasy) • katalyzují nehydrolytické štěpení vazeb či tvorbu vazeb H + + acetaldehyd CO 2

ROZDĚLENÍ ENZYMŮ DO TŘÍD 5. ISOMERASY • katalyzují izomerační reakce (přesouvají atomy nebo celé skupiny z jednoho uhlíku na jiný v rámci jedné molekuly)

ROZDĚLENÍ ENZYMŮ DO TŘÍD 6. LYGASY (synthetasy) • katalyzují syntézu molekul spojené se štěpením ATP

INHIBICE ENZYMŮ (snižování aktivity enzymů) 1. Kompetitivní inhibice (soutěživá) – inhibitor soutěží se substrátem o vazbu v aktivním místě • • inhibitor je strukturně podobný substrátu váže se do aktivního centra, ale není enzymem přeměňován zvýšením koncentrace substrátu lze inhibici potlačit (inhibitor vytěsnit) inhibice je vratná (reverzibilní)

INHIBICE ENZYMŮ (snižování aktivity enzymů) 2. Nekompetitivní inhibice • • • inhibitor se váže mimo aktivní centrum enzymu dochází ke změně aktivního centra inhibici nelze potlačit zvýšením koncentrace substrátu dochází ke snížení aktuální koncentrace aktivního enzymu vratná, pouze pokud se inhibitor neváže na enzym kovalentně animace inhibice ( po otevření klikněte „animation“ a poté „step-though“, vyberte animaci, „play“)

REGULACE ENZYMOVÉ AKTIVITY (regulační enzymy) 1. Allosterické enzymy obsahují kromě aktivního centra ještě allosterické místo, kam se váže modulátor a ovlivní aktivitu enzymu. Alosterickými modulátory jsou často produkty metabolismu (inhibice zpětnou vazbou) 2. Proenzymy – zymogeny (neaktivní formy enzymů) v době potřeby přecházejí účinkem jiných enzymů na aktivní formy enzymů pepsinogen na pepsin trypsinogen na trypsin animace inhibice ( po otevření klikněte „animation“ a poté „step-through“, „play“, „continue“)
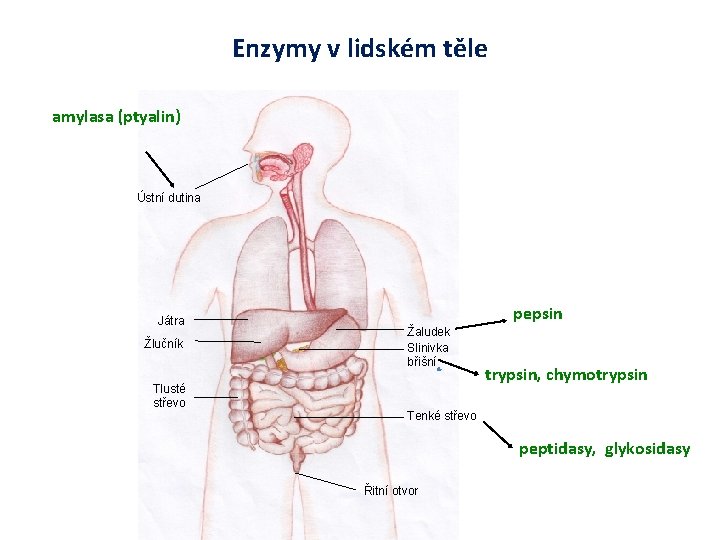
Enzymy v lidském těle amylasa (ptyalin) Ústní dutina Játra Žlučník Tlusté střevo pepsin Žaludek Slinivka břišní trypsin, chymotrypsin Tenké střevo peptidasy, glykosidasy Řitní otvor
- Slides: 36