Enzymer Biologiske katalysatorer Definisjon av katalysator En katalysator

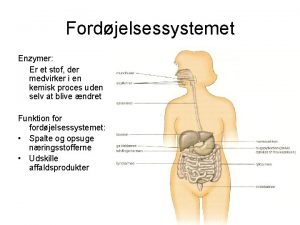
Enzymer Biologiske katalysatorer

Definisjon av katalysator • En katalysator øker reaksjonshastigheten • En katalysator påvirker ikke reaksjonslikevekten • En katalysator forbrukes ikke i reaksjonen

Enzymer Biologiske katalysatorer: • Høyt spesialiserte molekyler: I hovedsak proteiner, men kan være RNA • Kraftige katalysatorer, ofte sterkere enn uorganiske katalysatorer – Urease øker reaksjonshastigheten 1014 ganger • Svært spesifikke, skiller mellom stereoisomerer • Aktive i vandig miljø • Aktive under kjemisk milde forhold: lav temperatur, neutral p. H

Enzymer vs. kjemiske katalysatorer • Enzymer øker reaksjonshastigheten mye mer: 106 -1012 ganger mere enn kjemiske katalysatorer • Enzymer fungerer under milde betingelser: lave temperaturer, atmosferisk trykk og neutral p. H • Enzymer er mye mere spesifikke, både med hensyn til substrat og produkt. Ingen biprodukter. • Enzymaktivitet reguleres av cellens behov

Kofaktorer • Noen enzymer er aktive som rene proteiner • Andre trenger kofaktorer, hjelpemolekyler/ioner • Kofaktorene deltar i den katalytiske prosessen, ofte som midlertidige bærere av funksjonelle grupper • Kofaktorer deles i: – Koenzymer, periodevis assosiert til enzymproteinet, ikke kovalent. Regenereres av andre enzymer – Prostetiske grupper, alltid bundet til proteinet, ofte kovalent. Regenereres i løpet av den katalytiske prosessen • Holoenzym = enzymprotein + kofaktor • Apoenzym = enzymprotein uten kofaktor


Uorganiske kofaktorer • Essentielle sporstoffer • Beslektede sporstoffer kan være giftige: – Cd 2+ og Hg 2+ kan erstatte Zn 2+ i det aktive setet til visse enzymer, men ikke utføre Zn 2+’s funksjon. – Dermed inaktiveres enzymet. – Eksempel: RNA polymerase. Tap av funksjon er farlig

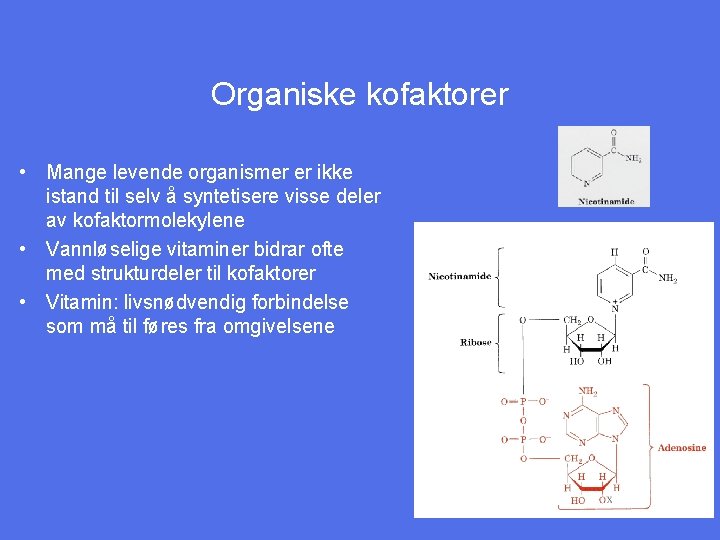
Organiske kofaktorer • Mange levende organismer er ikke istand til selv å syntetisere visse deler av kofaktormolekylene • Vannløselige vitaminer bidrar ofte med strukturdeler til kofaktorer • Vitamin: livsnødvendig forbindelse som må til føres fra omgivelsene

Konjugerte enzymer Selvom et protein ikke trenger kofaktorer kan dets aktivitet være avhengig av visse modifikasjoner: – Glykosylering – Fosforylering – Sulfatering – Farnesylering – Lipid påkopling Disse modifiserende forbindelser deltar ikke i den katalytiske prosessen, men regulerer aktivitet, lokalisering i cellen, nedbrytning av enzymet

Nomenklatur • Trivialnavn på enzymer er ofte vilkårlige og tvetydige, de forteller lite om hva enzymet gjør • Systematiske navn er innført • Enzymer gis navn og klassifiseres ifølge internasjonale regler • Enzymets navn skal fortelle noe om hva pågjeldende enzym gjør • Vanlig å benytte navnet på enzymets substrat, produkt eller den reaksjon enzymet katalyserer og sette ”ase” på slutten av ordet • Det internasjonale enzymklassifiseringssystem deler enzymene i 6 hovedkategorier • Hver hovedkategori har undergrupper, som igjen selv har undergrupper slik at ethvert enzym blir entydig beskrevet


Systematiske nummer og navn La oss se på et eksempel: • Enzymet med nummer E. C. 2. 7. 1. 1. (E. C. = enzyme classification) • Første tall ” 2” forteller ifølge tabell 8 -3 at enzymet er en transferase • Andre tall ” 3” forteller at det tilhører gruppen fosfotransferaser, dvs det overfører en fosfatgruppe fra et molekyle til et annet • Tredje tall ” 1” forteller at fosfatgruppen overføres til en hydroksylgruppe • Fjerde tall ” 1” forteller at det er D-glukose som denne fosfatgruppen overføres til Enzymets systematiske navn er: ATP: glukose-fosfotransferase ATP + D-glukose ADP + D-glukose-6 -fosfat Mange tungvinte systematiske navne byttes ofte ut med trivialnavnet som her er heksokinase

Hvordan fungerer enzymene? • Enzymer er biologiske katalysatorer, dvs de øker reaksjonshastigheten, uten selv å bli forbrukt eller påvirke likevekten mellom substrat og produkt • Cellens miljø er ikke gunstig med tanke på at reaksjoner skal skje spontant • Vandig miljø, neutral p. H og moderat temperatur • Cellen er i tillegg avhengig av full kontrol over alle kjemiske prosesser: – Hvilke molekyler deltar produkt A – Hvilken retning reaksjonene tar: substrat produkt B – Reaksjonenes hastighet produkt C

Substratspesifisitet • Alle enzymer har et aktivt sete – Substratbinding – Katalyse • Mange har bindingssete for en eller flere kofaktorer • Mange har bindingssete for andre regulatorer • Aktivt sete er ofte en lomme eller et hulrom i enzymet • Her har enzym og substrat svært tett kontakt • Krever komplementaritet mellom enzym og substrat i overgangstilstand
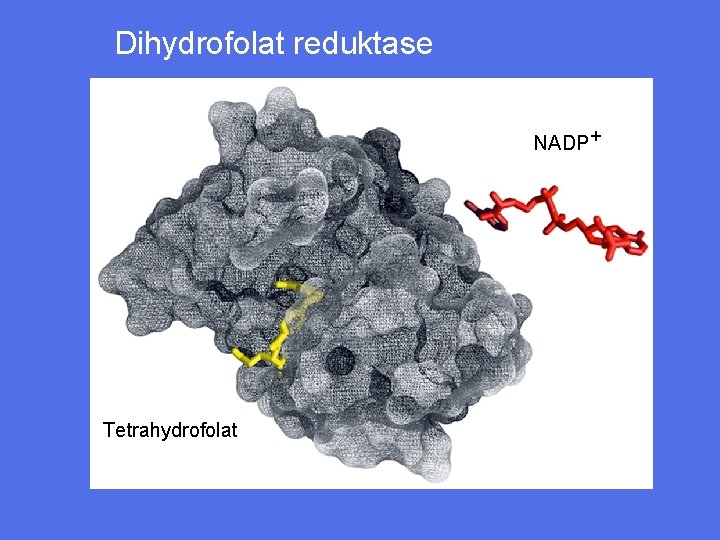
Dihydrofolat reduktase NADP+ Tetrahydrofolat


Binding av substrat til heksokinase viser et tilfelle av indusert tilpasning - ”induced fit” Proteinet lukker seg omkring substratet

Enzym-substratkomplekset • Enzymets aktive sete ”leser” overflatekonturen på substratet. • Dvs. rett plassering av - hydrogenbindingspartnere - positive og negative ladninger - hydrofobe områder • Aktivt sete er komplementært med substratet i overgangstilstand • Binding av substratet tvinger det inn i en konformasjon som er gunstig for den katalytiske prosessen

Reaksjonshastighet, reaksjonslikevekt • Reaksjonshastighet = den hastighet hvormed produkt dannes • Reaksjonslikevekt = mengden av substrat og produkt ved likevekt S P
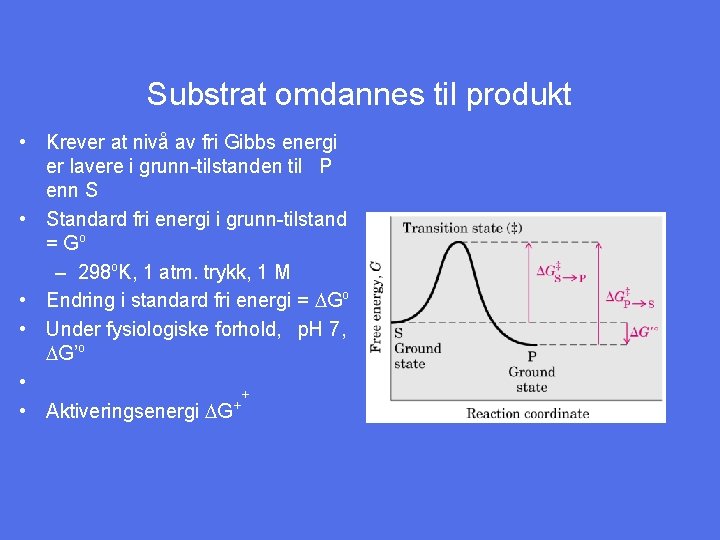
Substrat omdannes til produkt • Krever at nivå av fri Gibbs energi er lavere i grunn-tilstanden til P enn S • Standard fri energi i grunn-tilstand = Go – 298 o. K, 1 atm. trykk, 1 M • Endring i standard fri energi = DGo • Under fysiologiske forhold, p. H 7, DG’o • + + • Aktiveringsenergi DG
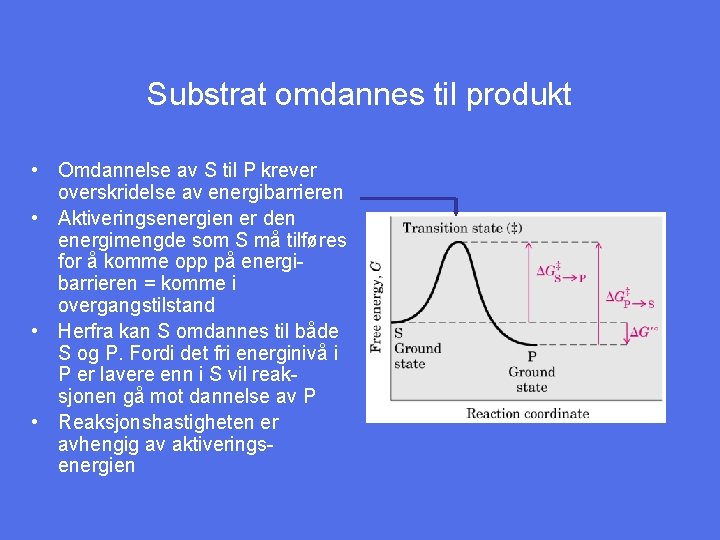
Substrat omdannes til produkt • Omdannelse av S til P krever overskridelse av energibarrieren • Aktiveringsenergien er den energimengde som S må tilføres for å komme opp på energibarrieren = komme i overgangstilstand • Herfra kan S omdannes til både S og P. Fordi det fri energinivå i P er lavere enn i S vil reaksjonen gå mot dannelse av P • Reaksjonshastigheten er avhengig av aktiveringsenergien
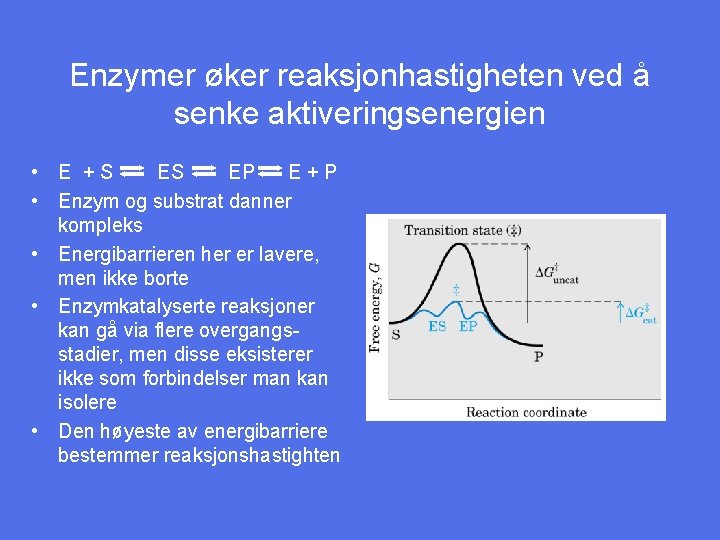
Enzymer øker reaksjonhastigheten ved å senke aktiveringsenergien • E +S ES EP E+P • Enzym og substrat danner kompleks • Energibarrieren her er lavere, men ikke borte • Enzymkatalyserte reaksjoner kan gå via flere overgangsstadier, men disse eksisterer ikke som forbindelser man kan isolere • Den høyeste av energibarriere bestemmer reaksjonshastighten
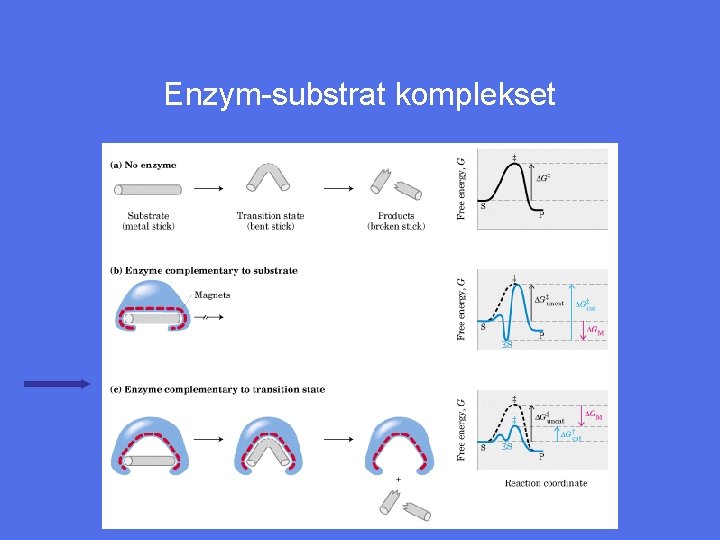
Enzym-substrat komplekset

Hvordan senkes energibarrieren? • Enzymer er store molekyler av flere årsaker • Binding av substrat til enzym fører til frigivelse av en betydelig energimengde = bindingsenergi, pga. dannelse av mange ikkekovalente bindinger – Ionebindinger – Hydrogenbindinger – Hydrofobe interaksjoner – Van der Waalske interaksjoner • Bindingsenergien reduserer energibarrieren og er i mange tilfelle tilstrekkelig til også å gjennomføre reaksjonen • De mange ikke-kovalente bindinger sikrer også spesifisiteten
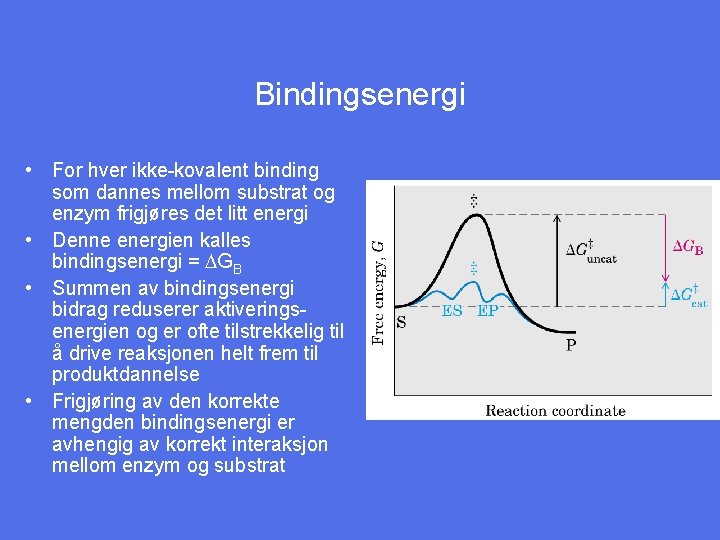
Bindingsenergi • For hver ikke-kovalent binding som dannes mellom substrat og enzym frigjøres det litt energi • Denne energien kalles bindingsenergi = DGB • Summen av bindingsenergi bidrag reduserer aktiveringsenergien og er ofte tilstrekkelig til å drive reaksjonen helt frem til produktdannelse • Frigjøring av den korrekte mengden bindingsenergi er avhengig av korrekt interaksjon mellom enzym og substrat
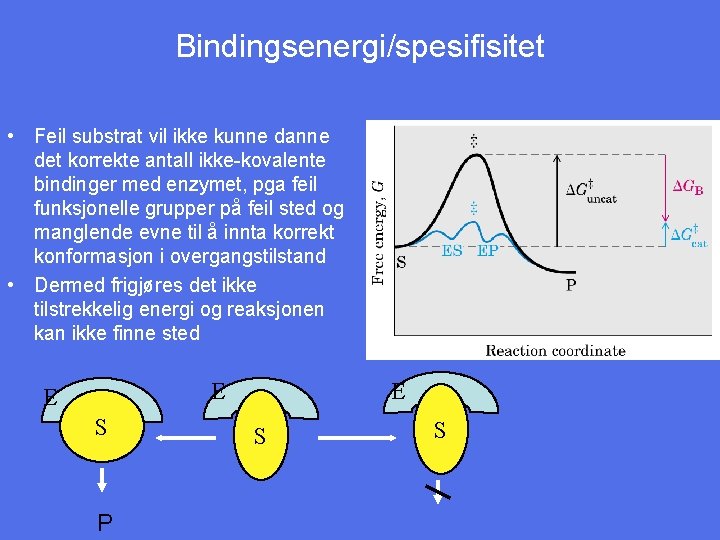
Bindingsenergi/spesifisitet • Feil substrat vil ikke kunne danne det korrekte antall ikke-kovalente bindinger med enzymet, pga feil funksjonelle grupper på feil sted og manglende evne til å innta korrekt konformasjon i overgangstilstand • Dermed frigjøres det ikke tilstrekkelig energi og reaksjonen kan ikke finne sted E E S P E E S S

Likevektskonstant er avhengig av forskjell i fri Gibbs energi i grunntilstand • Disse er innbyrdes forbundet • Reaksjonen S P • Likevektskonstanten – K’eq = P / S – DG’o = -RTln. K’eq – Når K’eq så DG’o

Reaksjonshastighet er en funksjon av aktiveringsenergi • Reaksjonen S P • Reaksjonshastighet i en første ordens reaksjon er V = k S • Reaksjonen S +S P • Reaksjonshastigheten i en annen ordens reaksjon er V = k S 1 S 2 • Hastighetskonstanten k er en funksjon av aktiveringsenergien

Katalytiske mekanismer Virkningsmekanismen for alle kjente enzymer kan grovt deles i flg. typer: ü Nærhetsmekanisme ü Generell syre-base mekanisme ü Elektrostatiske effekter ü Kovalent katalysemekanisme ü Strukturell fleksibilitet Disse mekanismer gjør det mulig for enzymer å utføre sin katalytiske aktivitet ved neutral p. H

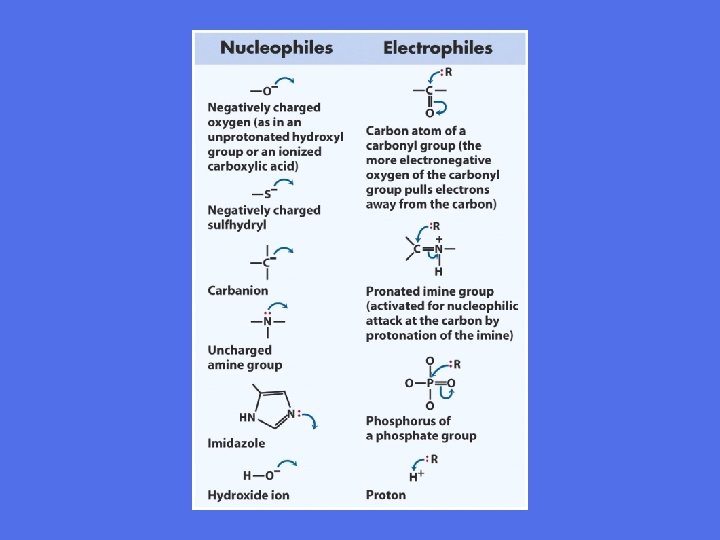
Elektrofil/nukleofil gruppe Funksjonelle grupper utfører jobben: • En funksjonell gruppe sies å være elektrofil hvis den har et underskudd av elektroner • En funksjonell gruppe sies å være nukleofil hvis den har et overskudd av elektroner Elektrofile grupper reagerer med nukleofile grupper Hverken nukleofile eller elektrofile grupper kan reagere med sin egen type funksjonell gruppe



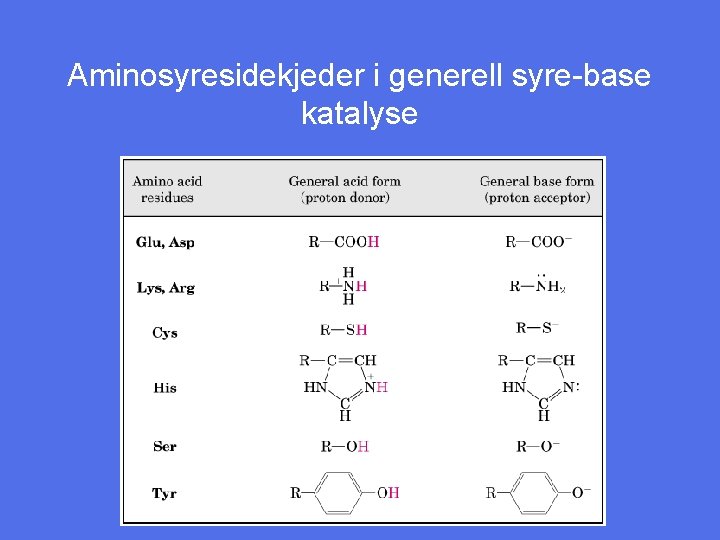
Aminosyresidekjeder i generell syre-base katalyse

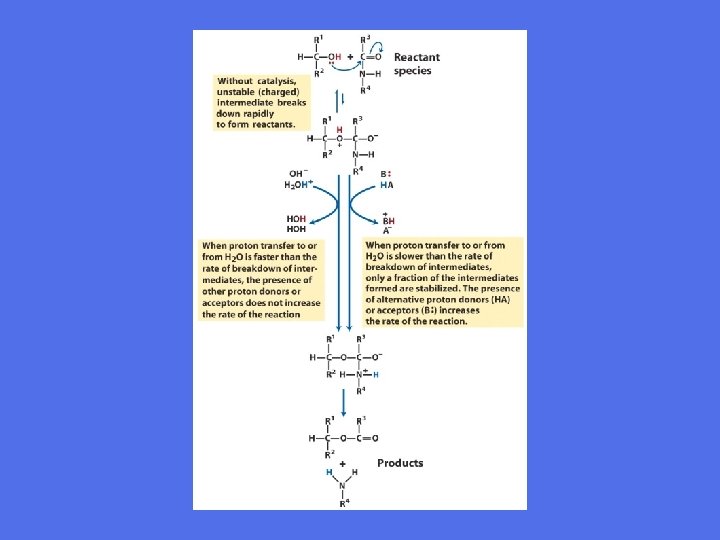
Generell syre-base katalyse • Under katalysen kan det dannes et ladet intermediat som er ustabilt • En proton kan overføres eller fjernes fra det for å hindre at det går tilbake til substratformen • Stabilisering muliggjør fortsettelse av prosessen mot produktdannelse • I enzymers katalytiske sete vil aminosyresidekjeder fungere som protondonorer såvel som protonakseptorer

Kovalent katalyse • Her dannes kortvarig kovalent binding mellom enzym og substrat • Eks. hydrolyse av bindingen mellom A og B • H 2 O • A B + X: A X+B A + X: + B • Endrer reaksjonsveien til ny med lavere aktiveringsenergi • Aminosyresidekjeder og koenzymer kan utføre nukleofile angrep på substrater og danne kovalente bindinger
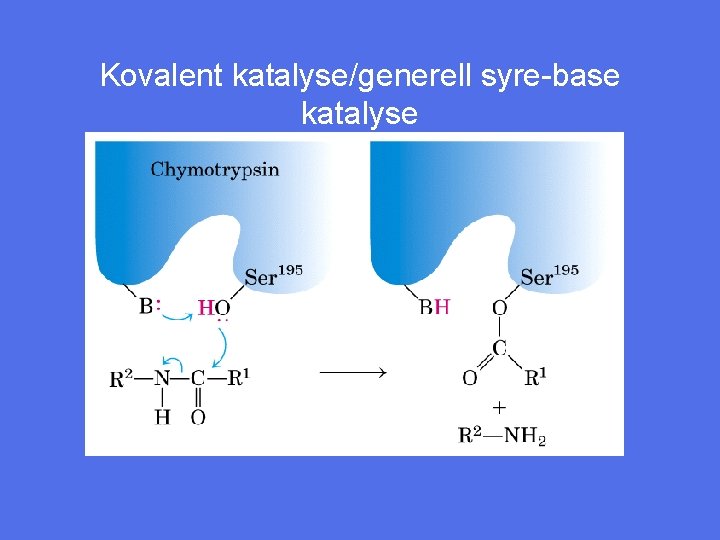
Kovalent katalyse/generell syre-base katalyse

Metallionkatalyse • Metallioner inngår i 1/3 av kjente enzymer • Metallion kan være kovalent bundet til enzymet eller løst assosiert • Kan danne ionebindinger til substratet => – korrekt orientering – stabilisere ladninger i overgangstilstanden • Ta imot eller avgi elektroner i redoksreaksjoner
- Slides: 41