ENZIMOLOGIA 1 ENZIMAS CONCEITO Protenas funcionando como catalisadores



![CINÉTICA ENZIMÁTICA E + S [ES] • CONCENTRAÇÃO da ENZIMA v P + E CINÉTICA ENZIMÁTICA E + S [ES] • CONCENTRAÇÃO da ENZIMA v P + E](https://slidetodoc.com/presentation_image_h/2c6118281fc20095fd8135fe667dda6a/image-13.jpg)


![INIBIÇÃO ENZIMÁTICA REVERSÍVEL O- O COMPETITIVA O CH 2 C C - [S] O INIBIÇÃO ENZIMÁTICA REVERSÍVEL O- O COMPETITIVA O CH 2 C C - [S] O](https://slidetodoc.com/presentation_image_h/2c6118281fc20095fd8135fe667dda6a/image-20.jpg)


- Slides: 32

ENZIMOLOGIA 1. ENZIMAS • CONCEITO • “Proteínas” funcionando como catalisadores de reações bioquímicas PODER CATALITICO: “Tornam realidade reações termodinamicamente possíveis, velocidade das reações” acelerando a C 12 H 22 O 11 + 12 O 2 12 CO 2 + 11 H 2 O GO’= -1360 kcal/mol CO 2 + H 2 O H 2 CO 3 (1: 105: seg) • COENZIMA – Molécula Org. : NAD+; FAD (Grupa/o Prostético) COFATOR: Íon (Cl-; Fe++; Mg++)

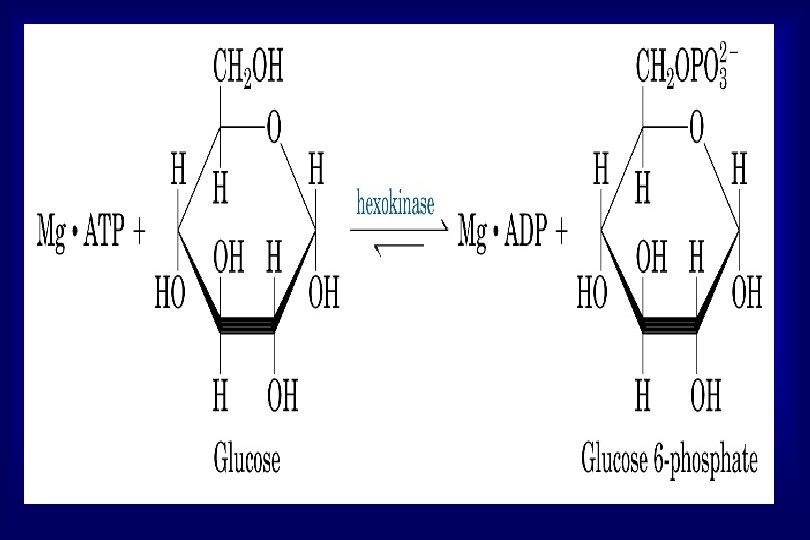
CLASSIFICAÇÃO 1. OXIDOREDUTASES: Transferência de elétrons 2. TRANSFERASES: Transferência de grupos entre moléculas 3. HIDROLASES: Reações de hidrolise (H 2 O) 4. LIASES: Adição de grupos a duplas ligações 5. ISOMERASES: Transferência de grupos dentro da molecula 6. LIGASES: Formação de ligações químicas (ATP) D-Glicose + ATP Glicose-6 P + ADP ATP: Glicose. Fosfo. Transferase (Hexoquinase – HK) D-Glicose + ATP (SUBSTRATOS); Glicose-6 P + ADP (PRODUTOS)


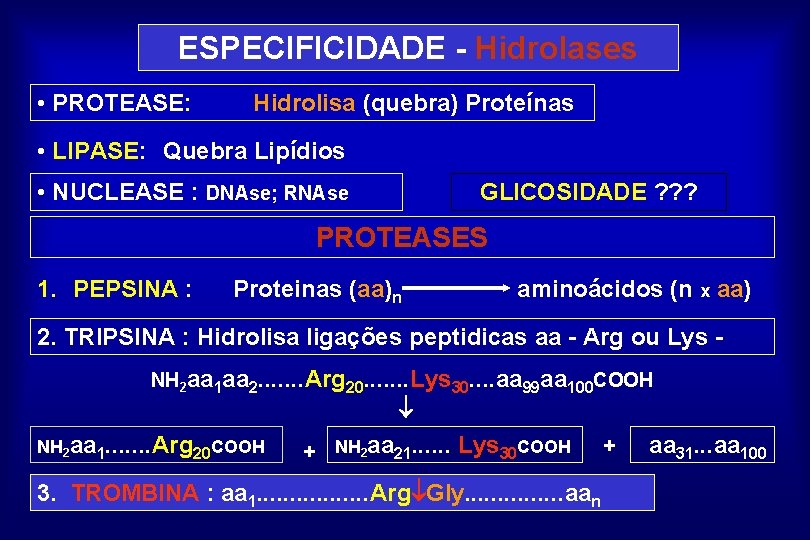
ESPECIFICIDADE - Hidrolases • PROTEASE: Hidrolisa (quebra) Proteínas • LIPASE: Quebra Lipídios • NUCLEASE : DNAse; RNAse GLICOSIDADE ? ? ? PROTEASES 1. PEPSINA : Proteinas (aa)n aminoácidos (n x aa) 2. TRIPSINA : Hidrolisa ligações peptidicas aa - Arg ou Lys NH 2 aa 1 aa 2. . . . Arg 20. . . . Lys 30. . aa 99 aa 100 COOH NH 2 aa 1. . . . Arg 20 COOH + NH 2 aa 21. . . Lys 30 COOH 3. TROMBINA : aa 1. . . . Arg Gly. . . . aan + aa 31. . . aa 100

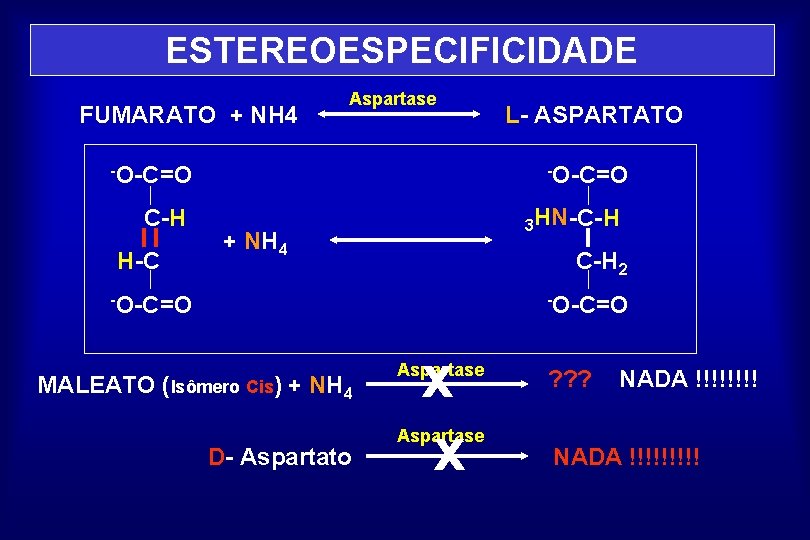
ESTEREOESPECIFICIDADE FUMARATO + NH 4 Aspartase -O-C=O C-H H-C L- ASPARTATO -O-C=O 3 HN-C-H + NH 4 C-H 2 -O-C=O MALEATO (Isômero Cis) + NH 4 D- Aspartato x x Aspartase ? ? ? NADA !!!!!!!!!

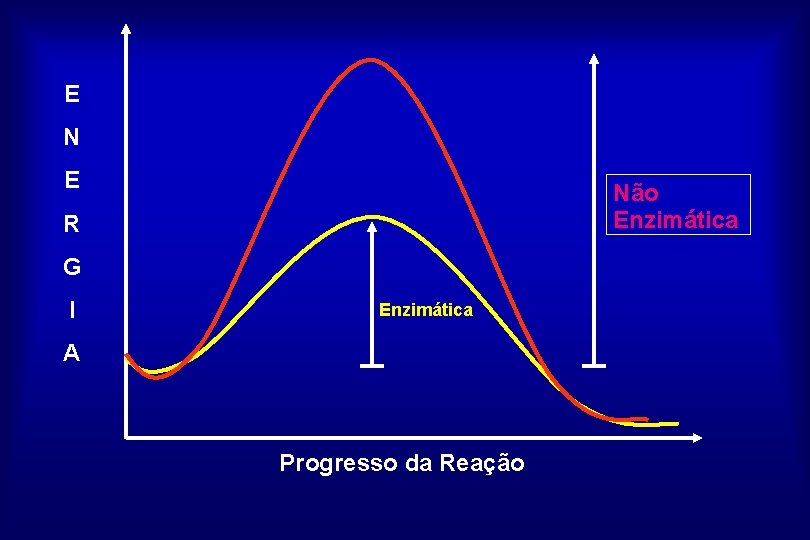
CATALISADORES BIOLÓGICOS A + B P “Moléculas para reagirem necessitam serem elevadas a um determinado nível de energia, denominado ENERGIA de ATIVAÇÃO” • CALOR • CATALISADOR Aumento de Energia Cinética Direcionando os Choques

E N E Não Enzimática R G I Enzimática A Progresso da Reação

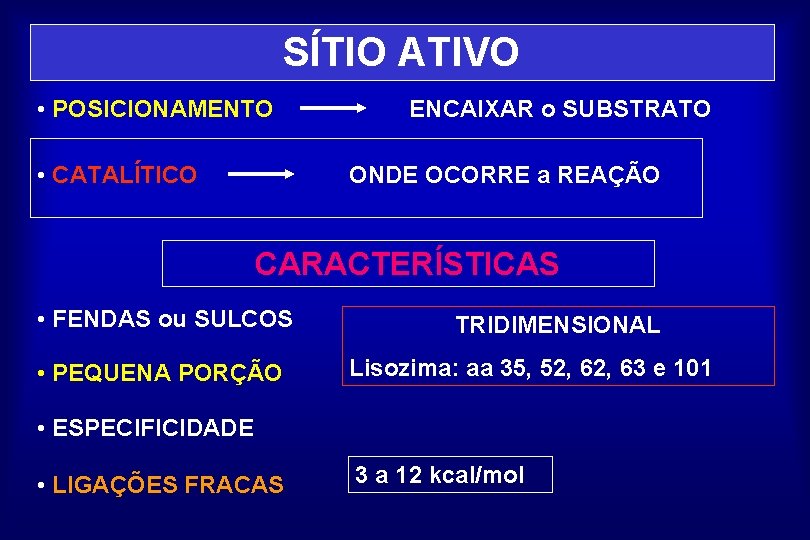
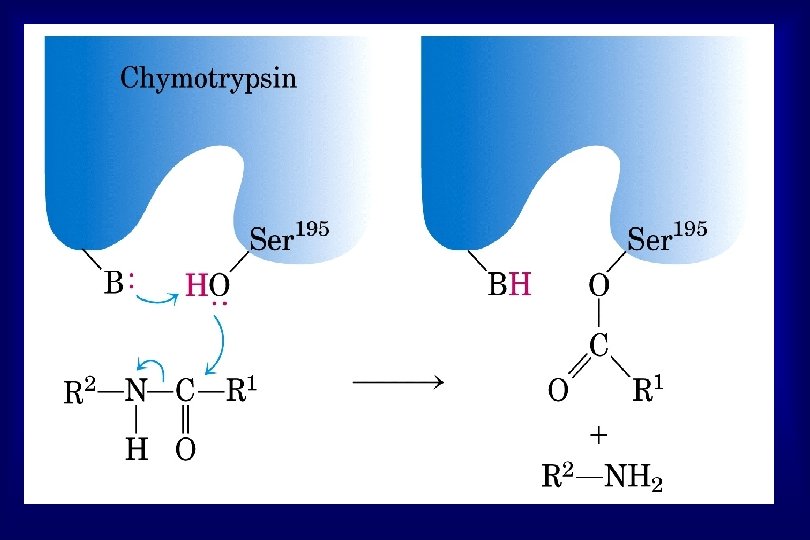
SÍTIO ATIVO • POSICIONAMENTO • CATALÍTICO ENCAIXAR o SUBSTRATO ONDE OCORRE a REAÇÃO CARACTERÍSTICAS • FENDAS ou SULCOS • PEQUENA PORÇÃO TRIDIMENSIONAL Lisozima: aa 35, 52, 63 e 101 • ESPECIFICIDADE • LIGAÇÕES FRACAS 3 a 12 kcal/mol

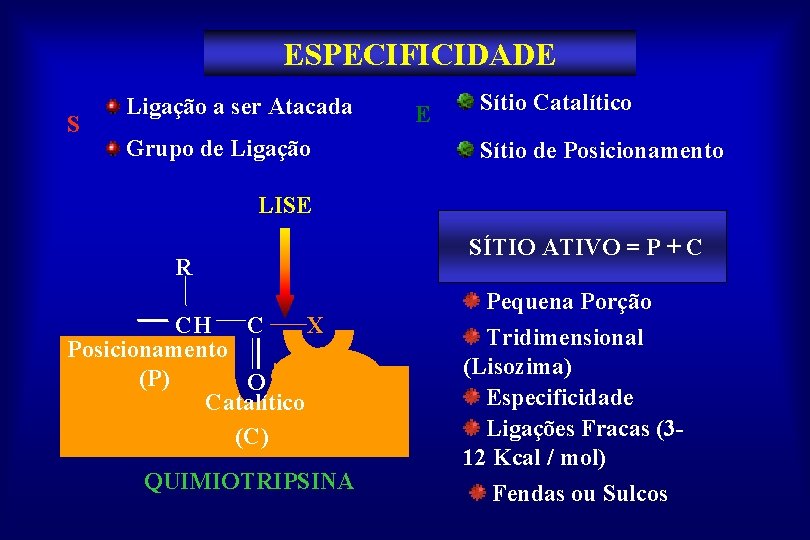
ESPECIFICIDADE S Ligação a ser Atacada Grupo de Ligação E Sítio Catalítico Sítio de Posicionamento LISE R CH C X Posicionamento (P) O Catalítico (C) QUIMIOTRIPSINA SÍTIO ATIVO = P + C Pequena Porção Tridimensional (Lisozima) Especificidade Ligações Fracas (312 Kcal / mol) Fendas ou Sulcos

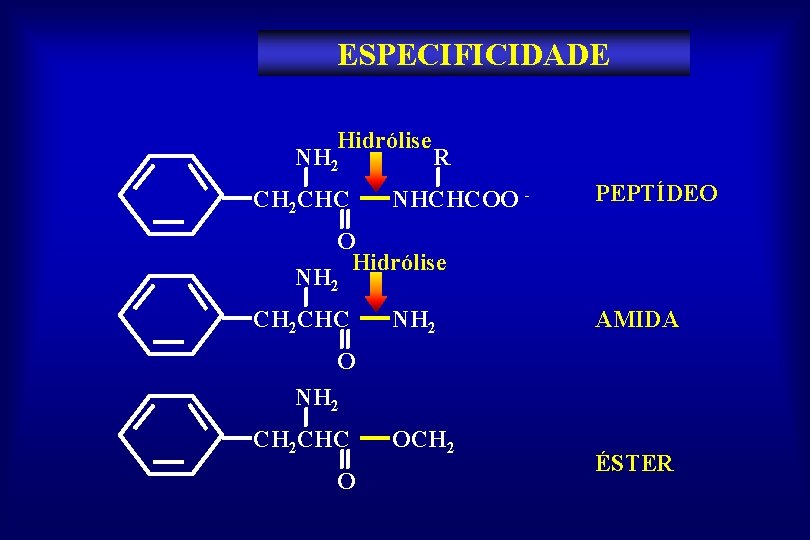
ESPECIFICIDADE Hidrólise NH 2 CH 2 CHC R NHCHCOO - PEPTÍDEO O Hidrólise NH 2 CH 2 CHC NH 2 AMIDA O NH 2 CH 2 CHC O OCH 2 ÉSTER


![CINÉTICA ENZIMÁTICA E S ES CONCENTRAÇÃO da ENZIMA v P E CINÉTICA ENZIMÁTICA E + S [ES] • CONCENTRAÇÃO da ENZIMA v P + E](https://slidetodoc.com/presentation_image_h/2c6118281fc20095fd8135fe667dda6a/image-13.jpg)
CINÉTICA ENZIMÁTICA E + S [ES] • CONCENTRAÇÃO da ENZIMA v P + E • . . . Do SUBSTRATO Vmax [S] VMAX v = Zero Km + [S] Mista Km 1 a Ordem Km [S] Afinidade ES


EFEITO CHAVE-FECHADURA?


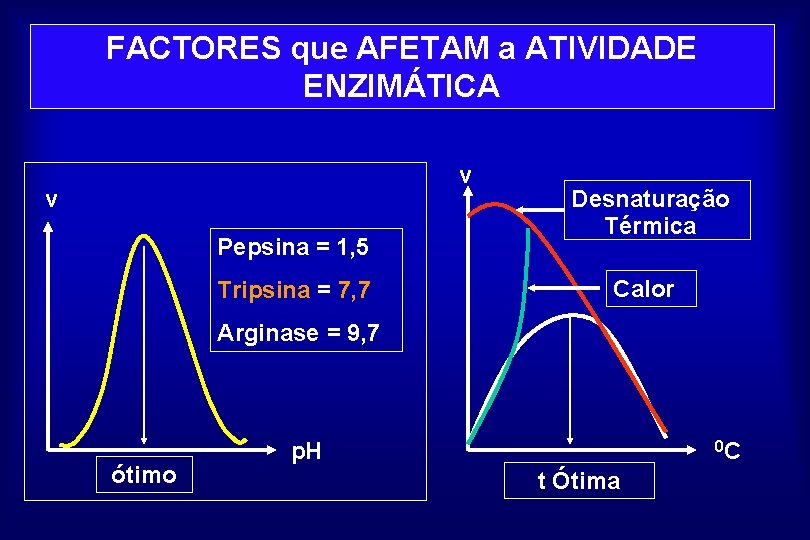
FACTORES que AFETAM a ATIVIDADE ENZIMÁTICA v v Pepsina = 1, 5 Tripsina = 7, 7 Desnaturação Térmica Calor Arginase = 9, 7 ótimo p. H 0 C t Ótima

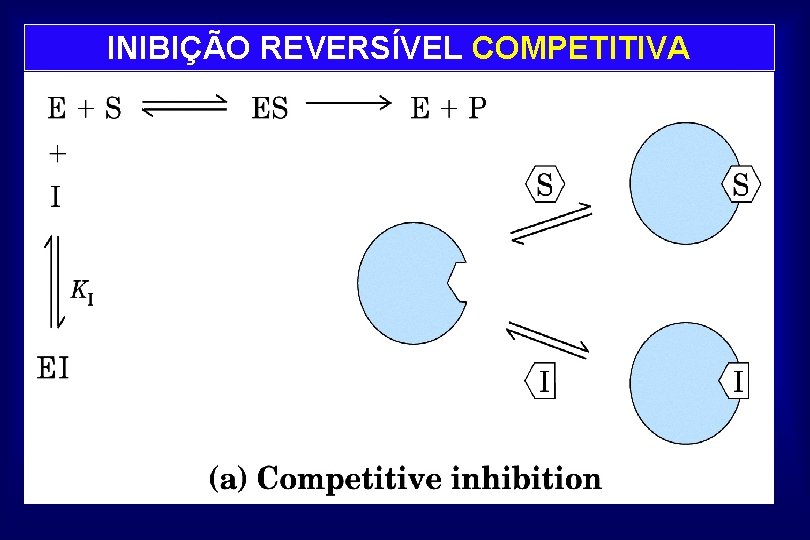
INIBIÇÃO REVERSÍVEL COMPETITIVA

INIBIÇÃO ENZIMÁTICA REVERSÍVEL COMPETITIVA Inibição é revertida pelo aumento de concentração do {S} COMPETIÇÃO PELO SÍTIO ATIVO
![INIBIÇÃO ENZIMÁTICA REVERSÍVEL O O COMPETITIVA O CH 2 C C S O INIBIÇÃO ENZIMÁTICA REVERSÍVEL O- O COMPETITIVA O CH 2 C C - [S] O](https://slidetodoc.com/presentation_image_h/2c6118281fc20095fd8135fe667dda6a/image-20.jpg)
INIBIÇÃO ENZIMÁTICA REVERSÍVEL O- O COMPETITIVA O CH 2 C C - [S] O O- O- O [I] O C SDH CH FADH 2 2 H+ FAD CH C O- O

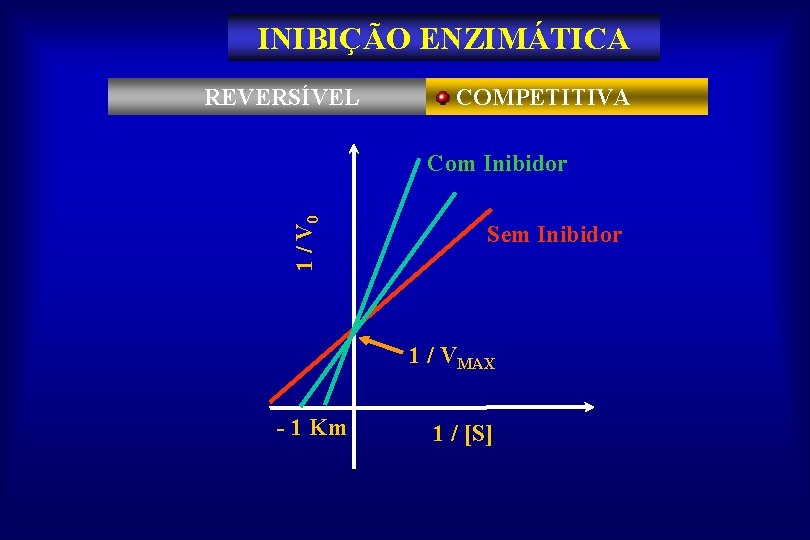
INIBIÇÃO ENZIMÁTICA REVERSÍVEL COMPETITIVA 1 / V 0 Com Inibidor Sem Inibidor 1 / VMAX - 1 Km 1 / [S]

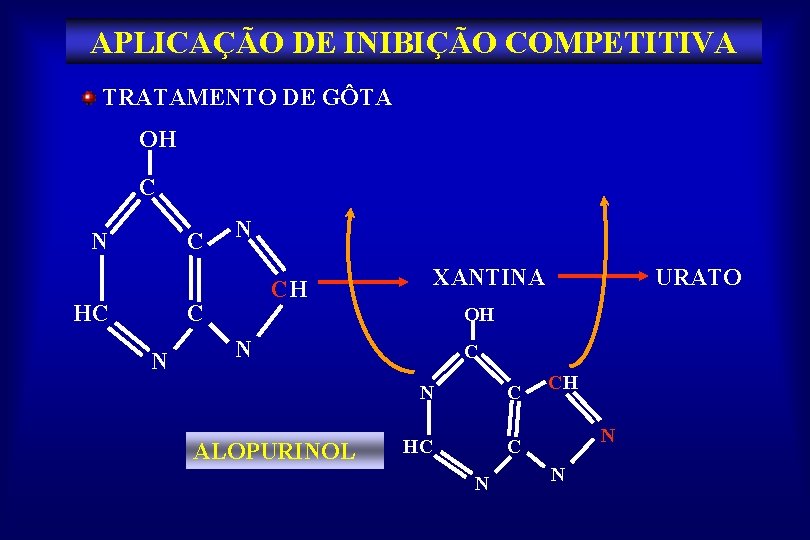
APLICAÇÃO DE INIBIÇÃO COMPETITIVA TRATAMENTO DE GÔTA OH C N C HC N XANTINA CH URATO OH N ALOPURINOL C N C HC C N CH N N

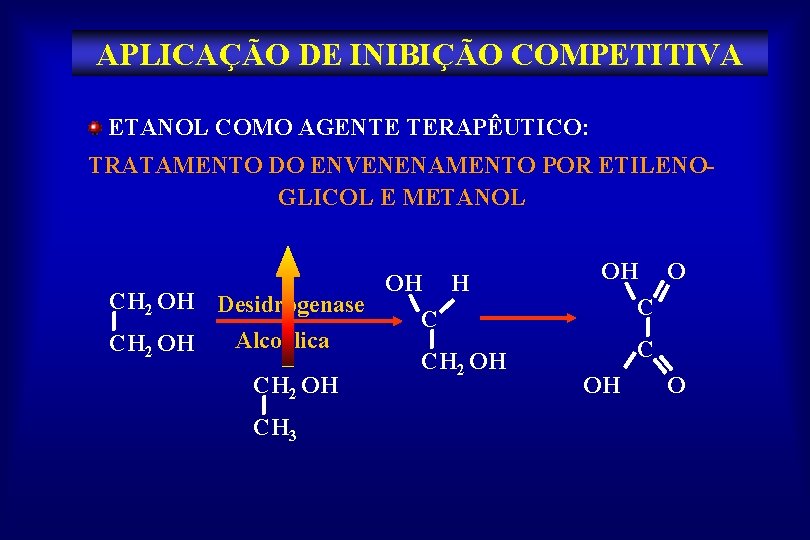
APLICAÇÃO DE INIBIÇÃO COMPETITIVA ETANOL COMO AGENTE TERAPÊUTICO: TRATAMENTO DO ENVENENAMENTO POR ETILENOGLICOL E METANOL CH 2 OH Desidrogenase Alcoólica CH 2 OH CH 3 H OH O C CH 2 OH C OH O

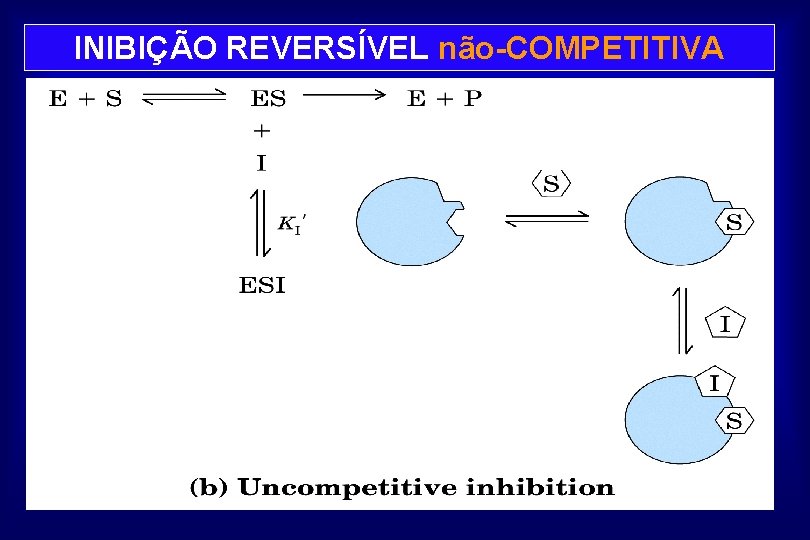
INIBIÇÃO REVERSÍVEL não-COMPETITIVA

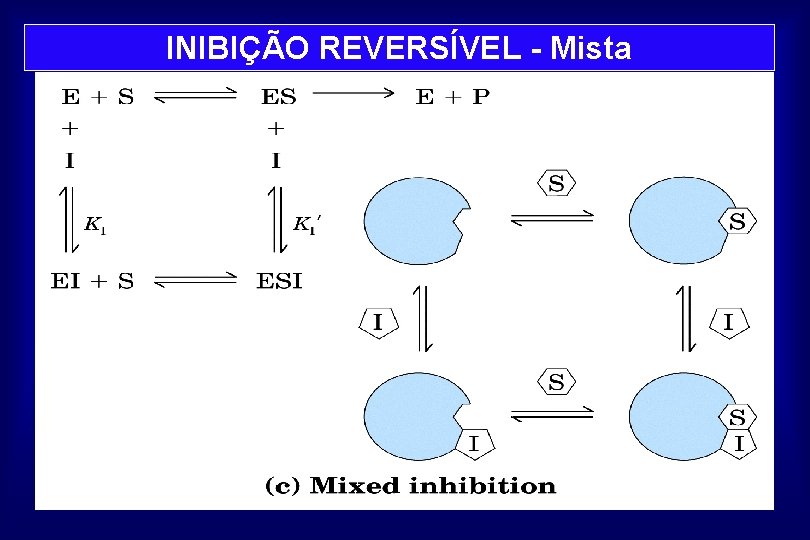
INIBIÇÃO REVERSÍVEL - Mista

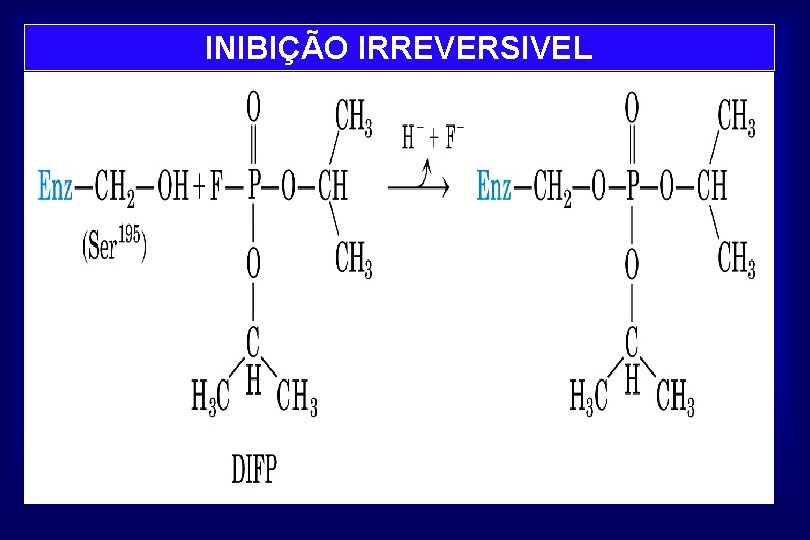
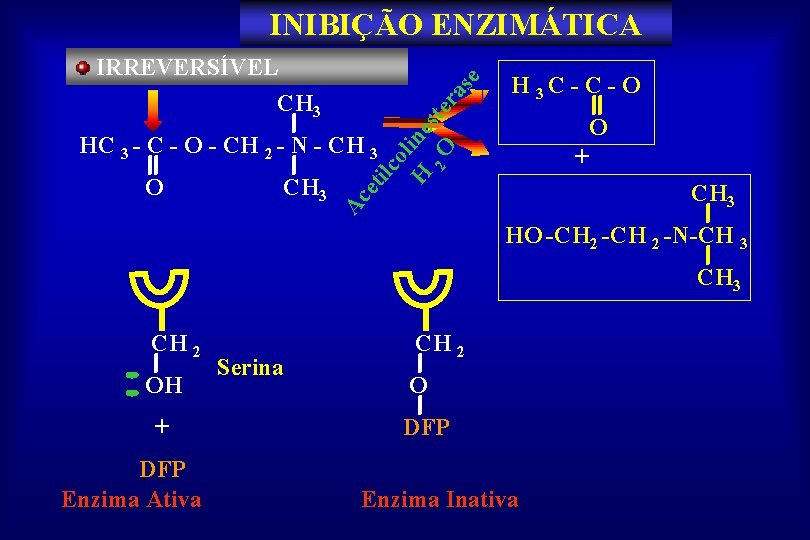
INIBIÇÃO IRREVERSIVEL

ilc ol H ine 2 O ste ra s IRREVERSÍVEL CH 3 e INIBIÇÃO ENZIMÁTICA H 3 C - O O HC 3 - C - O - CH 2 - N - CH 3 et CH 3 Ac O + HO -CH 2 -N-CH 3 CH 2 OH + DFP Enzima Ativa Serina CH 2 O DFP Enzima Inativa

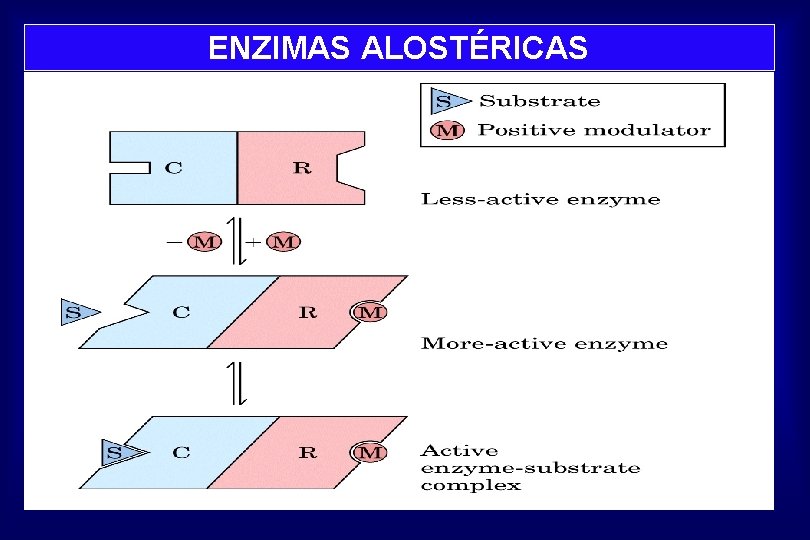
ENZIMAS ALOSTÉRICAS

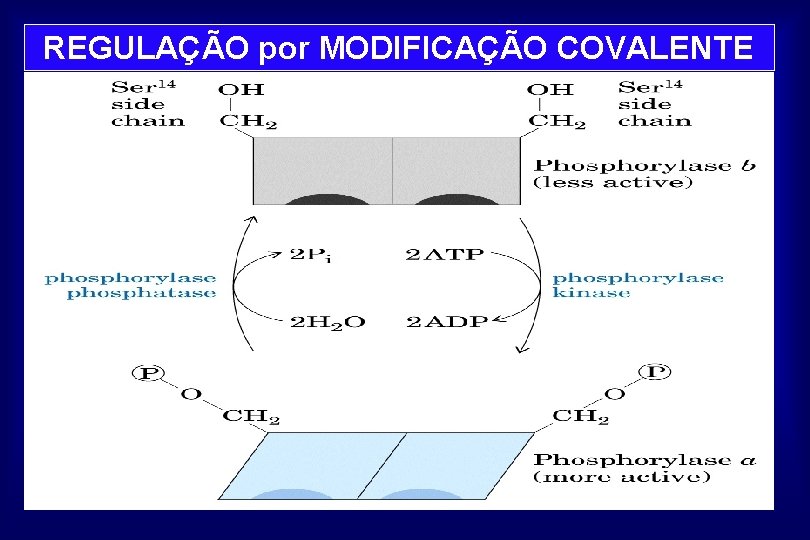
REGULAÇÃO por MODIFICAÇÃO COVALENTE

INIBIÇÃO pelo PRODUTO FINAL

INIBIÇÃO ENZIMÁTICA REVERSÍVEL NÃO COMPETITIVA O INIBIDOR SE LIGA NO SÍTIO ALOSTÉRICO
