Enzimolgia Lipz enzimek Dr Barta Zsolt Budapesti Mszaki

Enzimológia Lipáz enzimek Dr. Barta Zsolt Budapesti Műszaki és Gazdaságtudományi Egyetem Alkalmazott Biotechnológia és Élelmiszertudományi Tanszék

Lipidek Lipids Mi a lipid? § zsírsavak és származékaik (gliceridek és foszfolipidek) § zsírok (trigliceridek), viaszok § szteránvázas metabolitok (koleszterin) Funkciójuk § energia tárolás teljes oxidációjukkor kb. 9000 kcal/kg energia szabadul fel (szénhidrátból/proteinből kb. 4000 kcal/kg) § szignál molekulák § zsíroldható vitaminok (A, D, E, K) tárolása a foszfolipidek amfipatikus jellege Jellemzőjük § hidrofób vagy § amfipatikus: hidrofil (víz kedvelő) és lipofil (zsír kedvelő) vezikulumok, liposzómák, membránok 2

Zsírsavak Fatty acids Felépítésük § szénhidrogén lánc hidrofób § karboxil csoport hidrofil § 4 24 C atom szabad zsírsav § telített vagy telítetlen § a természetes zsírok/olajok → legalább 8 C atomos zsírsavak § C lánc alfa(α) végén karboxilcsoport ( COOH): vegyületképzés, másik végén: omega(ω) Néhány telített karbonsav / Saturated fatty acids jelölés: C atomszám + kettős kötések száma (ezen esetben 0) § Ecetsav (etánsav; C 2: 0): CH 3 COOH § Vajsav (butánsav; C 4: 0): CH 3(CH 2)2 COOH § Laurinsav (dodekánsav; C 12: 0): CH 3(CH 2)10 COOH § Mirisztinsav (tetradekánsav; C 14: 0): CH 3(CH 2)12 COOH § Palmitinsav (hexadekánsav; C 16: 0): CH 3(CH 2)14 COOH § Sztearinsav (oktadekánsav; C 18: 0): CH 3(CH 2)16 COOH § Arachidinsav (eikozánsav; C 20: 0): CH 3(CH 2)18 COOH 3

Zsírsavak Fatty acids Telítetlen zsírsavak / Unsaturated fatty acids § legalább egy kettős kötés ( CH=CH ) a láncban § két H atom állása szerint: cisz / transz zsírsav § természetes, többszörösen telítetlen: kettős kötések között 2 egyszeres kötés cisz konfiguráció (elhajlás lehetősége) § transz: többnyire mesterséges eredetű § kettős kötések helye: a) szénlánc "elejétől" (a karboxilcsoporttól, az alfa szénatomtól) számítva b) végétől (a metilcsoporttól, az ún. ω C atomtól) → ω 3, ω 6, ω 9 zsírsavak Néhány telítetlen karbonsav jelölés: C atomszám + kettős kötések száma + kötések láncvégtől számított helye § a linolénsav, ALA (oktadekatriénsav, C 18: 3 ω 3): CH 3 CH 2 CH=CHCH 2 CH=CH(CH 2)7 COOH § Linolsav (oktadekadiénsav, C 18: 2 ω 6): CH 3 (CH 2)4 CH=CHCH 2 CH=CH(CH 2)7 COOH § Olajsav (oktadecénsav, C 18: 1 ω 9): CH 3 (CH 2)7 CH=CH(CH 2)7 COOH § Erukasav (dokozénsav, C 22: 1 ω 9): CH 3 (CH 2)7 CH=CH(CH 2)11 COOH 4

Zsírsav észterek viaszok Fatty esters – wax esters Mi a viasz? hosszú szénláncú alifás alkoholok + zsírsavak észterei (+ alkánok, egyéb észterek, poliészterek) Előfordulás § méhviasz § termés (pl. napraforgó) külső héján → véd a nedvességtől § magban (pl. nyers napraforgó olajban) finomított rizskorpa és napraforgó viasz Felhasználás § gyertya § kozmetikai ipar (viasz+zsír+pigment → rúzsok, szemfestékek) § édességipar § sajtok bevonása § textil, papír vízhatlanítása § cipő és autóápoló, fa kezelő szerek § zsírkréta, színes ceruza, indigó papír 6

Glicerolipidek Glycerolipids Felépítésük § mono § di § triszubsztituált glicerin § Fischer képletben: a középső C atomon lévő zsírsav balra áll http: //lipidlibrary. aocs. org/Lipids/tag 1/index. htm felül lévő C atom sn 1, alul lévő C atom sn 3 Trigliceridek / Triglycerides § glicerin észtere 3 zsírsavval § 3 azonos / különböző alkillánc § alkillánc hossza változó, leggyakoribb: 16, 18, 20 C atom § természetes növényi és állati zsírsavak: jellemzően páros számúak, mert szintézisük során az acetil Co. A 2 C atomos acetát csoportokat képes szállítani § baktériumok képesek páratlan C atomszámú és elágazó láncú zsírsavak előállítására kérődzők zsírja is tartalmaz ilyet § zsírok / olajok: trigliceridek keveréke 7
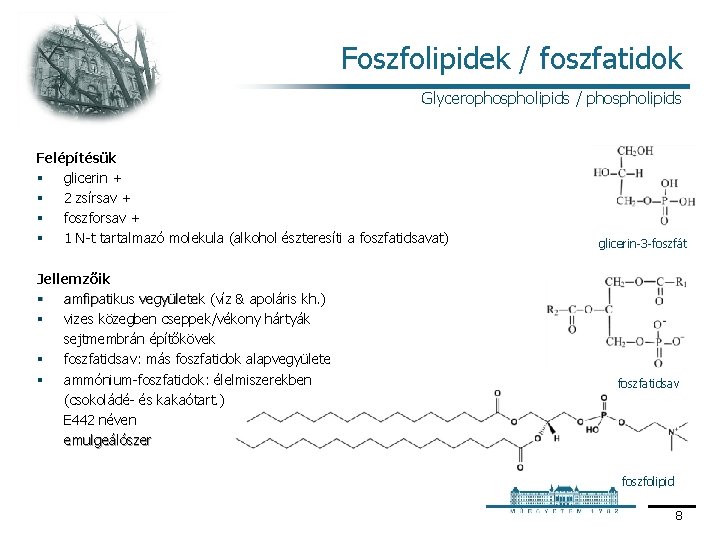
Foszfolipidek / foszfatidok Glycerophospholipids / phospholipids Felépítésük § glicerin + § 2 zsírsav + § foszforsav + § 1 N t tartalmazó molekula (alkohol észteresíti a foszfatidsavat) Jellemzőik § amfipatikus vegyületek (víz & apoláris kh. ) § vizes közegben cseppek/vékony hártyák sejtmembrán építőkövek § foszfatidsav: más foszfatidok alapvegyülete § ammónium foszfatidok: élelmiszerekben (csokoládé és kakaótart. ) E 442 néven emulgeálószer glicerin 3 foszfát foszfatidsav foszfolipid 8

Foszfolipidek / foszfatidok Glycerophospholipids / phospholipids Technikai lecitin § sárgás barnás zsíros anyag glikolipidek, trigliceridek, foszfolipidek keveréke § előfordulása állati és növényi szövetekben, tojássárgájában (lekithos ógörögül) § kinyerése napraforgó olaj nyálkátlanítása (a szója allergén) → nyálka üledék (olaj, víz, lecitin) bepárlása § élettani hatása koleszterin csökkentő (jó koleszterin szint növelő) kötött P és B vitamin (B 8 és B 11) tartalom jó hatás az idegrendszerre, agyműködésre, memóriára a vastagbélben támogatja a Lactobacillus és Bifidobacterium fajok elszaporodását § felhasználása tartósító (antioxidáns hatás), emulgeáló , stabilizálószer E 322 margarin , csokoládégyártás, sütőipar takarmányipar (zsíradék, pelletképzés javító) festékipar (stabilizáló, emulgeáló, rozsdaképződést gátló, színélénkítő) foszfatidil kolin / foszfátkolin 9

Lipázok Lipases Jellemzőik § lipidek észter kötésének hidrolízisét katalizálják § egyensúlyi reakció kis vízkoncentráció: katalizálják az alkoholok és savak észterképzését (lipid szintézis) § legtöbb mikrobiális lipáz mezofil, optimális körülményeik: p. H 7 9, 30 40°C termofilek: potenciális ipari jelentőség § Nem igényelnek kofaktorokat (ez jellemző a hidrolázokra is) § Affinitás csökken a di és monogliceridek esetén 10
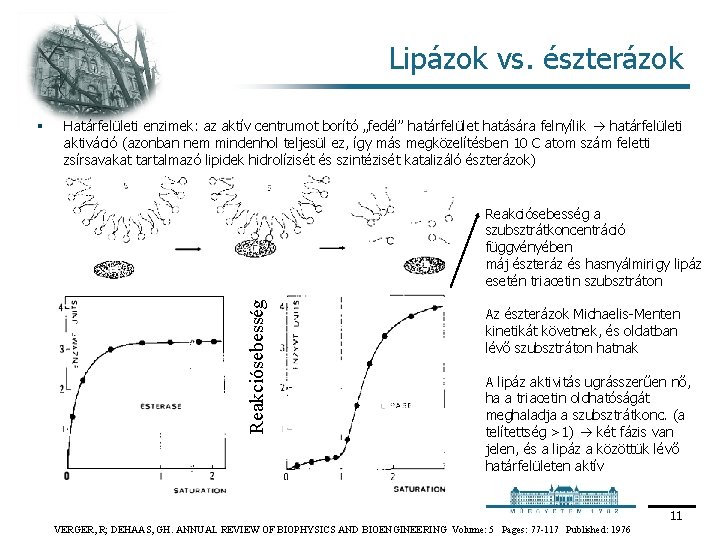
Lipázok vs. észterázok Határfelületi enzimek: az aktív centrumot borító „fedél” határfelület hatására felnyílik határfelületi aktiváció (azonban nem mindenhol teljesül ez, így más megközelítésben 10 C atom szám feletti zsírsavakat tartalmazó lipidek hidrolízisét és szintézisét katalizáló észterázok) Reakciósebesség a szubsztrátkoncentráció függvényében máj észteráz és hasnyálmirigy lipáz esetén triacetin szubsztráton Reakciósebesség § Az észterázok Michaelis Menten kinetikát követnek, és oldatban lévő szubsztráton hatnak A lipáz aktivitás ugrásszerűen nő, ha a triacetin oldhatóságát meghaladja a szubsztrátkonc. (a telítettség >1) két fázis van jelen, és a lipáz a közöttük lévő határfelületen aktív 11 VERGER, R; DEHAAS, GH. ANNUAL REVIEW OF BIOPHYSICS AND BIOENGINEERING Volume: 5 Pages: 77 -117 Published: 1976

Lipázok Lipases Reakcióik § észter hidrolízis § észter szintézis § átészterezés alkohollal észterrel savval 12 Salleh et al. (Eds), New lipases and proteases, 2006

Lipázok Lipases Szerkezetük § a/b hidroláz § többféle mechanizmus, többségük kimotripszin szerű katalitikus triád: szerin (mint nukleofil) + savas aminosav (ált. aszparaginsav) + hisztidin Hol termelődnek az emberi szervezetben? § száj § gyomor § hasnyálmirigy Hol működnek? § a sejt bizonyos részében (lizoszómában) § extracellulárisan, a sejten kívül pl. hasnyálmirigyben termelt lipáz gomba vagy baktérium által termelt egyes méhek, darazsak mérgében foszfolipid bontó enzimek csípés fokozottabb sérülés, gyulladás 13

p. H stat módszer § § § § § Az észterek hidrolízisének követésére hidrolízis kinetika vizsgálatára Enzimaktivitás méréshez szintén használható A p. H t mérhetjük pl. üvegelektróddal, vagy indikátorok alkalmazásával A lipázok aktivitásmérését is leggyakrabban p. H stat segítségével valósítják meg Állandó p. H t tartanak lúgoldat hozzáadásával Ebben az esetben legtöbbször tributirint (a glicerin vajsav észterét ) használnak szubsztrátként, de jellemző az olivaolaj emulzió is A p. H ilyen méréseknél jól követhető üvegelektróddal, mivel a felszabaduló vajsav vízoldható és az Na. OH oldattal jól mérhetően titrálható. Mikor van vége az enzimes reakciónak? Hogyan számítható a konverzió ismert mennyiségű tributirint tartalmazó reakcióelegy esetén? 14

Lipid víz kétfázisú rendszerek § I. Lipid emulzió A hidrofób tulajdonságok dominálnak § II. a) Lipid kettősréteg és b) Liposzóma Megjelenik töltés a molekulában Pl. foszfolipidek § III. Micella Egyre polárosabb a molekula Rövidebbek a zsírsavláncok Kis koncentrációban teljesen oldatban vannak CMC (kritikus micella koncentráció) felett gömb v. pálca, de optikailag tiszta a folyadék, gyors egyensúly Pl. detergensek 15 VERGER, R; DEHAAS, GH. ANNUAL REVIEW OF BIOPHYSICS AND BIOENGINEERING Volume: 5 Pages: 77 -117 Published: 1976

Lipáz kinetika § § Lipid emulzió a szubsztrát Formailag a Michaelis Menten kinetikához hasonló, de fontos eltérés a felületen történő adszorpció Üres kör: kis zsírcseppek, teli kör: nagy zsírcseppek „Felületi szubsztrátkoncentráció” esetén illeszkednek egyenesre 1/S S: anyagmennyiség/térfogat 1/SA SA: felület/térfogat 16 VERGER, R; DEHAAS, GH. ANNUAL REVIEW OF BIOPHYSICS AND BIOENGINEERING Volume: 5 Pages: 77 -117 Published: 1976

Lipázok ipari felhasználása Industrial uses of lipases Ipari felhasználás területei § régió és sztereospecifikusak lehetnek, vagy szelektívek lánchosszra, kettős kötés helyzetére § § § § § mosószerek tejipar olajkémia (pl. biokenőanyag, szappanok eá. ) gyógyászat kozmetikai ipar sütőipar (javítja a tészta állagát, szerkezetét) bőripar bioremediáció biodízelgyártás Szennyvízkezelés, biogáz előállítás 17

Lipáz források, termékek Sources of lipases, products Enzimforrások / Sources § állati szövet hasnyálmirigy ۰ marha, sertés fiatal kérődző előgyomra ۰ kecskegida (pikáns sajt íz), borjú (vajas, kicsit borsos), bárány (pecorino, „koszos zokni”) § mikrobiális előgyomor enzimek helyettesítésére egyedi lipázok vagy enzimkeverékek bakteriális eredetű gomba eredetű ۰ Aspergillus, Mucor, Rhyzopus, Candida nemzetségek Kereskedelmi termékek § folyadék extraktum § vákuum vagy fagyasztva szárított § immobilizált 19

Tisztítószerek Detergents Detergensek / Detergents § § § követelmények lúgos környezetben aktív kis szubsztrát specificitás kompatibilitás a detergensekkel teljes lipáz termelés kb. 1/3 a kereskedelemben 1988 (Lipolase Novo Nordisk) ipari és háztartási mosó mosogató egyéb tisztítószerekben Mosás után a szárítás során a lipáz aktivitás jelentősen nő (következő dia, jobb ábra). Oka: 20 30% nedvességtartalmú szövet az optimális az enzimműködéshez. A folteltávolítás a következő mosás során hatékonyabb (következő dia, bal ábra). 20
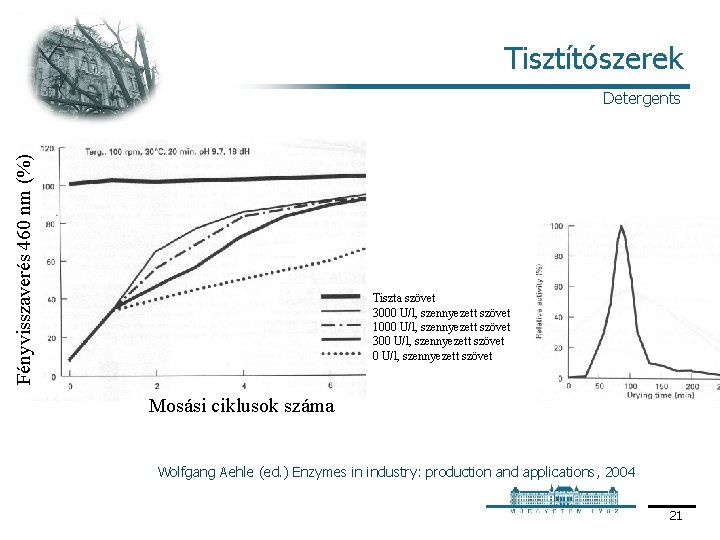
Tisztítószerek Fényvisszaverés 460 nm (%) Detergents Tiszta szövet 3000 U/l, szennyezett szövet 1000 U/l, szennyezett szövet 300 U/l, szennyezett szövet Mosási ciklusok száma Wolfgang Aehle (ed. ) Enzymes in industry: production and applications, 2004 21

Tejipar sajtgyártás Dairy industry – cheese making Tejipar / Dairy industry § joghurtgyártás § sajtgyártás / cheese making, ripening vajzsír és tejszín bontása érés gyorsítása ízfokozás (főleg lágy sajtok jellegzetes ízének kialakítása) ۰ lipáz rövid láncú zsírsav (ált. C 4, C 6) felszabadítása erős, csípős íz ۰ lipáz közepes lánchossz (C 12, C 14) zsírosabb íz ۰ lipázok részt vesznek egyszerű kémiai reakciókban egyéb ízanyagok íz imitálás ۰ utánozza a juh / kecske sajtok ízét feta és egyéb sajtok tehéntejből ۰ pasztőrözött tejből való sajtgyártásnál a nyers tejből előállítotthoz hasonló ízt ad EMC: enzim módosított sajtok (USA) ۰ a sajtot enzimmel termosztálják magas hőfokon 10 x nagyobb zsírsavkonc. 22 szószokhoz, saláta öntetekhez, levesekhez, rágcsálnivalókhoz
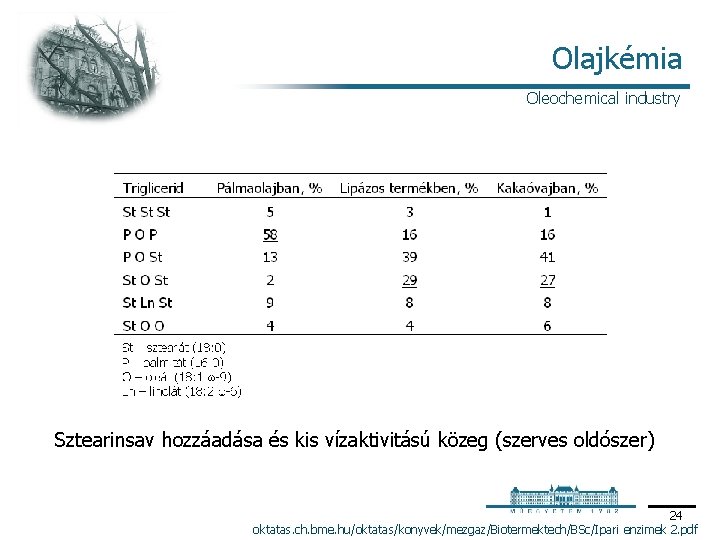
Olajkémia Oleochemical industry Sztearinsav hozzáadása és kis vízaktivitású közeg (szerves oldószer) 24 oktatas. ch. bme. hu/oktatas/konyvek/mezgaz/Biotermektech/BSc/Ipari enzimek 2. pdf
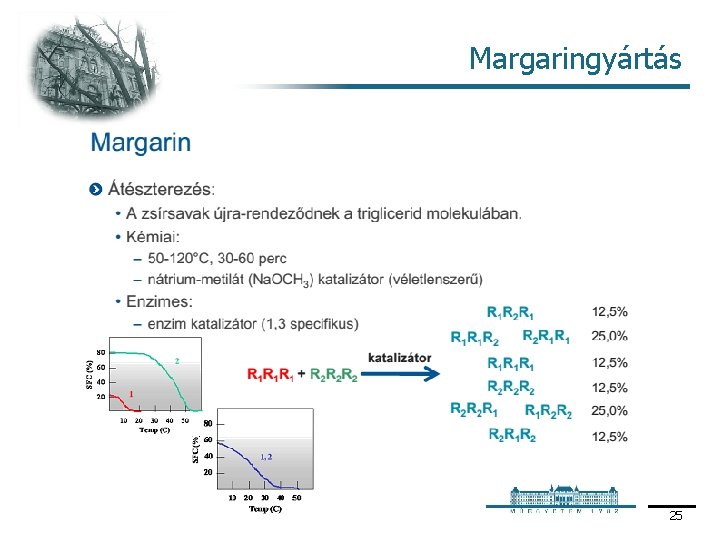
Margaringyártás 25
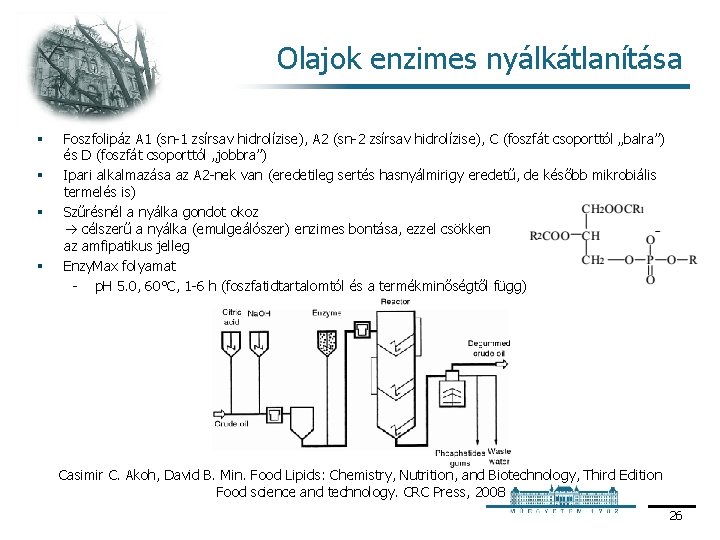
Olajok enzimes nyálkátlanítása § § Foszfolipáz A 1 (sn 1 zsírsav hidrolízise), A 2 (sn 2 zsírsav hidrolízise), C (foszfát csoporttól „balra”) és D (foszfát csoporttól „jobbra”) Ipari alkalmazása az A 2 nek van (eredetileg sertés hasnyálmirigy eredetű, de később mikrobiális termelés is) Szűrésnél a nyálka gondot okoz célszerű a nyálka (emulgeálószer) enzimes bontása, ezzel csökken az amfipatikus jelleg Enzy. Max folyamat p. H 5. 0, 60°C, 1 6 h (foszfatidtartalomtól és a termékminőségtől függ) Casimir C. Akoh, David B. Min. Food Lipids: Chemistry, Nutrition, and Biotechnology, Third Edition Food science and technology. CRC Press, 2008 26

Biogázosítás – lipid hidrolízis § § Az olajok és zsírok közvetlen beadagolva a biogázosító reaktorba rátapadhatnak a bakteriális ökoszisztémát adó aggregátumok, flokkulátumok felületére, gátolva ezzel az anyagtranszportot a vizes fázis és a szilárd részecskék között. Még ennél is kifejezettebb az az irreverzibilis gátlóhatás, amit az olajok és zsírok hidrolízisénél felszabaduló hosszúláncú zsírsavak – különösen a telítetlen zsírsavak – okoznak, beépülve egyes baktériumok membránjaiba, membránjaiba véglegesen meggátolva azok normális fiziológiai működését. A metanogén baktériumok erősen gátolhatók hosszúláncú zsírsavakkal. Állattenyésztők ki is használják ezt a jelenséget, amikor takarmányhoz adagolva azokat, nagymértékben csökkenthető a kérődzők metántermelése. Másrészről a zsírsavak biogázosítása kb. 3 szor annyi energianyeréssel jár, mint a szénhidrátoké! 28

Biogázosítás – lipid hidrolízis § § Az olajok és zsírok gyors hidrolízisét és ezáltal a gátló hosszúláncú zsírsavak felszaporodását a biogázosító reaktorban megakadályozni nem tudjuk, mivel a reaktorban jelentős lipáz aktivitás figyelhető meg, ezáltal a hidrolízis sebessége sokkal nagyobb, mint a biogázképzés sebessége A hosszúláncú zsírsavak Ca sói nem okoznak a fentiekhez hasonló gátlást, mivel oldhatóságuk vízben minimális. Ekvimoláris mennyiségû Ca 2+ szükséges a kívánt hatás eléréséhez, vagyis ha a hosszúláncú zsírsav (LCFA) és a Ca 2+ mólarányát fejezzük ki, akkor ha ez az arány : [LFCA] / [Ca] = 2 , vagy ennél kisebb, akkor nincs gátlás. § Ugyanakkor Ca. CO 3 adagolása nem csökkenti a gátlóhatást. Miért? 29
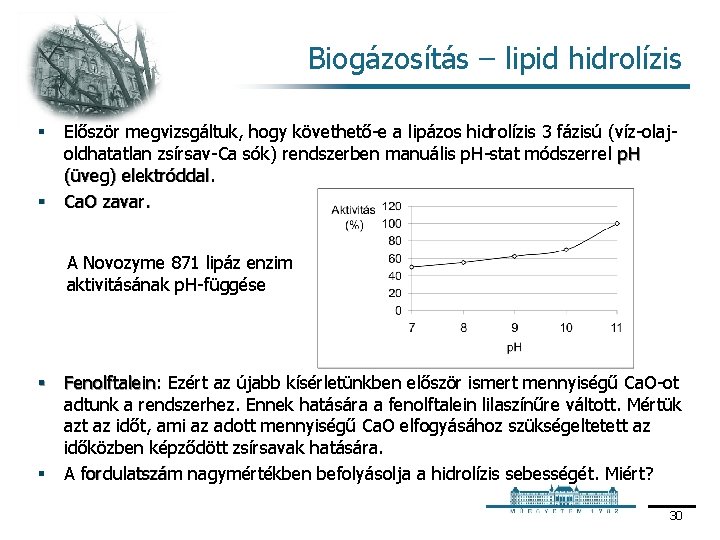
Biogázosítás – lipid hidrolízis Először megvizsgáltuk, hogy követhető e a lipázos hidrolízis 3 fázisú (víz olaj oldhatatlan zsírsav Ca sók) rendszerben manuális p. H stat módszerrel p. H (üveg) elektróddal § Ca. O zavar. § A Novozyme 871 lipáz enzim aktivitásának p. H függése § Fenolftalein: Fenolftalein Ezért az újabb kísérletünkben először ismert mennyiségű Ca. O ot adtunk a rendszerhez. Ennek hatására a fenolftalein lilaszínűre váltott. Mértük azt az időt, ami az adott mennyiségű Ca. O elfogyásához szükségeltetett az időközben képződött zsírsavak hatására. § A fordulatszám nagymértékben befolyásolja a hidrolízis sebességét. Miért? 30
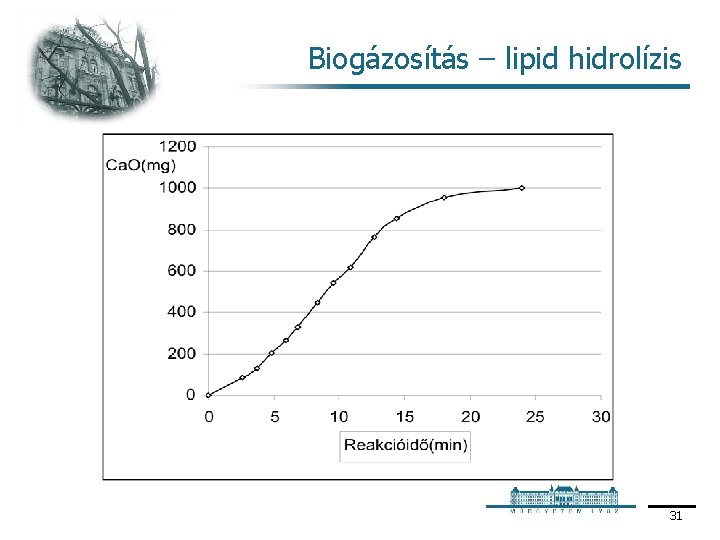
Biogázosítás – lipid hidrolízis 31

Biogázosítás – lipid hidrolízis A görbe szigmoid jellegű. Oka lehet a lipáz enzim határfelületen történő működése, amelynek első lépése az enzim adszorpciója a határfelületen Valószínűleg ennek időben elnyújtott jellege okozza a furcsa kinetikai viselkedést. A kezdeti görbekésés után viszont jó közelítéssel lineáris szakasz következik. Ez viszont csak nulladrendű hidrolízis kinetikával indokolható. Ismert, hogy nulladrend esetében a sebesség és a sebességi állandó nem függ a szubsztrát koncentrációjától, vagyis: Integrálva So és St , ill. 0 és t között: ahol S 0 = a kiindulási szubsztrátkoncentráció, St = adott t idő után még megmaradt szubsztrátkoncentáció, t = a reakcióidő [S 0] [St] viszont egyenlő a termékkoncentrációval, ill. esetünkben áttételesen a Ca. O fogyással. 32

Biogázosítás – lipid hidrolízis § § Ezt a furcsa hidrolízis kinetikai viselkedést, t. i. hogy a szubsztrátkoncentráció nem változik a hidrolízisnek egy jelentős szakaszán – mert, ha változna, akkor nem nulladrendű összefüggést kellene kapnunk – csak úgy tudjuk magyarázni, hogy amikor a Ca szappan csapadék jelentőssé válik a reakcióelegyben, akkor annak felületén kialakul egy olajfilm Ennek a felülete határozza meg a hidrolízis sebességét. De a film felülete mindaddig nem változik, amíg már csak molekuláris fedettség nem lesz a csapadék felületén. Ha ez bekövetkezik, akkortól már csökken a szokásoknak megfelelően a hidrolízis sebessége. Ennek egy indirekt bizonyítékát tapasztaltuk is, mert egy teljesen azonosan kivitelezett kísérletben reakció közben leállítottuk a lineáris szakasz közepe táján a keverést. Állás közben szétvált a rendszer szilárd csapadékká és vizes fázissá. A maradék olajfázis teljesen eltűnt, valószínűleg adszorbeálódott a csapadékon 33
- Slides: 29