Enzimek Az l szervezetben hmrsklet fldi atmoszfra nyomsviszonyai

Enzimek

• Az élő szervezetben (hőmérséklet, földi atmoszféra nyomásviszonyai mellett) nem, vagy csak nagyon lassan játszódnak le a különböző folyamatok → meggyorsításukhoz katalízisre van szükség. • A katalízist enzimeknek nevezett fehérjék végzik, amelyek a kémiai anyagok átalakításához szükséges időt lerövidítik, a reakciósebességet pedig 109 – 1012 – szeresére is fokozhatjuk.

• Újabb megfigyelések szerint néhány speciális biokémiai folyamatban RNS molekulák is képesek a katalizátor feladatát ellátni. A katalitikus képességgel rendelkező ribonukleinsavakat „ribozim”-nak nevezzük. (Vagy önmaguk átszerkesztődését katalizálják, de van olyan típus is, amely valódi katalizátornak tekinthető).

• Az enzimek csökkentik a reakciók aktiválási energiáját (Az aktiválási energia a kiindulási és az aktivált állapot energiaszintje közötti különbség) Animáció

• A szubsztrát(ok) és a végtermék(ek) stabil kémiai szerkezete között az átalakuló molekulának egy ún. tranzíciós (átmeneti) állapotba kell kerülnie, amelyben átmenetileg mind a kiindulási szerkezethez, mind a végtermék szerkezetéhez tartozó energiaszintnél magasabb energiaszintet ér el. Ez az átmeneti energiaszint növekedés a gátja a reakciónak. • Az enzimek az aktív helyen (centrumban) kötik meg az átalakítandó anyagot, a szubsztrátot (szubsztrát kötő hely)

• Az aktív helyhez tartoznak még azok a katalitikus csoportoknak nevezett aminosav oldalláncok, amelyek részt vesznek a szubsztrát átalakításában (katalitikus hely) →a kémiai átalakulást elvégzi • A szubsztrát és a szubsztrát kötő hely közötti kölcsönhatás hozza létre a komplementer szerkezetet • Bizonyos enzimek működéséhez, bizonyos kis molekulákkal, ún. kofaktorokkal történő kapcsolódás szükséges. Ilyen kofaktorok lehetnek bizonyos ionok, pl. Cu 2+ , Zn 2+. • Vannak enzimek, amelyek működésükhöz más kofaktorokat, ún. prosztetikus csoportokat vesznek segítségül. Ezek pl. vitamintermészetű anyagok.


Az enzim és szubsztrát közötti kapcsolatot gyenge, reverzibilis kölcsönhatások (elektrosztatikus kötések, H-hidak, hidrofób kölcsönhatások) biztosítják. a; kulcs-zár modell b; indukált illeszkedés (induced fit)

• Néhány toxikus nehézfém (pl. Cd 2+, Hg 2+) hatása részben azzal magyarázható, hogy helyettesíti a Zn 2+-t az aktív helyen (pl. RNS- polimeráz) • Kofaktorok lehetnek az ún. koenzimek is (pl. NAD, FAD) • A katalitikusan aktív enzim-kofaktor komplexet holoenzimeknek nevezzük. apoenzim (inaktív) + kofaktor holoenzim (aktív) Animáció

Az enzimek osztályozása • Az enzimeket katalizált reakció jellege szerint 6 osztályba soroljuk (ezen belül alosztályok, csoportok, majd maguk az egyes enzimek). Minden egyes enzimet így négy szám határoz meg. Pl. glükóz-6 -PDH : EC 1. 1. 1. 49

1; Oxidoreduktázok (elektron ill. H átvitel) pl. G-6 -P + NADP+ → 6 -foszfoglükonsav - lakton + NADPH + H+ almasav+NAD+→oxálecetsav+NADH+ H+ etanol + NAD+ →acetaldehid+NADH+ H+ 2; Transzferázok (csoportátvitel egy szubsztrátról egy másikra) Foszfátátvivők a kinázok pl. glükóz + ATP glükokináz G-6 -P + ADP

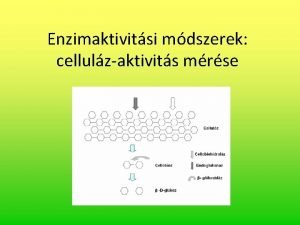
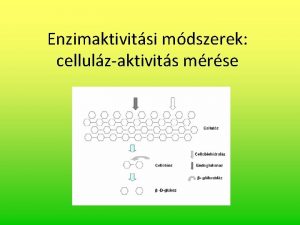
3; Hidrolázok (víz bevitellel hasítanak kovalens kötéseket) lipáz pl. triglicerid + 3 H 2 O glicerol + 3 zsírsav -amiláz keményítő + H 2 O dextrin →maltóz (glükóz) 4; Liázok (szintáz) A szubsztrátmolekulát úgy hasítják ketté, hogy az egyik termékben kettős kötés alakul ki (vagy visszafelé kettős kötésre való addíció játszódik le) Más szóval: víz, CO 2 vagy NH 3 adódik a szubsztráthoz vagy vonódik el pl. 2 -foszfoglicerát ↔ foszfoenolpiruvát + H 2 O fumársav + H 2 O almasav aldoláz F-6 -P GAP + DHAP

5; Izomerázok Különböző típusú izomerizációkat (cisz-transz, aldózketóz, stb. ) katalizálnak. G-6 -P F-6 -P 6; Ligázok (szintetázok) Energiaigényes szintéziseket katalizálnak (pl. DNSligáz)

Az enzimreakciók kinetikája • Már a múlt században kimutatták, hogy az enzimreakciók nem egyszerű másodrendű reakciók. A századfordulón több megfigyelésből azt a következtetést vonták le, hogy az enzim komplexet kell képezzen a szubsztrátjával, mielőtt átalakítja (BROWN, valamint HENRI, 1902). A legegyszerűbb, két egymást követő lépésből álló enzimes folyamat feltételezett mechanizmusát és kinetikáját MICHAELIS és MENTEN írták le 1913 -ban.

A általuk analizált legegyszerűbb enzimreakció a következő egyenlettel írható le: Ahol E enzimet, S a szubsztrátot, P pedig az enzimreakció termékét jelenti. A nyilakhoz írt sebességi állandók indexébe írt szám a reakciólépés számát, előjele a reakció irányát jelöli.

A kétlépéses mechanizmus egyenes következménye, hogy a teljes folyamat, azaz a termék képződésének a sebessége nem lineáris függvénye az [S] szubsztrátkoncentrációnak, hanem hiperbola szerint alakul A kezdeti sebesség hiperbolája végtelen nagy szubsztrátkoncentrációnál egy maximális értékhez a Vmax úgynevezett maximális sebességhez konvergál. A maximális sebesség feléhez tartozó szubsztrátkoncentráció az abszcisszatengelyen megadja a Michaelis féle állandó (KM) számértékét. Az enzimreakciók kezdeti sebességének a szubsztrátkoncentrációtól való függése.

• MICHAELIS és MENTEN elméletüket olyan enzimreakcióra írták le, amelyekben az ES komplex képződésének és visszafelé menő disszociációjának sebessége egyaránt nagyon nagy, sokkal nagyobb, mint a termék képződéséé az ES komplexből, azaz amelyekre nézve K-1 >> k 2

• Minthogy k 1 értéke általában mindig jóval nagyobb k -1 -nél, a fenti egyenlőtlenség fennállása olyan enzimreakciókra vonatkozik, amelyeknél az enzimszubsztrát komplex képződésének és elbomlásának gyorsasága miatt a reakció minden pillanatában az [E], [S], valamint az [ES] koncentrációk megfelelnek az enzim-szubsztrát komplex Ks disszociációs állandója által meghatározottaknak, vagyis fennáll a egyenlőség. Az ilyen eseteket „rapid ekvilibrium" mechanizmust követő enzimreakciónak nevezzük.

A Michaelis-Menten-féle reakciósémában nem szerepel a második lépés visszafelé játszódása. Elvileg minden kémiai reakció megfordítható, azonban a visszafelé haladó reakció aktiválási energiája olyan magas lehet, hogy gyakorlati szempontból a reakció lejátszódása elhanyagolható (végtelenül lassan játszódik le). Ettől eltekintve is elhanyagolhatjuk a második reakció visszafelé lejátszódását, ha az enzimreakciót a kezdetekor vizsgáljuk, az enzim és a szubsztrát összehozásakor, amikor még nincs jelen termék. A „kezdeti reakciósebesség”, (V 0), a P termék koncentrációjának időbeni változására a következő kifejezéssel írható le:

• Az enzimreakciók túlnyomó többségére nézve a v 0 sebessége a következő egyenlettel írható le: ahol Vmax és KM állandó. Az összefüggés könnyen levezethető a következő gondolatmenet alapján. Az enzim összes koncentrációja, [E]össz minden esetben két tagból áll, a szabad enzim [E], valamint a komplexben lévő enzim [ES] koncentrációból: [ES]össz=[E]+[S] A rapid ekvilibrium feltétel alapján nagyon jó közelítéssel igaz, hogy bármely időpontban az [E] értéke
![• Tegyük fel a kérdést: hogyan aránylik egy adott [S] koncentrációnál a v • Tegyük fel a kérdést: hogyan aránylik egy adott [S] koncentrációnál a v](http://slidetodoc.com/presentation_image/59fcbef5dbed07822fe3dbe12928b0f2/image-21.jpg)
• Tegyük fel a kérdést: hogyan aránylik egy adott [S] koncentrációnál a v 0 értéke a végtelen nagy szubsztrátkoncentrációnál elérhető maximális reakciósebesség, Vmax értékéhez? Az utóbbi esetben az ES komplex képződés egyensúlya teljesen eltolódott a komplex képződésének irányába, azaz nagyon jó megközelítéssel igaz hogy

Ez egy speciális eset, amikor a KM Michaelis-féle állandó számértékileg megegyezik az ES komplex disszociációs állandójával. Ez csak a rapid ekvilibrium mechanizmust követő enzimreakciókra érvényes. Kissé általánosabb eset, amikor a k-1 és a k 2 sebességi állandók számértéke nem különbözik nagyságrendileg, de az enzimreakció az eredeti sémát követi. BRIGGS és HALDANE (1925) szerint ilyenkor is érvényes a reakció sebességének a leírása a egyenlet.

A termék koncentrációja az enzimreakció során időben az ábrán látható módon változik, s egy hosszabb időtartamban az idővel lineárisan növekszik. Ez az úgynevezett steady-state állapot. A szaggatott vonallal kijelölt időtartományban a termék koncentrációja egyenletesen, az idővel arányosan növekszik. Ezt nevezzük steady state állapotnak. Ilyenkor az ES-komplex képződése, valamint kétféle irányú elbomlása azonos sebességgel folyik, azaz az ES koncentrációja ebben az időtartományban gyakorlatilag állandó.

Az ES komplex koncentrációja három reakció sebességétől függ, azaz A steady-state állapotban az ES komplex képződésének a sebessége megegyezik a disszociációjának + a termék kialakulásának a sebességével, vagyis az ES koncentrációja hosszabb időtartamban nem változik:

A rapid ekvilibrum esetére végzett levezetés gondolatmenetét követve kapjuk, hogy A nevezőben lévő, sebességi állandókból álló törtet, mint állandót KM-mel jelölve Olyan esetben, amikor az enzimreakció sémája E = S ↔ EP ↔ E+P Akkor a Michaelis-állandó értéke:

• Az enzimreakciók túlnyomó többségére jól alkalmazható két állandó számérték a későbbiekben szereplő hiperbola lefutása egyértelműen meghatározza. A Vmax a hiperbola vízszintes aszimptotájának magasságát jelöli, a KM pedig számértékileg megegyezik a Vmax/2 („fél-maximális”) sebességértékhez tartozó abszcisszaértékkel. A Vmax csak egy adott enzimkoncentrációjú rendszerben állandó, máskülönben a Vmax = k 2[E]össz egyenlet értelmében a k 2 sebességi állandó a valódi állandó az enzimkinetikát leíró hiperbola egyenletében.

A KM és a Vmax meghatározása alapvető feladat egy adott enzim kinetikájának jellemzéséhez. Az alapegyenlet formai átalakításával több olyan egyenletet dolgoztak ki, amelyek segítségével egyszerű grafikus úton meghatározható az állandók értéke. Pl. a egyenlet reciprokát véve az egyenlethez jutunk, s ha a Lineweaver-Burk szerinti kettős reciprok ábrázolását alkalmazzuk, azaz az 1/v 0 értéket ábrázoljuk a szubsztrátkoncentráció reciprokának függvényeként, egyenest kapunk.

Az így kapott egyenes ordinátametszete 1/Vmax értékét adja, az abszcissza metszete pedig a -1/KM értéket. Az egyenes meredeksége KM/Vmax értékével egyenlő. A reakciósebességi mérésekből számított reciprok értékek az adott szubsztrátkoncentráció reciprokának függvényében ábrázolva egyenesre esnek. Az egyenes extrapolálása bejelöli az ordinátán a maximális sebesség reciprokának értékét, az abszcissza tengelyen pedig a Michaelisféle állandó értékének negatív reciprokát.

A KM és a Vmax értéke grafikusan könnyen meghatározható az Eisenthal-Cornish-Bowden féle ábrázolás segítségével is. Az abszcisszán a szubsztrátkoncentráció negatív értékeit kijelölve, az ordinátatengelyen pedig az ezekhez tartozó v 0 értékeket, az ezeket a pontokat összekötő egyenesek metszéspontjának koordinátái megadják a KM illetve a Vmax értékét.

Az enzimműködést befolyásoló tényezők • A p. H hatása az enzimekre - befolyásolhatja a molekulák konformációját és a konformáció stabilitását, - hatással lehet a szubsztrát kötődésére, - befolyásolhatja a katalitikus csoportok működését • A hőmérséklet hatása az enzimek aktivitására - az enzim denaturálódik

Nem kovalensen kötődő aktivátorok és inhibitorok hatása Ki = inhibitor állandó Ka = aktivátor állandó Aktivátorok és inhibitorok: az aktív centrumon reverzibilisen kötődnek → térszerkezetet változtatja

Az aktív centrumra kötődő inhibitorok a; Kompetitív inhibitorok Az enzim szubsztrátkötő helyéhez kötődnek → meggátolják a szubsztrát kötődést KM nő, Vmax ugyanannyi

b; Nemkompetitív inhibitorok A szubsztrát kötődést nem befolyásolják, de megakadályozzák a kötött szubsztrát átalakulását KM változatlan, Vmax csökken

c; Vegyes típusú inhibitorok Az ES komplexen is képesek kötődni, de kisebb affinitással, mint a szabad enzimen. KM nő, Vmax csökken

d; Unkompetitív inhibitorok A szabad enzimre nem képesek kötődni, csak az ES komplexre; kötődésük után az enzim nem tudja a szubsztrátot átalakítani Párhuzamos egyeneseket kapunk A reverzibilisen kötődő aktivátorok, vagy az enzimszubsztrát kialakulására, vagy a kötött szubsztrát átalakítására hatnak → azaz vagy csökkentik a KM értéket, vagy növelik a Vmax-ot.

Az enzimek allosztérikus szabályozása Allosztérikus szabályozás: A szabályozóanyag nem az aktív, hanem a reguláló centrumon kötődik Ezek az enzimek is több alegységből állnak, a szubsztrátok is szabályozók. Homotrop kölcsönhatás Pozitív és negatív kooperativitás Heterotrop kölcsönhatás Effektorokkal (aktivátorral és inhibitorral)

• Magyarázat: a szubsztrát vagy effektor hatására bekövetkező konformációváltozás következménye a hatás • Szekvenciális mechanizmus a megkötődő szubsztrát megváltoztatja annak az alegységnek a konformációját, amelyhez kötődött (induced fit) • Összehangolt mechanizmus (concerted model) minden alegység csak azonos konformációban lehet, vagy aktív (relaxed, R) ←aktivátor kötő vagy inaktív (feszített, tensed, T) ←inhibitor ide kötődik Animáció
- Slides: 37