ENZIMAS ENZIMAS So catalisadores biolgicos aceleram a velocidade
ENZIMAS

ENZIMAS São catalisadores biológicos→ aceleram a velocidade das reações, sem alterar a proporção entre reagente e produtos encontrada no final da reação e sem serem consumidos durante o processo. A maioria das enzimas são proteínas Exceção: RNAs que tem ação enzimática (ribozima) A manutenção da vida celular depende de um conjunto de reações químicas que devem ocorrer com alta especificidade e a velocidades adequadas.
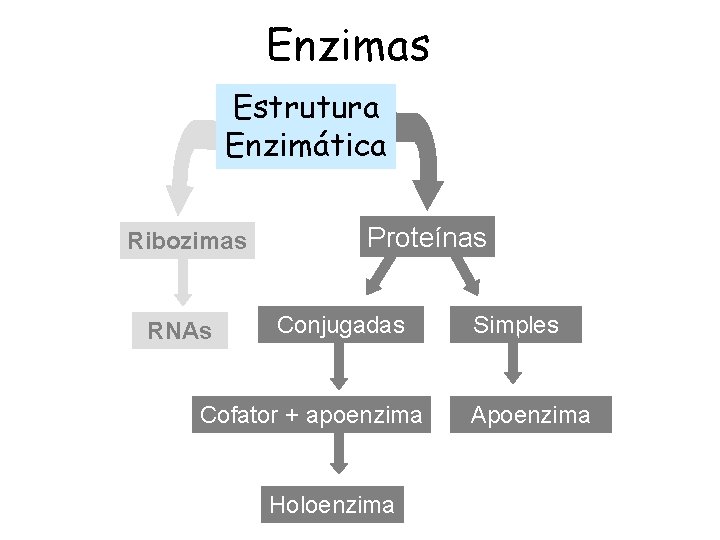
Enzimas Estrutura Enzimática Ribozimas RNAs Proteínas Conjugadas Cofator + apoenzima Holoenzima Simples Apoenzima

Enzimas - Nomenclatura No século XIX - poucas enzimas identificadas • Adicionava-se sufixo ASE ao nome do substrato – enzima que hidrolisam • gorduras (lipo - grego) - LIPASE • amido (amylon - grego) - AMILASE • proteínas - PROTEASE • • Nomes arbitrários • Tripsina e pepsina - proteases • Catalase - H 2 O 2

Enzimas - Nomenclatura • Sistema Oficial IUB (União Internacional de Bioquímica) • Cada enzima - no de código (E. C. - Enzime Comission) com 4 dígitos que caracterizam o tipo de reação • 1 o dígito - classe • 2 o dígito - subclasse • 3 o dígito - sub-subclasse • 4 odígito - indica o substrato
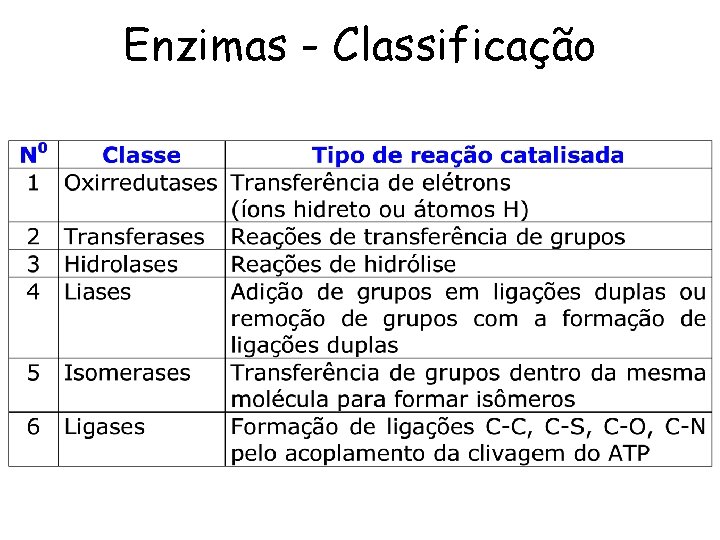
Enzimas - Classificação
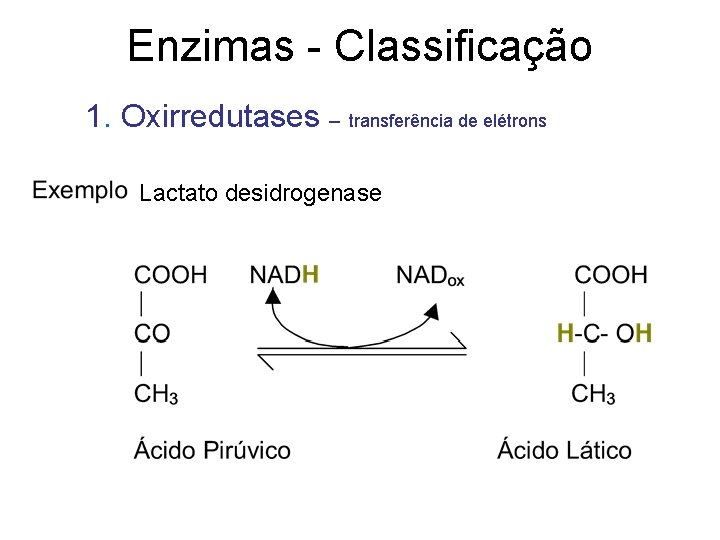
Enzimas - Classificação 1. Oxirredutases – transferência de elétrons Lactato desidrogenase
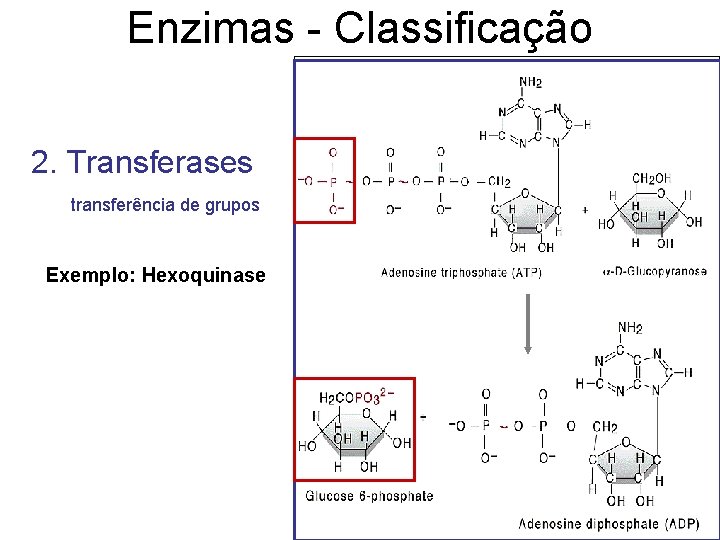
Enzimas - Classificação 2. Transferases transferência de grupos Exemplo: Hexoquinase
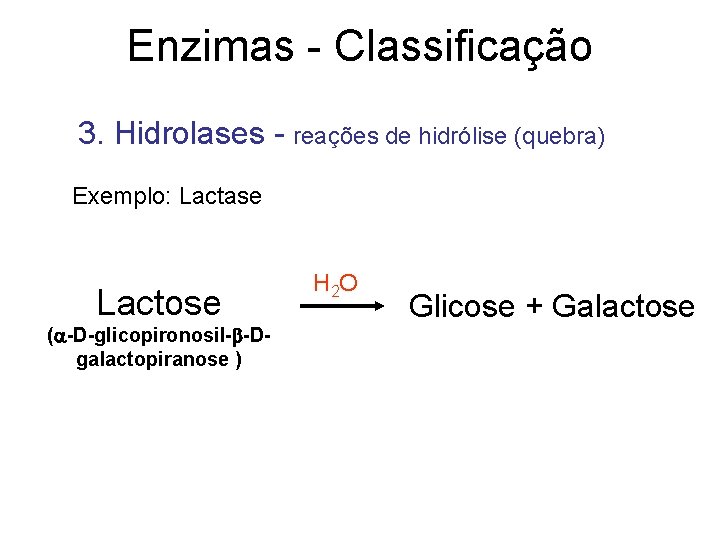
Enzimas - Classificação 3. Hidrolases - reações de hidrólise (quebra) Exemplo: Lactase Lactose ( -D-glicopironosil- -Dgalactopiranose ) H 2 O Glicose + Galactose
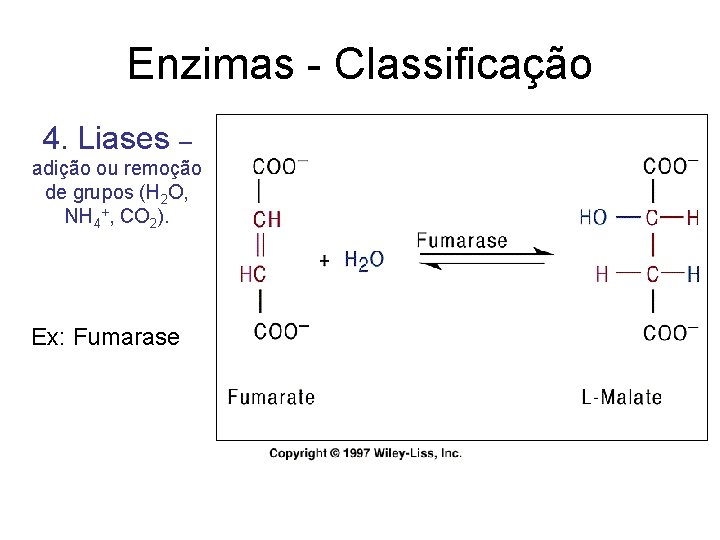
Enzimas - Classificação 4. Liases – adição ou remoção de grupos (H 2 O, NH 4+, CO 2). Ex: Fumarase
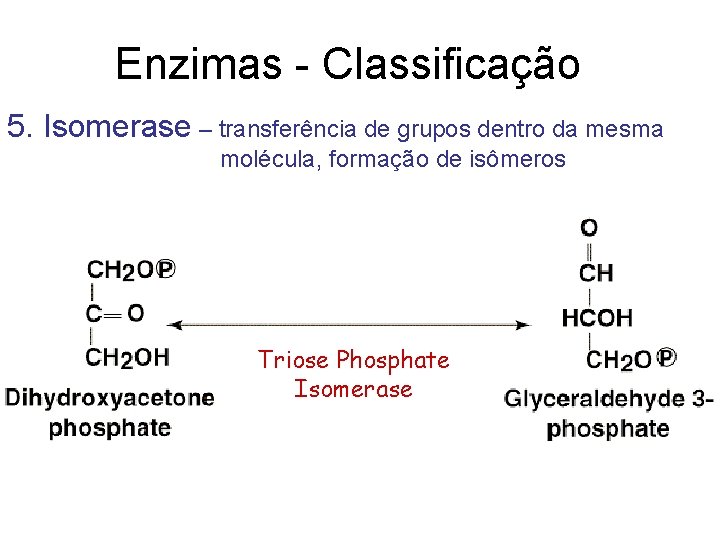
Enzimas - Classificação 5. Isomerase – transferência de grupos dentro da mesma molécula, formação de isômeros Triose Phosphate Isomerase
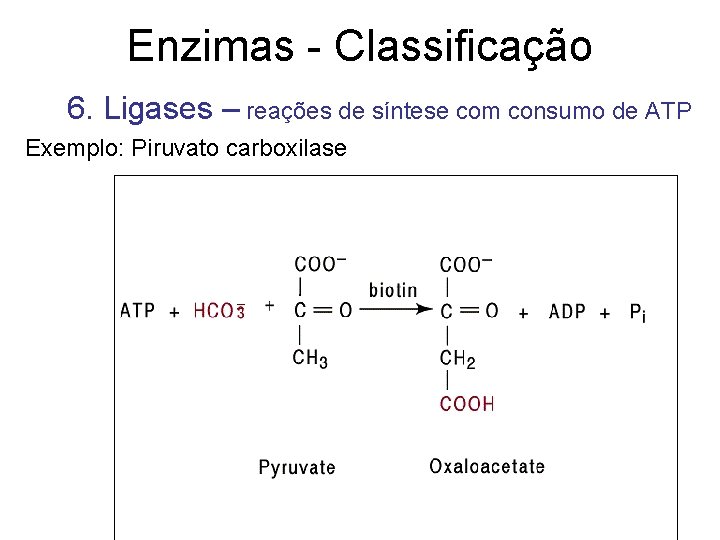
Enzimas - Classificação 6. Ligases – reações de síntese com consumo de ATP Exemplo: Piruvato carboxilase
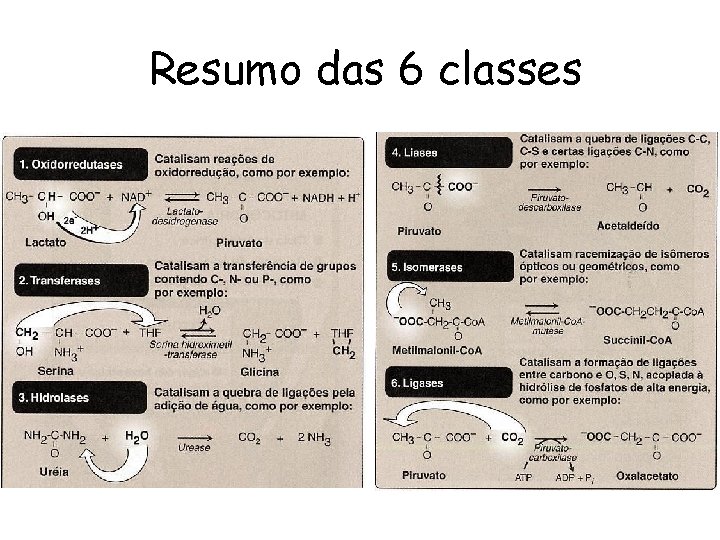
Resumo das 6 classes

Enzimas - Nomenclatura ATP + D-Glicose ADP + D-Glicose-6 -fosfato IUB - ATP: glicose fosfotransferase E. C. 2. 7. 1. 1 2 - classe - transferase 7 - sub-classe - fosfotransferase 1 - sub-subclasse - fosfotransferase que utiliza grupo hidroxila como receptor 1 - indica ser a D-glicose o aceptor do grupo fosfato Hexoquinase

Como as enzimas trabalham? • A enzima possui uma cavidade denominada centro ativo ou sítio catalítico. • Região na qual o substrato se liga. • Formados por aminoácidos trazidos à proximidade uns dos outros pelos dobramentos da cadeia polipeptídica. • Permite o reconhecimento do substrato. • O substrato deve ter a forma espacial adequada para alojar-se no centro ativo e grupos químicos capazes de estabelecer ligações precisas com os radicais do centro ativo.
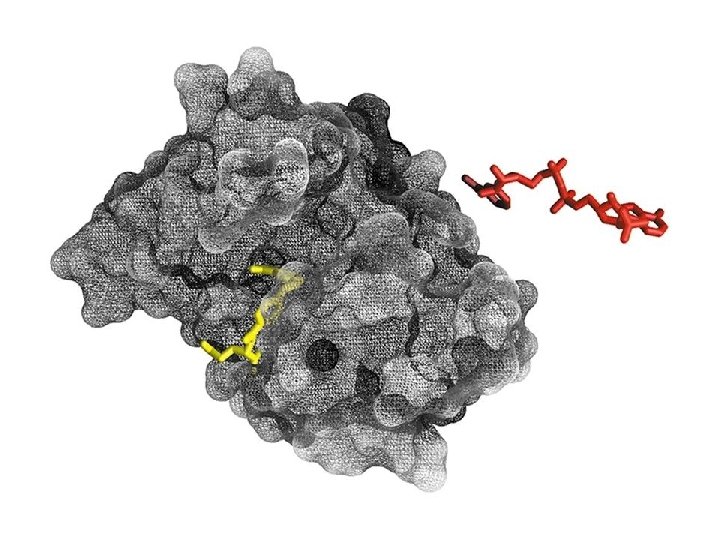
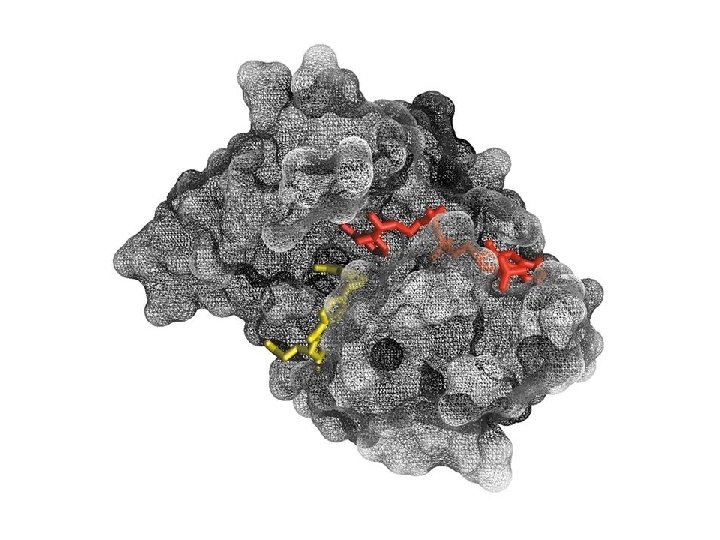
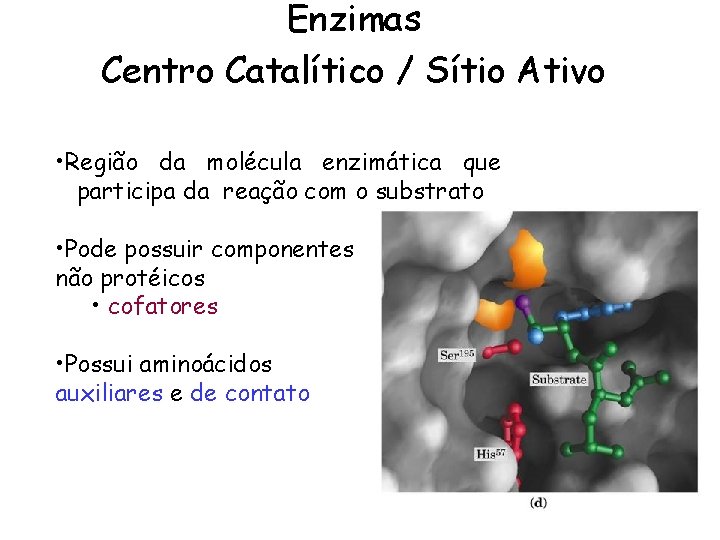
Enzimas Centro Catalítico / Sítio Ativo • Região da molécula enzimática que participa da reação com o substrato • Pode possuir componentes não protéicos • cofatores • Possui aminoácidos auxiliares e de contato
Enzimas Catalisadores Aumentam a velocidade das reações Atuam diminuindo a energia de ativação
Enzimas Componentes da Reação Enzimática E+S ES E+P E - Enzima S - Substrato(s) ES - Complexo Enzima -Substrato P – Produto(s)
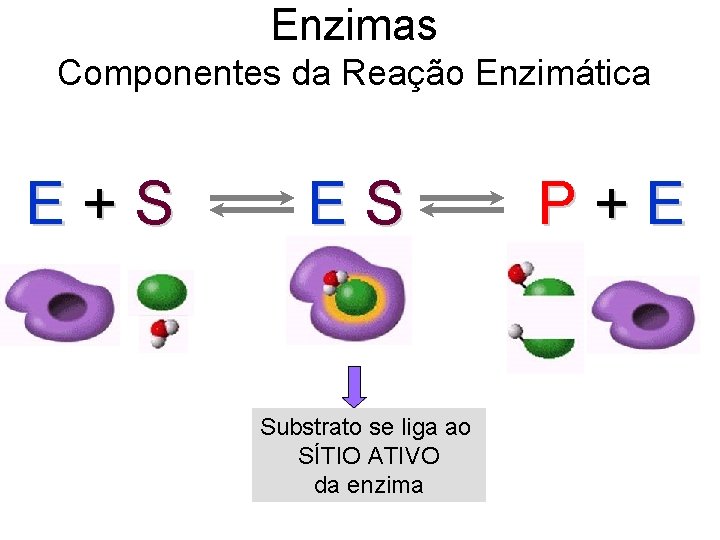
Enzimas Componentes da Reação Enzimática E+S ES Substrato se liga ao SÍTIO ATIVO da enzima P+E
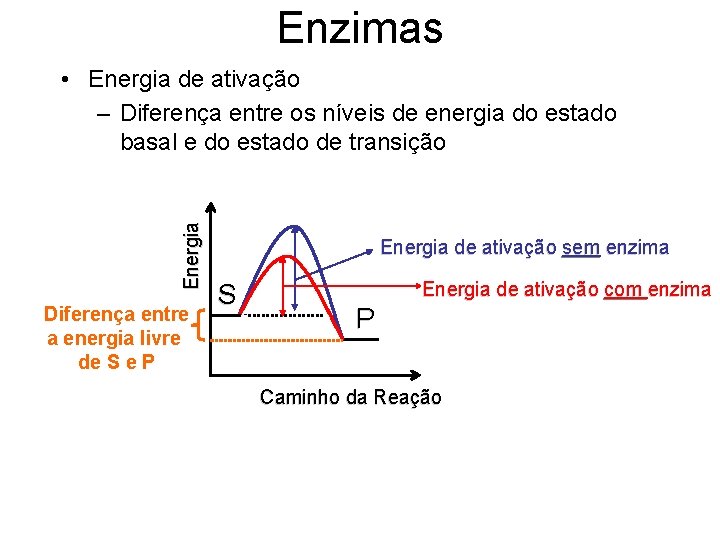
Enzimas Energia • Energia de ativação – Diferença entre os níveis de energia do estado basal e do estado de transição Diferença entre a energia livre de S e P Energia de ativação sem enzima S Energia de ativação com enzima P Caminho da Reação

Enzimas Ligação da Enzima ao Substrato
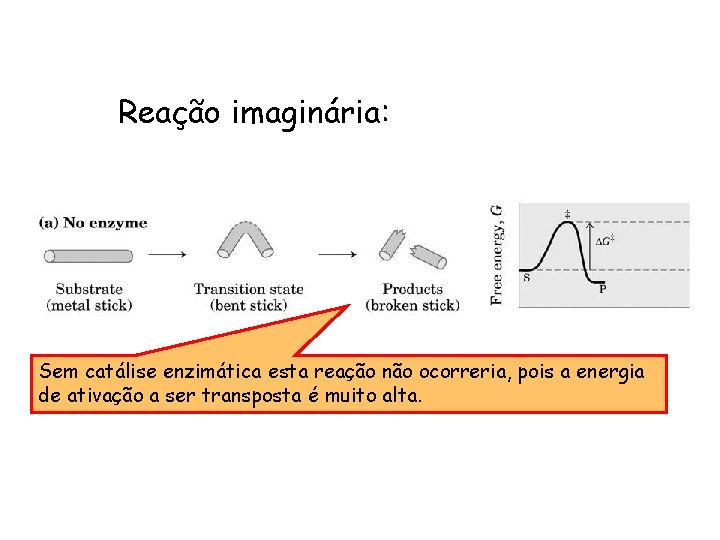
Reação imaginária: Sem catálise enzimática esta reação não ocorreria, pois a energia de ativação a ser transposta é muito alta.
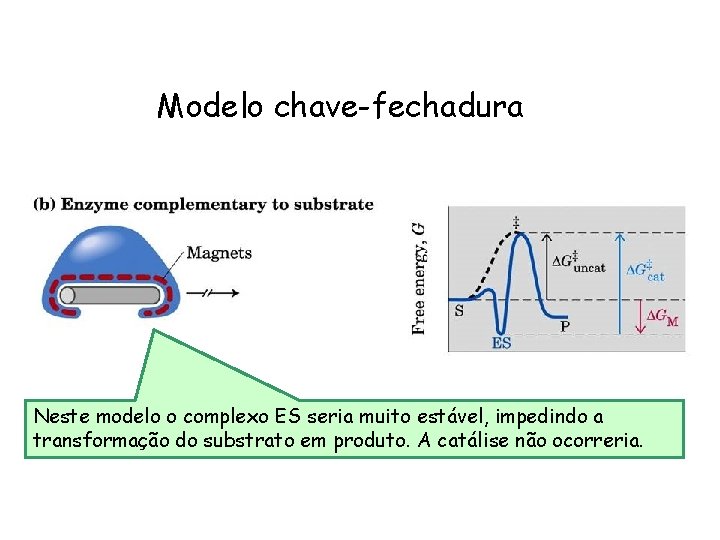
Modelo chave-fechadura Neste modelo o complexo ES seria muito estável, impedindo a transformação do substrato em produto. A catálise não ocorreria.
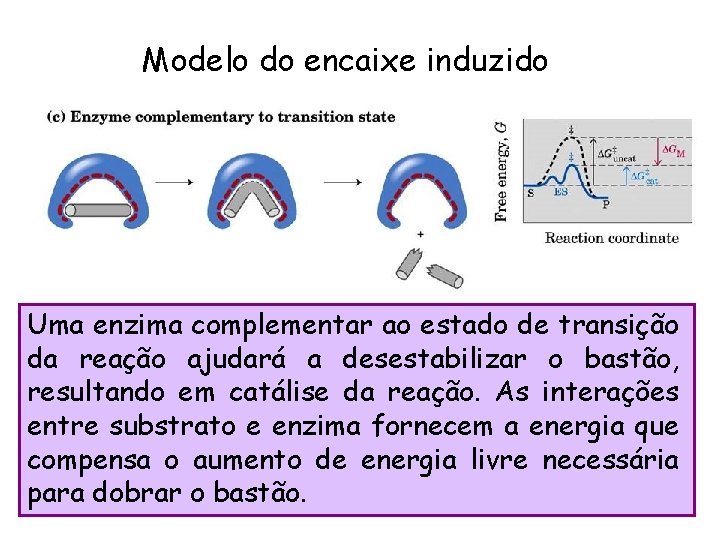
Modelo do encaixe induzido Uma enzima complementar ao estado de transição da reação ajudará a desestabilizar o bastão, resultando em catálise da reação. As interações entre substrato e enzima fornecem a energia que compensa o aumento de energia livre necessária para dobrar o bastão.

Modelo do encaixe induzido
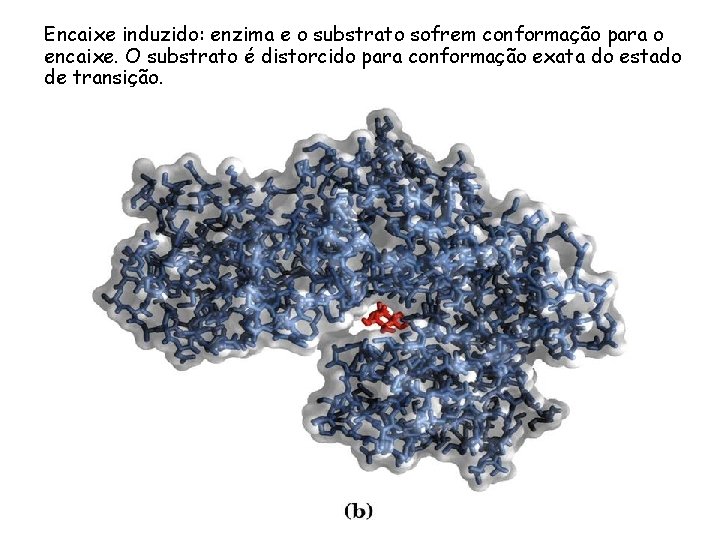
Encaixe induzido: enzima e o substrato sofrem conformação para o encaixe. O substrato é distorcido para conformação exata do estado de transição.
Sítio ativo Inúmeras interações fracas entre enzimas e substratos são formadas (pontes de hidrogênio, interações hidrofóbicas, pontes iônicas) A energia livre liberada pela formação destas interações parcialmente supre a energia para atingir o topo da colina energética. Esta mesma energia de ligação faz com que a enzima seja específica
- Slides: 29