ENZIM Mikchaell Panjaitan S Pi APA ITU ENZIM



































- Slides: 44

ENZIM Mikchaell Panjaitan S. Pi

APA ITU ENZIM ? • 1800 Pencernaan daging oleh sekresi lambung. Perubahan pati mjd gula oleh air liur • 1850 LOUIS PASTEUR. Fermentasi gula mjd alkohol oleh ragi dikatalis fermen dsb enzim (tdk dpt dipisahkan dr sel ragi hidup) • 1897 EDUARD BUCKNER. Berhasil mengekstrak bentuk aktif sel ragi yi enzim ferment gula mjd alkohol • 1926 Kristal urease ekstrak kacang tdr dari protein shg semua ensim adalah protein. Richard Willstatter (jerman) menentang kristal urease. Enzim adalah senyawa BM rendah. Kristal urease adalah cemaran • 1930 Isolasi proteolitik yaitu mengkristalan pepsin dan tripsin (keduanya protein).

DEFINISI ENSIM 1. Protein yang mempunyai daya katalitik spesifik 2. Protein pembeda non enzimatik katalis 3. Enzim adalah protein spesifik katalis reaksi biologis (dsb biokatalis)

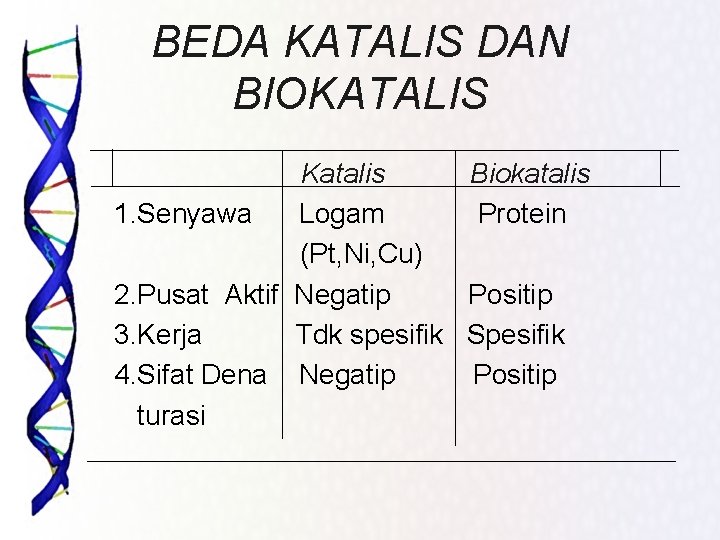
BEDA KATALIS DAN BIOKATALIS Katalis Biokatalis 1. Senyawa Logam Protein (Pt, Ni, Cu) 2. Pusat Aktif Negatip Positip 3. Kerja Tdk spesifik Spesifik 4. Sifat Dena Negatip Positip turasi

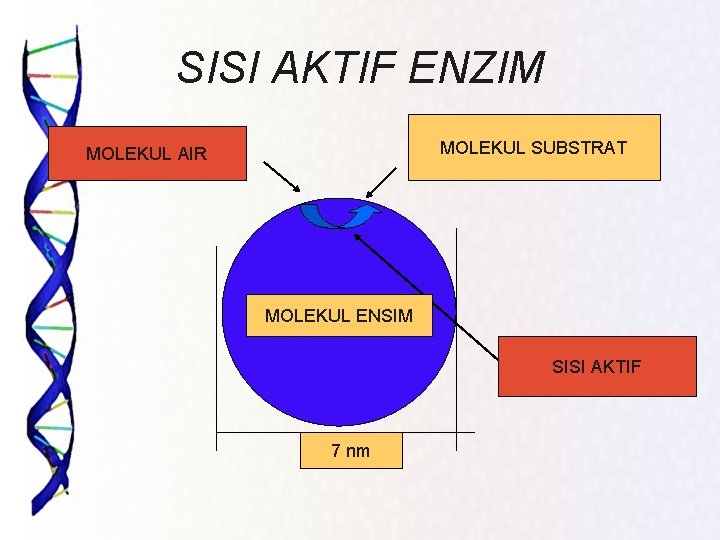
SISI AKTIF ENZIM MOLEKUL SUBSTRAT MOLEKUL AIR MOLEKUL ENSIM SISI AKTIF 7 nm

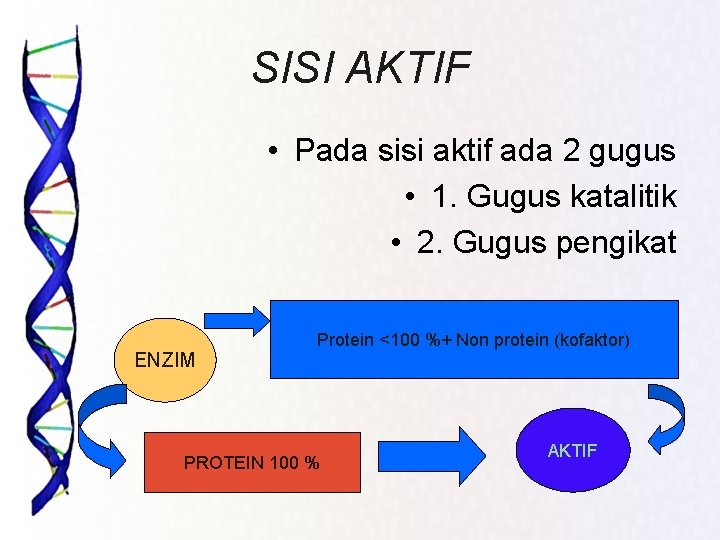
SISI AKTIF • Pada sisi aktif ada 2 gugus • 1. Gugus katalitik • 2. Gugus pengikat ENZIM Protein <100 %+ Non protein (kofaktor) PROTEIN 100 % AKTIF

RUMUS DASAR REAKSI ENZIMATIS • E+S ES + P • Sebelum melakukan katalitik • Enzim bergabung Substrat menjadi ES. • Tidak semua enzim dapat bergabung substrat tapi hanya pada satu sisi yi sisi aktip (tempat dimana E bergabung S)

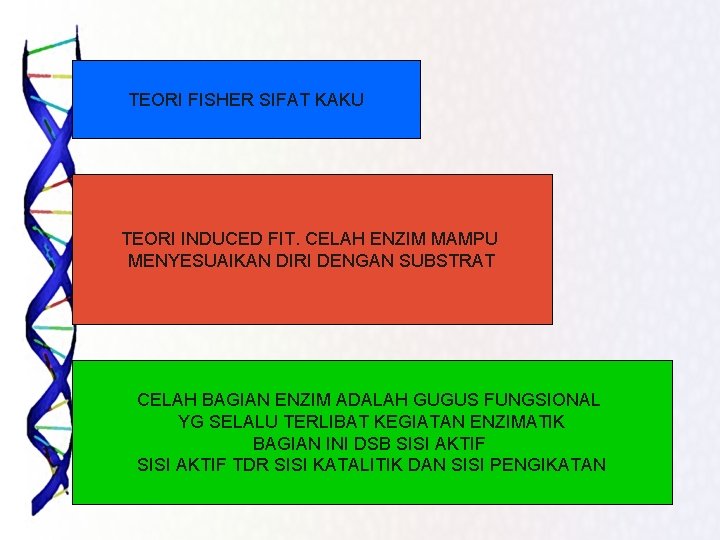
ENZIM 1. Hipotesis Emil Fisher 1894. Substrat dan ensim hrs cocok supaya enzim dpt mengubah substrat. Dikenal LOCK and KEY 2. KOAHLAND. Substrat masuk celah enzim mk bagian itu mengatur sendiri shg substrat cocok (terjadi perubahan geometrik pd protein enzim). Dikenal teori INDUCED FIT

TEORI FISHER SIFAT KAKU TEORI INDUCED FIT. CELAH ENZIM MAMPU MENYESUAIKAN DIRI DENGAN SUBSTRAT CELAH BAGIAN ENZIM ADALAH GUGUS FUNGSIONAL YG SELALU TERLIBAT KEGIATAN ENZIMATIK BAGIAN INI DSB SISI AKTIF TDR SISI KATALITIK DAN SISI PENGIKATAN

FAKTOR YG MEMPENGARUHI KECEPATAN REAKSI ENZIMATIK • • • 1. KADAR SUBSTRAT 2. KADAR ENZIM 3. PH 4. SUHU 5. ZAT PENGHAMBAT 6. AKTIVATOR

KEAKTIFAN ENZIM • 1. KUANTITATIF (LAJU REAKSI) • 2. KUALITATIF (REAKSI KIMIA DNG SUBSTRAT YG DPT DIKATALIS ENZIM TERSEBUT) • 3. SATUAN (UNIT ENZIM) ad jumlah enzim yg mampu mengkatalis perubahan 1 mikromol substrat per menit pada kondisi tertentu

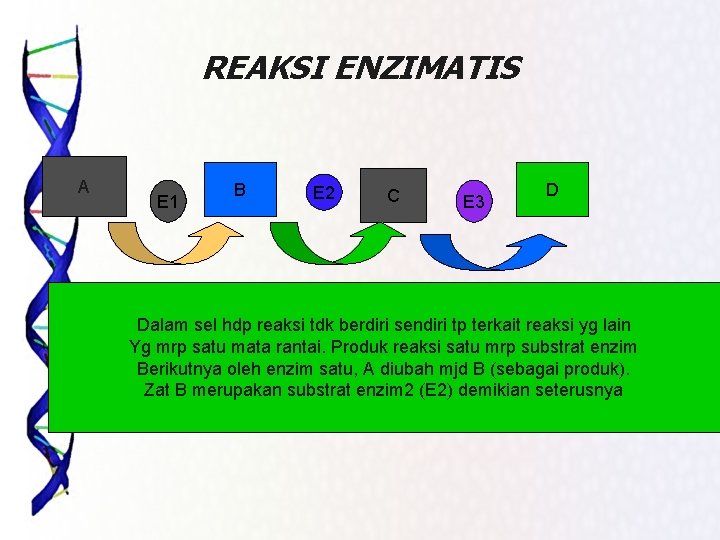
REAKSI ENZIMATIS A E 1 B E 2 C E 3 D Dalam sel hdp reaksi tdk berdiri sendiri tp terkait reaksi yg lain Yg mrp satu mata rantai. Produk reaksi satu mrp substrat enzim Berikutnya oleh enzim satu, A diubah mjd B (sebagai produk). Zat B merupakan substrat enzim 2 (E 2) demikian seterusnya

ENZIM 1. Adalah biokatalisator yg mampu meningkatkan kecepatan reaksi tanpa merubah tetapan seimbang 2. Katalitik bekerja jika ada kofaktor yg terdiri dari (gugus prostetik, koenzim, logam)

REAKSI BIOKIMIAWI ADA 6 MACAM • 1. OKSIDOREDUKSI Enzimnya dsb oksireduktase. Bernomor 1 Enzim ini mampu mengoksidasi atau mereduksi substrat dng memindahkan hidrogen atau elektron. • 2. TRANSFER Enzim yg menstransfer gugus selain hidrogen. Nomor dlm daftar 2

3. Hidrolisis • Enzim hidrolase • Reaksi ini terjadi lisis dng bantuan air • Nomor urut 3 4. Liasi Enzim Liase yg mhilangkan gugus dari substrat dan membentuk ikatan rangkap pada substrat. Enzim ini nomor urut 4.

5. ISOMERASI • Enzim isomerase • Enzim ini mempengaruhi isomer substrat • Nomor urut 5 6. LIGASI Ensim ligase. Enzim yg menggabungkan 2 mol substrat dng bantuan energi hidrolisis pirofosfat (ATP). Nomor urut 6

HIDROLASE DIBAGI SUB GOLONGAN • • • EC 3. 1 Bekerja pd ikatan ester EC 3. 2 Ikatan glikosidik EC 3. 3 Ikatan eter EC 3. 4 Ikatan peptida EC 3. 5 Ikatan C-N lain EC 3. 6 Ikatan asam anhidrida EC 3. 7 Ikatan C-C EC 3. 8 Ikatan halida EC 3. 9 Ikatan P-N

AMILASE • 1. ALFA AMILASE • 2. BETA AMILASE • 3. GLUKO AMILASE SUB GOLONGAN ENZIM YG MECAH IKATAN C-N PEPTIDA Contoh mecah protein dsb proteolitik

Enzim yg menghidrolisis ikatan peptida jika karboksil terminal bebas atau ggs NH 2 bebas • 1. Kelompok pertama dsb karboksipeptidase • 2. Kelompok kedua dsb aminopeptidase Keduanya msk EKSOPEPTIDASE HEWAN : TRIPSIN, PEPSIN, RENIN KHEMOTRIPSIN, KHATEPSIN. TUMBUHAN PAPAIN, BROMELIN, FICIN msk ENDOPEPTIDASE

Berdasarkan gugus fungsional sub gol enzim yg memecah ikatan peptida dibagi • • 1. Protease serina 2. Protease sulfhidril 3. Protease logam 4. Protease asam

PROTEASE SERINA • 1. Gugus aktif mgd serina • 2. Dihambat DIISOPROPIL FOSFOFLUORIDAT 3. Enzim yg termasuk khimotripsin, trombin, elastase, subtilisin. Semua termasuk endopeptidase

PROTEASE LOGAM • 1. Tdr Karboksipeptidase A, B Glisil-glisina dipeptidase, Karnosinase dan Leusina aminopeptidase 2. Termasuk eksopeptidase 3. Keaktifan tgt Logam Mg, Co, Fe, Hg, Ni, Zn 4. Dihambat oleh EDTA (ethylene diamine tetra acetic acid)

KARBOKSIPEPTIDASE A • 1. Semua Residu AA kecuali arginina, lisina, prolina • 2. Sisi aktip mengandung logam residu aa tirosil dan histidil KARBOKSIPEPTIDASE B Arginina atau lisina

PROTEASE ASAM • Tdr enzim pepsin dan rennin • p. H optimal pepsin (2) rennin (4) RENNIN • Rennin pd anak sapi yg msh menyusu dlm btk zimogen yi prorennin. Setelah dewasa tdk menyusu tdk lagi produksi rennin • p. H 3, 5 rennin autolisis • Rennin mantap p. H 5 • Rennin denaturasi p. H diatas 6

PEPSIN • • • 1. AA 321 2. BM 35000 3. ada 3 ikatan SS 4. ada 1 ikatan fosfat 5. Gugus fosfat terikat hidroksil Residu AA serina • 6. p. H optimal 2 • 7. Menghidrolisis C-N yg Nnya dimiliki Residu AA Fenilalanin, tirosin, triptofan.

UTK MENGETAHUI AKTIVITAS PROTEASE ASAM • 1. Protein sbg substrat (kasein, hemoglobin) yg didenaturasikan asam atau urea. Media reaksi TCA • Caranya Protein masuk TCA. Jk dimasuk enzim mk tjd hidrolisis protein oleh ensim. Jmlh peptida lrt TCA tgt kadar enzim dan wkt inkubasi. Perubahan dibaca 280 nm. • Selain TCA dpt dgnk ninhidrin utk mgt jum ikat peptida terhidrolisis ninhidrin bereaksi aa bebas memberi warna lembayung dibaca pada panjang gelombang 570 nm

2. Substrat sintetik • Mengandung ester, amida, atau ikatan peptida. Contoh ester nitrophenil • Hidrolisis ester ini dpt dibaca pada 400 nm pd p. H >7 • p. H <7 pada 340 nm • Senyawa yg digunakan N benzoil L arginina etil ester

CONTOH PROTEASE SERINA KHIMOTRIPSIN • 1. Mempunyai 246 residu AA • 2. Mempunyai 5 gugus aktif (N terminal AA Leusin 16, Residu aspartil 194, Residu aspartil 102, Residu seril 195 dan Residu histidil 57). 3. Dua ggs aktif pertama mengatur konformasi sisi aktif. 3 berikutnya sbg katalitik 4. Tdk semua peptida dipecah khimotripsin hanya aa aromatik (tirosin, fenilalanin, triptophan dan aa hidrofobik metionin

CONTOH PROTEIN SERINA TRIPSIN • 1. Diekstrak dari pankreas • 2. Bersifat endopeptidase • 3. Tripsin sapi terdiri dari 233 residu asam amino 4. Stabil pada p. H <6 5. p. H optimal 3 6. Pemecah ikatan peptida antara lisina dan arginina

CONTOH PROTEASE SERINA ELASTASE • 1. Menghidrolisis elastin yaitu jaringan ikat btk serabut otot leher • 2. Dibanding kolagen. elastin lebih tahan panas, asam, basa • 3. Diekstrak daripankreas dan mikroba • 4. Terdiri 240 Res aa • 5. Stabil p. H <6. • 6. p. H 8 autolisis • 7. Mampu mecah ikatan peptida nonaromatik yg tdk bercabang

PROTEASE SULFHIDRIL • 1. PAPAIN a. BM 23000 b. JUMLAH AA 211 c. ADA 3 IKATAN DISULFIDA d. ADA 2 GUGUS AKTIF sisteina 25 dan histidina 158 e. p. H optimal 6 dan 7, 5 f. Suhu stabil 70 o. C g. Kemantapan turun p. H <3 dan p. H>11 h. Bisa dari getah pepaya, daun, batang, bunga, buah i. Larut alkohol 70% j. Tdk stabil mdh teroksidasi

2. FICIN 3. BROMELIN • p. H optimal ketiga enzim 6 dan 7, 5 • Spesifikasi agak luas papain dan ficin dalam menghidrolisis substrat Residu AA L arginina, L lisina, glisina dan L sitrulina • Utk bir tahan dingin

ENZIM

• Enzim merupakan senyawa organik bermolekul besar yang berfungsi untuk mempercepat jalannya reaksi metabolisme di dalam tubuh tumbuhan tanpa mempengaruhi keseimbangan reaksi • Enzim tidak ikut bereaksi, struktur enzim tidak berubah baik sebelum dan sesudah reaksi tetap • Enzim sebagai biokatalisator • Bagian enzim yang aktif adalah sisi aktif dari enzim

Tata nama enzim • Enzim diberi nama sesuai dengan nama substrat dan reaksi yang dikatalisis • Biasanya ditambah akhiran ase • Enzim dibagi ke dalam 7 golongan besar

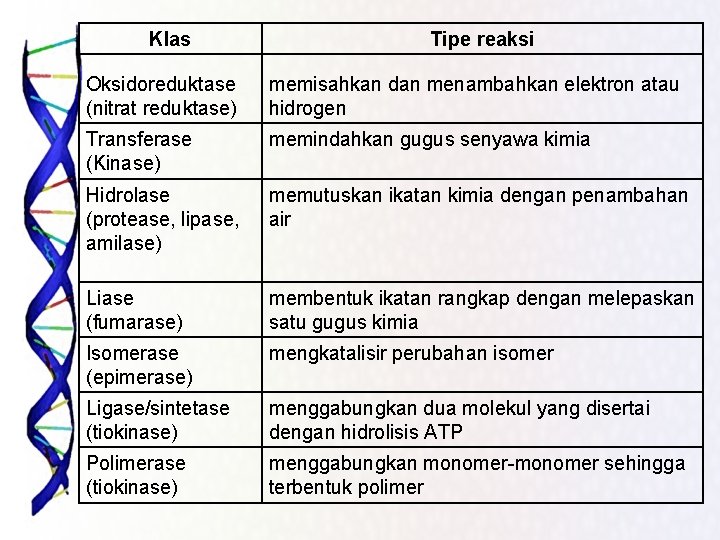
Klas Tipe reaksi Oksidoreduktase (nitrat reduktase) memisahkan dan menambahkan elektron atau hidrogen Transferase (Kinase) memindahkan gugus senyawa kimia Hidrolase (protease, lipase, amilase) memutuskan ikatan kimia dengan penambahan air Liase (fumarase) membentuk ikatan rangkap dengan melepaskan satu gugus kimia Isomerase (epimerase) mengkatalisir perubahan isomer Ligase/sintetase (tiokinase) menggabungkan dua molekul yang disertai dengan hidrolisis ATP Polimerase (tiokinase) menggabungkan monomer-monomer sehingga terbentuk polimer

Susunan enzim • Komponen utama enzim adalah protein • Protein yang sifatnya fungsional, bukan protein struktural • Tidak semua protein bertindak sebagai enzim

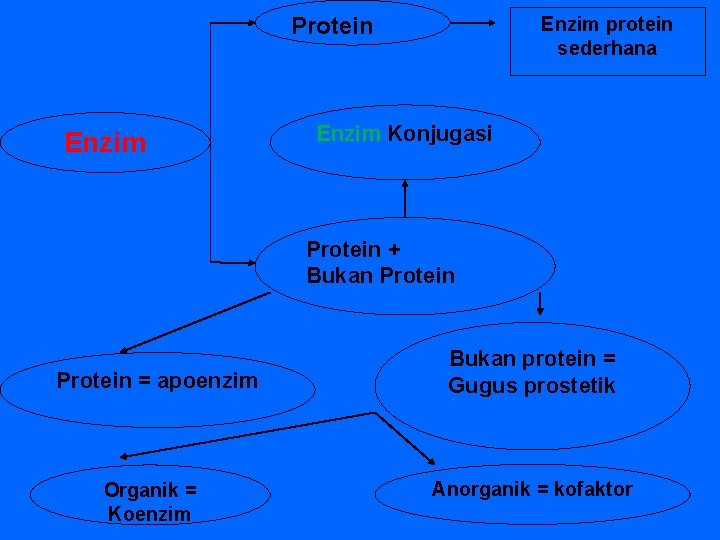
Protein Enzim protein sederhana Enzim Konjugasi Protein + Bukan Protein = apoenzim Organik = Koenzim Bukan protein = Gugus prostetik Anorganik = kofaktor

Contoh koenzim 1. 2. 3. 4. 5. 6. NAD (koenzim 1) NADP (koenzim 2) FMN dan FAD Cytokrom: cytokrom a, a 3, b, b 6, c, dan f Plastoquinon, plastosianin, feredoksin ATP: senyawa organik berenergi tinggi, mengandung 3 gugus P dan adenin ribose

Sifat enzim • Enzim dibentuk dalam protoplasma sel • Enzim beraktifitas di dalam sel tempat sintesisnya (disebut endoenzim) maupun di tempat yang lain diluar tempat sintesisnya (disebut eksoenzim) • Sebagian besar enzim bersifat endoenzim

1. 2. 3. 4. 5. 6. 7. 8. Enzim bersifat koloid, luas permukaan besar, bersifat hidrofil Dapat bereaksi dengan senyawa asam maupun basa, kation maupun anion Enzim sangat peka terhadap faktor-faktor yang menyebabkan denaturasi protein misalnya suhu, p. H dll Enzim dapat dipacu maupun dihambat aktifitasnya Enzim merupakan biokatalisator yang dalam jumlah sedikit memacu laju reaksi tanpa merubah keseimbangan reaksi Enzim tidak ikut terlibat dalam reaksi, struktur enzim tetap baik sebelum maupun setelah reaksi berlangsung Enzim bermolekul besar Enzim bersifat khas/spesifik

• Suhu: optimum 300 C, minimum 0 0 C, maksimum 40 • Logam, memacu aktifitas enzim: Mg, Mn, Co, Fe • Logam berat, menghambat aktivitas enzim: Pb, Cu, Zn, Cd, Ag • p. H, tergantung pada jenis enzimnya (pepsin aktif kondisi masam, amilase kondisi netral, tripsin kondisi basa) • Konsentrasi substrat, substrat yang banyak mula memacu aktifitas enzim, tetapi kemudian menghambat karena: penumpukan produk (feed back effect) • Konsentrasi enzim, peningkatan konsentrasi enzim memacu aktifitasnya • Air, memacu aktifitas enzim • Vitamin, memacu aktifitas enzim

Penghambatan aktifitas enzim ada dua tipe: 1. Kompetitif: zat penghambat mempunyai struktur yang mirip dengan substrat sehingga dapat bergabung dengan sisi aktif enzim. Terjadi kompetisi antara substrat dengan inhibitor untuk bergabung dengan sisi aktif enzim (misal feed back effect) 2. Non kompetitif: zat penghambat menyebabkan struktur enzim rusak sehingga sisi aktifnya tidak cocok lagi dengan substrat

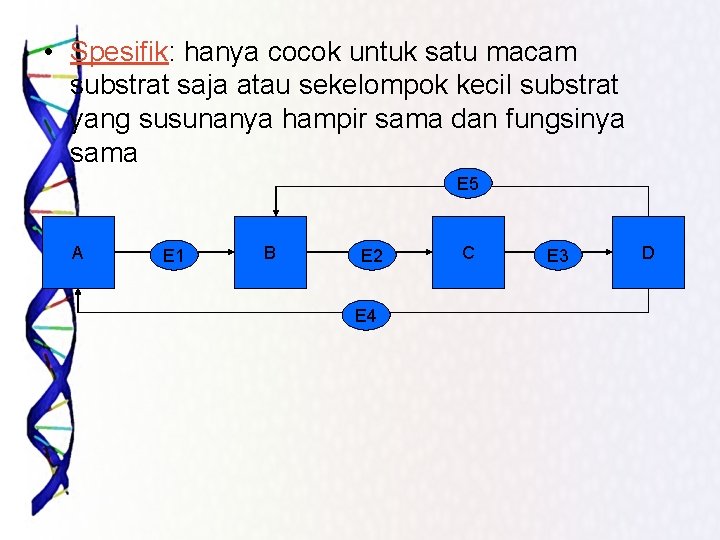
• Spesifik: hanya cocok untuk satu macam substrat saja atau sekelompok kecil substrat yang susunanya hampir sama dan fungsinya sama E 5 A E 1 B E 2 E 4 C E 3 D