ENZIM 15 November 2017 Enzim Enzim adalah katalis

ENZIM 15 November 2017

Enzim • Enzim adalah katalis biologis yang berfungsi menurunkan kebutuhan energi aktivasi sehingga dapat mempercepat reaksi. • Enzim merupakan biokatalisator, yaitu bahan yang mempercepat laju reaksi, namun tidak ikut serta dalam reaksi.

Ciri-Ciri Enzim a. b. c. d. e. f. Biokatalisator Protein Bekerja secara khusus Rusak oleh panas Tidak ikut bereaksi Kerjanya dipengaruhi faktor lingkungan, misalnya suhu, p. H, inhibitor dan aktivator.
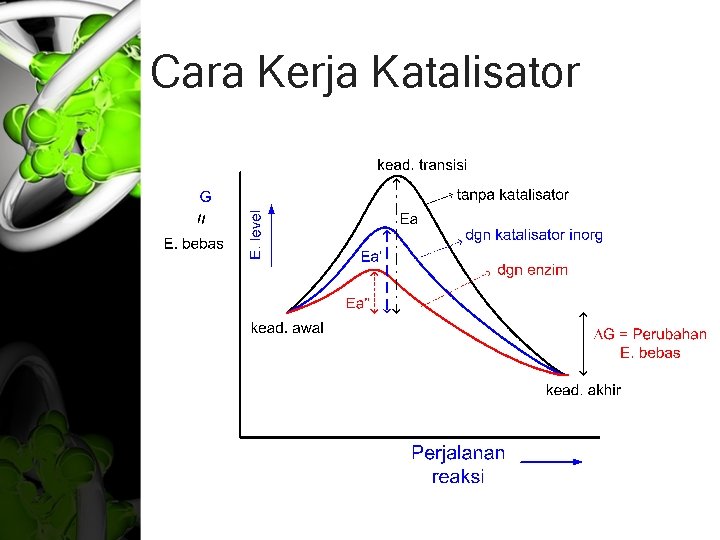
Cara Kerja Katalisator

Cara Kerja Katalisator • KESIMPULAN : * katalisator menurunkan energi aktivasi * enzim menurunkan energi aktivasi lebih banyak • Ea = ENERGI AKTIVASI : jumlah energi yang diperlukan untuk membawa semua molekul dalam 1 mole bahan pada suatu suhu tertentu dari keadaan awal menuju keadaan transisi • ΔG = Perubahan energi bebas

Enzim Bereaksi Spesifik • Artinya : suatu enzim hanya dapat bereaksi dengan substrat tertentu atau pada sejumlah senyawa sejenis Contoh: Laktosa (substrat) Laktase (enzim) glukosa + galaktosa (produk)

Tata Nama Enzim • Nama enzim terdiri dari 2 bagian Bagian 1 nama substrat + ase : - maltase - urease Bagian 2 jenis reaksi + ase : - transferase - hidrogenase • Menurut IUBMB, enzim dibagi dalam 6 kelas utama

Tata Nama Enzim Contoh: - Enzim selulase yang menguraikan selulosa, - Enzim lipase yang menguraikan lipid atau lemak, dan - Enzim protease yang menguraikan protein.

Tata Nama Enzim Kelas Tipe reaksi Oksidoreduktase (nitrat reduktase) memisahkan dan menambahkan elektron atau hidrogen Transferase (Kinase) memindahkan gugus senyawa kimia Hidrolase memutuskan ikatan kimia dengan (protease, lipase, penambahan air amilase) Liase (fumarase) membentuk ikatan rangkap dengan melepaskan satu gugus kimia Isomerase (epimerase) mengkatalisir perubahan isomer Ligase/sintetase (tiokinase) menggabungkan dua molekul yang disertai dengan hidrolisis ATP
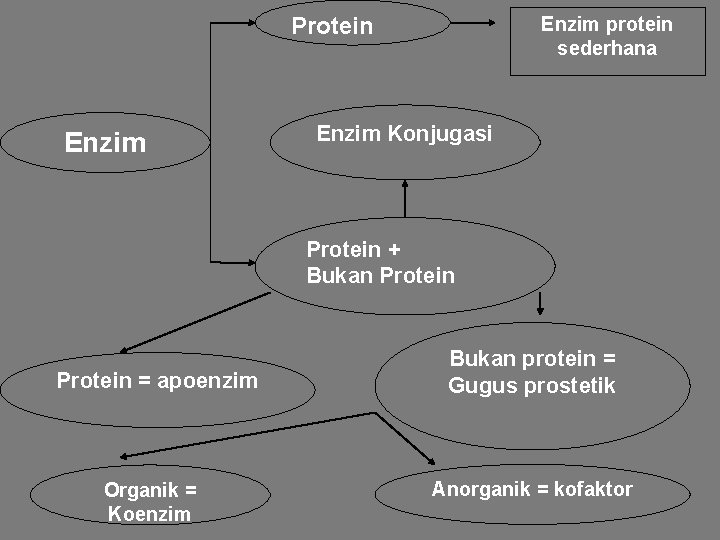
Protein Enzim protein sederhana Enzim Konjugasi Protein + Bukan Protein = apoenzim Organik = Koenzim Bukan protein = Gugus prostetik Anorganik = kofaktor

Struktur Enzim lengkap (holoenzim) tersusun atas 2 bagian, yaitu: a. Bagian protein (apoenzim): - tersusun atas asam-asam amino, - Bersifat labil, misalnya karena suhu dan keasaman. b. Gugus prostetik (gugusan yang aktif): - Berasal dari molekul anorganik (kofaktor), misalnya Fe, Cu dan Zn. - Berasal dari senyawa organik kompleks (koenzim), misalnya NADH, FADH dan tiamin.

Kofaktor • Sejumlah enzim masih perlu senyawa lain yg bukan protein agar dapat melaksanakan fungsi katalitiknya perlu kofaktor • Enzim sederhana protein saja Enzim yg lebih kompleks protein + kofaktor • Kofaktor logam senyawa organik nonprotein yang spesifik • Ikatan enzim + kofaktor : ada yg kuat (kovalen) ada yang lemah
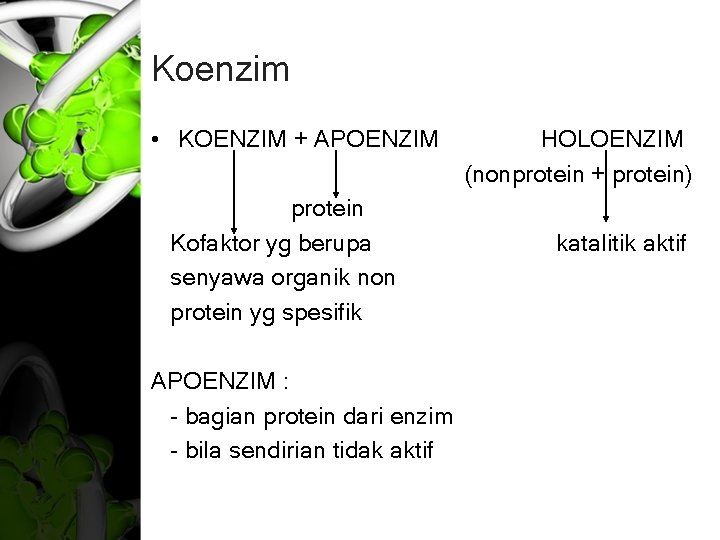
Koenzim • KOENZIM + APOENZIM protein Kofaktor yg berupa senyawa organik non protein yg spesifik APOENZIM : - bagian protein dari enzim - bila sendirian tidak aktif HOLOENZIM (nonprotein + protein) katalitik aktif

Koenzim • Ikatan enzim + koenzim * kuat membentuk gugus prostetik * lemah membentuk kosubstrat • Fungsi koenzim : sebagai zat perantara pembawa : gugus-gugus, atom-atom dan elektron-elektron yg dipindahkan dalam reaksi enzimatik • Contoh : 1. Pembawa atom H NAD, NADP, FMN, Ko. Q 2. Pembawa elektron heme, NHI 3. Pembawa gugus fosfat ATP 4. Pembawa gugus aldehid TPP

Mekanisme Kerja Enzim • Enzim adalah suatu protein yg tersusun dari asam amino • Asam amino dalam larutan selalu berbentuk ion tergantung p. H larutan • Rumus umum asam amino : R – COOH NH 2 • Aktivitas katalitik enzim erat hubungannya dengan struktur enzim (protein)
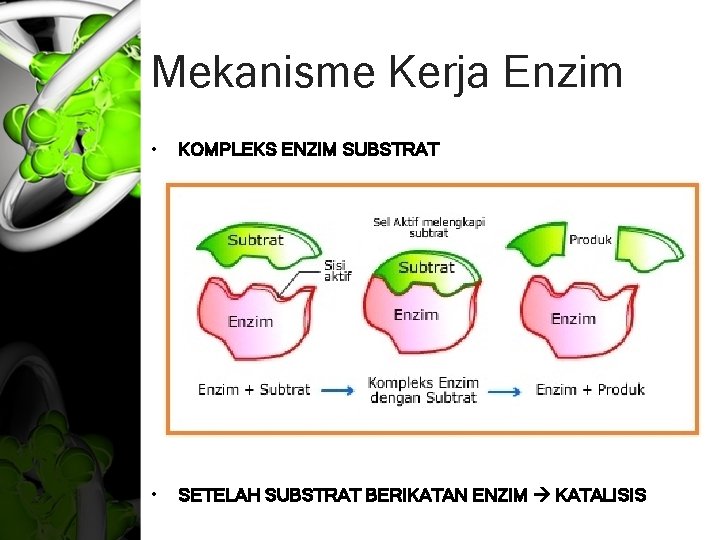
Mekanisme Kerja Enzim • KOMPLEKS ENZIM SUBSTRAT • SETELAH SUBSTRAT BERIKATAN ENZIM KATALISIS
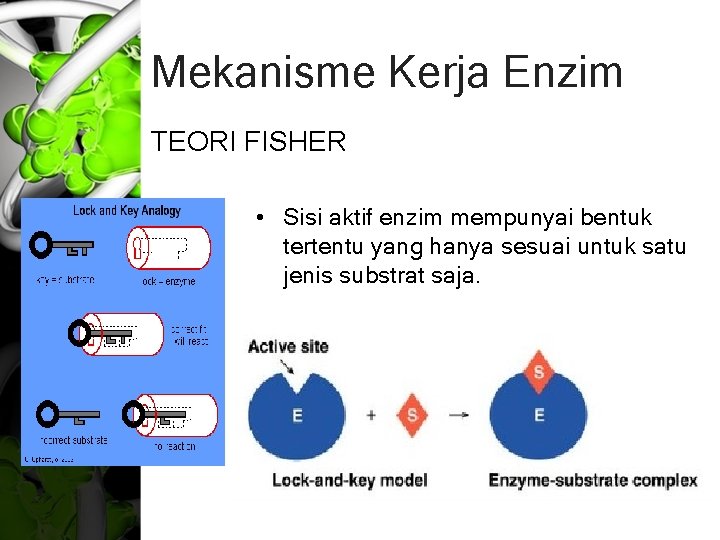
Mekanisme Kerja Enzim TEORI FISHER • Sisi aktif enzim mempunyai bentuk tertentu yang hanya sesuai untuk satu jenis substrat saja.
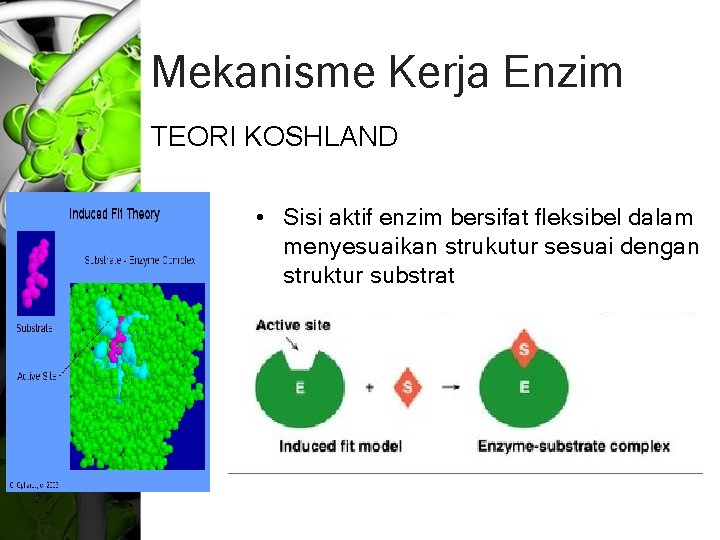
Mekanisme Kerja Enzim TEORI KOSHLAND • Sisi aktif enzim bersifat fleksibel dalam menyesuaikan strukutur sesuai dengan struktur substrat

Faktor yang Mempengaruhi Aktivitas Enzim 1. Kadar enzim 2. Kadar substrat 3. Inhibitor 4. p. H 5. Suhu

Konsentrasi Substrat • Seiring dengan meningkatnya konsentrasi substrat, kecepatan reaksi juga akan meningkat akibat makin cepatnya substrat terikat pada enzim. • Kecepatan reaksi ini akan terus meningkat hingga dicapai titik jenuh, dimana seluruh situs aktif dari enzim telah terikat secara konstan pada substrat. • Peningkatan konsentrasi substrat pada titik jenuh ini tidak lagi dapat meningkatkan kecepatan laju reaksi.
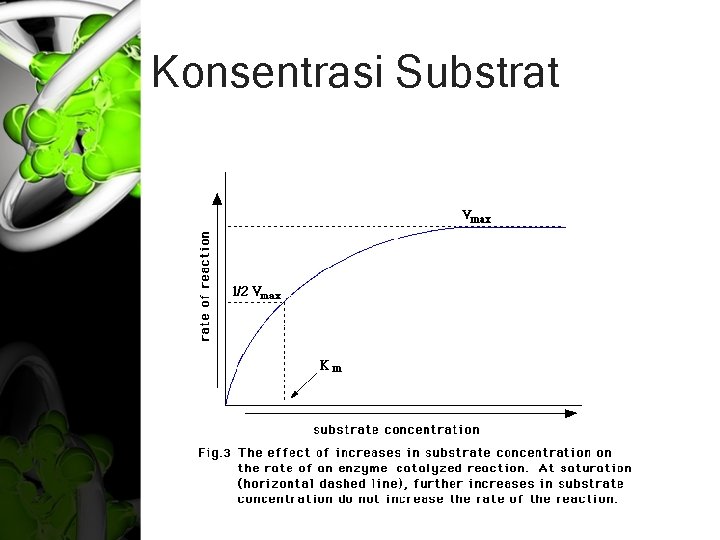
Konsentrasi Substrat

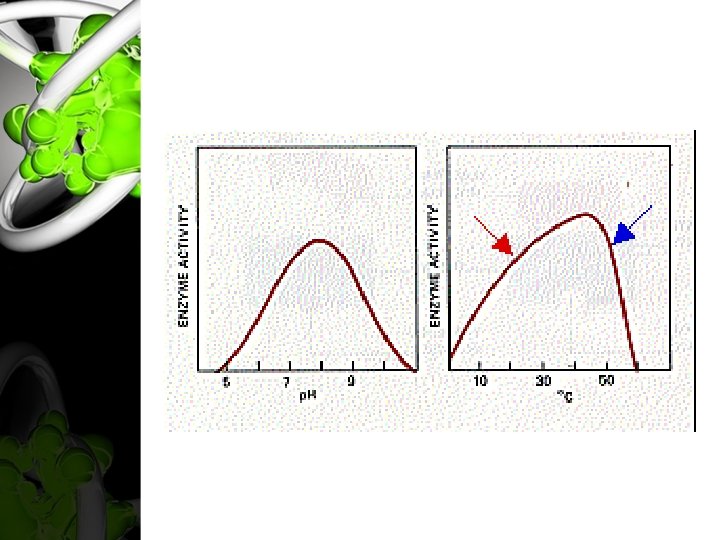
Pengaruh Suhu • Enzim memerlukan jumlah panas tertentu untuk dapat aktif. • Semakin meningkatnya suhu, makin meningkat pula aktivitas enzim. • Secara umum, tiap peningkatan sebesar 10°C di atas temperatur minimum, aktivitas enzim akan meningkat 2 x lipat. • Peningkatan temperatur di atas titik optimum akan menyebabkan lemahnya ikatan di dalam enzim, sehingga menyebabkan kerusakan enzim secara struktural. Akibatnya fungsi katalis enzim juga menurun. • Pada temperatur maks, enzim akan terdenaturasi & tidak berfungsi lagi dalam mengkatalisis reaksi.

Pengaruh p. H • p. H optimal enzim adalah sekitar p. H 7 (netral) dan jika medium menjadi sangat asam atau sangat alkalis enzim mengalami inaktivasi. Akan tetapi beberapa enzim hanya beroperasi dalam keadaan asam atau alkalis. Sebagai contoh, pepsin, enzim yang dikeluarkan ke lambung, hanya dapat berfungsi dalam kondisi asam, dengan p. H optimal 2 (Gaman & Sherrington, 1994). • Enzim memiliki konstanta disosiasi pada gugus asam ataupun gugus basa terutama pada residu terminal karboksil dan asam aminonya. Namun dalam suatu reaksi kimia, p. H untuk suatu enzim tidak boleh terlalu asam maupun terlalu basa karena akan menurunkan kecepatan reaksi dengan terjadinya denaturasi. Sebenarnya enzim juga memiliki p. H optimum tertentu, pada umumnya sekitar 4, 5– 8, dan pada kisaran p. H tersebut enzim mempunyai kestabilan yang tinggi (Williamson & Fieser, 1992).

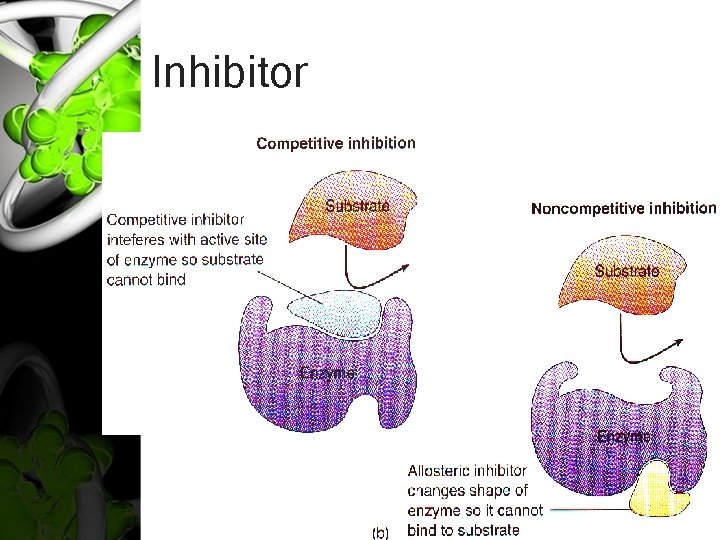
Inhibitor – – Adalah zat yang dapat menghambat kerja enzim. Dibedakan berdasarkan sifatnya, a. l: a. Inhibitor reversibel, yaitu tidak berikatan kuat dengan enzim. Macamnya: 1) Inhibitor kompetitif - Inhibitor menempati sisi aktif enzim sehingga substrat tidak dapat masuk. - Terjadi kompetisi antara substrat dengan inhibitor untuk bergabung dengan sisi aktif enzim (misal feed back effect) 2). Inhibitor non kompetitif - Tidak mirip dengan substrat dan berikatan pada sisi selain sisi aktif konformasi enzim berubah
Inhibitor

Inhibitor b. Inhibitor irreversibel: - Berikatan dengan sisi aktif enzim secara kuat sehingga tidak dapat terlepas. - Enzim menjadi tidak aktif dan tidak dapat kembali seperti semula (irreversibel).

- Slides: 29