Entropia Estatstica e o Ensino da 2 Lei
















































































- Slides: 127

Entropia Estatística e o Ensino da 2ª Lei da Termodinâmica Carlos Eduardo Aguiar Programa de Pós-Graduação em Ensino de Física Instituto de Física - UFRJ VII EEEFis – UFRGS Porto Alegre, agosto de 2017

Baseado na dissertação de mestrado de Marcos Moura “Entropia Estatística e o Ensino da 2ª Lei da Termodinâmica” Mestrado Nacional Profissional em Ensino de Física Instituto de Física - UFRJ, 2016

Sumário • Ensino e aprendizagem da segunda lei da termodinâmica • Entropia e a segunda lei da termodinâmica: uma sequência didática 1. 2. 3. 4. 5. A seta do tempo Entropia, energia e temperatura Entropia, volume e pressão Equação de estado de sistemas ideais A distribuição de Boltzmann • Comentários finais

Ensino e Aprendizagem da Segunda Lei da Termodinâmica

Os Fatos da Vida “Agora, na segunda lei da termodinâmica. . . ”

Nenhuma outra lei científica contribuiu mais para a liberação do espírito humano que a segunda lei da termodinâmica. Ela é a base para a compreensão do motivo de qualquer mudança ocorrer. P. Atkins, Four Laws that Drive the Universe

Entropia e a 2ª Lei da Termodinâmica • Temas fundamentais para a compreensão de boa parte da física, química e biologia. • “Não conhecer a 2ª lei da termodinâmica equivale a nunca ter lido um trabalho de Shakespeare” (C. P. Snow, The Two Cultures) • “Na verdade eu tenho sérias dúvidas sobre se Snow entendia a 2ª lei, mas concordo com seus sentimentos” (P. Atkins, Four Laws that Drive the Universe)

Entropia e a 2ª Lei da Termodinâmica • “Termodinâmica é algo que alguma outra pessoa certamentende. ” (opinião de muitos estudantes de Física, segundo E. Lieb e J. Yngvason) • “Ninguém sabe o que é entropia, de modo que você sempre terá a vantagem em um debate. ” (conselho de J. von Neumann a C. Shannon)

Entropia e a 2ª Lei da Termodinâmica • “A termodinâmica é uma ciência com fundamentos seguros e definições claras. ” (J. C. Maxwell) • “Todo matemático sabe que é impossível entender um curso elementar de termodinâmica. ” (V. I. Arnold)

As leis da termodinâmica no ensino superior • • • Equilíbrio. Lei Zero. Temperatura e termômetros. Trabalho adiabático. Energia interna: ∆U = ‒W(adiab. ) Calor e a 1ª lei da termodinâmica: ∆U = Q ‒ W Processos termodinâmicos. Máquinas térmicas. Eficiência. 2ª lei da termodinâmica: formulações de Kelvin e Clausius. Irreversibilidade. Teorema de Carnot. Definição termodinâmica de temperatura. Teorema de Clausius. Entropia. Formulação entrópica da 2ª lei: ∆S ≥ 0 num sistema isolado. Por exemplo: Nussenzweig, Física Básica; Zemansky & Dittman, Heat and Thermodynamics

As leis da termodinâmica no ensino médio • • • Temperatura e termômetros. Calor: transferência de energia por diferença de temperatura. Trabalho e a 1ª lei da termodinâmica: ∆U = Q ‒ W Processos termodinâmicos. Máquinas térmicas. Eficiência. 2ª lei da termodinâmica: formulações de Kelvin e Clausius. Irreversibilidade e noções sobre entropia. Por exemplo: Máximo & Alvarenga, Curso de Física; Hewitt, Conceptual Physics

Aprendizagem da 2ª lei da termodinâmica Dificuldades comuns entre os estudantes: • Não tratar a entropia como função de estado; por exemplo, tomar S ≠ 0 em um ciclo. • Considerar que a entropia é uma grandeza conservada. • Confundir sistema e universo e supor que entropia do sistema nunca diminui. • Não utilizar a 2ª lei para determinar se um dado processo pode ocorrer; usar apenas a 1ª lei.

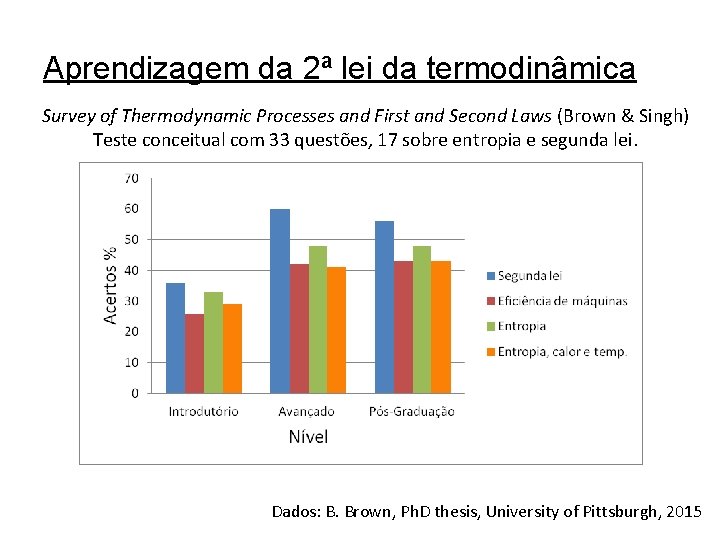
Aprendizagem da 2ª lei da termodinâmica Survey of Thermodynamic Processes and First and Second Laws (Brown & Singh) Teste conceitual com 33 questões, 17 sobre entropia e segunda lei. Dados: B. Brown, Ph. D thesis, University of Pittsburgh, 2015

Problemas da abordagem tradicional • Pouco atraente; boa parte dos alunos não demonstra interesse por máquinas térmicas. • Entropia, o conceito central, só aparece após um longo e tortuoso processo. • Ao final desse processo temos uma definição de entropia, mas não uma interpretação intuitiva do conceito e da origem da irreversibilidade.

Problemas da abordagem tradicional É um eufemismo dizer que os estudantes têm dificuldades com a abordagem tradicional [da definição de entropia]. Os argumentos que levam a ela são sutis e sofisticados e o resultado final, d. S = d. Qrev / T, não tem um significado físico evidente. Mais ainda, como a entropia pode mudar em processos irreversíveis mesmo quando d. Q = 0, essa definição gera uma confusão considerável. Harvey Leff, Am. J. Phys. 64, 1261 (1996)

É possível fazer melhor? • Abordagem diferente da tradicional (Carnot. Kelvin-Clausius), mas ainda macroscópica. Por exemplo, o enfoque axiomático de H. Callen em Thermodynamics and an Introduction to Thermostatistics (Wiley, 1985), talvez o livro de termodinâmica mais citado na literatura em física. • Abordagem microscópica (estatística). Entropia definida pelo número de estados microscópicos compatíveis com o estado termodinâmico. Explicação estatística da irreversibilidade.

Abordagem microscópica: “Física Térmica” • F. Reif, Fundamentals of Statistical and Thermal Physics (Mc. Graw-Hill, 1965). • C. Kittel, H. Kroemer, Thermal Physics (Freeman, 1997). • R. Bairlein, Thermal Physics (Cambridge U. P. , 1999). • D. V. Schroeder, An Introduction to Thermal Physics (Addison-Wesley, 2000).

Física Térmica nos cursos básicos • F. Reif, Statistical Physics, Berkeley Physics Course v. 5 (Mcgraw-Hill, 1967) • R. Chabay, B. Sherwood, Matter & Interactions (Wiley, 2015)

Referências • F. Reif, Thermal physics in the introductory physics course: Why and how to teach it from a unified atomic perspective, Am. J. Phys. , p. 1051 (1999). • R. Baierlein, Entropy and the second law: A pedagogical alternative, Am. J. Phys. 62, p. 15 (1994). • T. A. Moore, D. V. Schroeder, A different approach to introducing statistical mechanics, Am. J. Phys. 65, p. 26 (1997). • R. W. Chabay, B. A. Sherwood, Bringing atoms into firstyear physics, Am. J. Phys. 67, p. 1045 (1999).

Física Térmica no ensino médio Mesmo os textos mais recentes mencionam a definição estatística da entropia apenas ao final da apresentação da 2ª lei (quando o fazem).

Entropia e a Segunda Lei da Termodinâmica _______ Uma Sequência Didática

“A culpa é da entropia. ”

Características da sequência didática • O ponto de partida é a seta do tempo, um tema mais atraente que máquinas térmicas. • O conceito de entropia é introduzido logo ao início da sequência. • A definição estatística fornece diretamente uma interpretação intuitiva da entropia (contagem). • A irreversibilidade tem uma explicação simples. • A entropia é reconhecida facilmente como função de estado.

Características da sequência didática • Os principais resultados associados à 2ª lei são obtidos com facilidade: – Formulações de Clausius e Kelvin. – Teorema de Carnot. – Desigualdade de Clausius. – Definição clássica (não-estatística) de entropia. • Pode-se ir além da termodinâmica clássica: – Equação de estado de sistemas simples. – Distribuição de Boltzmann

Pré-requisitos: • Conceitos de equilíbrio, temperatura e calor. • Trabalho, energia e a 1ª lei da termodinâmica. • Variáveis de estado e de processo • Gases ideais • Um pouco de análise combinatória Podem ser reduzidos à conservação da energia numa versão simplificada da sequência.

A Seta do Tempo

O tempo acaba o ano, o mês e a hora, a força, a arte, a manha, a fortaleza; o tempo acaba a fama e a riqueza, o tempo o mesmo tempo de si chora. Luís de Camões

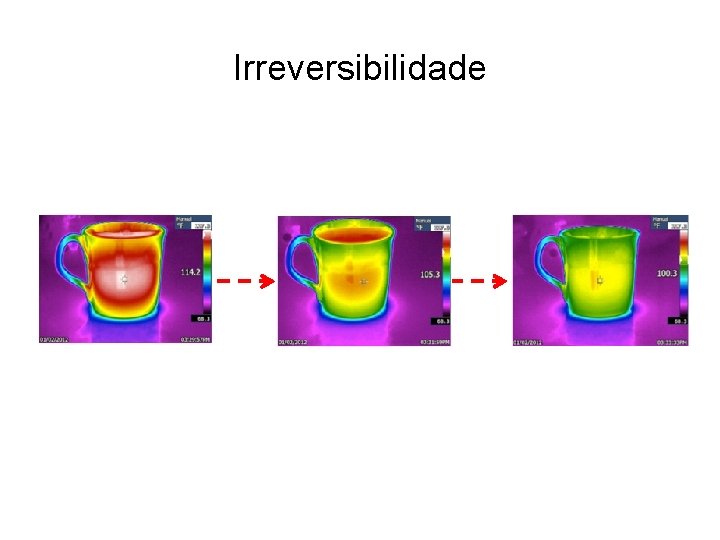
Irreversibilidade

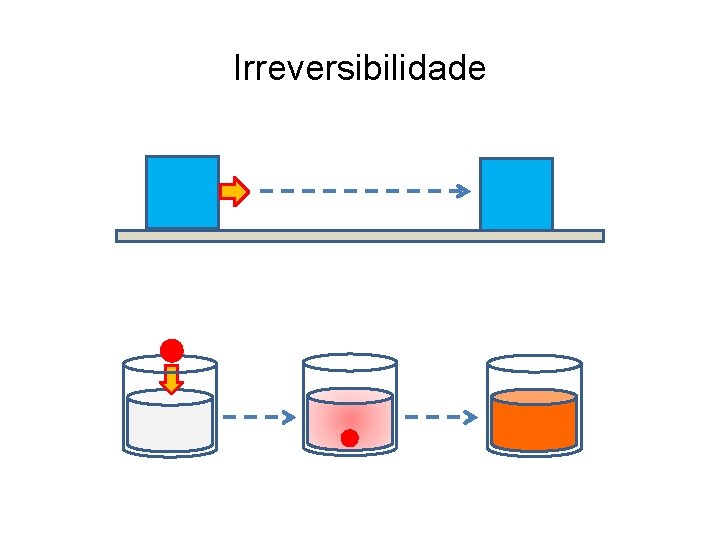
Irreversibilidade

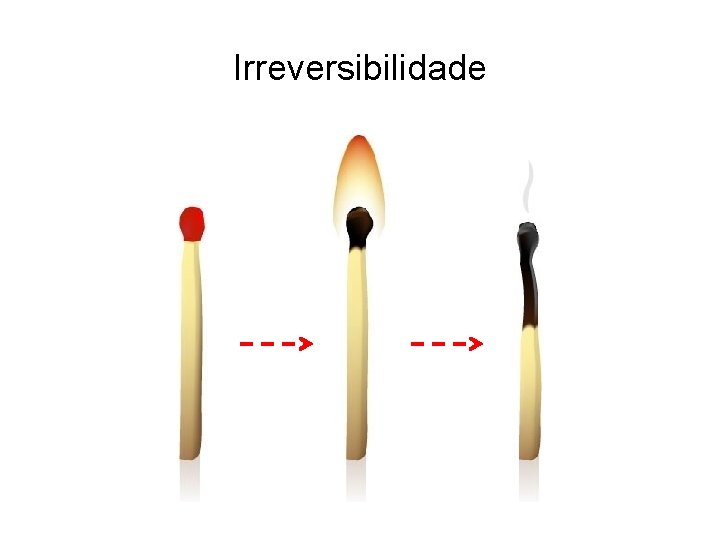
Irreversibilidade

Irreversibilidade Os processos cotidianos são irreversíveis; eles não ocorrem espontaneamente na ordem temporal reversa.

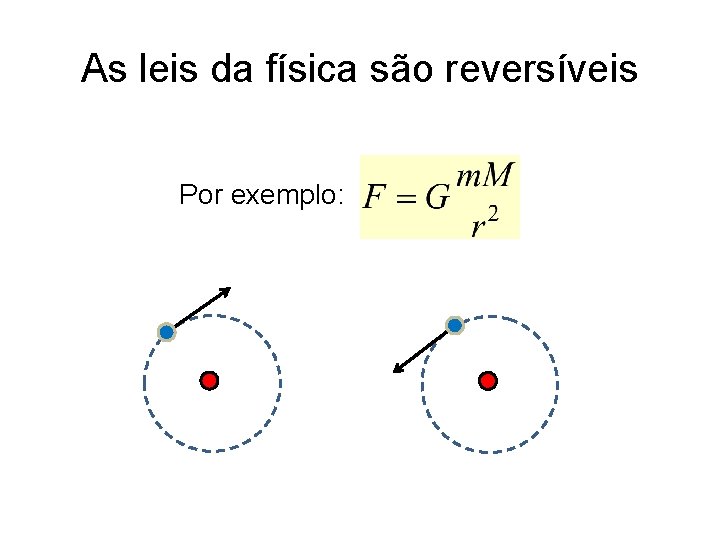
Pergunta: Qual lei dinâmica (microscópica) da física determina um sentido para a passagem do tempo? Resposta: Nenhuma. As leis físicas fundamentais não distinguem passado de futuro. Há uma exceção: a interação fraca viola a simetria de inversão temporal.

As leis da física são reversíveis Por exemplo:

As leis fundamentais da física não distinguem passado de futuro. mas. . . As transformações à nossa volta são irreversíveis.

Ludwig Boltzmann

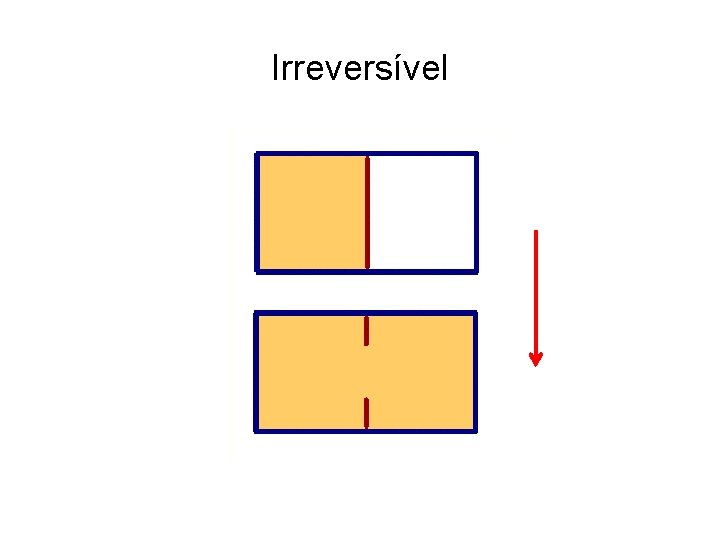
Irreversível

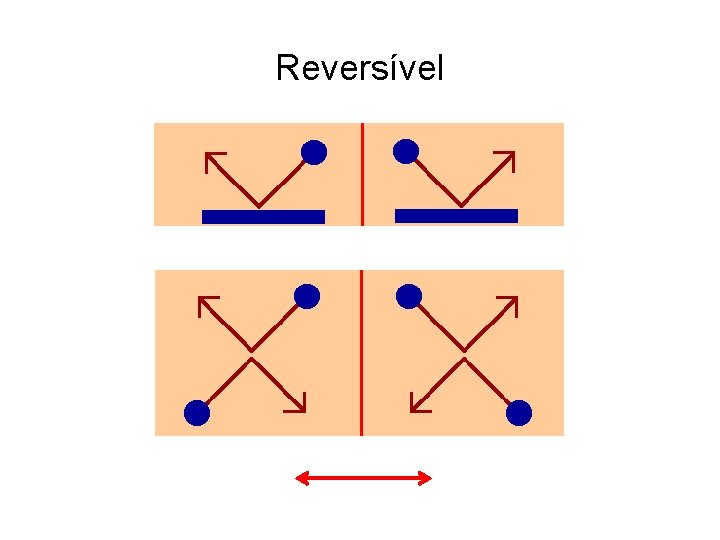
Reversível

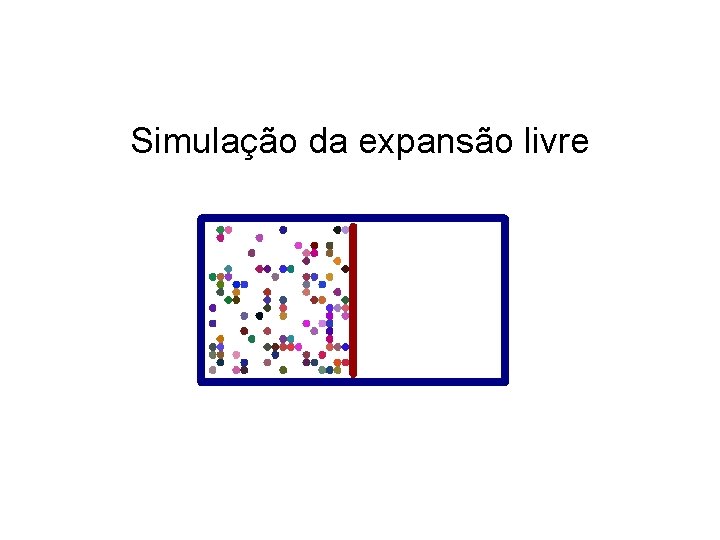
Simulação da expansão livre

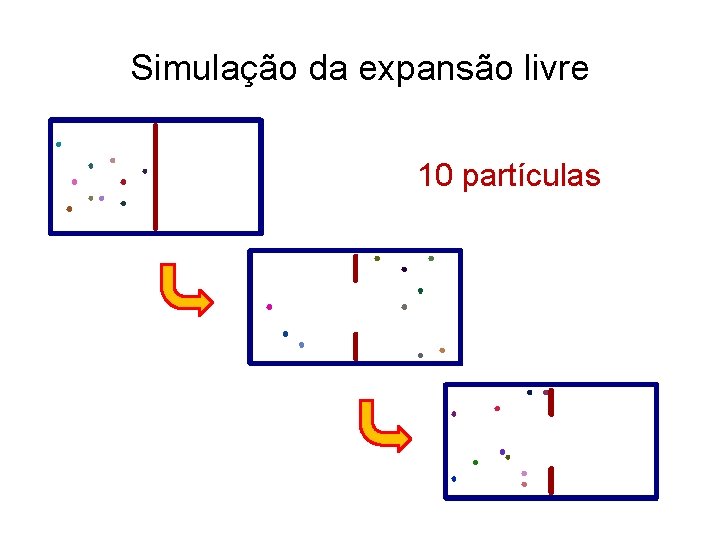
Simulação da expansão livre 10 partículas

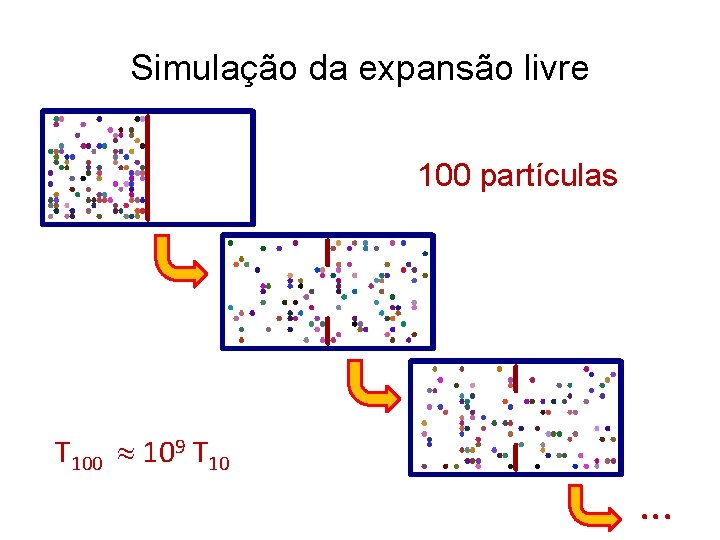
Simulação da expansão livre 100 partículas T 100 109 T 10 . . .

A seta do tempo (irreversibilidade) surge quando o número de partículas é grande! Por quê?

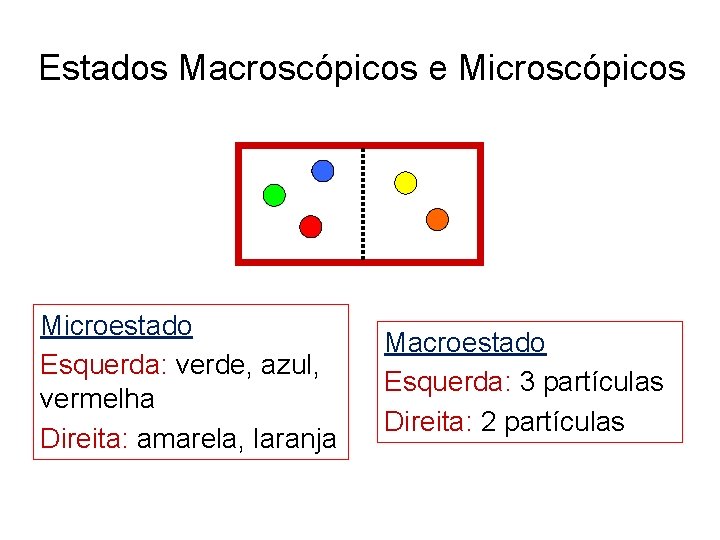
Estados Macroscópicos e Microscópicos Microestado Esquerda: verde, azul, vermelha Direita: amarela, laranja Macroestado Esquerda: 3 partículas Direita: 2 partículas

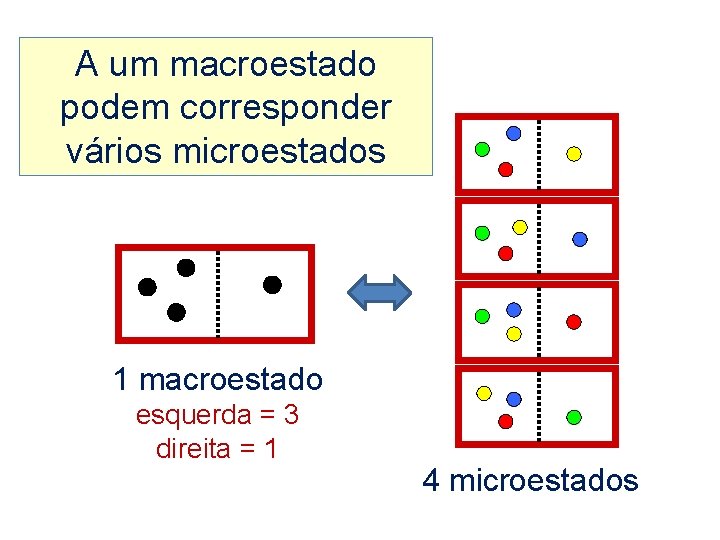
A um macroestado podem corresponder vários microestados 1 macroestado esquerda = 3 direita = 1 4 microestados

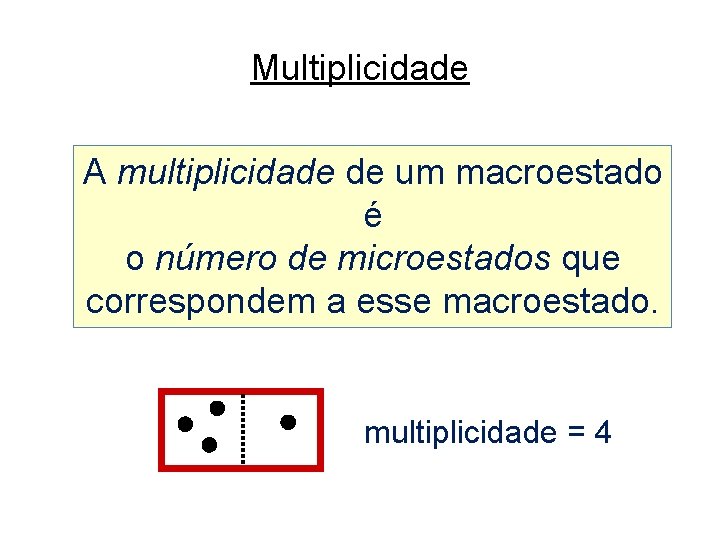
Multiplicidade A multiplicidade de um macroestado é o número de microestados que correspondem a esse macroestado. multiplicidade = 4

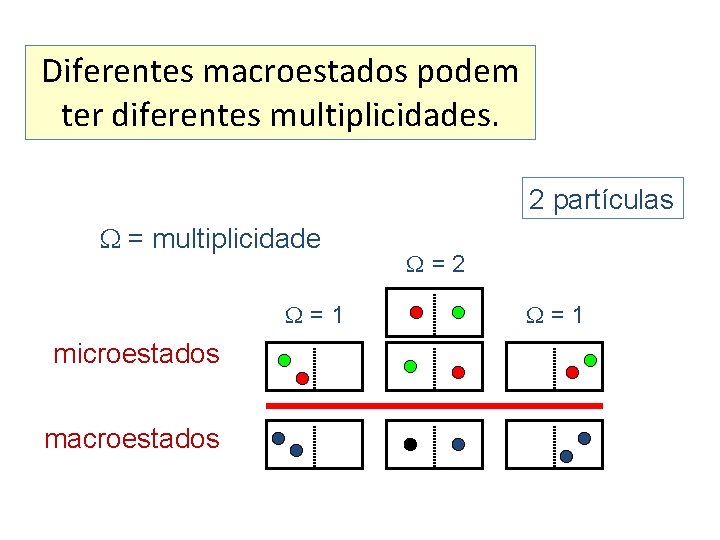
Diferentes macroestados podem ter diferentes multiplicidades. 2 partículas = multiplicidade =1 microestados macroestados =2 =1

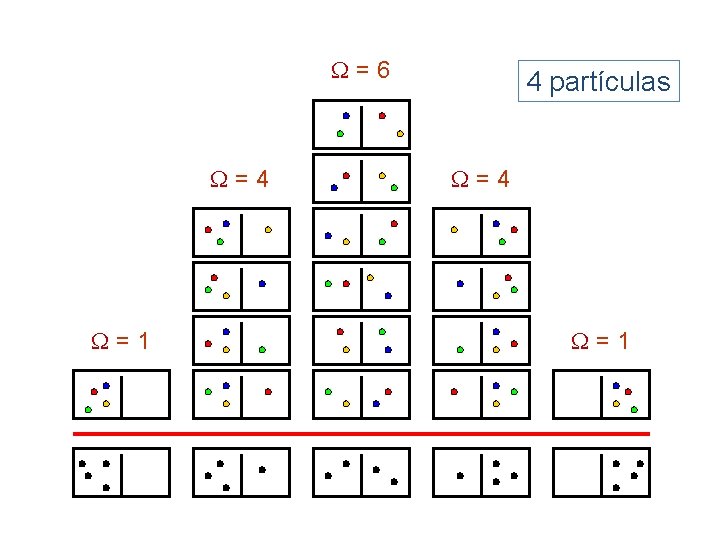
=6 =4 =1 4 partículas =4 =1

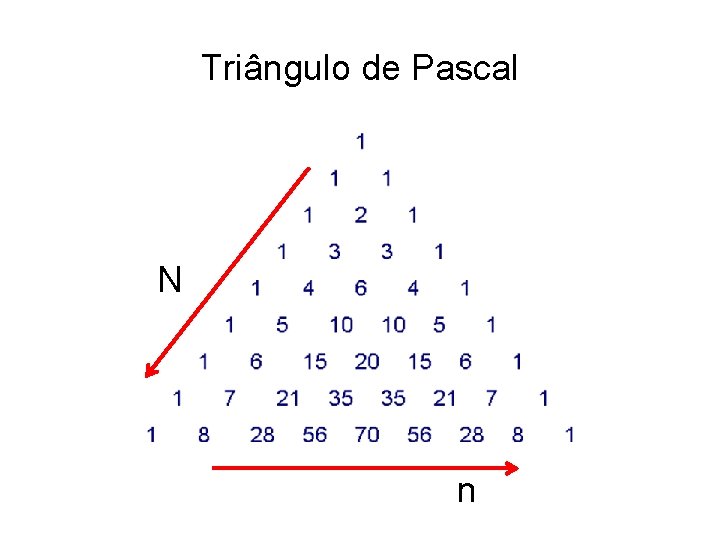
Cálculo da Multiplicidade. . . n N‒n N partículas (n, N) = multiplicidade do macroestado com n partículas à esquerda e N‒n à direita

Triângulo de Pascal N n

Multiplicidade máxima Para N (aproximação de Stirling): Quase todos os 2 N microestados correspondem a n N / 2.

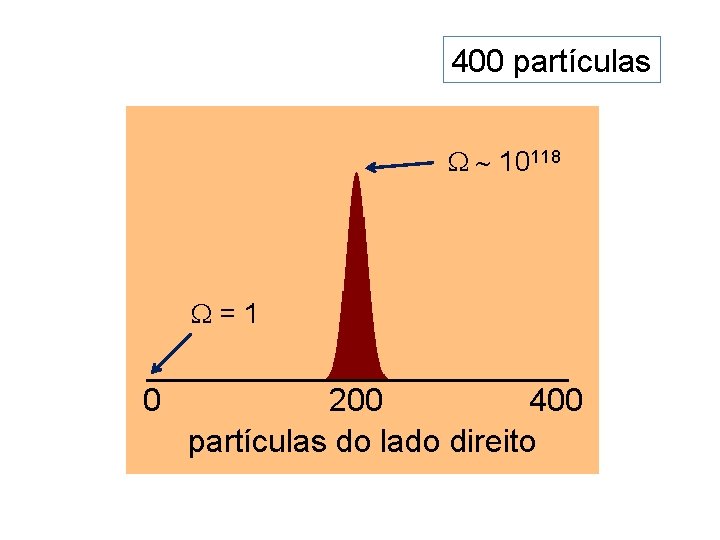
400 partículas 10118 =1 0 200 400 partículas do lado direito

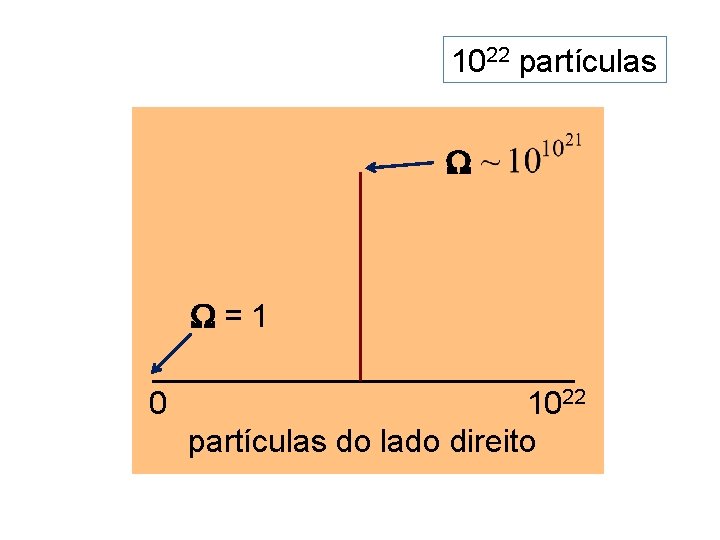
1022 partículas =1 0 1022 partículas do lado direito

Para um sistema de muitas partículas, a diferença de multiplicidades entre macroestados distintos pode ser enorme! Sistemas macroscópicos típicos têm N~1023 partículas.

Equiprobabilidade Microscópica Todos os microestados de um sistema isolado são igualmente prováveis. O sistema divide seu tempo igualmente por todos os microestados acessíveis.

Probabilidade Macroscópica Os macroestados de um sistema isolado não são igualmente prováveis. A probabilidade do sistema ser encontrado em um dado macroestado é proporcional à multiplicidade do macroestado.

A origem da irreversibilidade Para um sistema isolado de muitas partículas: Muitíssimo provável (sempre) baixa multiplicidade alta multiplicidade Pouquíssimo provável (nunca) alta multiplicidade baixa multiplicidade

A 2ª Lei da Termodinâmica Um sistema isolado nunca passa espontaneamente de um estado de alta multiplicidade para um de baixa multiplicidade.

Uma analogia (cruel) oásis bêbado deserto R. Baierlein, Am. J. Phys. 46, 1042 (1978)

Entropia S constante de Boltzmann: k = 1, 4 10‒ 23 J/K = R / NAvog. 1 2 1 1+2 = 1 2 S 1+2 = S 1 + S 2

A 2ª Lei da Termodinâmica A entropia de um sistema isolado nunca diminui. Em qualquer transformação do sistema:

Processos Reversíveis • Reversível: • Irreversível: • Impossível: S é a entropia total do sistema (isolado).

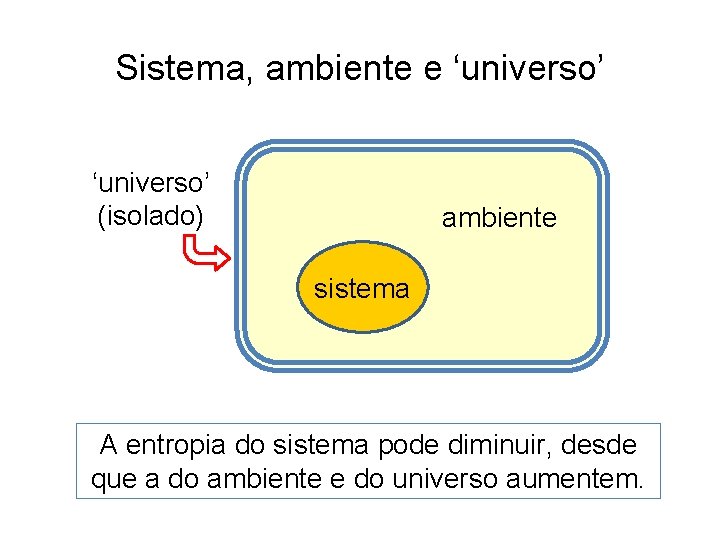
Sistema, ambiente e ‘universo’ (isolado) ambiente sistema A entropia do sistema pode diminuir, desde que a do ambiente e do universo aumentem.

O epitáfio de Boltzmann

Entropia, Energia e Temperatura

A entropia é uma função de estado macroestado termodinâmico U, V, N, T, P. . . independentes equações de estado

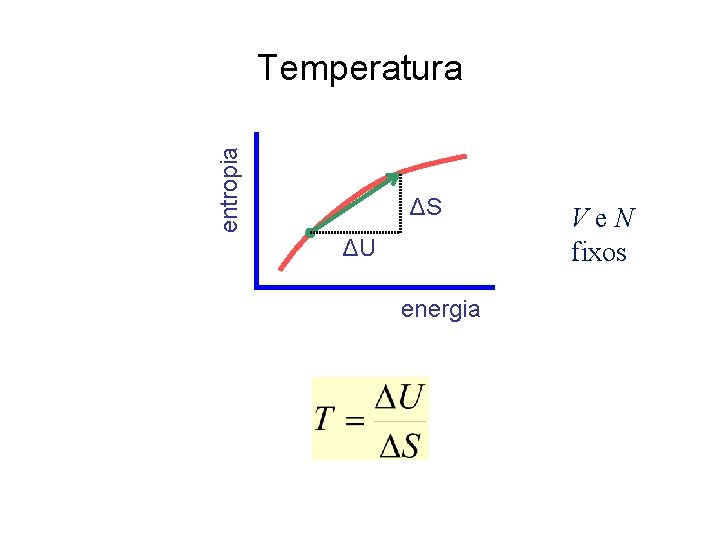
entropia Temperatura ΔS ΔU energia Ve. N fixos

Temperatura Dado S (U, V, N), é a definição termodinâmica de temperatura.

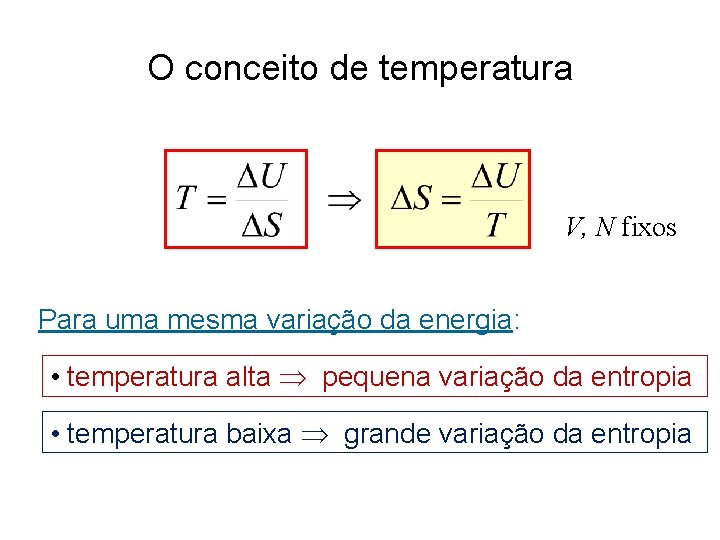
O conceito de temperatura V, N fixos Para uma mesma variação da energia: • temperatura alta pequena variação da entropia • temperatura baixa grande variação da entropia

O conceito (usual) de temperatura • Aquilo que se mede com um termômetro. • A coisa que se torna igual após dois objetos ficarem em contato por muito tempo. • Calor flui espontaneamente do corpo de maior temperatura para o de menor temperatura. • Grau de agitação das moléculas de um corpo.

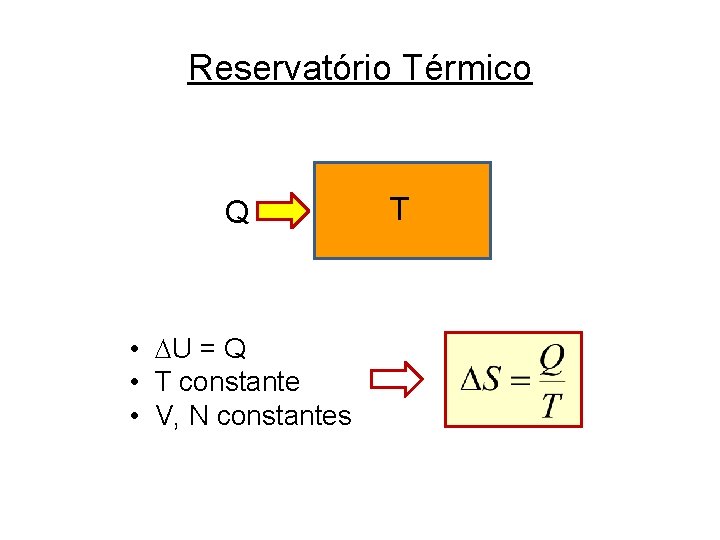
Reservatório Térmico Q • U = Q • T constante • V, N constantes T

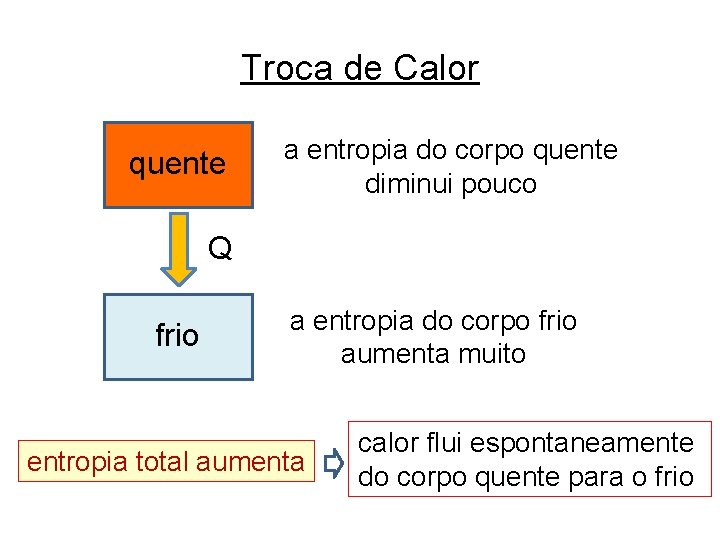
Troca de Calor quente a entropia do corpo quente diminui pouco Q frio a entropia do corpo frio aumenta muito entropia total aumenta calor flui espontaneamente do corpo quente para o frio

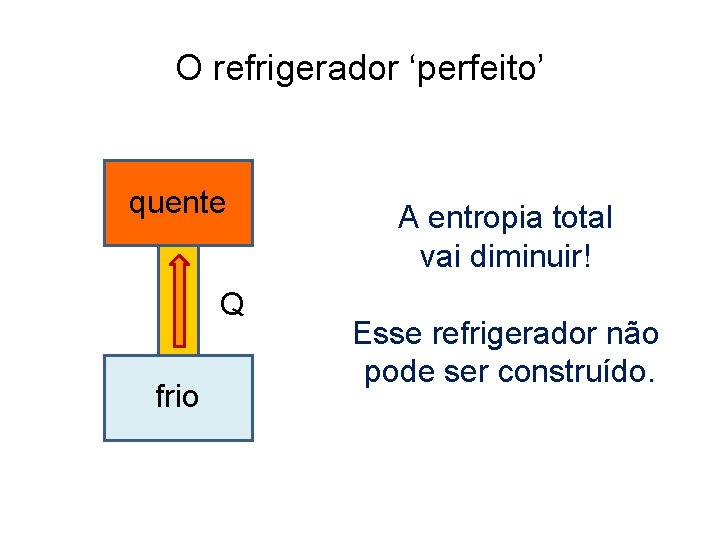
O refrigerador ‘perfeito’ quente Q frio A entropia total vai diminuir! Esse refrigerador não pode ser construído.

A 2ª Lei da Termodinâmica (Clausius) É impossível realizar um processo cujo único efeito seja transferir calor de um corpo frio para um corpo mais quente. R. Clausius (1822 -1888)

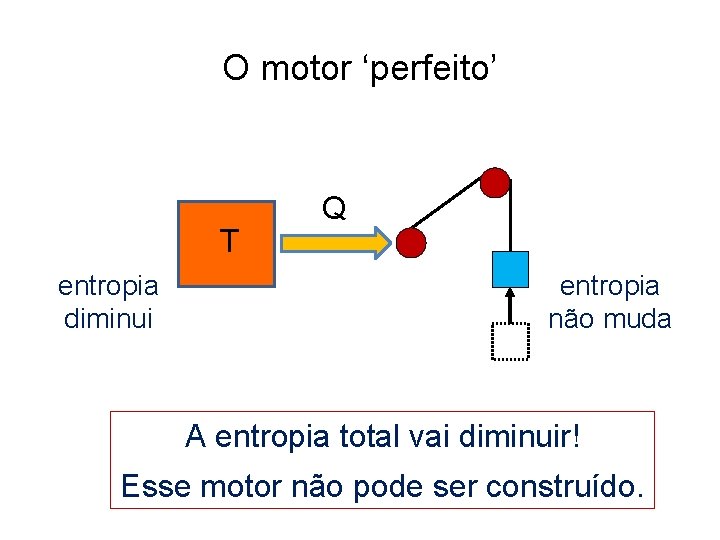
O motor ‘perfeito’ T entropia diminui Q entropia não muda A entropia total vai diminuir! Esse motor não pode ser construído.

A 2ª Lei da Termodinâmica (Kelvin) É impossível realizar um processo cujo único efeito seja remover calor de um corpo e produzir uma quantidade equivalente de energia mecânica. W. Thomson Lord Kelvin (1824 -1907)

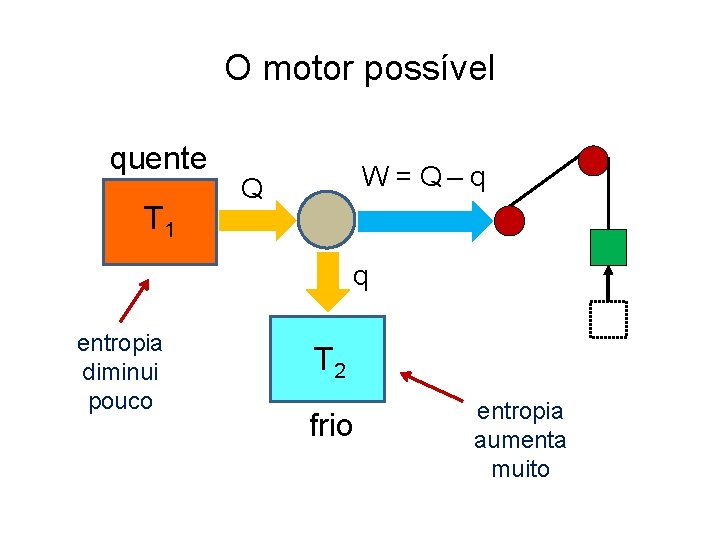
O motor possível quente T 1 W = Q‒ q Q q entropia diminui pouco T 2 frio entropia aumenta muito

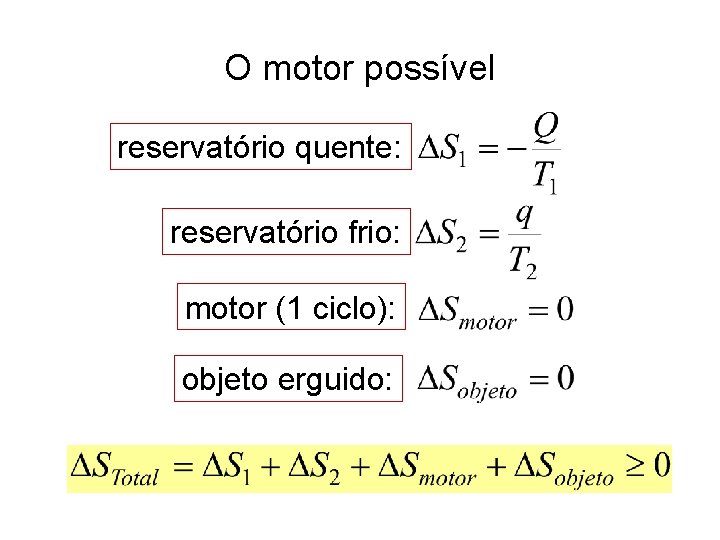
O motor possível reservatório quente: reservatório frio: motor (1 ciclo): objeto erguido:

O motor possível Há sempre um ‘desperdício’ q/Q. O menor desperdício possível é q/Q = T 2/T 1

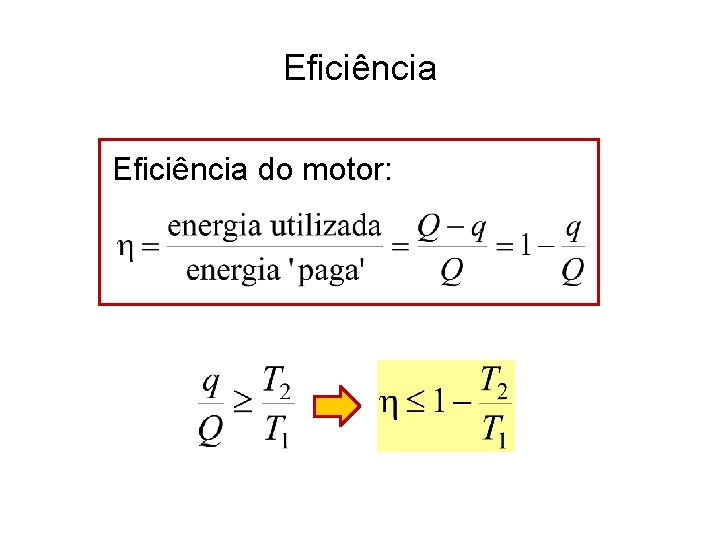
Eficiência do motor:

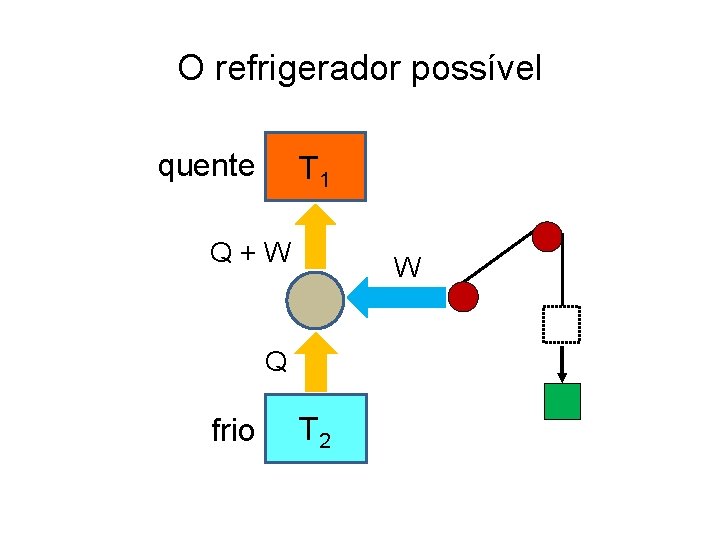
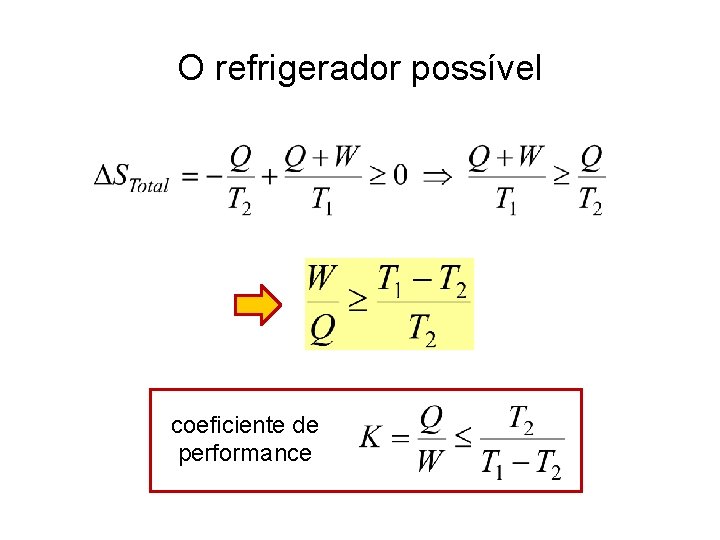
O refrigerador possível quente T 1 Q+W W Q frio T 2

O refrigerador possível coeficiente de performance

A Máquina de Carnot máquina reversível operando entre T 1 e T 2 Sadi Carnot (1796 -1832)

O Teorema de Carnot • As máquinas reversíveis são as máquinas mais eficientes operando entre T 1 e T 2. • A eficiência das máquinas reversíveis depende apenas de T 1 e T 2

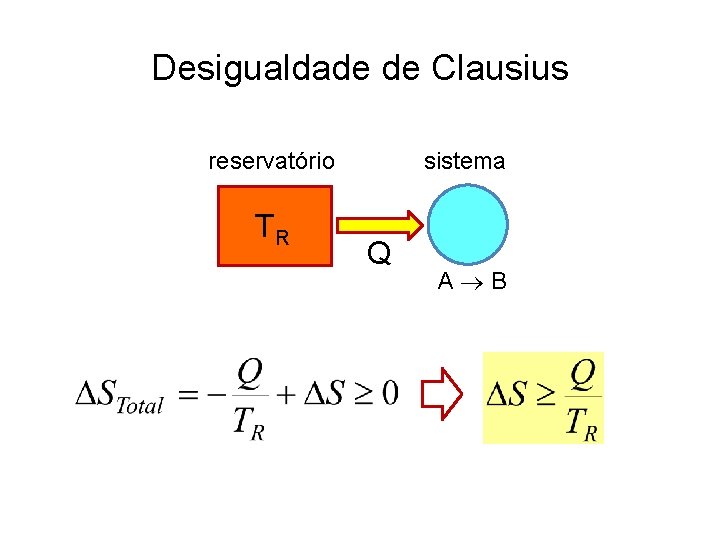
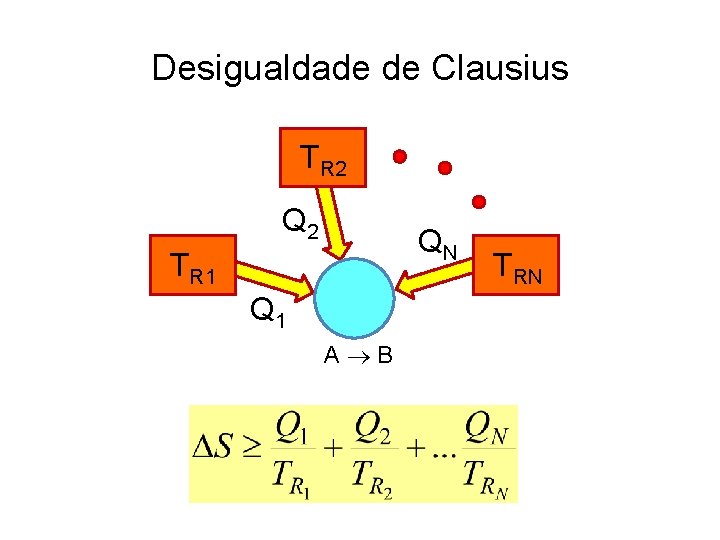
Desigualdade de Clausius sistema reservatório TR Q A B

Desigualdade de Clausius TR 2 QN TR 1 Q 1 A B TRN

Desigualdade de Clausius • Infinitos reservatórios com diferenças infinitesimais de temperatura: • Processo cíclico A = B S = 0

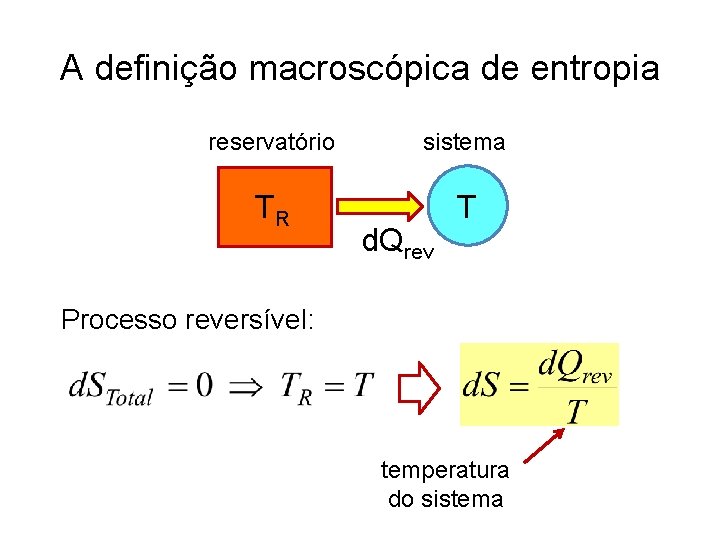
A definição macroscópica de entropia reservatório sistema TR T d. Qrev Processo reversível: temperatura do sistema

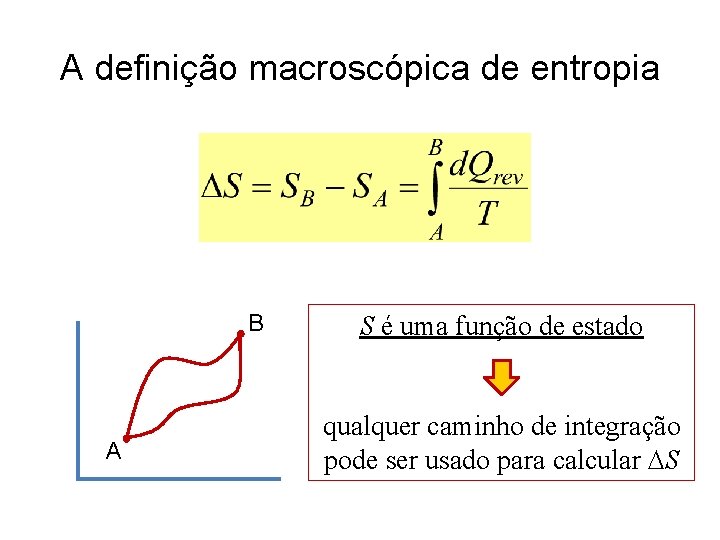
A definição macroscópica de entropia B A S é uma função de estado qualquer caminho de integração pode ser usado para calcular S

A definição macroscópica de entropia: Clausius, 1865

Entropia, Volume e Pressão

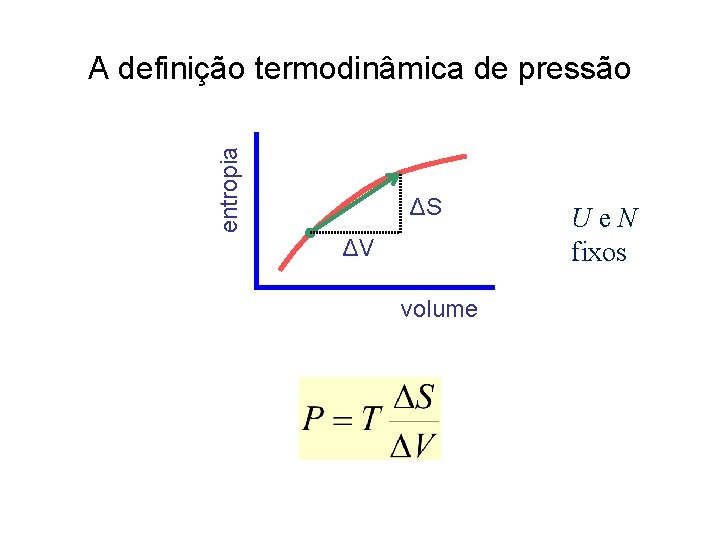
entropia A definição termodinâmica de pressão ΔS ΔV volume Ue. N fixos

A definição termodinâmica de pressão Dado S (U, V, N), é a definição termodinâmica de pressão.

O conceito termodinâmico de pressão V, N fixos Para T fixo e uma mesma variação de volume: • pressão alta grande variação da entropia • pressão baixa pequena variação da entropia

O conceito mecânico de pressão • Definição: F A • Na ausência de outras forças (gravitacional, etc. ) a pressão em um fluido em equilíbrio mecânico é uniforme. • Um corpo imerso num fluido será empurrado no sentido da maior para a menor pressão.

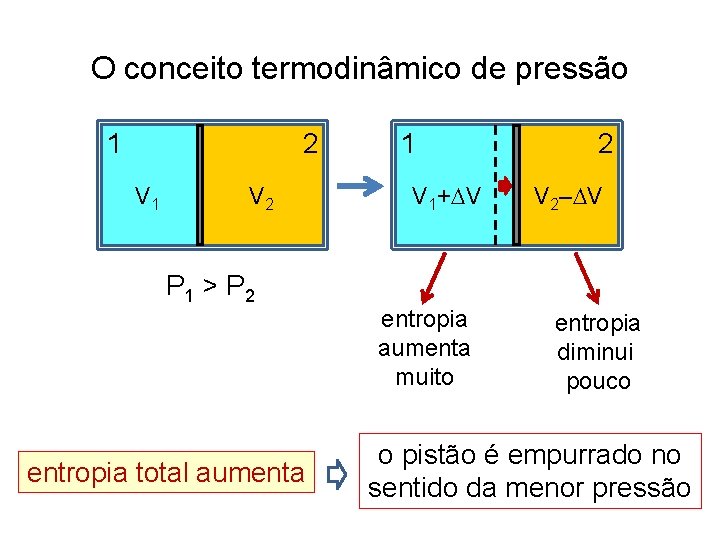
O conceito termodinâmico de pressão 1 2 V 1 V 2 P 1 > P 2 entropia total aumenta 1 V 1+ V entropia aumenta muito 2 V 2‒ V entropia diminui pouco o pistão é empurrado no sentido da menor pressão

Formalmente:

A identidade termodinâmica

A identidade termodinâmica 1ª lei da termodinâmica: Identid. termodinâmica: Processo reversível: A definição termodinâmica da pressão é consistente com a expressão usual para o trabalho reversível.

Equação de Estado de Sistemas Simples

Gás Ideal

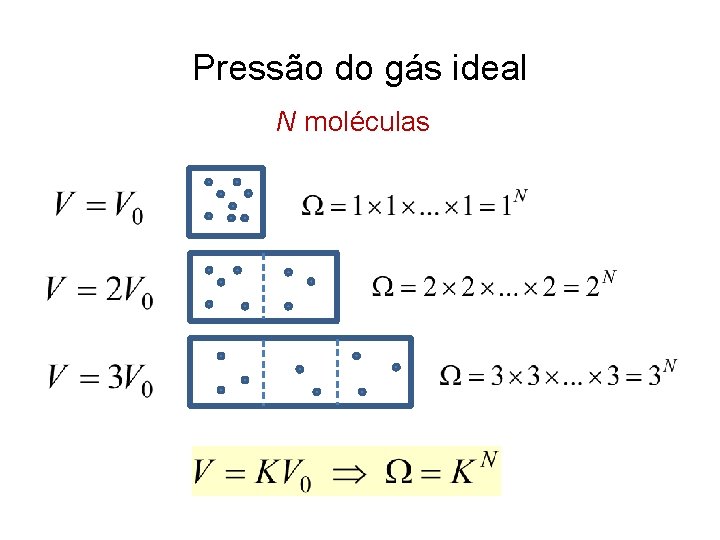
Pressão do gás ideal N moléculas

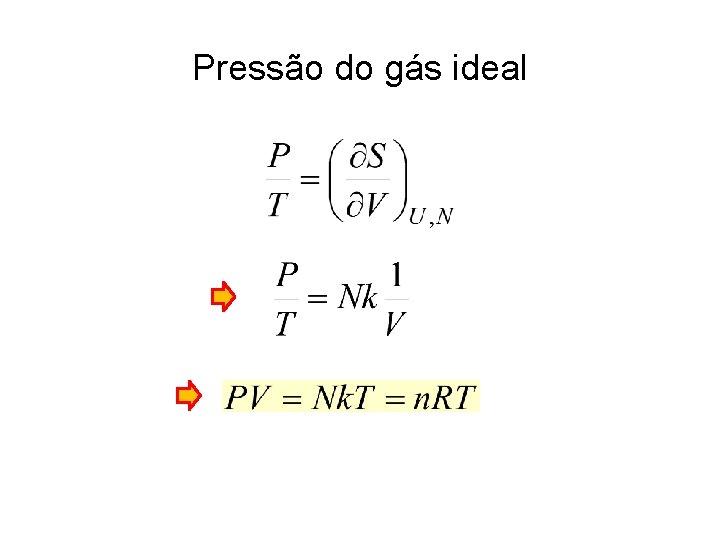
Pressão do gás ideal depende de U e N

Pressão do gás ideal

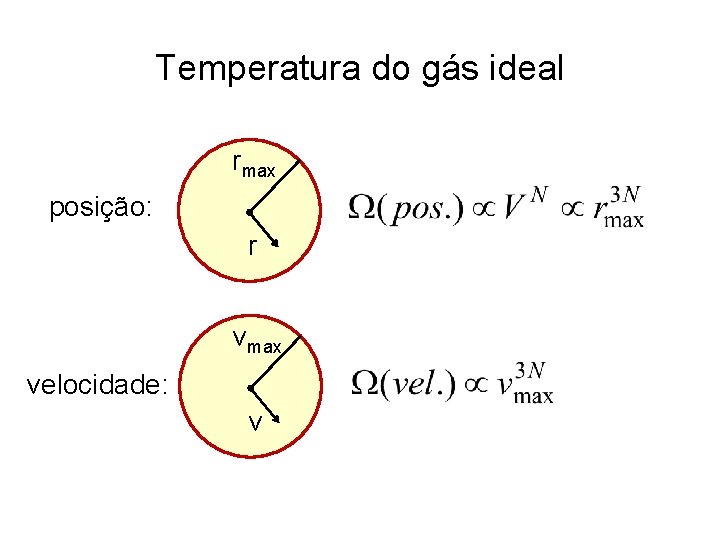
Temperatura do gás ideal rmax posição: r vmax velocidade: v

Temperatura do gás ideal depende de V e N

Temperatura do gás ideal energia cinética média:

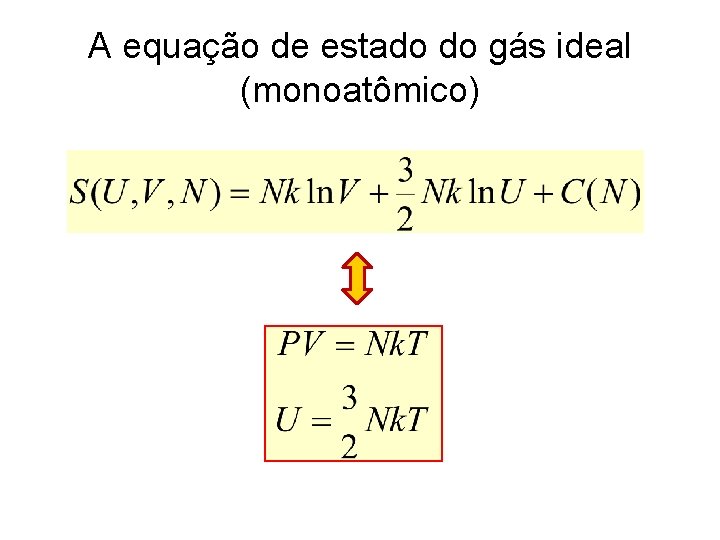
A equação de estado do gás ideal (monoatômico)

Borracha ideal

Modelo de uma fita elástica ‘monômero’ barra rígida de comprimento a N monômeros: N 1 para a direita, N 2 para a esquerda comprimento: comprimento máximo:

Modelo de uma fita elástica multiplicidade:

Entropia da fita elástica depende de N e U

Força elástica F > 0 com a troca de sinal lei de Hooke

Força elástica • A força elástica aumenta com a temperatura. • A força elástica é puramente entrópica. Vídeo completo em https: //youtu. be/ov. VO 8 NDdon 4

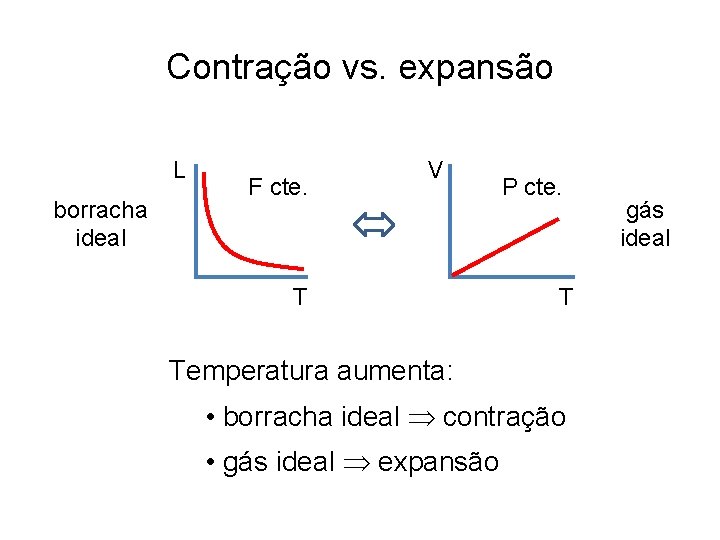
Contração vs. expansão L borracha ideal F cte. V T P cte. T Temperatura aumenta: • borracha ideal contração • gás ideal expansão gás ideal

Extensão adiabática d. Q = 0 , d. L > 0 F e CL positivos temperatura aumenta durante a extensão (diminui numa contração)

Extensão adiabática Vídeo completo em https: //youtu. be/vqz. W 25 gj 0 EI Vídeo completo em https: //youtu. be/lfmrvx. B 154 w

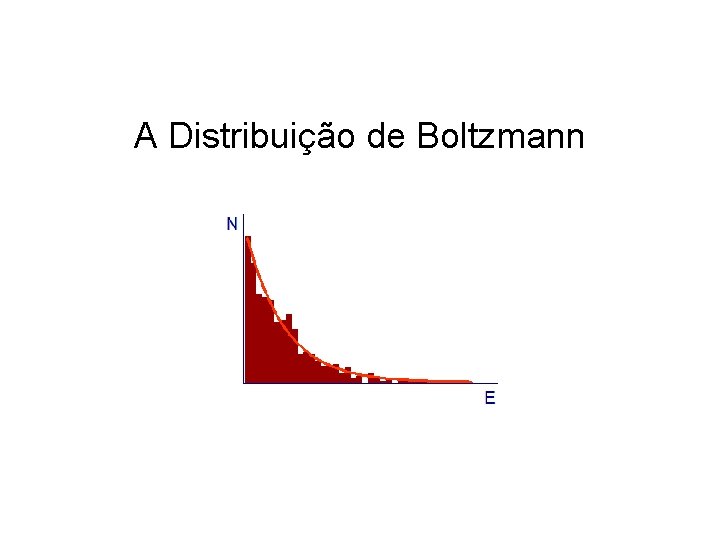
A Distribuição de Boltzmann

A Distribuição de Boltzmann sistema e U–e T reservatório térmico

A Distribuição de Boltzmann

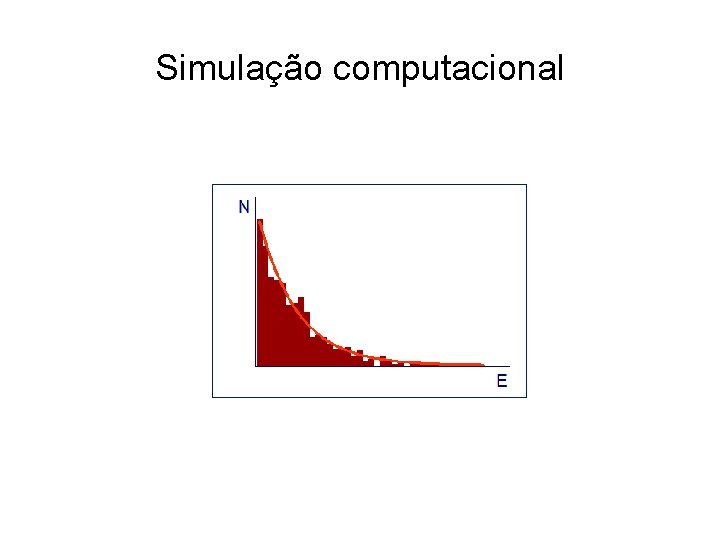
Simulação computacional

Comentários Finais

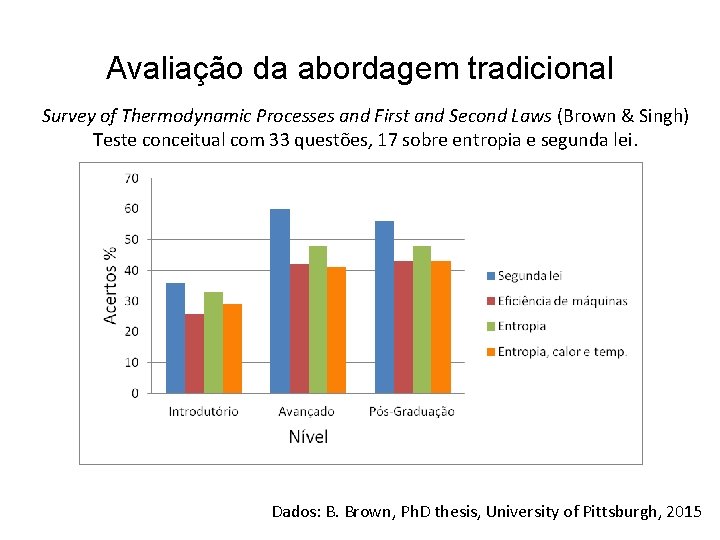
Avaliação da abordagem tradicional Survey of Thermodynamic Processes and First and Second Laws (Brown & Singh) Teste conceitual com 33 questões, 17 sobre entropia e segunda lei. Dados: B. Brown, Ph. D thesis, University of Pittsburgh, 2015

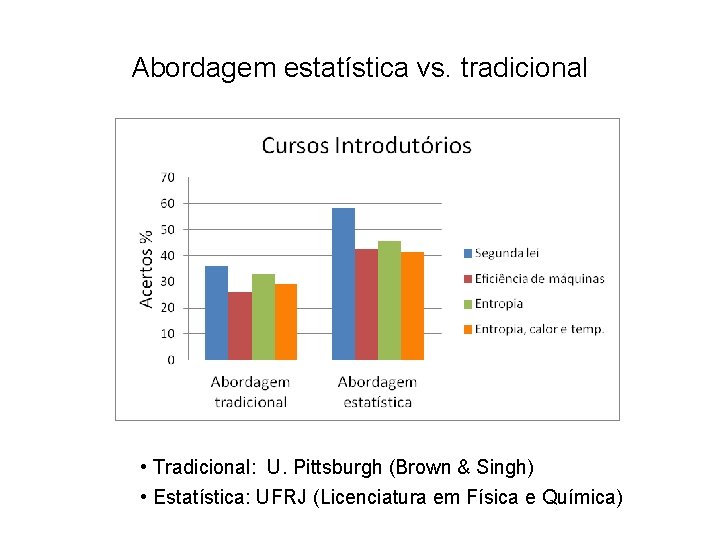
Abordagem estatística vs. tradicional • Tradicional: U. Pittsburgh (Brown & Singh) • Estatística: UFRJ (Licenciatura em Física e Química)

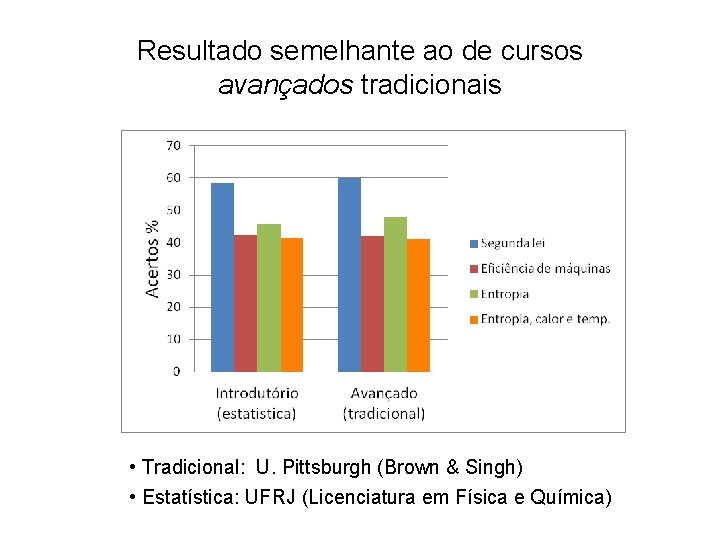
Resultado semelhante ao de cursos avançados tradicionais • Tradicional: U. Pittsburgh (Brown & Singh) • Estatística: UFRJ (Licenciatura em Física e Química)

Comentários finais • A 2ª lei da termodinâmica e o conceito de entropia são temas de aprendizagem notoriamente difícil. • A introdução do conceito estatístico de entropia logo ao início do estudo da 2ª lei parece reduzir essas dificuldades. • A definição da temperatura termodinâmica a partir da entropia permite obter imediatamente a maioria dos resultados associados à 2ª lei.

Comentários finais • A abordagem estatística da entropia pode levar além da 2ª lei: – Equação de estado de sistemas simples (gás ideal, por exemplo). – Distribuição de Boltzmann. • Com adaptações, a abordagem pode ser utilizada no ensino médio.

http: //www. if. ufrj. br/~carlos/palestras/ setadotempo/livro-2 a-lei. pdf