ENSAYOS CLNICOS EN MXICO RETOS Y OPORTUNIDADES Academia














- Slides: 24

ENSAYOS CLÍNICOS EN MÉXICO RETOS Y OPORTUNIDADES Academia Nacional de Medicina de México Julio 22, 2015

CONTENIDO Introducción Proceso de desarrollo de medicamentos Outsourcing de ensayos clínicos: requerimientos internacionales y criterios de evaluación Ensayos clínicos México Conclusiones Recomendaciones

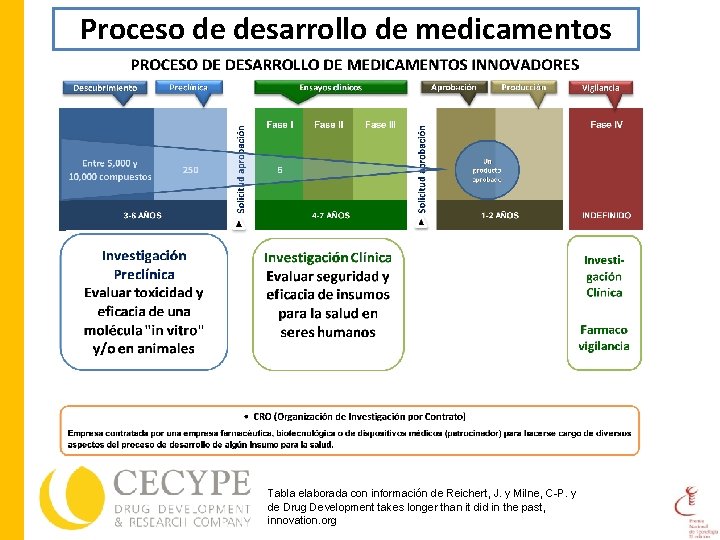
Proceso de desarrollo de medicamentos Tabla elaborada con información de Reichert, J. y Milne, C-P. y de Drug Development takes longer than it did in the past, innovation. org

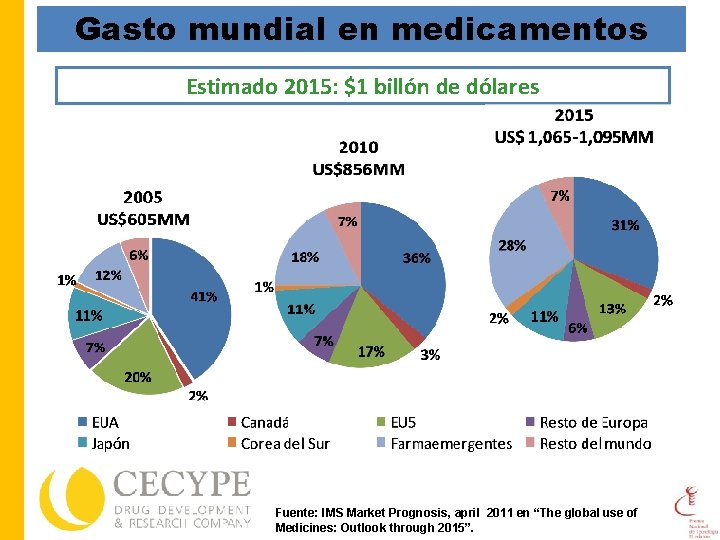
Gasto mundial en medicamentos Estimado 2015: $1 billón de dólares Fuente: IMS Market Prognosis, april 2011 en “The global use of Medicines: Outlook through 2015”.

Outsourcing de ensayos clínicos REQUERIMIENTOS INTERNACIONALES Y CRITERIOS DE EVALUACIÓN.

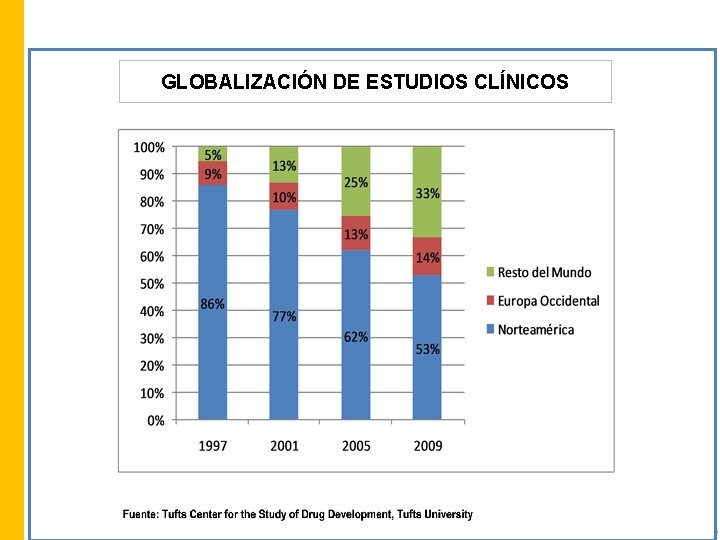
GLOBALIZACIÓN DE ESTUDIOS CLÍNICOS

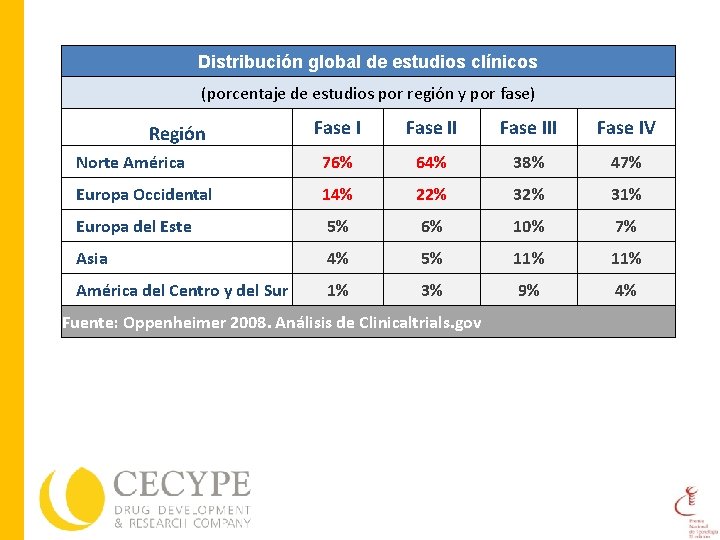
Distribución global de estudios clínicos (porcentaje de estudios por región y por fase) Fase III Fase IV Norte América 76% 64% 38% 47% Europa Occidental 14% 22% 31% Europa del Este 5% 6% 10% 7% Asia 4% 5% 11% América del Centro y del Sur 1% 3% 9% 4% Región Fuente: Oppenheimer 2008. Análisis de Clinicaltrials. gov

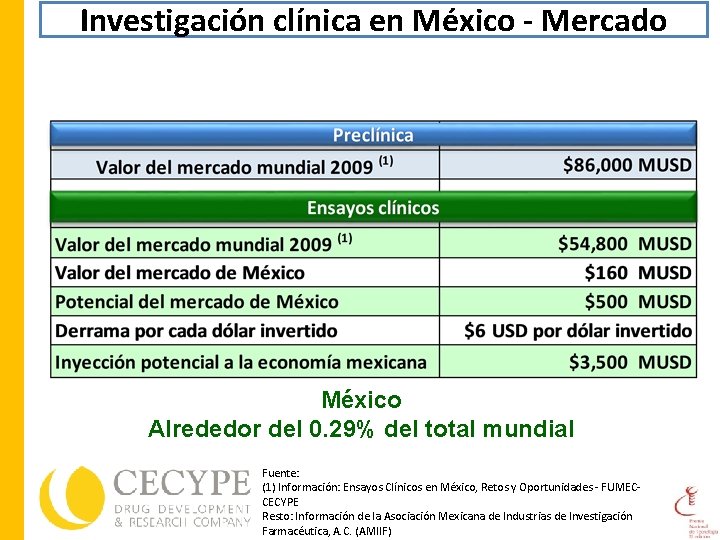
Investigación clínica en México - Mercado México Alrededor del 0. 29% del total mundial Fuente: (1) Información: Ensayos Clínicos en México, Retos y Oportunidades - FUMECCECYPE Resto: Información de la Asociación Mexicana de Industrias de Investigación Farmacéutica, A. C. (AMIIF)

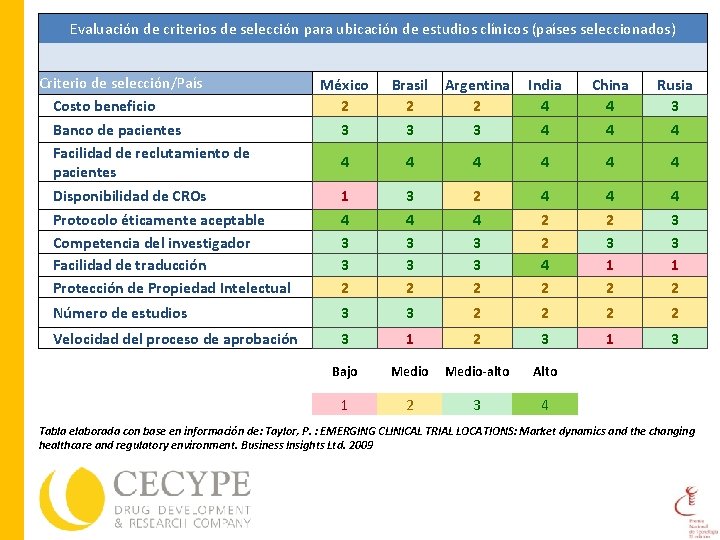
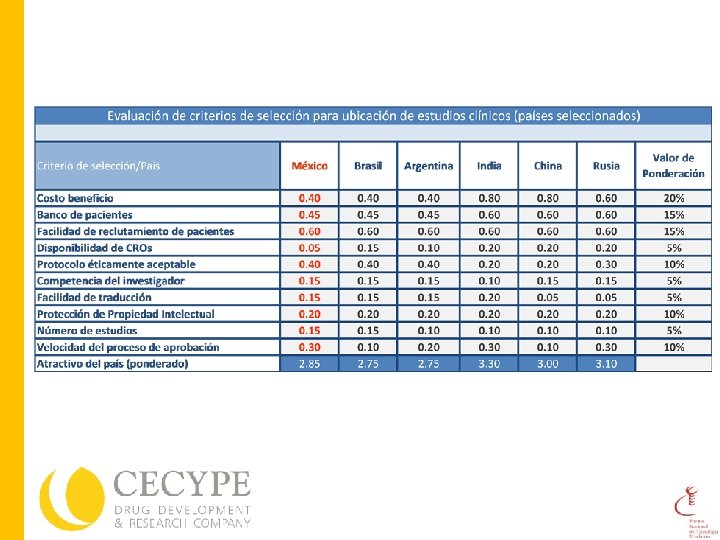
Evaluación de criterios de selección para ubicación de estudios clínicos (países seleccionados) Criterio de selección/País Costo beneficio México 2 Brasil Argentina India China Rusia 2 2 4 4 3 Banco de pacientes Facilidad de reclutamiento de pacientes Disponibilidad de CROs 3 3 3 4 4 4 4 4 1 3 2 4 4 4 Protocolo éticamente aceptable Competencia del investigador Facilidad de traducción Protección de Propiedad Intelectual 4 3 3 2 2 2 4 2 2 3 1 2 3 3 1 2 Número de estudios 3 3 2 2 Velocidad del proceso de aprobación 3 1 2 3 1 3 Bajo Medio-alto Alto 1 2 3 4 Tabla elaborada con base en información de: Taylor, P. : EMERGING CLINICAL TRIAL LOCATIONS: Market dynamics and the changing healthcare and regulatory environment. Business Insights Ltd. 2009

Modelo desarrollado por A. T. Kearney


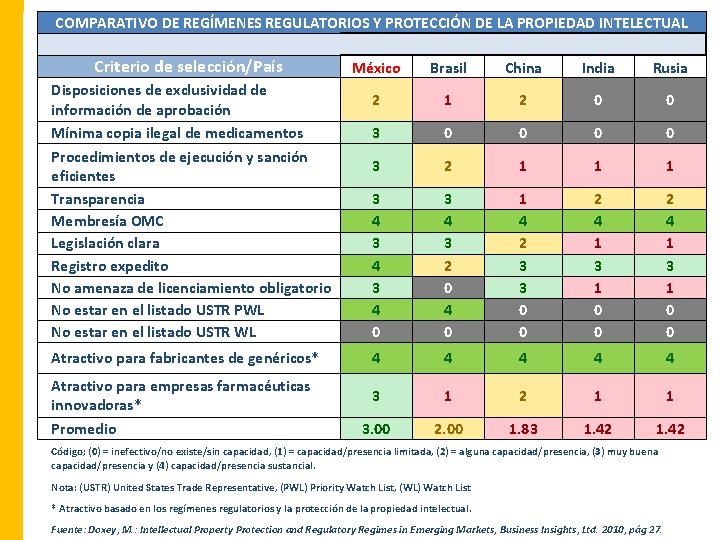
COMPARATIVO DE REGÍMENES REGULATORIOS Y PROTECCIÓN DE LA PROPIEDAD INTELECTUAL Criterio de selección/País México Brasil China India Rusia Disposiciones de exclusividad de 2 1 2 0 0 información de aprobación Mínima copia ilegal de medicamentos 3 0 0 Procedimientos de ejecución y sanción 3 2 1 1 1 eficientes Transparencia 3 3 1 2 2 Membresía OMC 4 4 4 Legislación clara 3 3 2 1 1 Registro expedito 4 2 3 3 3 No amenaza de licenciamiento obligatorio 3 0 3 1 1 No estar en el listado USTR PWL 4 4 0 0 0 No estar en el listado USTR WL 0 0 0 Atractivo para fabricantes de genéricos* Atractivo para empresas farmacéuticas innovadoras* Promedio 4 4 4 3 1 2 1 1 3. 00 2. 00 1. 83 1. 42 Código; (0) = inefectivo/no existe/sin capacidad, (1) = capacidad/presencia limitada, (2) = alguna capacidad/presencia, (3) muy buena capacidad/presencia y (4) capacidad/presencia sustancial. Nota: (USTR) United States Trade Representative, (PWL) Priority Watch List, (WL) Watch List * Atractivo basado en los regímenes regulatorios y la protección de la propiedad intelectual. Fuente: Doxey, M. : Intellectual Property Protection and Regulatory Regimes in Emerging Markets, Business Insights, Ltd. 2010, pág 27.

MÉXICO

Preclínica • Prácticamente no existe con enfoque a registro de medicamentos • Investigación básica en instituciones de educación superior e instituciones de salud • Está desarticulada y fragmentada • Enfoque asistencial o académico como prioridad • Estructuras operativas que no dan entrada a proyectos o empresas que puedan hacer investigación preclínica • Prácticamente no hay bioterios • No se siguen lineamientos internacionales ni buenas prácticas de laboratorio

Preclínica • Existen especialistas para transmitir conocimiento en investigación básica. • Orientación a la ciencia biomédica básica y no al desarrollo de tecnología e innovación porque se considera que esa ciencia es “de segunda” (no da créditos, no lleva al SNI) • Las instituciones privadas no forman científicos de posgrado o forman muy pocos porque no hay fuentes de trabajo. • Falta de empresas de investigación preclínica.

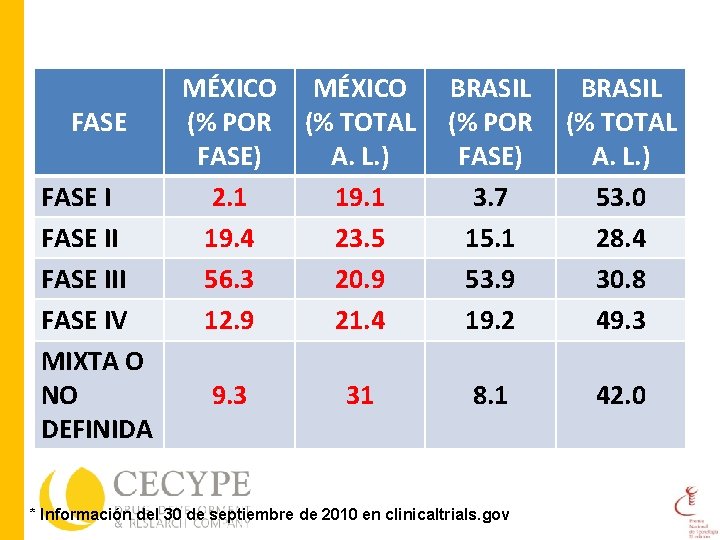
FASE III FASE IV MIXTA O NO DEFINIDA MÉXICO (% POR (% TOTAL FASE) A. L. ) 2. 1 19. 4 23. 5 56. 3 20. 9 12. 9 21. 4 9. 3 31 BRASIL (% POR FASE) 3. 7 15. 1 53. 9 19. 2 BRASIL (% TOTAL A. L. ) 53. 0 28. 4 30. 8 49. 3 8. 1 42. 0 * Información del 30 de septiembre de 2010 en clinicaltrials. gov

FODA

FUERZAS • Sistema regulatorio en evolución y competitivo – modificaciones recientes dan nivel satisfactorio de seguridad a las empresas. – el proceso de aprobación más rápido entre los principales países atractivos para hacer ensayos clínicos. – Legislación de avanzada en biotecnológicos. • Precios competitivos. • Velocidad de reclutamiento y tamaño de mercado atractivos. • Reconocimiento internacional en investigación básica (sobre todo en biológicos).

DEBILIDADES • No siempre se aplican las normas de protección intelectual ni se respeta la “exclusividad de información”. • México opera por debajo de su potencial en investigación (inversión, maquila, fases tempranas, CROs locales) – Desconocimiento de las normas internacionales, BPC, BPL, ICH, etc. por parte de los investigadores. – Normatividad y cultura limitante en instituciones públicas de salud e instituciones de educación superior. – Comités de ética e investigación con escaso apego a lineamientos internacionales, como ICH, por ejemplo. – Muy pocas empresas dedicadas a la investigación preclínica y clínica. • México compara desfavorablemente a nivel internacional en indicadores de investigación clínica (número de investigadores, patentes, inversión como % del PIB, educación, personal calificado)

OPORTUNIDADES • Altos costos y complejidad del proceso de desarrollo de nuevos medicamentos y presión para las empresas innovadoras sobre tiempos de entrada al mercado. • Estudios Fase I y Fase II. • La investigación preclínica, pues sólo hay dos grandes jugadores (China e India) y dos seguidores (Rusia y Brasil) y las barreras de entrada son mayores (México tiene el potencial en investigadores y regulación; faltan instalaciones y organizaciones que la lleven a cabo) • Investigación por parte de empresas farmacéuticas locales para desarrollar genéricos y biosimilares. • Desarrollo de patentes tanto en investigación (preclínica y clínica) así como en dispositivos médicos. • La nueva regulación para biológicos y biosimilares.

AMENZAS • Otros países, como Brasil están mejorando su legislación con mayor población y calidad similar. • China e India concentran el 34% de la población mundial. Muy atractivos por esa razón para las empresas farmacéuticas. Si mejoran su legislación serán una mayor amenaza. • La percepción internacional de inseguridad limita la inversión en investigación clínica.

RECOMENDACIONES DEL REPORTE jorge. herrera@cecype. com

PRINCIPALES RECOMENDACIONES jorge. herrera@cecype. com
