ENLACE QUMICO Y ESTRUCTURA ENLACE INICO Y ESTRUCTURA









![Ejemplos • CCl 4 • [NH 4]+ • NF 3 • SF 2 • Ejemplos • CCl 4 • [NH 4]+ • NF 3 • SF 2 •](https://slidetodoc.com/presentation_image/21e7e08261e93a4ef7ce85a7be450440/image-18.jpg)










- Slides: 29

ENLACE QUÍMICO Y ESTRUCTURA • • • ENLACE IÓNICO Y ESTRUCTURA ENLACE COVALENTE ESTRUCTURAS COVALENTES FUERZAS INTERMOLECULARES ENLACE METÁLICO

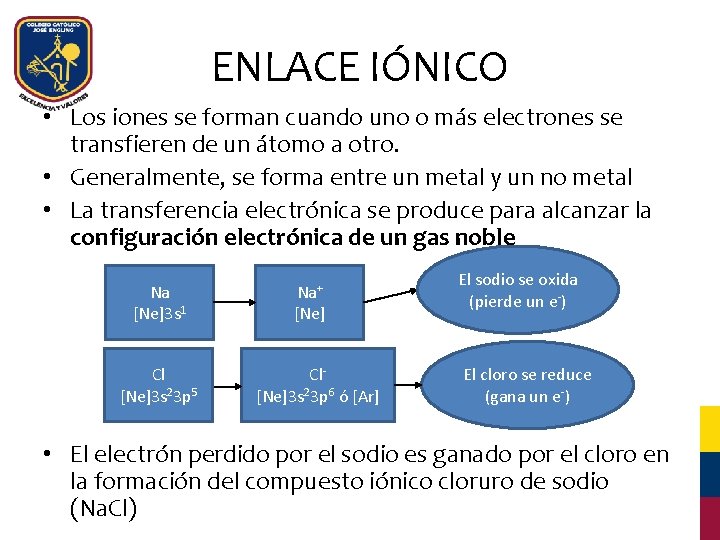
ENLACE IÓNICO • Los iones se forman cuando uno o más electrones se transfieren de un átomo a otro. • Generalmente, se forma entre un metal y un no metal • La transferencia electrónica se produce para alcanzar la configuración electrónica de un gas noble Na [Ne]3 s 1 Cl [Ne]3 s 23 p 5 Na+ [Ne] Cl[Ne]3 s 23 p 6 ó [Ar] El sodio se oxida (pierde un e-) El cloro se reduce (gana un e-) • El electrón perdido por el sodio es ganado por el cloro en la formación del compuesto iónico cloruro de sodio (Na. Cl)

• Mg. O En este enlace iónico entre magnesio y oxígeno ¿Qué sucede con el magnesio y con el oxígeno? Escribir la ecuación de ionización de estos elementos ¿Qué configuración electrónica alcanzan?

ENLACE IÓNICO Iones Poliatómicos • Por definición un enlace iónico está relacionado con fuerzas electrostáticas entre cationes y aniones. Ion Nombre NH 4+ Amonio • NH 4+ + Cl- → NH 4 Cl OH- Hidróxido NO 3 - Nitrato HCO 3 - Bicarbonato CO 22 - Carbonato SO 42 - Sulfato PO 43 - Fosfato

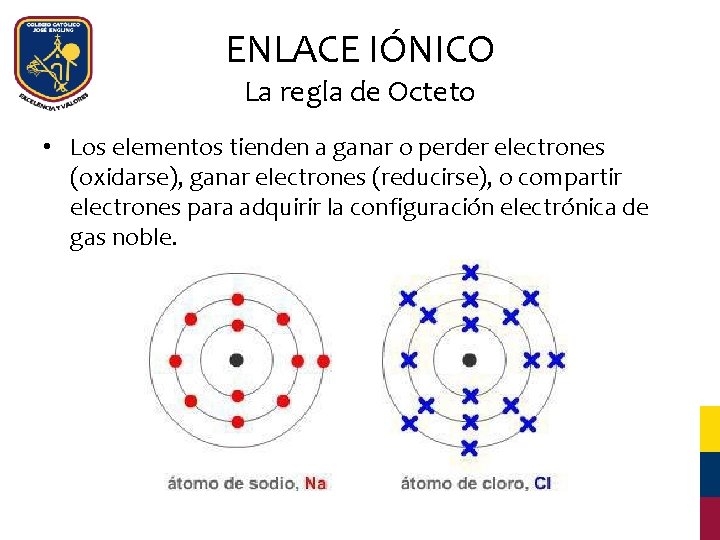
ENLACE IÓNICO La regla de Octeto • Los elementos tienden a ganar o perder electrones (oxidarse), ganar electrones (reducirse), o compartir electrones para adquirir la configuración electrónica de gas noble.

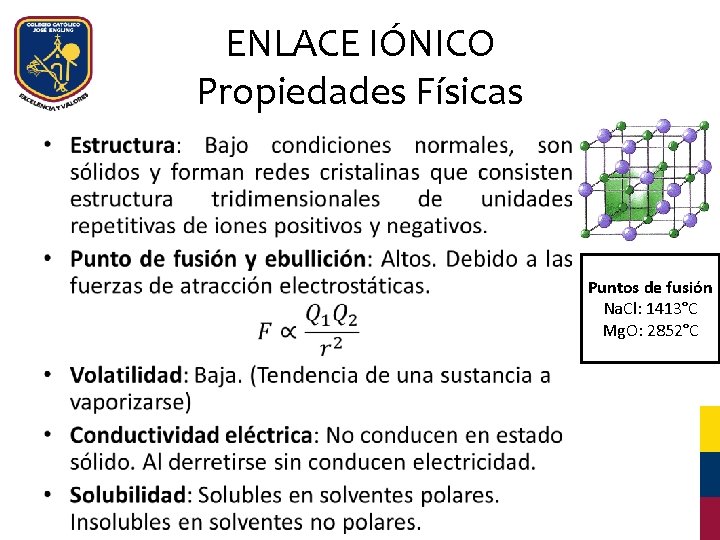
ENLACE IÓNICO Propiedades Físicas • Puntos de fusión Na. Cl: 1413°C Mg. O: 2852°C

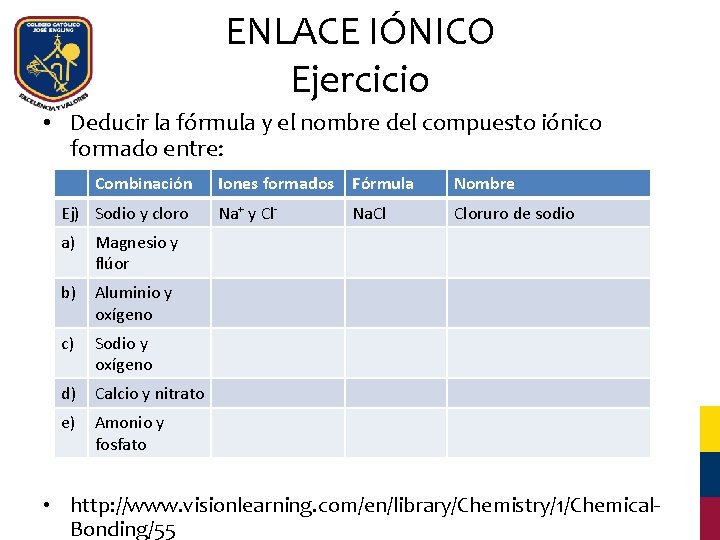
ENLACE IÓNICO Ejercicio • Deducir la fórmula y el nombre del compuesto iónico formado entre: Combinación Ej) Sodio y cloro a) Magnesio y flúor b) Aluminio y oxígeno c) Sodio y oxígeno d) Calcio y nitrato e) Amonio y fosfato Iones formados Fórmula Nombre Na+ y Cl- Na. Cl Cloruro de sodio • http: //www. visionlearning. com/en/library/Chemistry/1/Chemical. Bonding/55

ENLACE COVALENTE • Se produce cuando los átomos comparten electrones para obtener la configuración electrónica de un gas noble. • Generalmente, ocurre entre no metales.

ENLACE COVALENTE Símbolos de Lewis • Para observar claramente este tipo de enlace, es útil la idea de los símbolos de Lewis. • Símbolo de Lewis: Representa los electrones de valencia de los elementos.

ENLACE COVALENTE • Flúor (F 2) enlace simple 1 par de e- enlazados, 6 pares de e- no enlazados • Oxígeno (O 2) enlace doble 2 pares de e- enlazados, 4 pares de e- no enlazados • Nitrógeno (N 2) enlace triple 3 pares de e- enlazados, 2 pares de e- no enlazados • Ácido fluorhídrico, fluoruro de hidrógeno (HF) enlace simple 1 par de e- enlazados, 3 pares de e- no enlazados • Deducir la estructura de Lewis de las moléculas de CO 2 y H 2 O

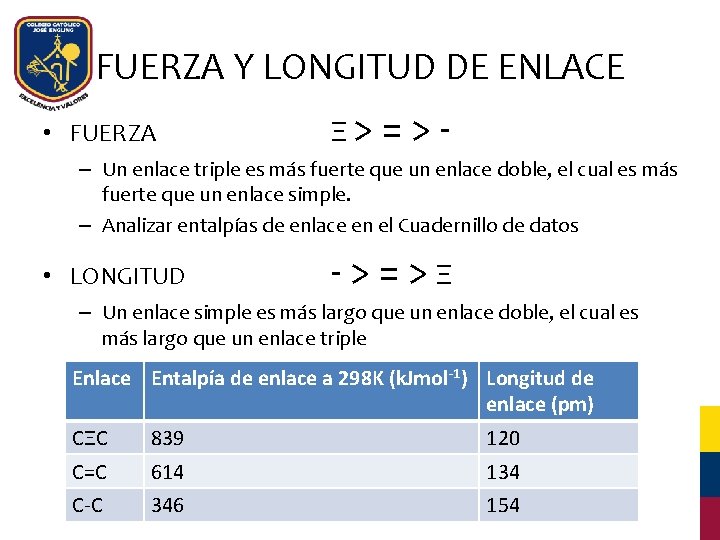
FUERZA Y LONGITUD DE ENLACE • FUERZA Ξ> = > - – Un enlace triple es más fuerte que un enlace doble, el cual es más fuerte que un enlace simple. – Analizar entalpías de enlace en el Cuadernillo de datos • LONGITUD ->=>Ξ – Un enlace simple es más largo que un enlace doble, el cual es más largo que un enlace triple Enlace Entalpía de enlace a 298 K (k. Jmol-1) Longitud de enlace (pm) CΞC 839 120 C=C 614 134 C-C 346 154

POLARIDAD • Enlace covalente polar: Cuando los pares de electrones compartidos, no son compartidos equitativamente. – Un átomo tendrá una carga parcial negativa δ– Un átomo tendrá una carga parcial positiva δ+ – La separación de carga se puede representar vectorialmente con un momento dipolo, μ • Enlace covalente puro (no polar): Si ambos átomos del enlace covalente son idénticos.

ELECTRONEGATIVIDAD (Xp) • Atracción relativa de un átomo de un elemento por el par de electrones compartidos en un enlace covalente. • En el cuadernillo de datos se encuentra valores de escala de electronegatividad – El flúor es el elemento con la mayor electronegatividad, con un valor de 4. 00 • Con la electronegatividad se puede estimar si un enlace es iónico, covalente no polar o covalente polar. Tipo de enlace Iónico Covalente puro (no polar) Covalente polar

Ejemplos • F • HF • Na. F

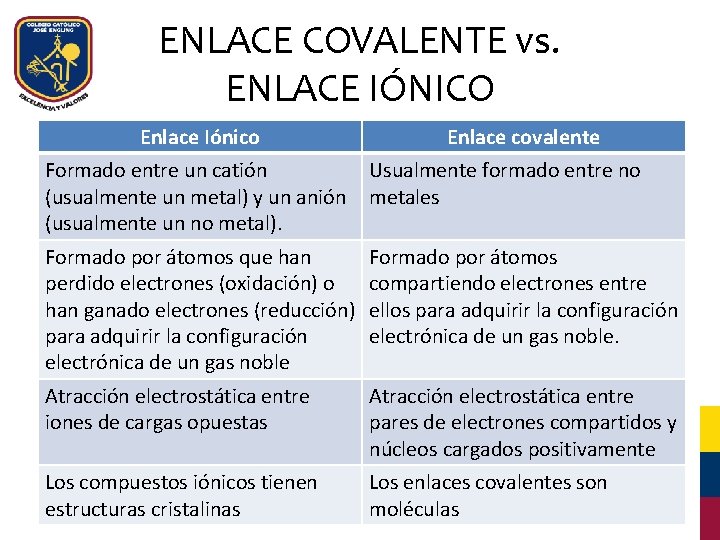
ENLACE COVALENTE vs. ENLACE IÓNICO Enlace Iónico Enlace covalente Formado entre un catión Usualmente formado entre no (usualmente un metal) y un anión metales (usualmente un no metal). Formado por átomos que han perdido electrones (oxidación) o han ganado electrones (reducción) para adquirir la configuración electrónica de un gas noble Formado por átomos compartiendo electrones entre ellos para adquirir la configuración electrónica de un gas noble. Atracción electrostática entre iones de cargas opuestas Atracción electrostática entre pares de electrones compartidos y núcleos cargados positivamente Los compuestos iónicos tienen estructuras cristalinas Los enlaces covalentes son moléculas

ENLACE COVALENTE vs. ENLACE IÓNICO Enlace Iónico Enlace covalente Los compuestos iónicos tienen Los compuestos covalentes tienen puntos de fusión y ebullición más elevados bajos. Los compuestos iónicos tiene baja Los compuestos covalentes son volatilidad más volátiles Los compuestos iónicos tienden a Los compuestos covalentes son ser solubles en agua típicamente insolubles en agua Los compuestos iónicos conducen electricidad ya que los iones están libres para moverse en estado fusionado. No conducen electricidad en estado sólido, al no tener iones libres para moverse Los compuestos covalentes no conducen electricidad al no tener iones presentes para pasar la carga

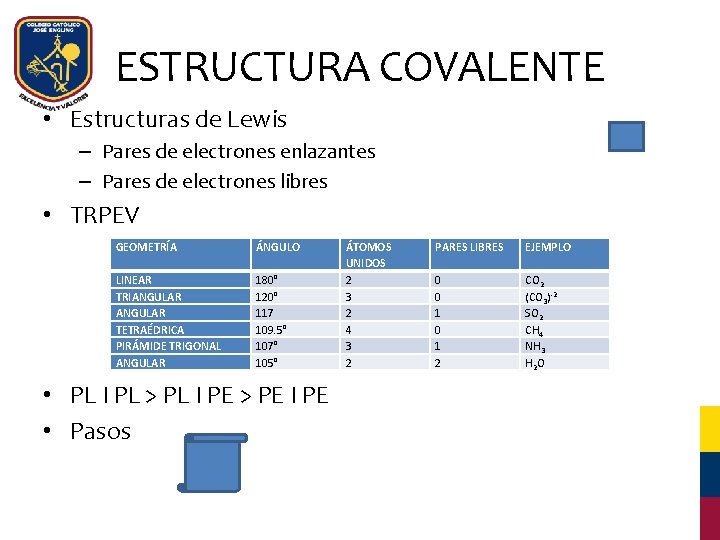
ESTRUCTURA COVALENTE • Estructuras de Lewis – Pares de electrones enlazantes – Pares de electrones libres • TRPEV GEOMETRÍA ÁNGULO LINEAR TRIANGULAR TETRAÉDRICA PIRÁMIDE TRIGONAL ANGULAR 180° 120° 117 109. 5° 107° 105° • PL І PL > PL І PE > PE І PE • Pasos ÁTOMOS UNIDOS 2 3 2 4 3 2 PARES LIBRES EJEMPLO 0 0 1 2 CO 2 (CO 3)-2 SO 2 CH 4 NH 3 H 2 O
![Ejemplos CCl 4 NH 4 NF 3 SF 2 Ejemplos • CCl 4 • [NH 4]+ • NF 3 • SF 2 •](https://slidetodoc.com/presentation_image/21e7e08261e93a4ef7ce85a7be450440/image-18.jpg)
Ejemplos • CCl 4 • [NH 4]+ • NF 3 • SF 2 • [NO 2] • [SO 3] • CO 2

Alótropos • Los alótropos del mismo elemento pueden variar tanto el propiedades físicas como en las químicas. • Estructuras covalentes sólidas: – Los átomos están sujetos mediante enlaces covalentes en una estructura de reja tridimensional gigante – Grafito, diamante, grafeno y cuarzo • Moleculares: – Fullereno C 60

Enlaces covalentes coordinados • Enlace covalente típico: el par de electrones compartidos se origina de ambos átomos que forman en enlace. • Enlace covalente coordinado: un par de electrones compartidos es donado por uno solo de los dos átomos. • Ejemplos – [NH 4]+ – [H 3 O]+ – CO – Al 2 Cl 6 Se representa con una flecha. Dativo

Fuerzas intermoleculares • Interacciones entre moléculas en un compuesto. • Responsables de las propiedades como punto de ebullición y fusión • Los tres tipos de fuerzas de atracción intermolecular principales son: – Fuerzas de London – Fuerzas dipolo-dipolo – Enlaces de hidrógeno

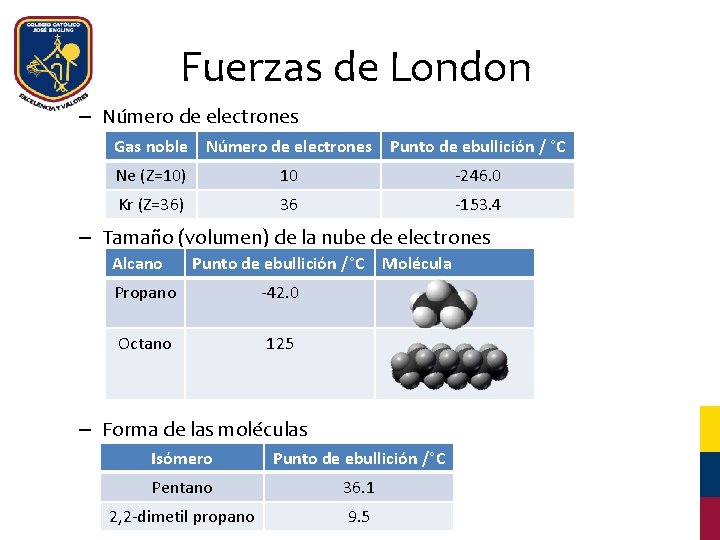
Fuerzas de London – Número de electrones Gas noble Número de electrones Punto de ebullición / °C Ne (Z=10) 10 -246. 0 Kr (Z=36) 36 -153. 4 – Tamaño (volumen) de la nube de electrones Alcano Punto de ebullición /°C Molécula Propano -42. 0 Octano 125 – Forma de las moléculas Isómero Punto de ebullición /°C Pentano 36. 1 2, 2 -dimetil propano 9. 5

Fuerzas dipolo-dipolo • Atracción entre el lado positivo de un dipolo permanente con el lado negativo de otro dipolo permanente en la molécula adyacente Isómero Punto de ebullición /°C Tipos de fuerzas intermoleculares presentes ICl (M=162. 35 gmol-1) 97. 4 Fuerzas de London + fuerzas dipolo-dipolo Br 2 (M=159380 gmol-1) 58. 5 Solo fuerzas de London

Enlaces de Hidrógeno • Fuerzas de atracción entre el átomo de hidrógeno de una molécula o de un fragmento de una molécula y un átomo o grupo de átomos. • Ocurre entre moléculas donde haya enlaces – H-F – O-H – N-H • Se representa con puntos o con guiones • Ejemplos – – H 2 O NH 3 HF (CH 3)2 O




