Enlace qumico I conceptos bsicos Captulo 9 Copyright

Enlace químico I: conceptos básicos Capítulo 9 Copyright © The Mc. Graw-Hill Companies, Inc. Permission required for reproduction or display.
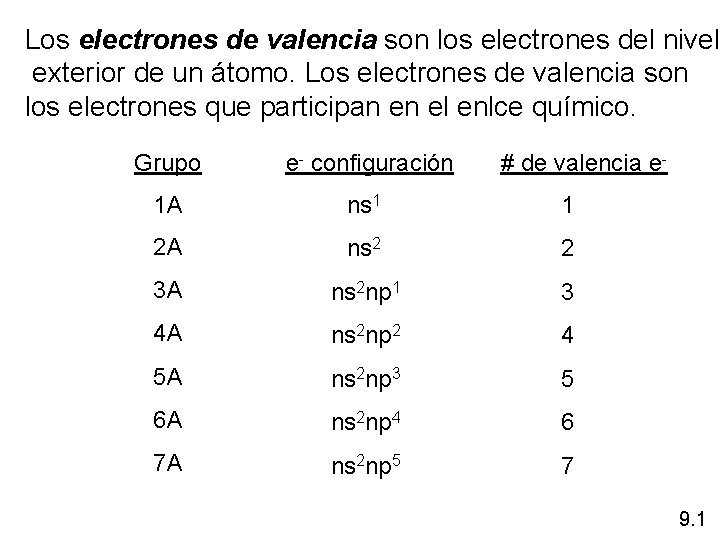
Los electrones de valencia son los electrones del nivel exterior de un átomo. Los electrones de valencia son los electrones que participan en el enlce químico. Grupo e- configuración # de valencia e- 1 A ns 1 1 2 A ns 2 2 3 A ns 2 np 1 3 4 A ns 2 np 2 4 5 A ns 2 np 3 5 6 A ns 2 np 4 6 7 A ns 2 np 5 7 9. 1
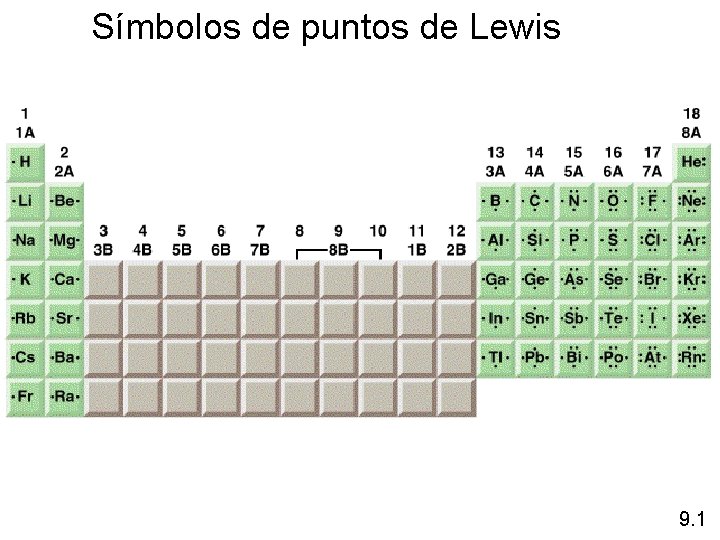
Símbolos de puntos de Lewis 9. 1
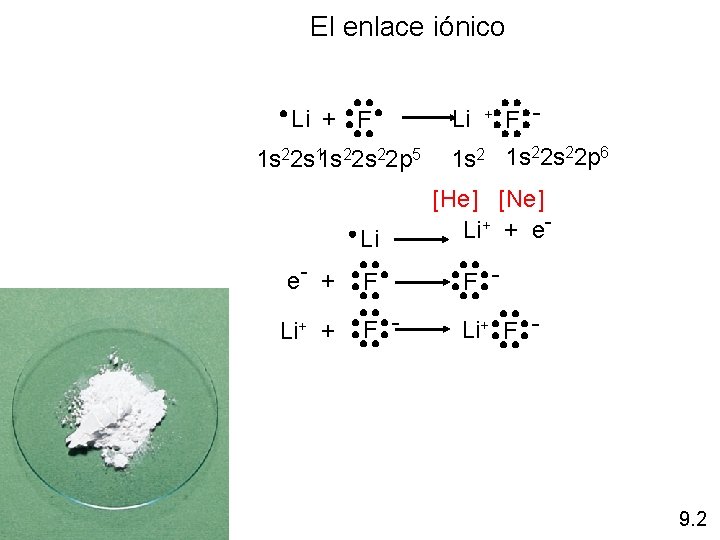
El enlace iónico Li + F 1 22 s 22 p 5 1 s 22 s 1 s Li e- + Li+ + Li + F 1 s 22 s 22 p 6 [He] [Ne] Li+ + e- F F - Li+ F - 9. 2
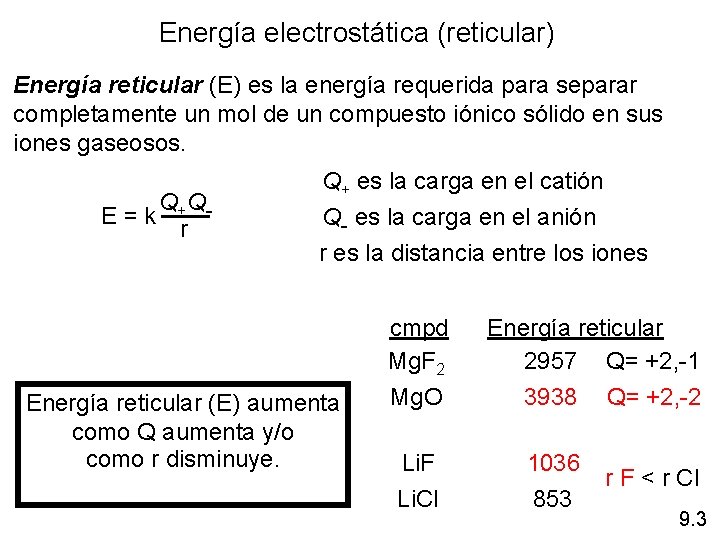
Energía electrostática (reticular) Energía reticular (E) es la energía requerida para separar completamente un mol de un compuesto iónico sólido en sus iones gaseosos. Q+QE = k r Q+ es la carga en el catión Q- es la carga en el anión r es la distancia entre los iones Energía reticular (E) aumenta como Q aumenta y/o como r disminuye. cmpd Mg. F 2 Mg. O Li. F Li. Cl Energía reticular 2957 Q= +2, -1 3938 Q= +2, -2 1036 853 r F < r Cl 9. 3
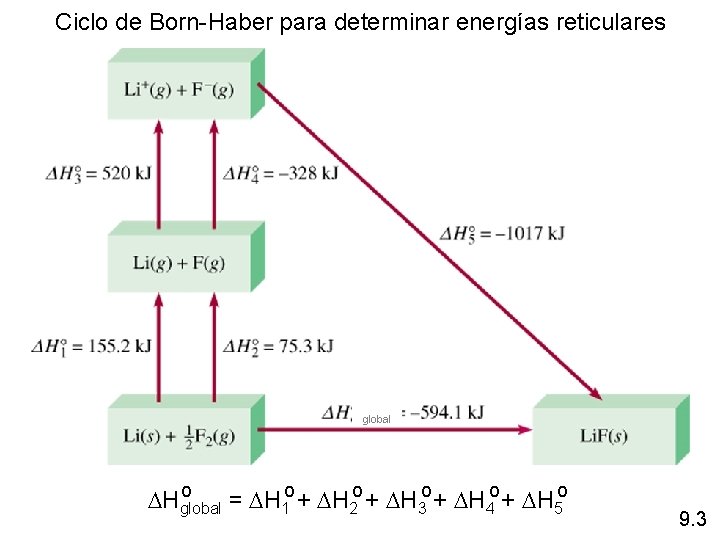
Ciclo de Born-Haber para determinar energías reticulares global o DHglobal = DH 1 o + DH 2 o + DH 3 o + DH 4 o + DH 5 o 9. 3
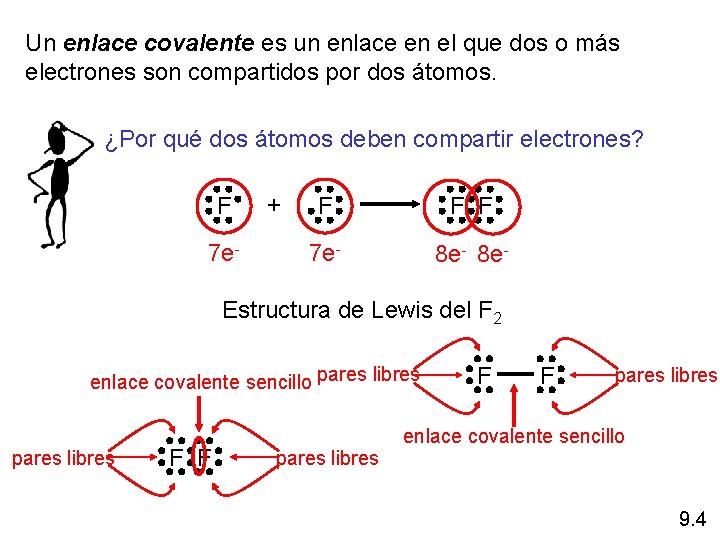
Un enlace covalente es un enlace en el que dos o más electrones son compartidos por dos átomos. ¿Por qué dos átomos deben compartir electrones? F 7 e- + F F F 7 e- 8 e- Estructura de Lewis del F 2 enlace covalente sencillo pares libres F F pares libres enlace covalente sencillo 9. 4
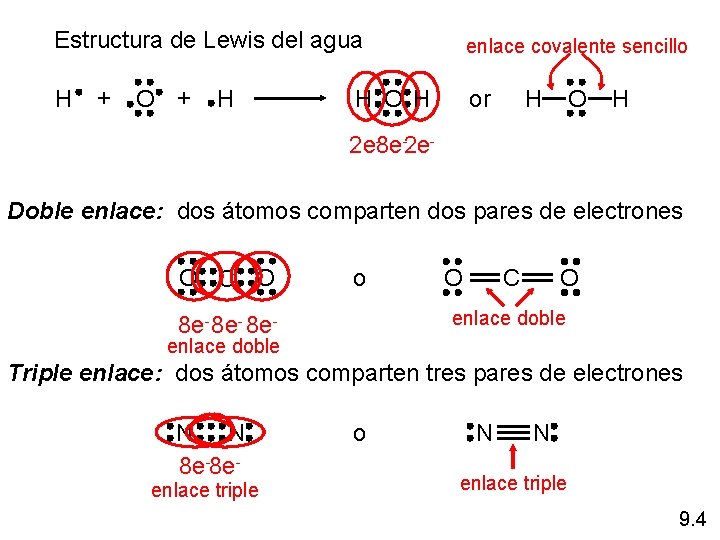
Estructura de Lewis del agua H + O + H enlace covalente sencillo H O H or H O H 2 e-8 e-2 e. Doble enlace: dos átomos comparten dos pares de electrones O C O o O O C enlace doble 8 e- 8 e- enlace doble Triple enlace: dos átomos comparten tres pares de electrones N N 8 e-8 e- enlace triple o N N enlace triple 9. 4
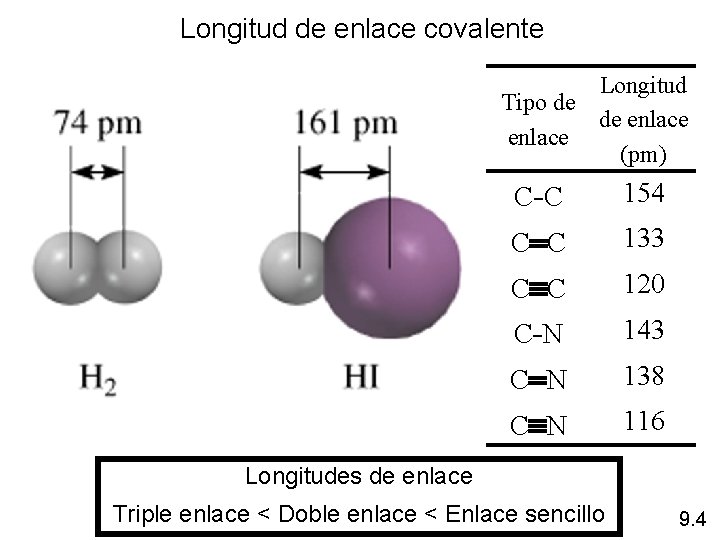
Longitud de enlace covalente Longitud Tipo de de enlace (pm) C -C 154 C C 133 C C 120 C -N 143 C N 138 C N 116 Longitudes de enlace Triple enlace < Doble enlace < Enlace sencillo 9. 4
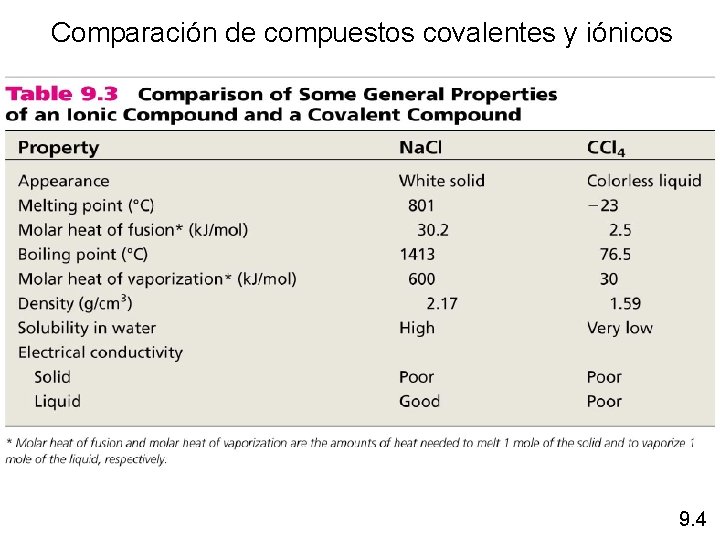
Comparación de compuestos covalentes y iónicos 9. 4
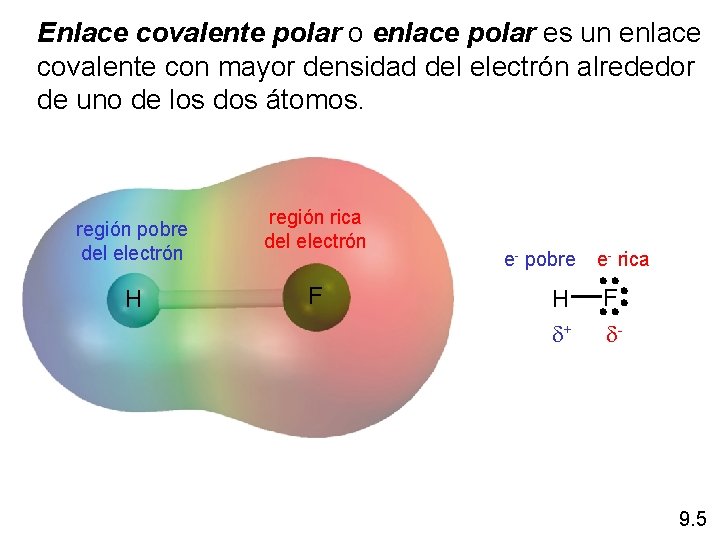
Enlace covalente polar o enlace polar es un enlace covalente con mayor densidad del electrón alrededor de uno de los dos átomos. región pobre del electrón H región rica del electrón F e- pobre H d+ e- rica F d- 9. 5
Electronegatividad es la capacidad de un átomo para atraer hacia sí los electrones de un enlace químico. Afinidad electrónica medible, Cl es más alta X (g) + e- X-(g) Electronegatividad relativa, F es más alta 9. 5

Electronegatividad de los elementos comunes Aumento de electronegatividad 9. 5
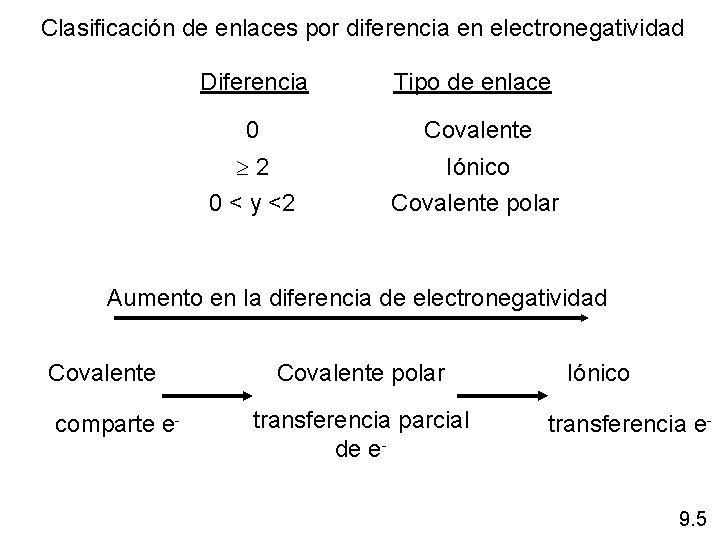
Clasificación de enlaces por diferencia en electronegatividad Diferencia Tipo de enlace 0 Covalente 2 0 < y <2 Iónico Covalente polar Aumento en la diferencia de electronegatividad Covalente comparte e- Covalente polar transferencia parcial de e- Iónico transferencia e- 9. 5

Clasifique los enlaces siguientes como iónico, covalente polar, o covalente: El enlace en Cs. Cl; el enlace en H 2 S y los enlaces en H 2 NNH 2. Cs – 0. 7 Cl – 3. 0 – 0. 7 = 2. 3 Iónico H – 2. 1 S – 2. 5 – 2. 1 = 0. 4 Covalente polar N – 3. 0 – 3. 0 = 0 Covalente 9. 5

Escritura de las estructuras de Lewis 1. Escriba la estructura fundamental del compuesto mostrando qué átomos están unidos entre sí. Ponga el elemento menos electronegativo en el centro. 2. Cuente el número total de electrones de valencia. Agregue 1 para cada carga negativa. Reste 1 para cada carga positiva. 3. Complete un octeto para todos los átomos excepto el hidrógeno. 4. Si la estructura contiene demasiados electrones, forme enlaces dobles y triples en el átomo 9. 6 central como necesite.
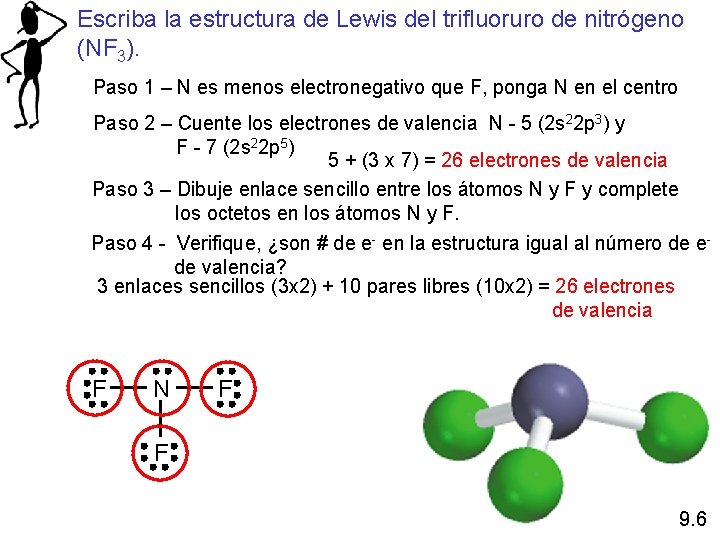
Escriba la estructura de Lewis del trifluoruro de nitrógeno (NF 3). Paso 1 – N es menos electronegativo que F, ponga N en el centro Paso 2 – Cuente los electrones de valencia N - 5 (2 s 22 p 3) y F - 7 (2 s 22 p 5) 5 + (3 x 7) = 26 electrones de valencia Paso 3 – Dibuje enlace sencillo entre los átomos N y F y complete los octetos en los átomos N y F. Paso 4 - Verifique, ¿son # de e- en la estructura igual al número de e- de valencia? 3 enlaces sencillos (3 x 2) + 10 pares libres (10 x 2) = 26 electrones de valencia F N F F 9. 6

Escriba la estructura de Lewis del ion carbonato (CO 32 -). Paso 1 – C es menos electronegativo que O, ponga C en el centro Paso 2 – Cuente los electrones de valencia C - 4 (2 s 22 p 2) y O - 6 (2 s 22 p 4) -2 carga – 2 e- 4 + (3 x 6) + 2 = 24 electrones de valencia Paso 3 – Dibuje enlace sencillo entre los átomos C y O y complete los octetos en los átomos C y O. Paso 4 - Verifique, son # de e- en la estructura igual al número de e- de valencia? 3 enlaces sencillos (3 x 2) + 10 pares libres (10 x 2) = 26 electrones de valencia Paso 5 - Demasiados electrones, forme el enlace doble y reverifique # de e 2 enlace sencillos (2 x 2) = O C O 4 1 enlace doble = 4 8 pares libres (8 x 2) = 16 Total = 24 O 9. 6
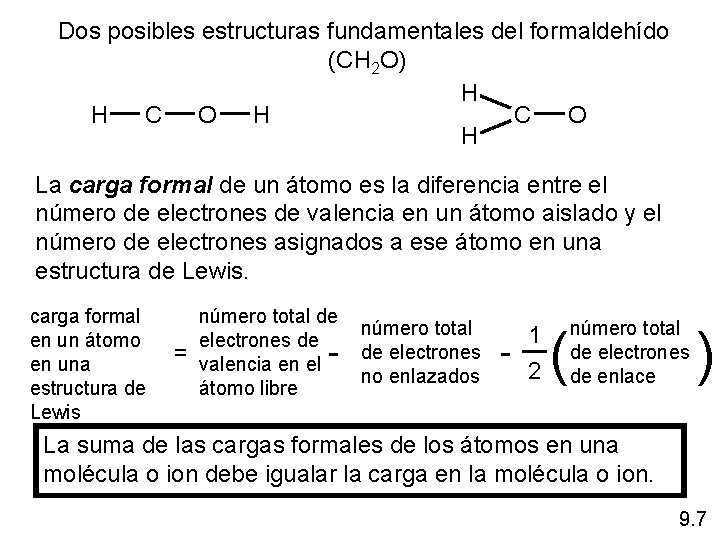
Dos posibles estructuras fundamentales del formaldehído (CH 2 O) H H C O H La carga formal de un átomo es la diferencia entre el número de electrones de valencia en un átomo aislado y el número de electrones asignados a ese átomo en una estructura de Lewis. carga formal en un átomo en una estructura de Lewis = número total de número total electrones de de electrones valencia en el no enlazados átomo libre - - 1 2 ( número total de electrones de enlace ) La suma de las cargas formales de los átomos en una molécula o ion debe igualar la carga en la molécula o ion. 9. 7
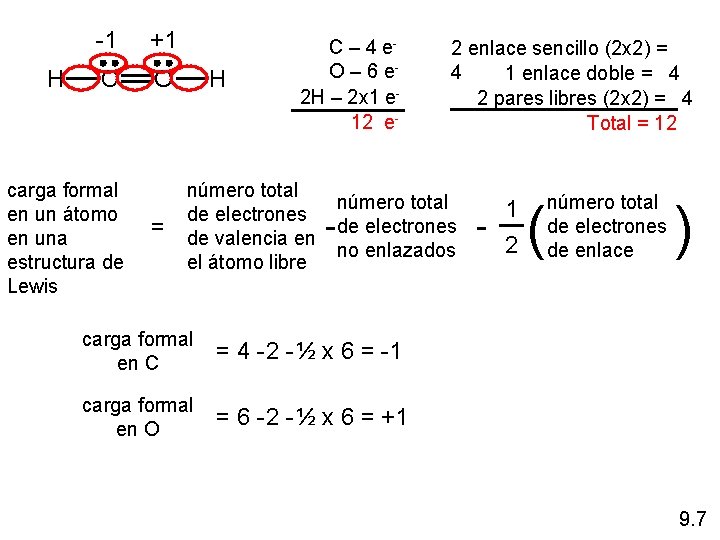
H -1 +1 C O carga formal en un átomo en una estructura de Lewis = H C – 4 e. O – 6 e 2 H – 2 x 1 e 12 e- 2 enlace sencillo (2 x 2) = 4 1 enlace doble = 4 2 pares libres (2 x 2) = 4 Total = 12 número total de electrones de valencia en no enlazados el átomo libre - carga formal en C = 4 -2 - ½ x 6 = -1 carga formal en O = 6 -2 - ½ x 6 = +1 - 1 2 ( número total de electrones de enlace ) 9. 7

H H 0 C carga formal en un átomo en una estructura de Lewis 0 O = C – 4 e. O – 6 e 2 H – 2 x 1 e 12 e- 2 enlace sencillo (2 x 2) = 4 1 enlace doble = 4 2 pares libres (2 x 2) = 4 Total = 12 número total de electrones de valencia en no enlazados el átomo libre - carga formal en C = 4 - 0 - ½ x 8 = 0 carga formal en O = 6 -4 - ½ x 4 = 0 - 1 2 ( número total de electrones de enlace ) 9. 7

Carga formal y estructura de Lewis 1. Para las moléculas neutras, una estructura de Lewis en que no hay cargas formales es preferible a una en que las cargas formales están presentes. 2. La estructura de Lewis con cargas formales grandes es menos probable que aquéllas con cargas formales pequeñas. 3. Entre las estructuras de Lewis que tienen distribuciones similares de cargas formales, la estructura más probable es la que las cargas formales negativas se ponen en los átomos más electronegativos. ¿Cuál es la estructura de Lewis más probable para CH 2 O? H -1 +1 C O H H H 0 C 0 O 9. 7
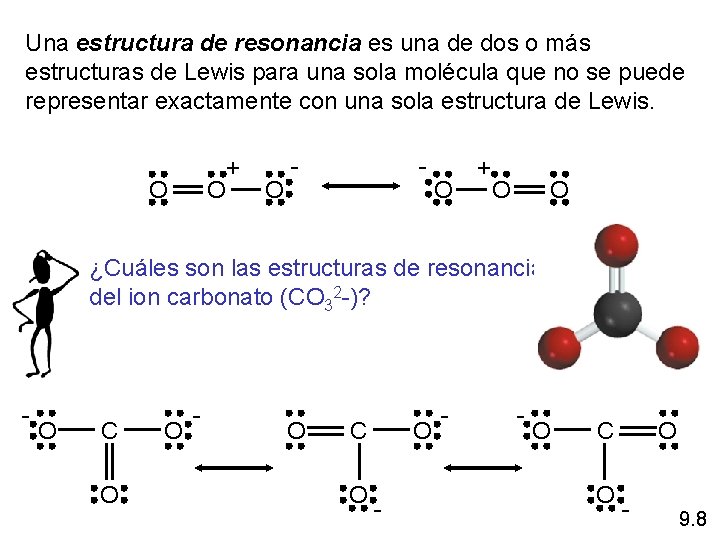
Una estructura de resonancia es una de dos o más estructuras de Lewis para una sola molécula que no se puede representar exactamente con una sola estructura de Lewis. O O + O - - O + O O ¿Cuáles son las estructuras de resonancia del ion carbonato (CO 32 -)? - O C O O - - - O C O O - 9. 8
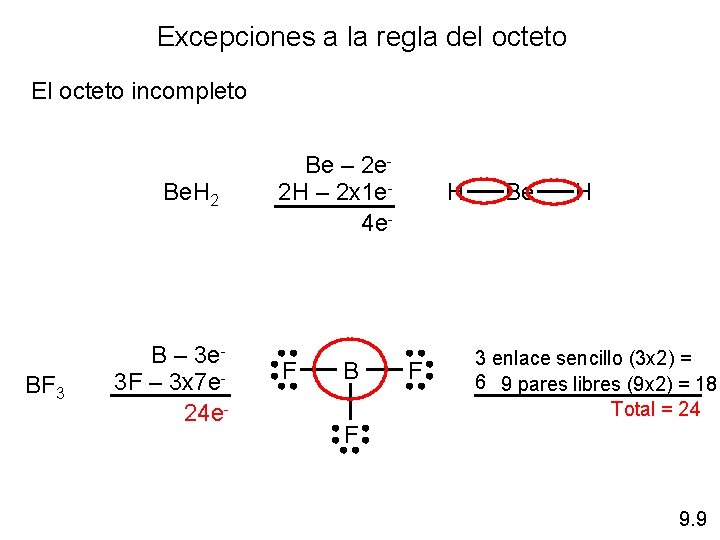
Excepciones a la regla del octeto El octeto incompleto Be. H 2 BF 3 B – 3 e 3 F – 3 x 7 e 24 e- Be – 2 e 2 H – 2 x 1 e 4 e- F B H F Be H 3 enlace sencillo (3 x 2) = 6 9 pares libres (9 x 2) = 18 Total = 24 F 9. 9
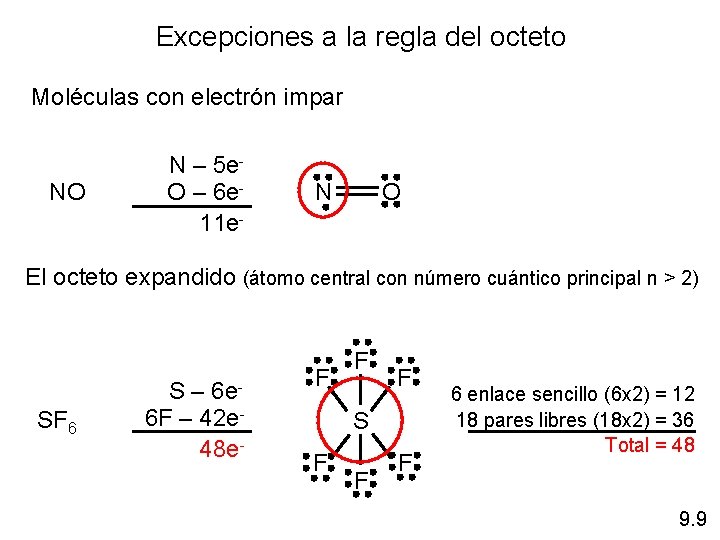
Excepciones a la regla del octeto Moléculas con electrón impar NO N – 5 e. O – 6 e 11 e- N O El octeto expandido (átomo central con número cuántico principal n > 2) SF 6 S – 6 e 6 F – 42 e 48 e- F F F S F F F 6 enlace sencillo (6 x 2) = 12 18 pares libres (18 x 2) = 36 Total = 48 9. 9
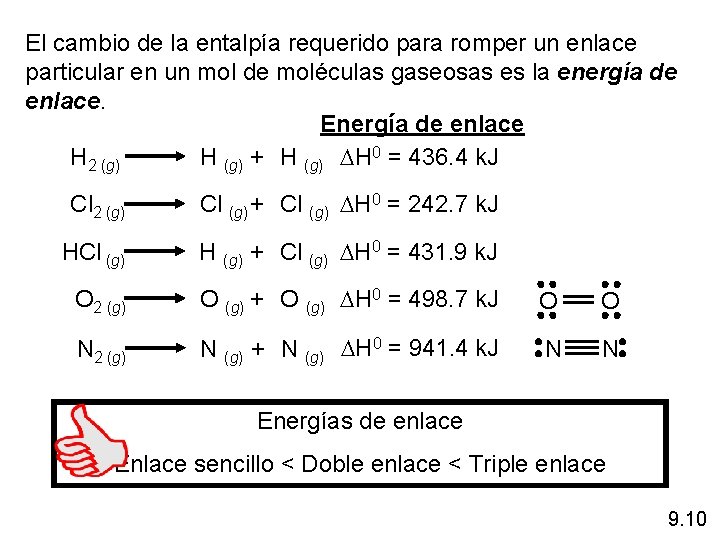
El cambio de la entalpía requerido para romper un enlace particular en un mol de moléculas gaseosas es la energía de enlace. Energía de enlace H 2 (g) H (g) + H (g) DH 0 = 436. 4 k. J Cl 2 (g) Cl (g) + Cl (g) DH 0 = 242. 7 k. J HCl (g) H (g) + Cl (g) DH 0 = 431. 9 k. J O 2 (g) O (g) + O (g) DH 0 = 498. 7 k. J O O N 2 (g) N (g) + N (g) DH 0 = 941. 4 k. J N N Energías de enlace Enlace sencillo < Doble enlace < Triple enlace 9. 10
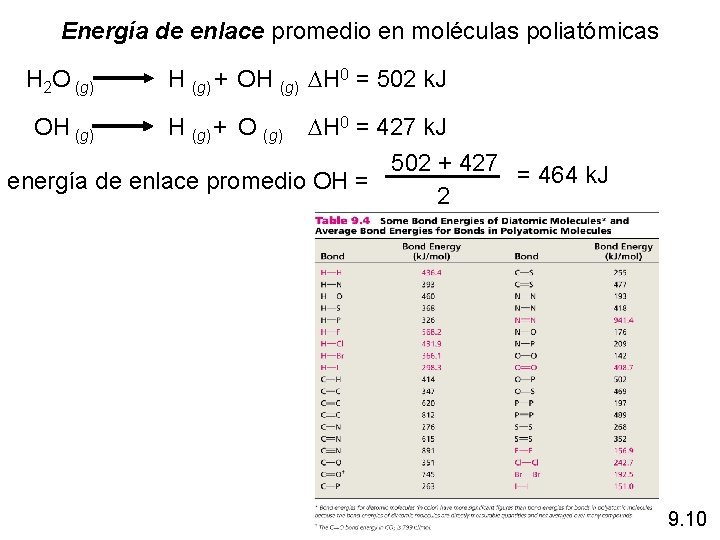
Energía de enlace promedio en moléculas poliatómicas H 2 O (g) H (g) + OH (g) DH 0 = 502 k. J DH 0 = 427 k. J 502 + 427 = 464 k. J energía de enlace promedio OH = 2 OH (g) + O (g) 9. 10
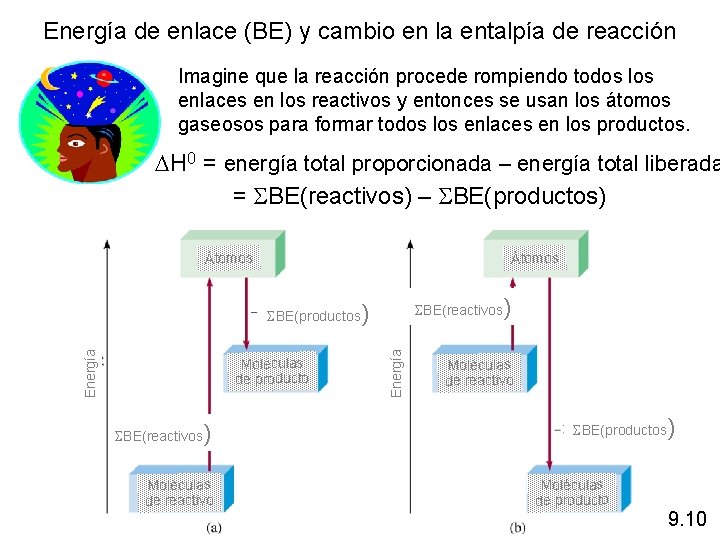
Energía de enlace (BE) y cambio en la entalpía de reacción Imagine que la reacción procede rompiendo todos los enlaces en los reactivos y entonces se usan los átomos gaseosos para formar todos los enlaces en los productos. DH 0 = energía total proporcionada – energía total liberada = SBE(reactivos) – SBE(productos) Átomos Moléculas de producto SBE(reactivos ) Moléculas de reactivo ) SBE(reactivos Energía SBE(productos ) Moléculas de reactivo SBE(productos Moléculas de producto ) 9. 10

Use la energía de enlaces para calcular el cambio de entalpía para: H + F 2 (g) 2 HF (g) DH 0 = SBE(reactivos) – SBE(productos) Tipo de enlaces que se rompen H H F F H F Tipo de enlaces formados Número de enlaces que se rompen 1 1 Número de enlaces formados 2 Energía de enlace (k. J/mol) Cambio de energía (k. J) 436. 4 156. 9 Energía de enlace (k. J/mol) Cambio de energía(k. J) 568. 2 1136. 4 DH 0 = 436. 4 + 156. 9 – 2 x 568. 2 = -543. 1 k. J 9. 10
- Slides: 29