ENLACE QUMICO 8 ao bsicos Propiedad Intelectual Cpech

ENLACE QUÍMICO 8° año básicos

Propiedad Intelectual Cpech

HABILIDADES Las habilidades que se desarrollarán en esta clase son: • • Reconocimiento Comprensión Aplicación Análisis Propiedad Intelectual Cpech
APRENDIZAJES ESPERADOS • Conocer y relacionar los diferentes tipos de enlaces químicos. • Conocer la geometría molecular de distintos compuestos químicos. Propiedad Intelectual Cpech
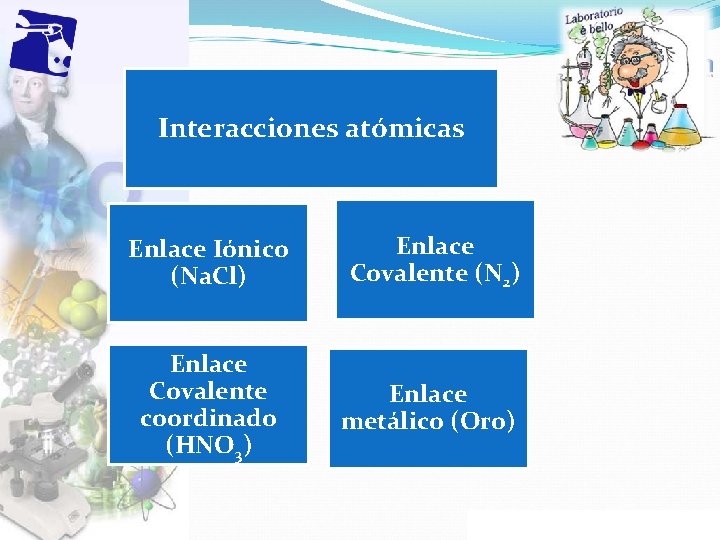
Interacciones atómicas Enlace Iónico (Na. Cl) Enlace Covalente (N 2) Enlace Covalente coordinado (HNO 3) Enlace metálico (Oro) Propiedad Intelectual Cpech
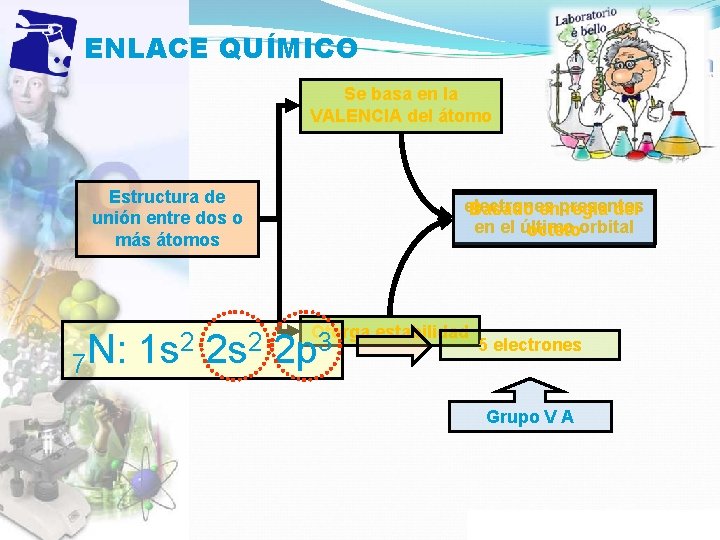
ENLACE QUÍMICO Se basa en la VALENCIA del átomo Estructura de unión entre dos o más átomos 7 N: 1 s 2 2 s 2 electrones Basado enpresentes regla del en el último octetoorbital Otorga estabilidad 2 p 3 5 electrones Grupo V A Propiedad Intelectual Cpech
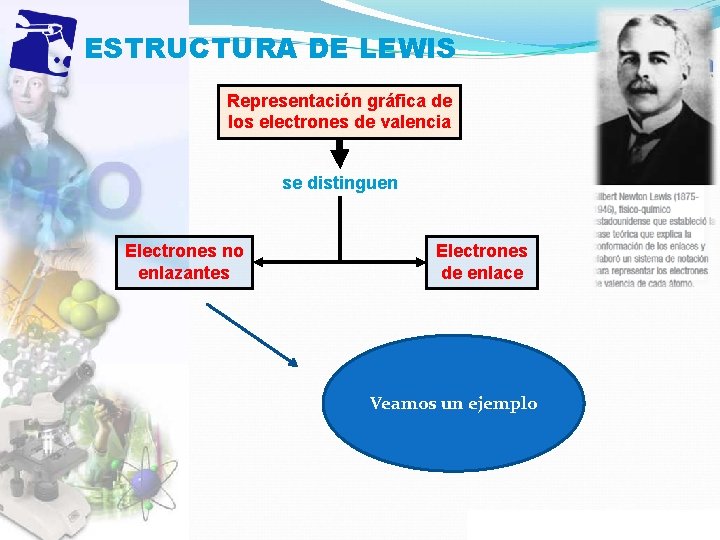
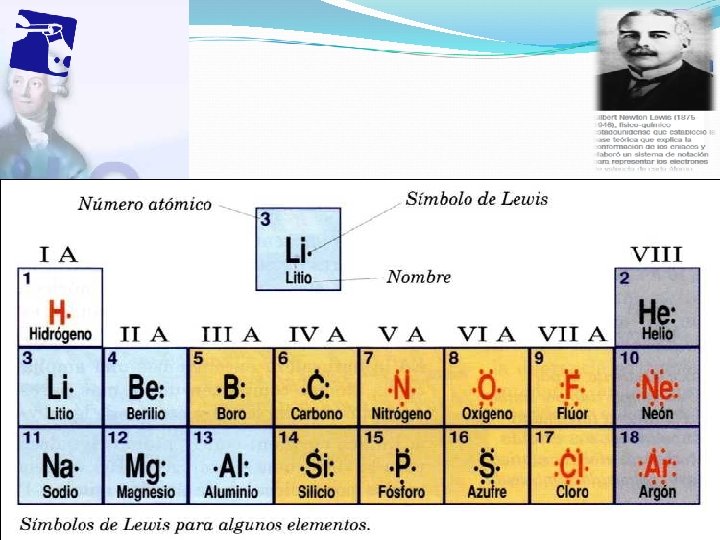
ESTRUCTURA DE LEWIS Representación gráfica de los electrones de valencia se distinguen Electrones no enlazantes Electrones de enlace Veamos un ejemplo Propiedad Intelectual Cpech
Propiedad Intelectual Cpech
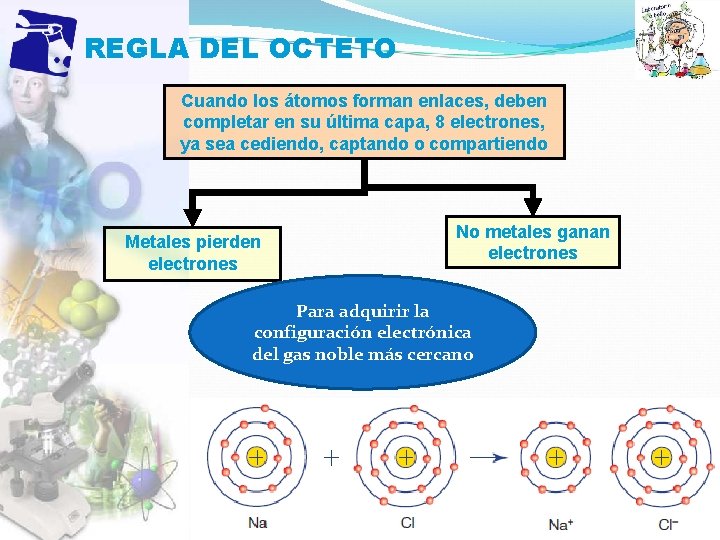
REGLA DEL OCTETO Cuando los átomos forman enlaces, deben completar en su última capa, 8 electrones, ya sea cediendo, captando o compartiendo Metales pierden electrones No metales ganan electrones Para adquirir la configuración electrónica del gas noble más cercano Propiedad Intelectual Cpech

Regla del Dueto Existen átomos como el: Hidrógeno Helio Litio Que completan en su última capa solo 2 electrones Propiedad Intelectual Cpech
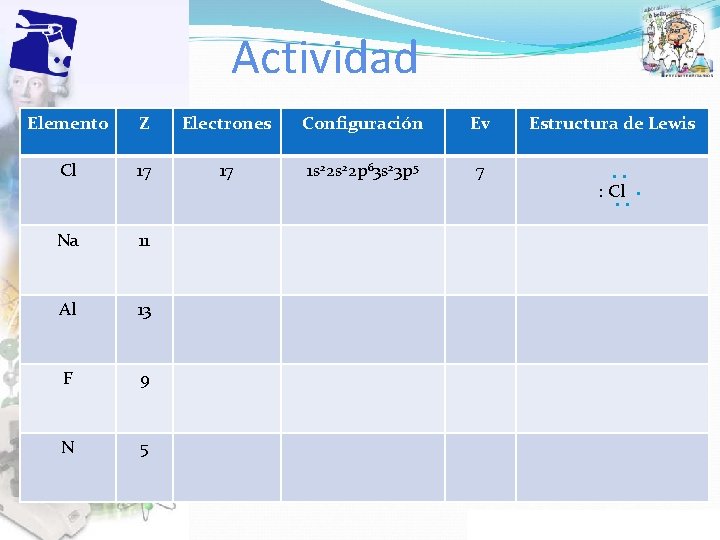
Actividad Elemento Z Electrones Configuración Ev Cl 17 17 1 s 22 p 63 s 23 p 5 7 Na 11 Al 13 F 9 N 5 Estructura de Lewis. . : Cl. . . Propiedad Intelectual Cpech

Objetivo de la clase Conocen y relacionan los diferentes tipos de enlaces químicos. Realizan Enlace Iónico Realizan Enlace Covalente Propiedad Intelectual Cpech
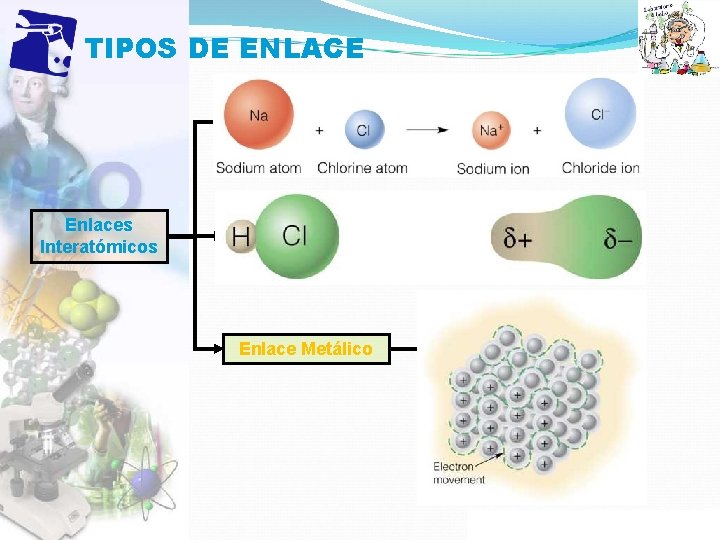
TIPOS DE ENLACE Enlaces Interatómicos Enlace Iónico Unión entre iones de cargas opuestas Enlace Covalente Unión por “compartición” de electrones Enlace Metálico Unión entre átomos por electrones deslocalizados y móviles Propiedad Intelectual Cpech
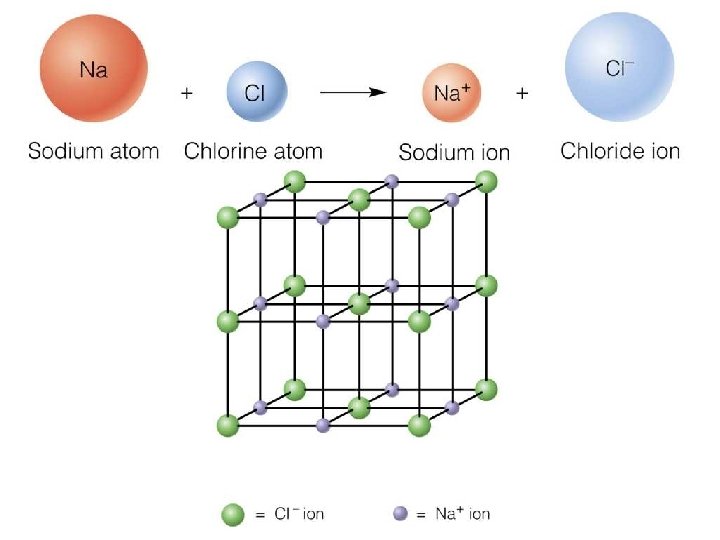
ENLACE IÓNICO Unión entre iones de cargas opuestas Se establece entre elementos con gran diferencia de electronegatividades Transferencia de electrones Metal No Metal IA – IIA VIA – VIIA Propiedad Intelectual Cpech 1, 7

El enlace iónico Ø Se forma entre elementos que tienen bajas energías de ionización (forman cationes fácilmente) y elementos que tienen altas afinidades electrónicas (forman aniones con facilidad) Ø Resultan de la combinación de metales alcalinos y alcalinotérreos con los halógenos u oxígeno Ø Las fuerzas de unión entre iones son de tipo electrostático (ley de Coulomb) Ejemplo: Li. F es un compuesto iónico típico. El Li pierde un electrón y forma Li+ y el F gana un electrón y forma F. Nótese que el Li+ tiene la configuración electrónica del He y el F la del Ne Propiedad Intelectual Cpech
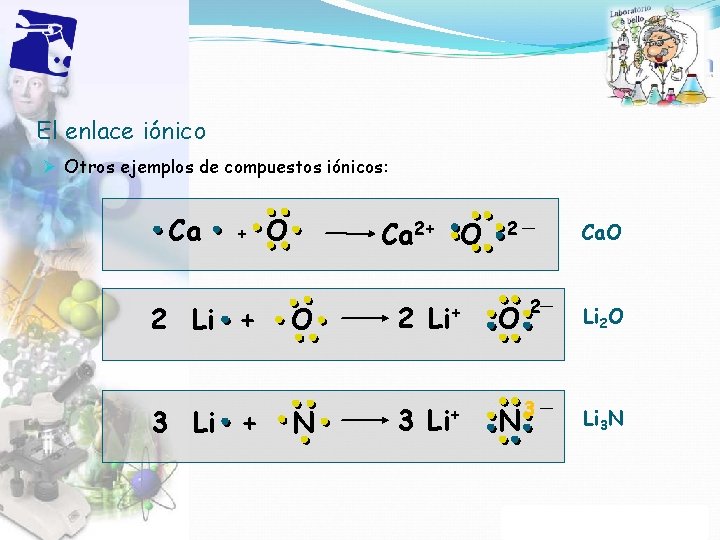
El enlace iónico Ø Otros ejemplos de compuestos iónicos: Ca + 2 Li + 3 Li + O Ca 2+ O 2 Li+ O N Li+ 3 N Ca. O 2 3 Li 2 O Li 3 N Propiedad Intelectual Cpech

Propiedades de los compuestos iónicos Ø Compuestos cristalinos Ø Los iones se disponen según unos ordenamientos específicos que se repiten periódicamente en el espacio Ø Altos puntos de fusión y de ebullición (elevadas fuerzas de unión entre los iones de la red cristalina) Ø Sólidos duros, rígidos (no se deforman) y quebradizos (se rompen sin deformarse) Propiedad Intelectual Cpech

Propiedades de los compuestos iónicos Ø No son conductores de la electricidad en estado sólido pero sí lo hacen en estado fundido o en disolución Sólido iónico fundido Sólido iónico disuelto en agua Propiedad Intelectual Cpech

Objetivo de la clase Conocer características de un enlace covalente Formular enlace covalente ENLACE COVALENTE Propiedad Intelectual Cpech

Enlace Covalente A diferencia del enlace Iónico, donde los metales pierden sus electrones de valencia y los no metales ganan electrones de valencia. En el enlace covalente, se produce entre elementos No Metálicos, donde sus electrones de valencia no se transfieren de un átomo a otro. En este caso los átomos comparten sus electrones. ¿Para qué? . . . Para lograr la estabilidad… Propiedad Intelectual Cpech
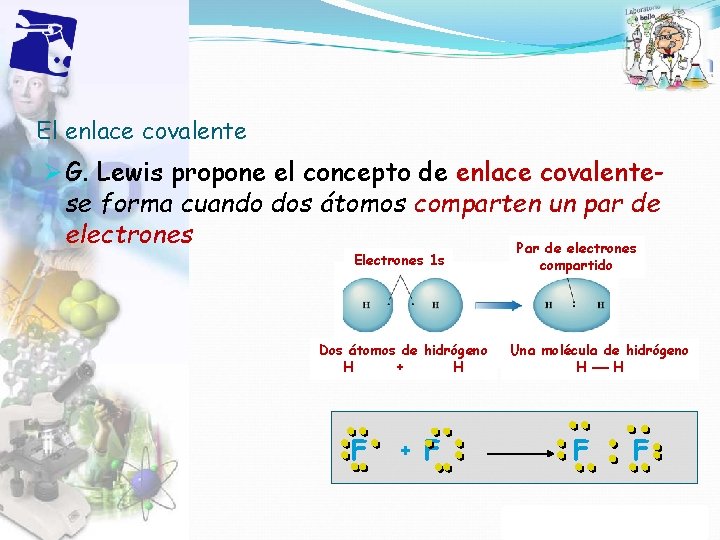
El enlace covalente Ø G. Lewis propone el concepto de enlace covalentese forma cuando dos átomos comparten un par de electrones Par de electrones Electrones 1 s Dos átomos de hidrógeno H + H F + F compartido Una molécula de hidrógeno H H F Propiedad Intelectual Cpech F
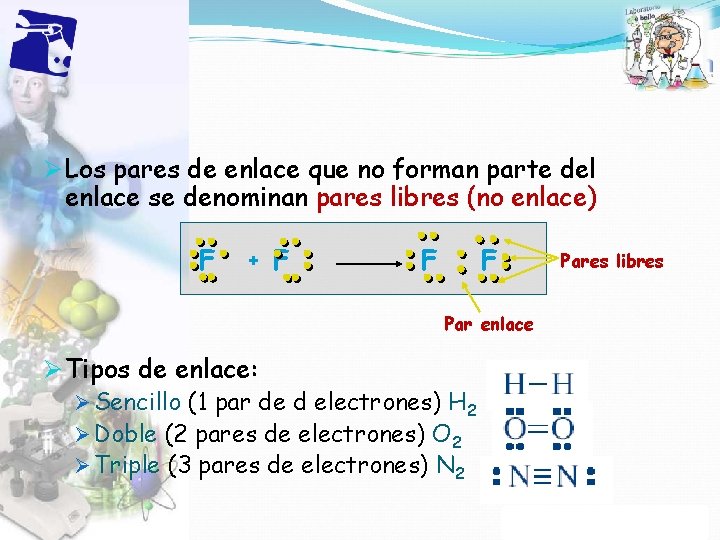
Ø Los pares de enlace que no forman parte del enlace se denominan pares libres (no enlace) F + F F F Pares libres Par enlace Ø Tipos de enlace: Ø Sencillo (1 par de d electrones) H 2 Ø Doble (2 pares de electrones) O 2 Ø Triple (3 pares de electrones) N 2 Propiedad Intelectual Cpech

Recordemos… Objetivo: ØConocer características de un enlace covalente ØFormular enlace covalente ØIdentificar enlace covalente polar y apolar Propiedad Intelectual Cpech
Actividad: Desarrolle estructura de Lewis en cada una de las moléculas Configuración ev electrónica Estructura de lewis Conformación de enlace covalente H 2 O Cl 2 S 2 HCl. O Propiedad Intelectual Cpech

Enlace covalente: Por medio de la EN, también podemos determinar que tipo de enlace se trata Enlace Covalente Apolar: se produce entre átomos de igual EN Si la ∆EN es 0: el enlace covalente es Apolar Ejemplo: Cl 2 ∆EN= 3. 5 -3. 5=0 Enlace covalente Polar: Se produce entre átomos que tienen distinta EN Si la ∆EN es mayor a 0 y menor a 1, 7: el enlace covalente es Polar Ejemplo: H 2 O ∆EN= 3. 0 – 2. 5= 0. 5 Propiedad Intelectual Cpech

Propiedades del enlace covalente Según como se unan los átomos, se pueden encontrar las sustancias RETICULARES y MOLECULARES Sustancia Reticular üSolo se presentan en estado sólido üPunto de fusión y ebullición muy altos üExtremadamente duros üInsolubles en todo tipo de solvente Ej: diamante Sustancia Molecular üSe presentan en los 3 estados de la materia üPuntos de fusión y ebullición relativamente bajos üMalos conductores de calor y electricidad üSon solubles en solventes Ej: Nitrógeno, alcohol, azúcar Propiedad Intelectual Cpech
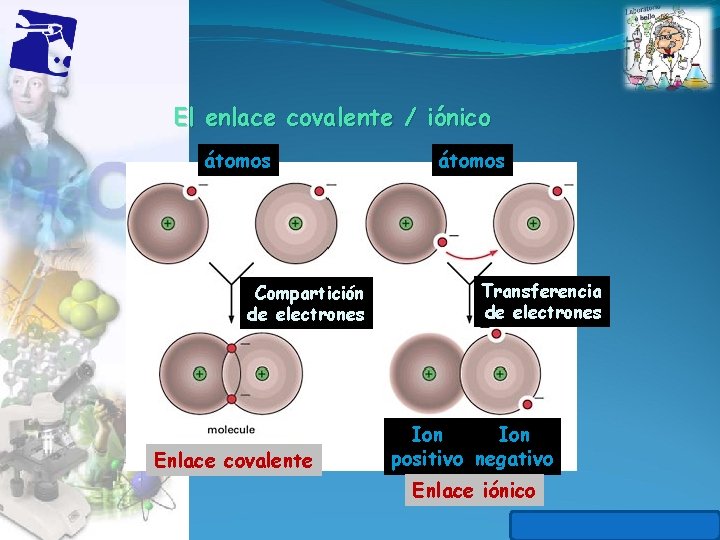
El enlace covalente / iónico átomos Compartición de electrones Enlace covalente átomos Transferencia de electrones Ion positivo negativo Enlace iónico Propiedad Intelectual Cpech

Enlace covalente coordinado En este tipo de enlace, una especie dona sus 2 electrones no compartidos y la otra los acepta átomo donador átomo aceptor Ejemplos: H 3 O+, NH 4+, SO 2, SO 3, HNO 3 Propiedad Intelectual Cpech
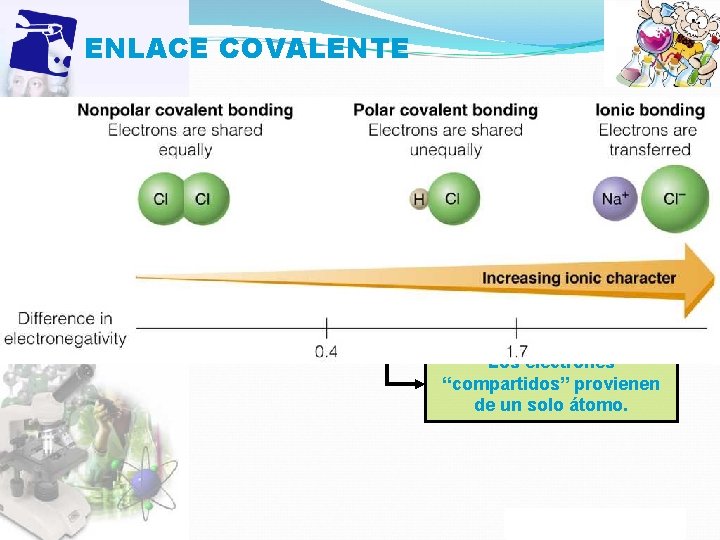
ENLACE COVALENTE Enlace Covalente Apolar Δ E. N. ≈ 0 Polar Δ E. N. ≤ 1, 7 núcleos ejercen una fuerza denúcleo atracción equivalente un tiene mas fuerza (enlace perfecto) que otro para atraer Coordinado electrones de enlace e. g. moléculas semonoelementales establecen dipolos También es(O un 2, enlace diatómicas H 2, N 2) covalente polar Los electrones “compartidos” provienen de un solo átomo. Propiedad Intelectual Cpech
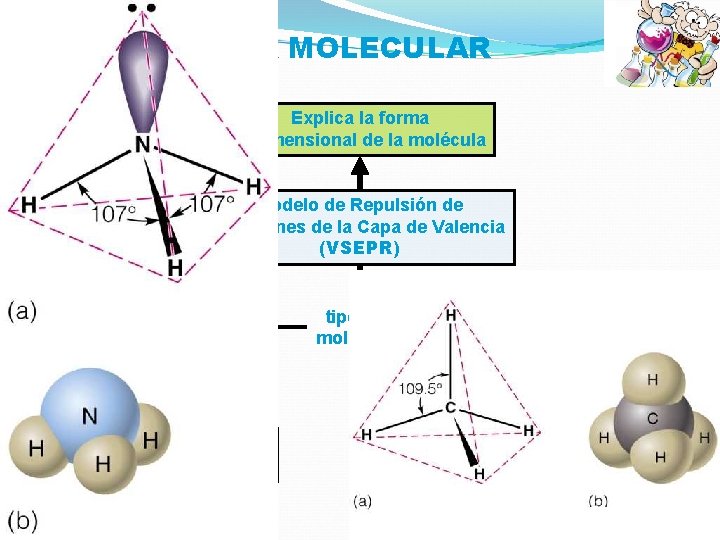
GEOMETRÍA MOLECULAR Explica la forma tridimensional de la molécula Modelo de Repulsión de Electrones de la Capa de Valencia (VSEPR) Sin pares de electrones libres en el átomo central Electrones enlazantes mantienen equidistancia tipos de moléculas Con pares de electrones libres en el átomo central Electrones libres repelen a electrones enlazantes Propiedad Intelectual Cpech
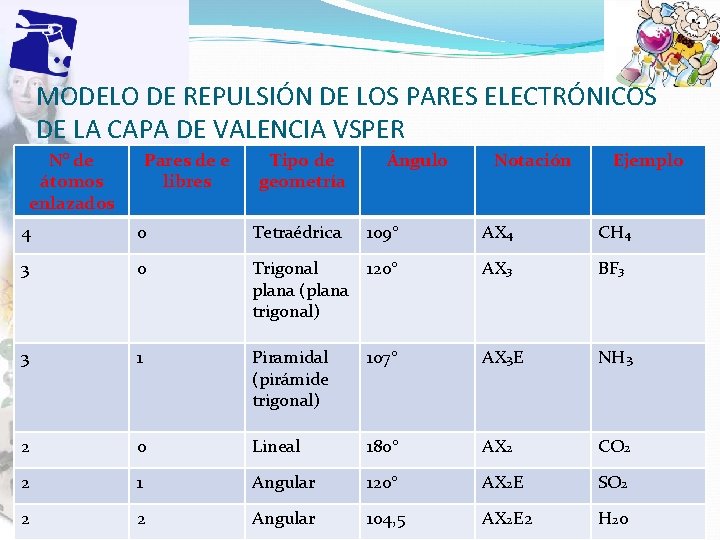
MODELO DE REPULSIÓN DE LOS PARES ELECTRÓNICOS DE LA CAPA DE VALENCIA VSPER N° de átomos enlazados Pares de e libres Tipo de geometría Ángulo Notación Ejemplo 4 0 Tetraédrica 109° AX 4 CH 4 3 0 Trigonal plana (plana trigonal) 120° AX 3 BF 3 3 1 Piramidal (pirámide trigonal) 107° AX 3 E NH 3 2 0 Lineal 180° AX 2 CO 2 2 1 Angular 120° AX 2 E SO 2 2 2 Angular 104, 5 AX 2 Propiedad E 2 Intelectual Cpech H 2 0
- Slides: 31