ENLACE COVALENTE OBJETIVO Conocer como se produce el
ENLACE COVALENTE

OBJETIVO • Conocer como se produce el enlace covalente • Conocer las propiedades y características del enlace covalente • Determinar la configuración electrónica de los átomos que participan en un enlace covalente • Conocer los tipos de enlace covalente que existen • Diferenciar entre enlace simple, doble y triple

ENLACE COVALENTE • La reacción entre dos no metales produce un enlace covalente. • El enlace covalente se forma por la compartición de uno o más pares de electrones entre dos átomos. • Existe un balance entre las fuerzas de atracción y repulsión
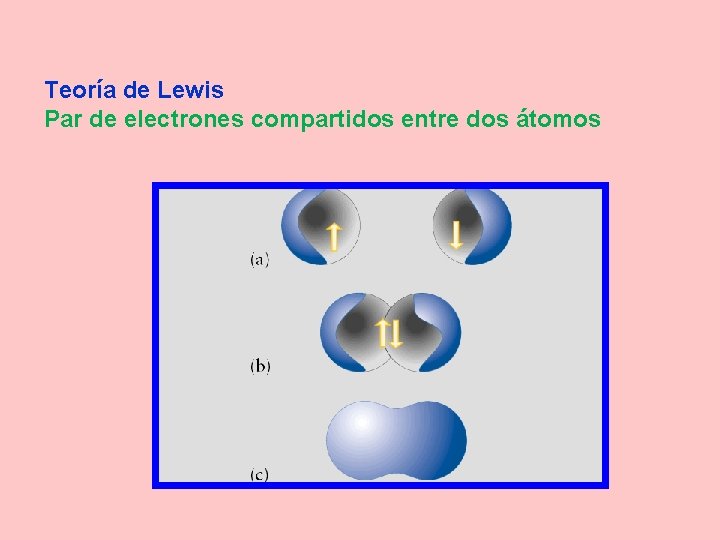
Teoría de Lewis Par de electrones compartidos entre dos átomos
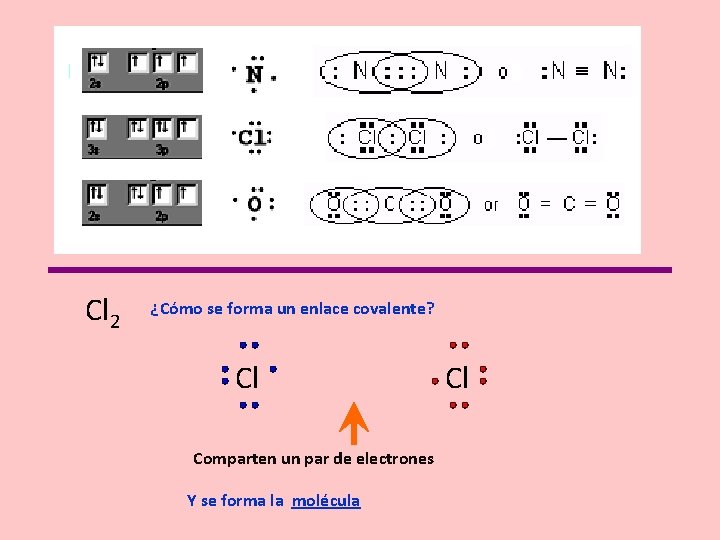
Cl 2 ¿Cómo se forma un enlace covalente? Cl Comparten un par de electrones Y se forma la molécula Cl
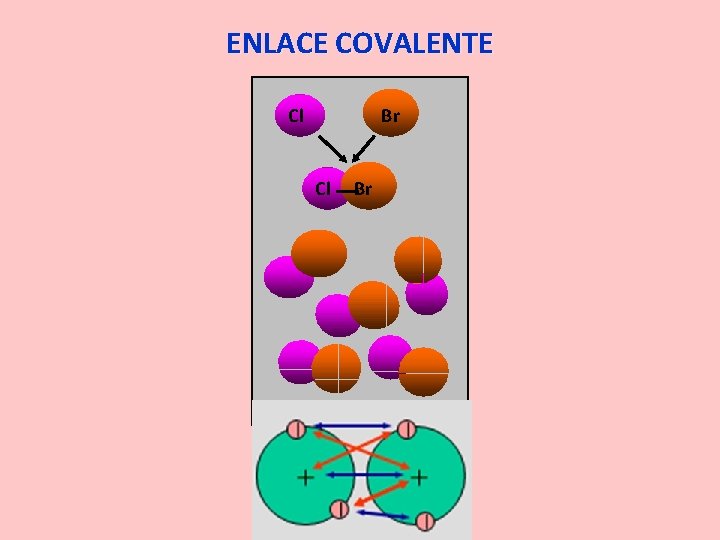
ENLACE COVALENTE Cl Br

_ Existen tres tipos de enlace covalente • Enlace covalente puro o apolar • Enlace covalente coordinado o dativo • Los electrones que forman enlace covalente puro (apolar) y polar son los desapareados del nivel de valencia
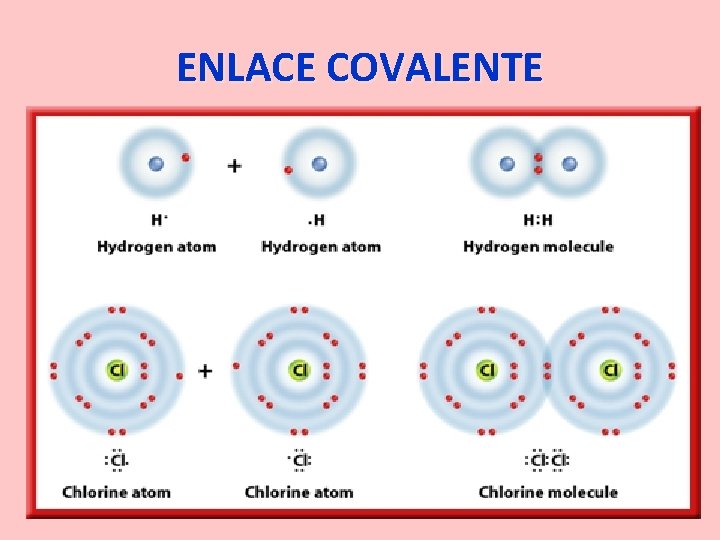
ENLACE COVALENTE
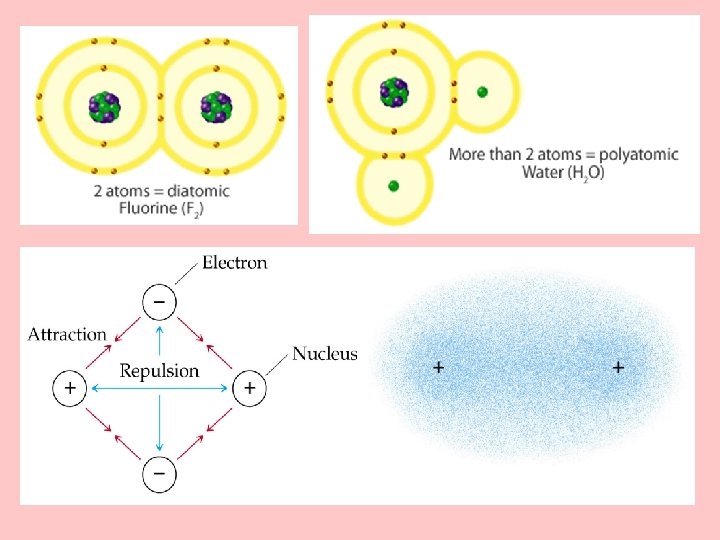

Tipos de Enlace Covalente Según número de electrones que participen en el enlace:
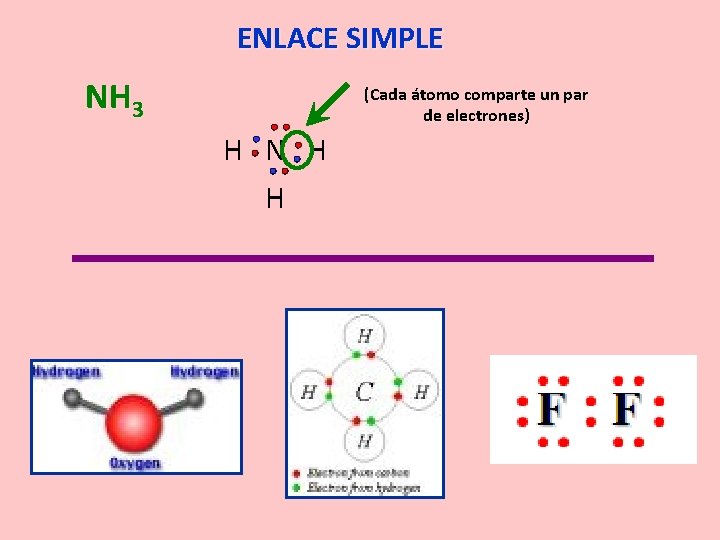
ENLACE SIMPLE NH 3 (Cada átomo comparte un par de electrones) H N H H
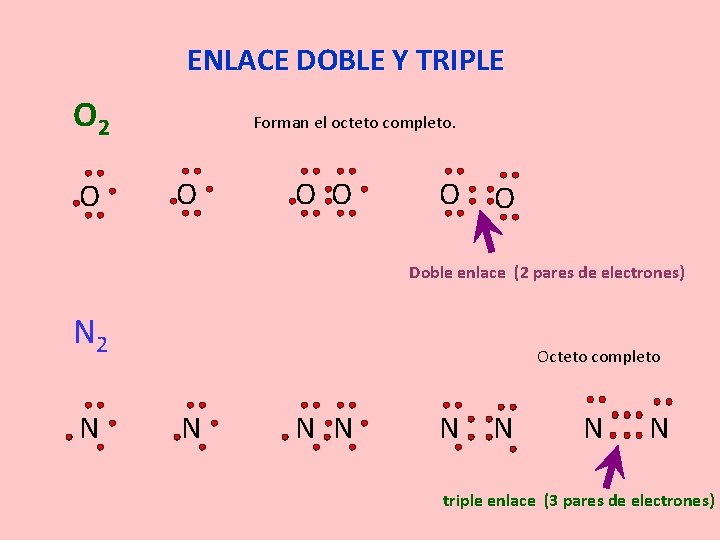
ENLACE DOBLE Y TRIPLE O 2 O Forman el octeto completo. O O O Doble enlace (2 pares de electrones) N 2 N Octeto completo N N N N triple enlace (3 pares de electrones)
Tipos de Enlace ENLACE COVALENTE CON ENLACE : ● ● ● SIMPLE DOBLE TRIPLE 13
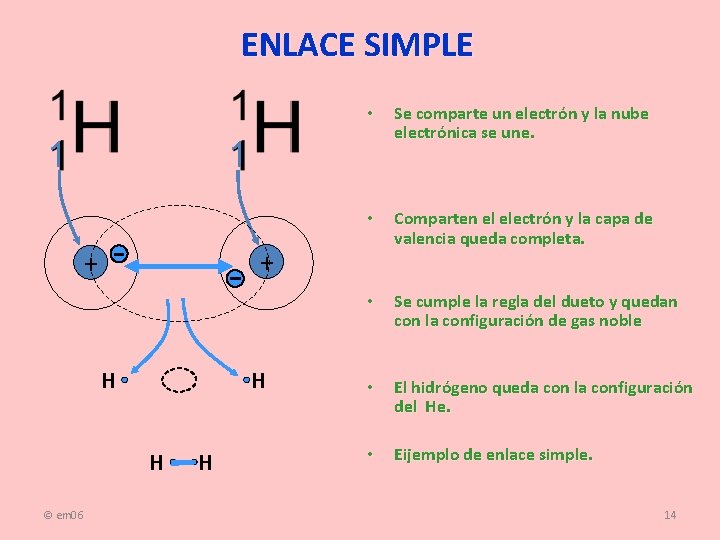
ENLACE SIMPLE 1 Se comparte un electrón y la nube electrónica se une. • Comparten el electrón y la capa de valencia queda completa. • Se cumple la regla del dueto y quedan con la configuración de gas noble • El hidrógeno queda con la configuración del He. • Eijemplo de enlace simple. 1 + + H H H © em 06 • H 14
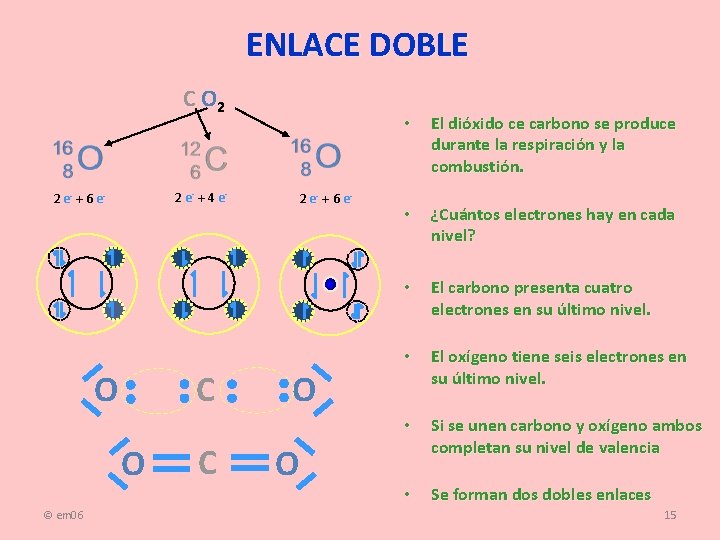
ENLACE DOBLE C O 2 2 e- + 4 e- 2 e- + 6 e- C O O © em 06 C 2 e- + 6 e- O O • El dióxido ce carbono se produce durante la respiración y la combustión. • ¿Cuántos electrones hay en cada nivel? • El carbono presenta cuatro electrones en su último nivel. • El oxígeno tiene seis electrones en su último nivel. • Si se unen carbono y oxígeno ambos completan su nivel de valencia • Se forman dos dobles enlaces 15
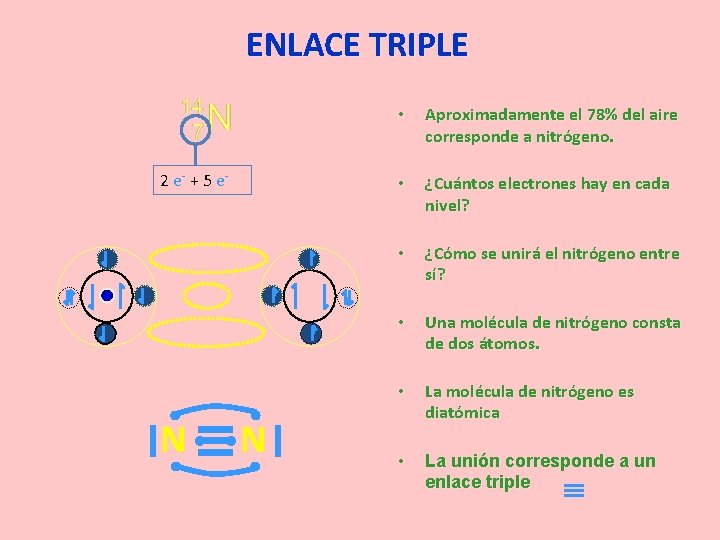
ENLACE TRIPLE 2 e- + 5 e- N N • Aproximadamente el 78% del aire corresponde a nitrógeno. • ¿Cuántos electrones hay en cada nivel? • ¿Cómo se unirá el nitrógeno entre sí? • Una molécula de nitrógeno consta de dos átomos. • La molécula de nitrógeno es diatómica • La unión corresponde a un enlace triple

Enlace covalente
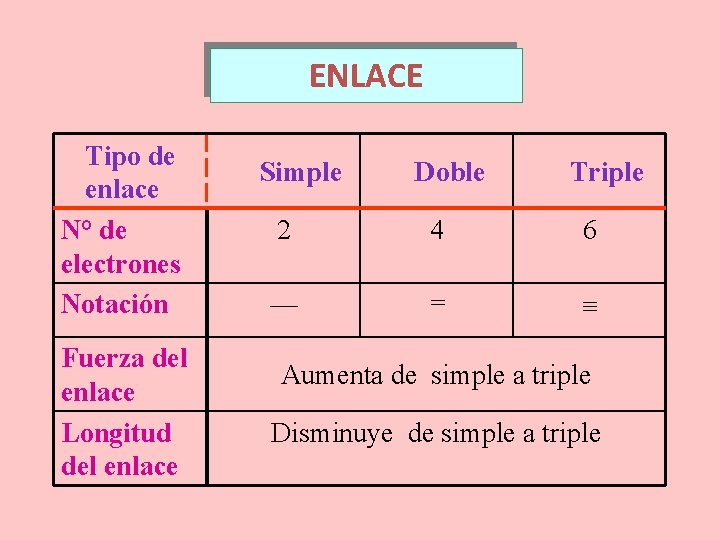
ENLACE Tipo de enlace N° de electrones Notación Fuerza del enlace Longitud del enlace Simple Doble Triple 2 4 6 — = Aumenta de simple a triple Disminuye de simple a triple

PROPIEDADES DEL ENLACE COVALENTE • Los compuestos líquidos o fundidos no conducen la electricidad • La mayoría es soluble en disolventes no polares, como el hexano C 6 H 14. • Son gases, líquidos o sólidos con bajos puntos de fusión y ebullición. • Las soluciones acuosas suelen ser malas conductoras de la electricidad porque no contienen partículas con carga. • Muchos de ellos son insolubles en disolventes polares.
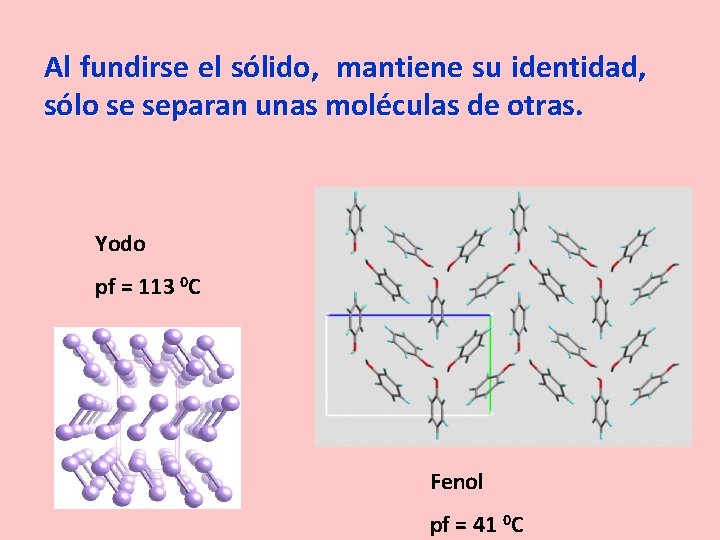
Al fundirse el sólido, mantiene su identidad, sólo se separan unas moléculas de otras. Yodo pf = 113 0 C Fenol pf = 41 0 C

Según la diferencia de electronegatividad, se clasifican en: • Enlace Covalente Polar • Enlace covalente Apolar Diferencia de Electronegatividad (∆EN): Enlace covalente Polar Diferencia de electronegatividad: Mayor que 0 y menor a 1, 7 Enlace covalente Apolar Diferencia de Electronegatividad es igual a 0
- Slides: 21