Energiebnder im Festkrper Inhalt Klassisch Energieniveaus eines freien

Energiebänder im Festkörper

Inhalt Klassisch: • Energieniveaus eines freien Atoms • Energie des Bohrschen Atommodells – Aufspaltung der Energieniveaus durch Kopplung bei Annäherung eines zweiten Atoms Quantenmechanik: • Alle Elektronen eines Festkörpers bilden eine quantenmechanische Gesamtheit, jedem Elektron wird eine Welle zugeordnet – Lösung der Schrödingergleichung für Elektronen im „Kasten“ • Daraus resultiert das Bändermodell für – Isolator – Halbleiter – Leiter
Kristalline Festkörper
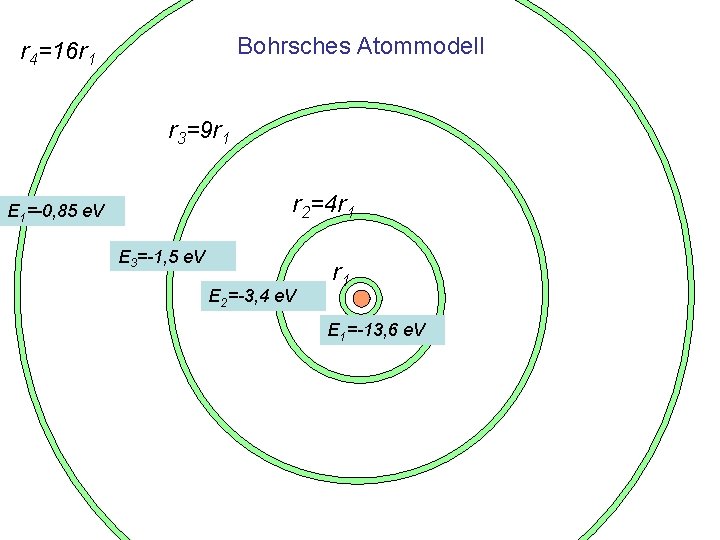
Bohrsches Atommodell r 4=16 r 1 r 3=9 r 1 r 2=4 r 1 E 1=-0, 85 e. V E 3=-1, 5 e. V E 2=-3, 4 e. V r 1 E 1=-13, 6 e. V

Klassisches Modell • Aufbau der Atome nach Bohrs Modell • Aufspaltung der Energieniveaus bei Kopplung an benachbarte Atome (analog dem Doppelpendel)
![Energie der Elektronen in Bohrs Atommodell Abstand vom Kern mal 0, 0529 [nm] Bindungsenergie Energie der Elektronen in Bohrs Atommodell Abstand vom Kern mal 0, 0529 [nm] Bindungsenergie](http://slidetodoc.com/presentation_image_h2/a5cdef12335bac6a54044f523c16e9b8/image-6.jpg)
Energie der Elektronen in Bohrs Atommodell Abstand vom Kern mal 0, 0529 [nm] Bindungsenergie E [e. V]
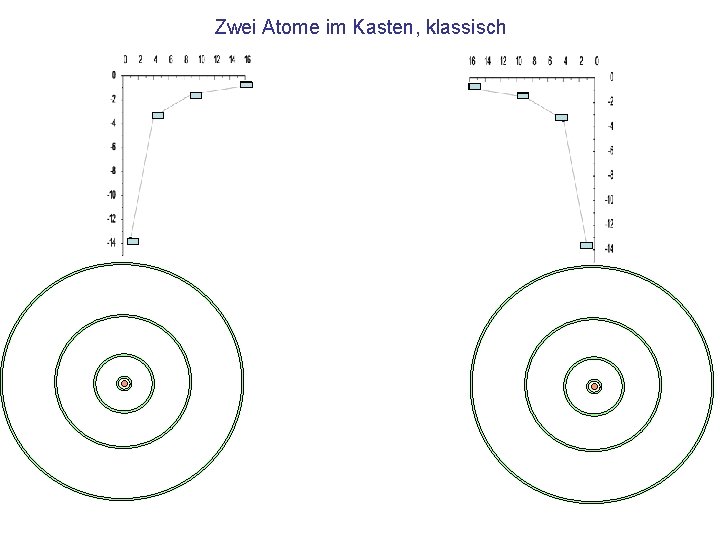
Zwei Atome im Kasten, klassisch
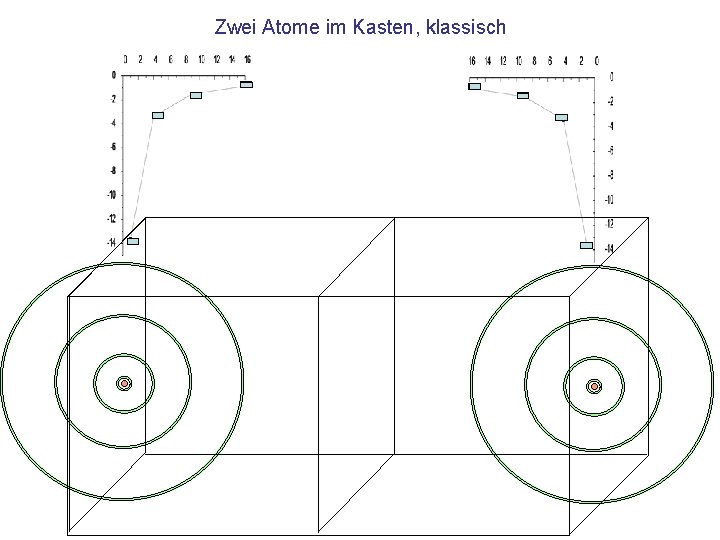
Zwei Atome im Kasten, klassisch

Quantenmechanisches Modell Die Elektronen von den in einem Festkörper gebundenen Atome werden als ein „gebundener Zustand“ aufgefasst • Anstelle der lokalisierten Atome treten stehende Wellen im „Kasten“ – Die Wellenlängen sind Teiler doppelten Kastenlänge • Anstelle der Energie der Elektronen in Abhängigkeit vom Bahnradius tritt die Energie der Wellen in Abhängigkeit von der Wellenzahl Berechnung mit der Schrödingergleichung für das Kastenpotential
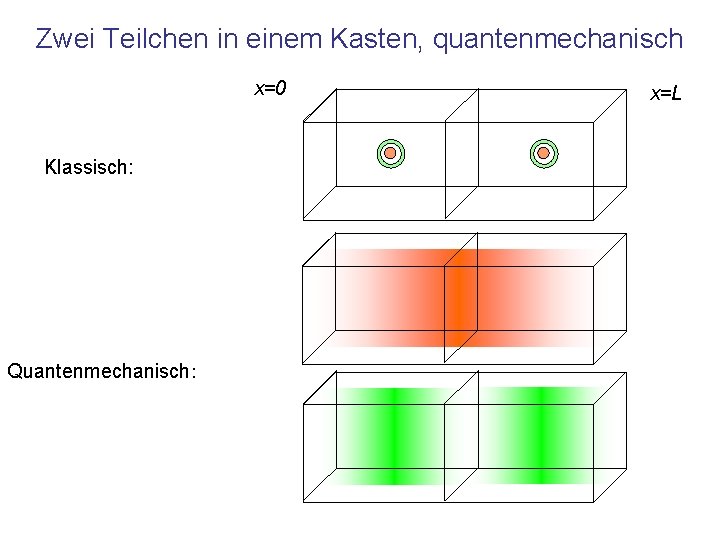
Zwei Teilchen in einem Kasten, quantenmechanisch x=0 Klassisch: Quantenmechanisch: x=L
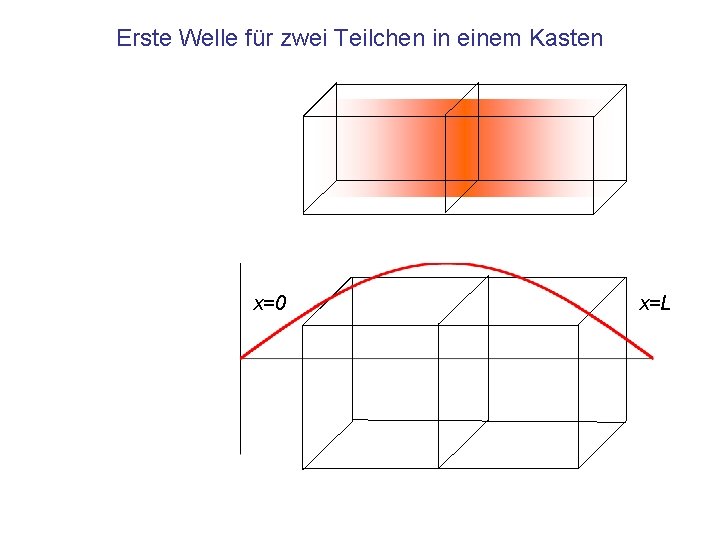
Erste Welle für zwei Teilchen in einem Kasten x=0 x=L
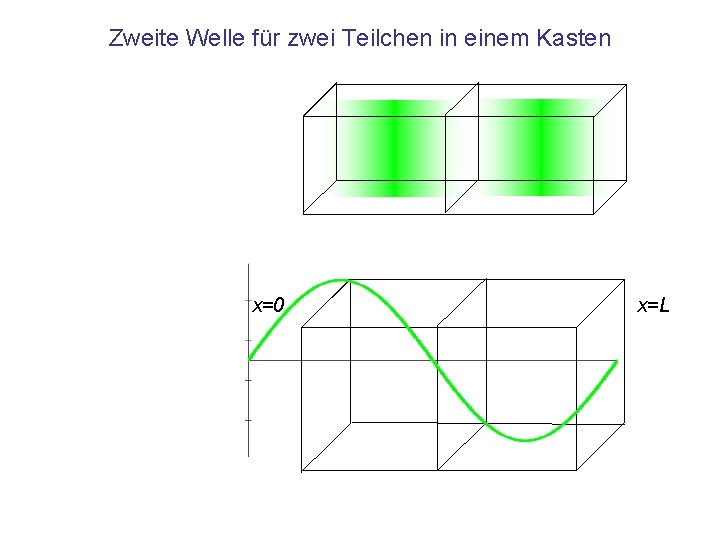
Zweite Welle für zwei Teilchen in einem Kasten x=0 x=L
Wellenzahl und Energie • Was kostet die Anregung einer Welle mit Wellenzahl n ? 1/m Wellenzahlen „die in den Kasten passen“ 1 J 1 J 1 J Energie zu Wellen mit Quantenzahl n
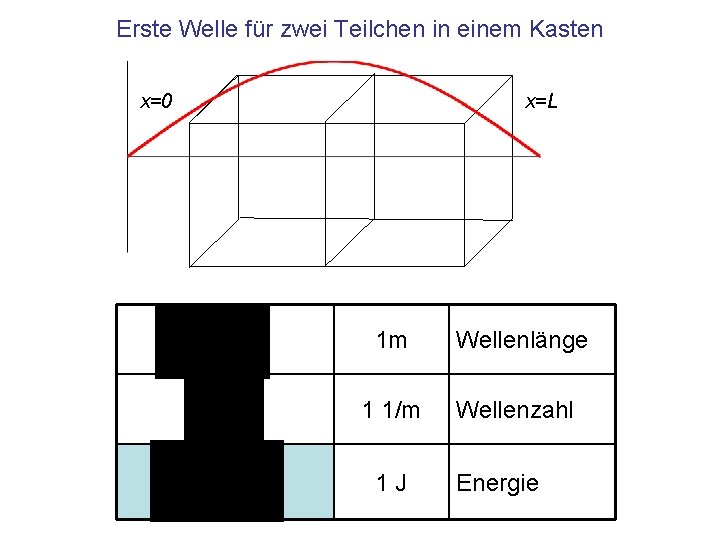
Erste Welle für zwei Teilchen in einem Kasten x=0 x=L 1 m 1 1/m 1 J Wellenlänge Wellenzahl Energie
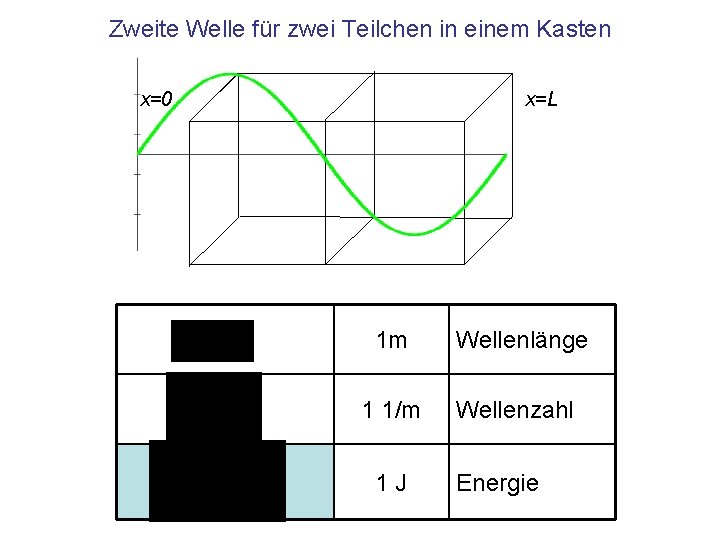
Zweite Welle für zwei Teilchen in einem Kasten x=0 x=L 1 m 1 1/m 1 J Wellenlänge Wellenzahl Energie

Elektronen sind „Fermionen“ Wellenzahl und Energie zur Wellenzahl können für eine Spin-Richtung nur einmal vergeben werden • Der Festkörper (zunächst eine lineare Kette) habe die Länge L, er enthalte N Elementarzellen mit 2 N Elektronen • Man beginnt mit der Wellenzahl k 1 =π/L und ordnet sie zwei Elektronen mit unterschiedlichem Spin zu • Man erhöhe die Wellenzahl bis k. N =N·π/L

De Broglie Beziehung zwischen Wellen- und Teilcheneigenschaft • Eine Welle mit Wellenzahl k entspricht einem Teilchen mit Impuls p=ħ·k
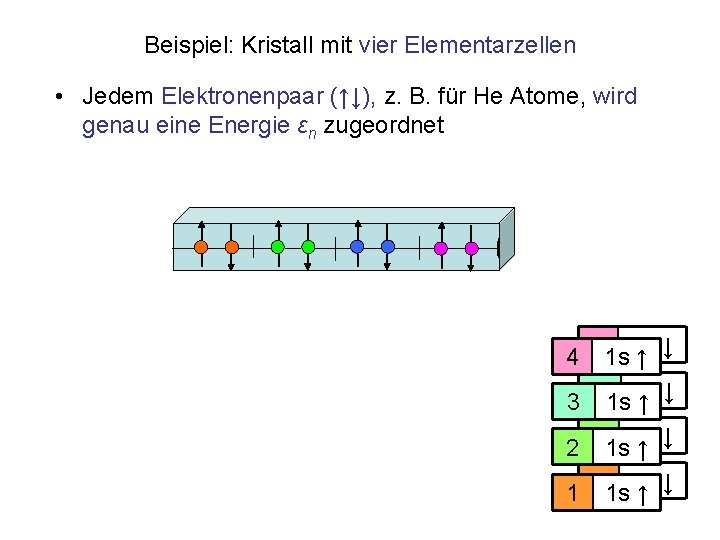
Beispiel: Kristall mit vier Elementarzellen • Jedem Elektronenpaar (↑↓), z. B. für He Atome, wird genau eine Energie εn zugeordnet 4 41 s 1 s ↑ ↓ 3 31 s 1 s ↑ ↓ 2 21 s 1 s ↑ ↓ 1 11 s 1 s ↑ ↓
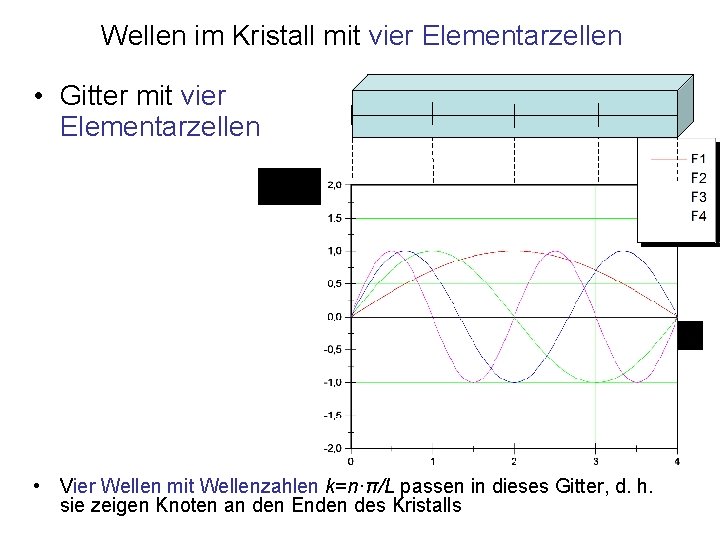
Wellen im Kristall mit vier Elementarzellen • Gitter mit vier Elementarzellen • Vier Wellen mit Wellenzahlen k=n·π/L passen in dieses Gitter, d. h. sie zeigen Knoten an den Enden des Kristalls
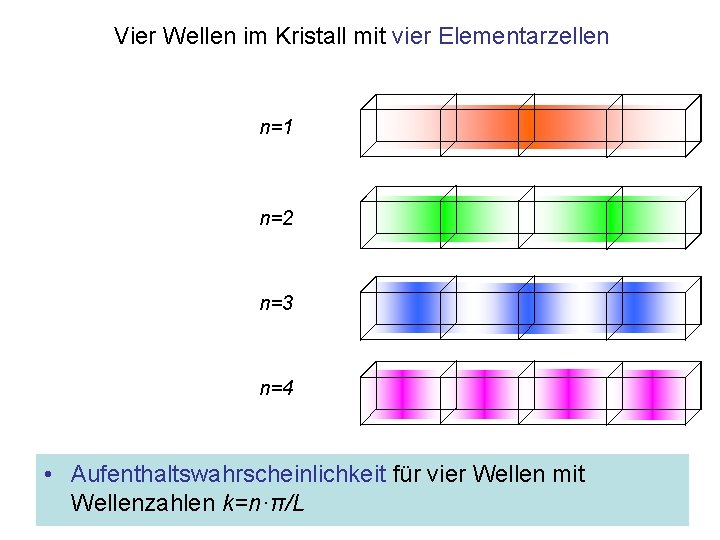
Vier Wellen im Kristall mit vier Elementarzellen n=1 n=2 n=3 n=4 • Aufenthaltswahrscheinlichkeit für vier Wellen mit Wellenzahlen k=n·π/L
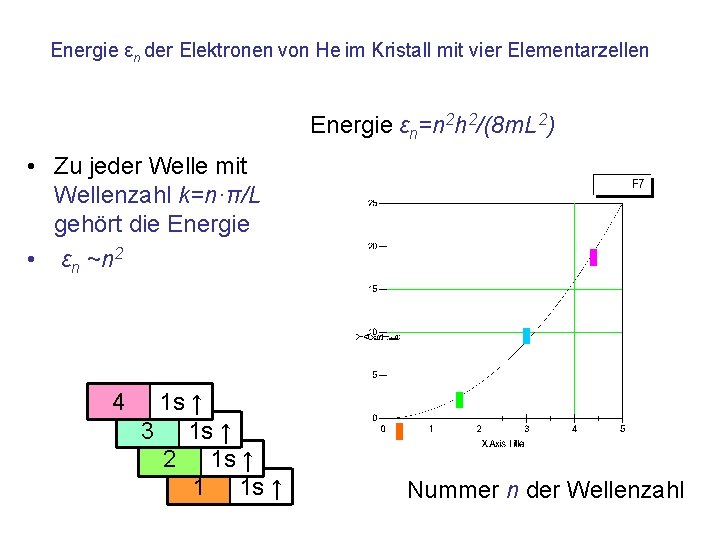
Energie εn der Elektronen von He im Kristall mit vier Elementarzellen Energie εn=n 2 h 2/(8 m. L 2) • Zu jeder Welle mit Wellenzahl k=n·π/L gehört die Energie • εn ~n 2 4 1 s ↑ 3 1 s ↑ 2 1 s ↑ 1 1 s ↑ ~n Nummer n. Impuls der Wellenzahl
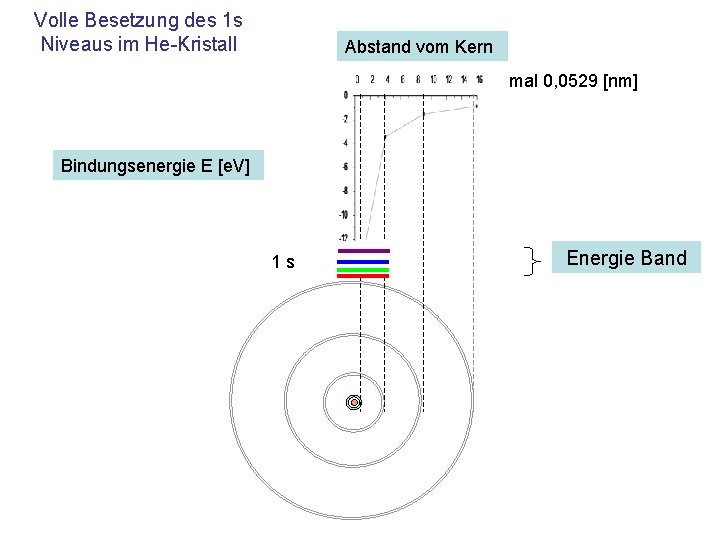
Volle Besetzung des 1 s Niveaus im He-Kristall Abstand vom Kern mal 0, 0529 [nm] Bindungsenergie E [e. V] 1 s Energie Band
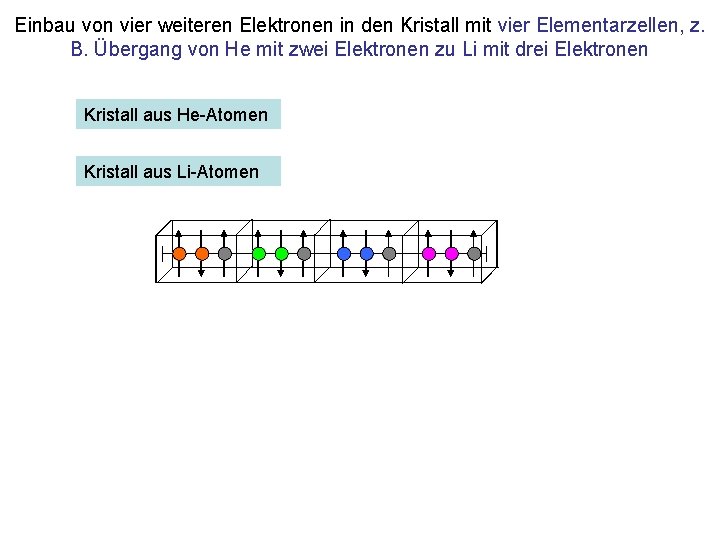
Einbau von vier weiteren Elektronen in den Kristall mit vier Elementarzellen, z. B. Übergang von He mit zwei Elektronen zu Li mit drei Elektronen Kristall aus He-Atomen Kristall aus Li-Atomen
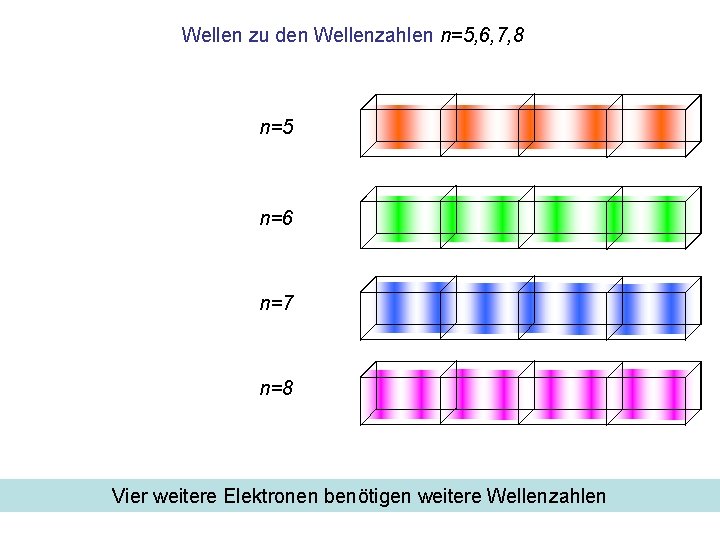
Wellen zu den Wellenzahlen n=5, 6, 7, 8 n=5 n=6 n=7 n=8 Vier weitere Elektronen benötigen weitere Wellenzahlen
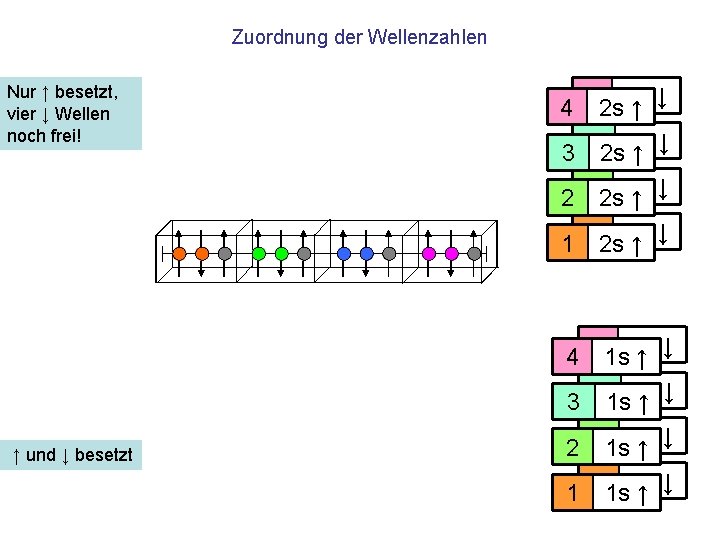
Zuordnung der Wellenzahlen Nur ↑ besetzt, vier ↓ Wellen noch frei! 4 42 s 2 s ↑ ↓ 3 32 s 2 s ↑ ↓ 2 22 s 2 s ↑ ↓ 1 12 s 2 s ↑ ↓ 4 41 s 1 s ↑ ↓ 3 31 s 1 s ↑ ↓ ↑ und ↓ besetzt 2 21 s 1 s ↑ ↓ 1 11 s 1 s ↑ ↓
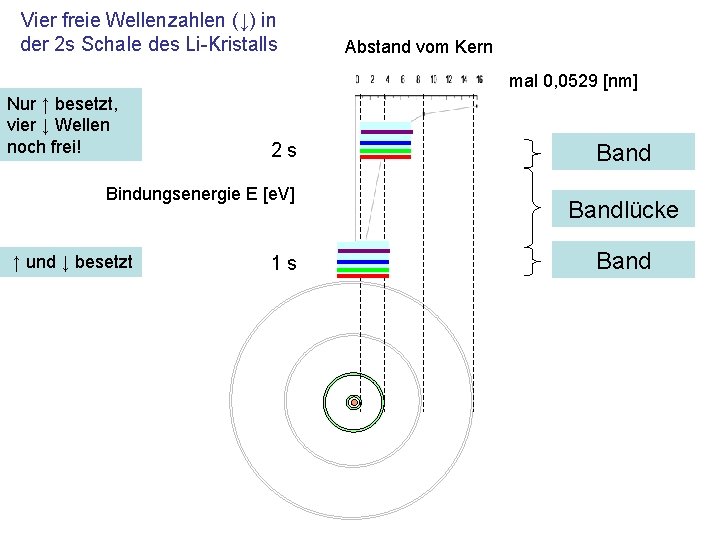
Vier freie Wellenzahlen (↓) in der 2 s Schale des Li-Kristalls Abstand vom Kern mal 0, 0529 [nm] Nur ↑ besetzt, vier ↓ Wellen noch frei! 2 s Bindungsenergie E [e. V] ↑ und ↓ besetzt 1 s Bandlücke Band
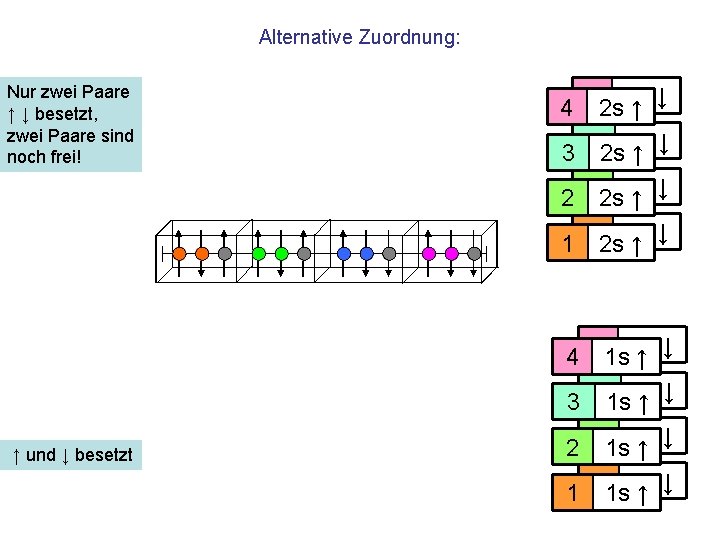
Alternative Zuordnung: Nur zwei Paare ↑ ↓ besetzt, zwei Paare sind noch frei! 4 42 s 2 s ↑ ↓ 3 32 s 2 s ↑ ↓ 2 22 s 2 s ↑ ↓ 1 12 s 2 s ↑ ↓ 4 41 s 1 s ↑ ↓ 3 31 s 1 s ↑ ↓ ↑ und ↓ besetzt 2 21 s 1 s ↑ ↓ 1 11 s 1 s ↑ ↓
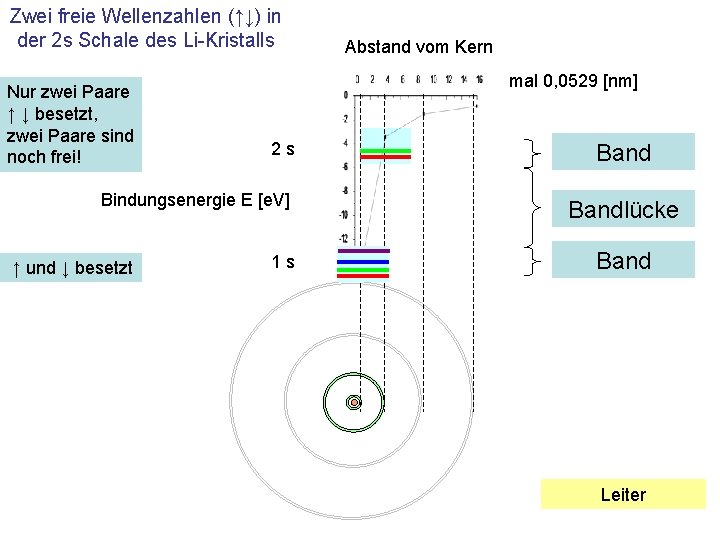
Zwei freie Wellenzahlen (↑↓) in der 2 s Schale des Li-Kristalls Nur zwei Paare ↑ ↓ besetzt, zwei Paare sind noch frei! mal 0, 0529 [nm] 2 s Bindungsenergie E [e. V] ↑ und ↓ besetzt Abstand vom Kern 1 s Bandlücke Band Leiter

Freie Plätze im „Band“, elektrische Leiter • Freie Wellenzahlen in einem Band erlauben den Elektronen – Energie und – Impuls (p=ħ·k) aufzunehmen, – das Material ist elektrisch leitfähig • Im Beispiel der Li-Kristall

Voll Besetzte Bänder, Nichtleiter Voll besetzt ist ein Band, wenn alle Wellenzahlen vergeben sind • In diesen Bändern können die Elektronen keine Energie und keinen Impuls aufnehmen – Im Beispiel der He-Kristall • diese Materialien sind Nichtleiter
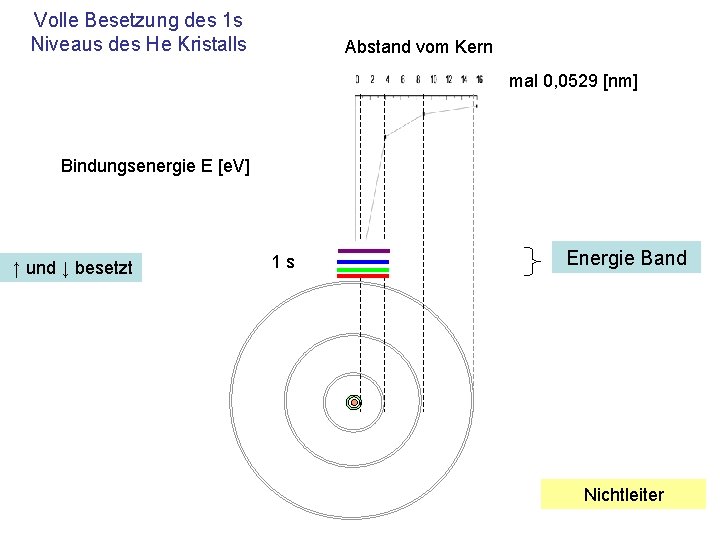
Volle Besetzung des 1 s Niveaus des He Kristalls Abstand vom Kern mal 0, 0529 [nm] Bindungsenergie E [e. V] ↑ und ↓ besetzt 1 s Energie Band Nichtleiter

Kleine Bandlücke: Halbleiter Bei genügend kleiner Bandlücke • Zwischen einem voll besetzten und • dem nächsten, unbesetzten Band genügt eine kleine Energiezufuhr, um das Material vom nichtleitenden in den leitenden Zustand zu überführen • Diese Materialien nennt man Halbleiter
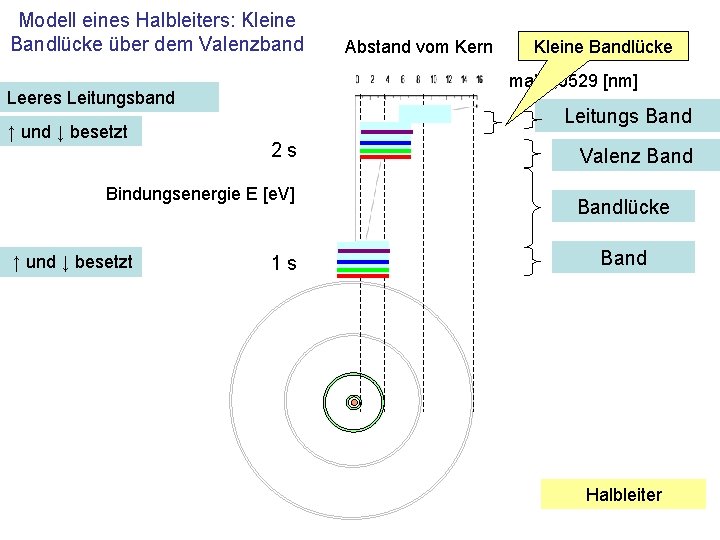
Modell eines Halbleiters: Kleine Bandlücke über dem Valenzband Leitungs Band 2 s Bindungsenergie E [e. V] ↑ und ↓ besetzt Kleine Bandlücke mal 0, 0529 [nm] Leeres Leitungsband ↑ und ↓ besetzt Abstand vom Kern 1 s Valenz Bandlücke Band Halbleiter

Zusammenfassung Klassisch: • Energieniveaus eines freien Atoms • Energie des Bohrschen Atommodells – Aufspaltung der Energieniveaus durch Kopplung bei Annäherung eines zweiten Atoms Quantenmechanik: • Alle Elektronen eines Bandes bilden eine quantenmechanische Gesamtheit, jedem Elektron wird eine Welle zugeordnet – Lösung der Schrödingergleichung für Elektronen im „Kasten“ • Daraus resultiert das Bändermodell für – Isolator – Halbleiter – Leiter
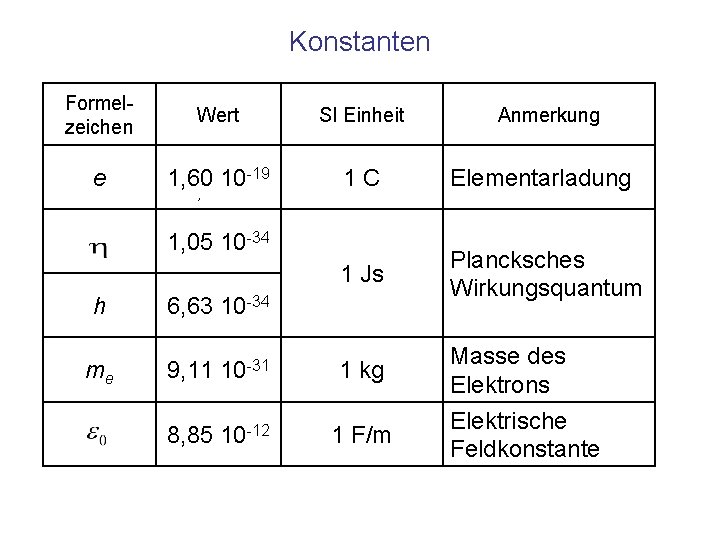
Konstanten Formelzeichen Wert SI Einheit e 1, 60 10 -19 1 C Elementarladung 1 Js Plancksches Wirkungsquantum , 1, 05 10 -34 h me 6, 63 10 -34 9, 11 10 -31 8, 85 10 -12 1 kg 1 F/m Anmerkung Masse des Elektrons Elektrische Feldkonstante
- Slides: 35