ENERGA CALRICA Unidad 1 Termoqumica Objetivo de la

ENERGÍA CALÓRICA Unidad 1: Termoquímica Objetivo de la clase: Los estudiantes deberán explicar el concepto de calor como un proceso de transferencia de energía térmica entre dos o más cuerpos.

CALOR O TEMPERATURA Cazando expresiones El café con leche está muy caliente. El abrigo calienta. Esta nevera da mucho frío. Está enfermo, porque tiene mucho calor. Esta alfombra de lana da mucho calor. No toques la estufa, que está muy caliente y te quemas.

Definamos el concepto de Calor y Temperatura: Es una magnitud física que se refiere a la sensación de frio o caliente al tocar alguna sustancia. Calor: Es una transferencia de energía de una parte a otra de un cuerpo, o entre diferentes cuerpos, producida por una diferencia de calor.
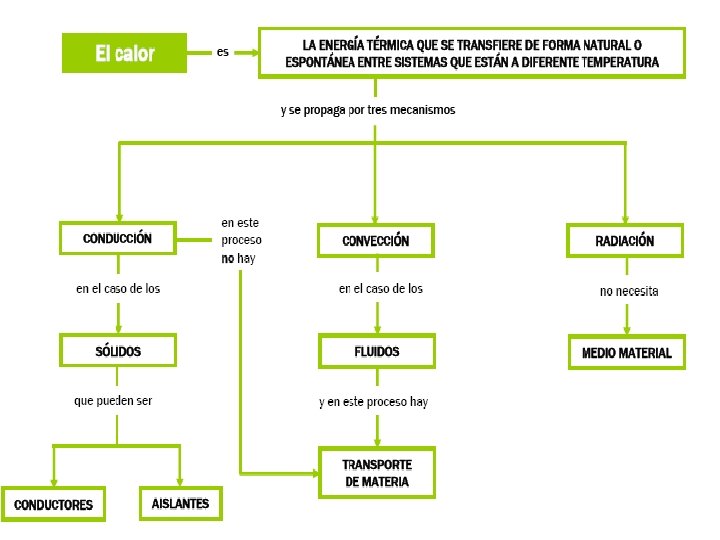
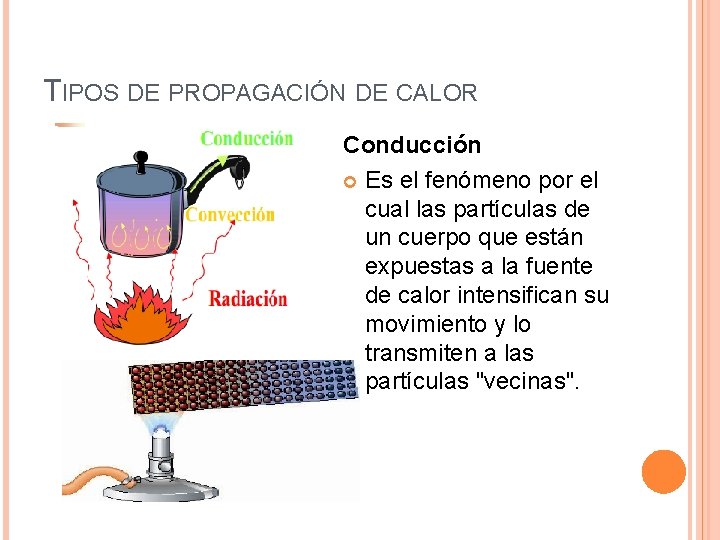
TIPOS DE PROPAGACIÓN DE CALOR Conducción Es el fenómeno por el cual las partículas de un cuerpo que están expuestas a la fuente de calor intensifican su movimiento y lo transmiten a las partículas "vecinas".

TIPOS DE PROPAGACIÓN DE CALOR Convección El fenómeno de convección típico de los materiales fluidos, como los líquidos o los gases. Al igual que el resto de los materiales, al calentarse los fluidos se dilatan. Esto provoca que las masas de aire o agua caliente asciendan, y las que están a menor temperatura, desciendan.
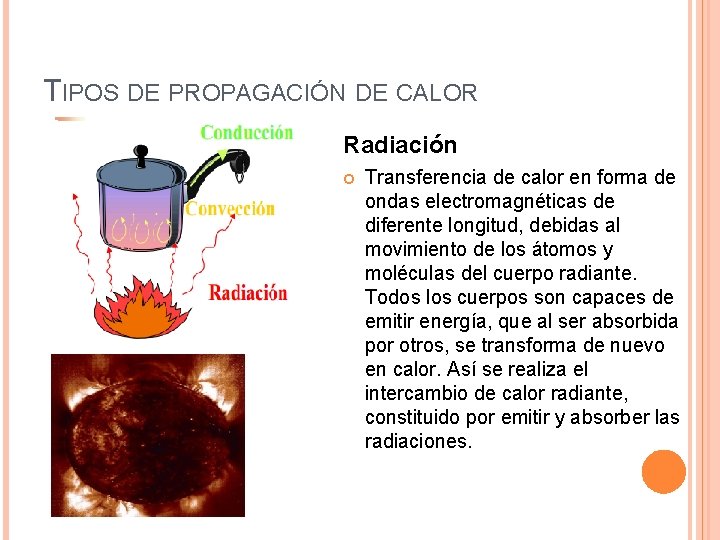
TIPOS DE PROPAGACIÓN DE CALOR Radiación Transferencia de calor en forma de ondas electromagnéticas de diferente longitud, debidas al movimiento de los átomos y moléculas del cuerpo radiante. Todos los cuerpos son capaces de emitir energía, que al ser absorbida por otros, se transforma de nuevo en calor. Así se realiza el intercambio de calor radiante, constituido por emitir y absorber las radiaciones.

CONDUCTORES Y AISLANTES TÉRMICOS Si tocamos con una mano la madera de un martillo y con la otra la parte metálica, tendremos la sensación de que la primera está más caliente que la segunda. Sin embargo, si con un termómetro medimos la temperatura de ambas partes, podremos comprobar que se encuentran a la misma temperatura. La distinta capacidad de los sustancias para conducir el calor permite distinguir dos tipos de materiales: conductores y aislantes térmicos

CONDUCTORES TÉRMICOS Son materiales que conducen bien el calor de un punto a otro. En general, todos los metales, como el oro, la plata, el hierro, etc. , son buenos conductores del calor. Los materiales conductores producen sensaciones de frío o calor al tocarlos, debido a que en estos materiales el intercambio de energía se produce a gran velocidad

AISLANTES TÉRMICOS Son materiales que no conducen bien el calor. Suelen ser porosos o fibrosos, con aire en su interior, como la madera o el plástico. El aire es un buen aislante. Las ventanas de doble cristal, con cámara de aire aíslan bien y evitan las pérdidas de calor, al contrario de lo que sucede con las de un solo cristal.

¿DA CALOR LA ROPA DE ABRIGO? Solemos pensar que un jersey de lana o una manta «nos dan calor» y, así nos protegen del frío. Sin embargo, los cuerpos no contienen calor, por tanto, ¿podemos decir que dan calor las prendas de abrigo?

ACTIVIDADES 1. Si tapamos un hielo con una manta, y dejamos otro hielo fuera, ¿Cuál de ellos se derretirá antes? Explica la respuesta 2. ¿Por qué decimos que la ropa “nos da calor”? 3. Explica para qué sirven las ventanas de doble cristal 4. Explica qué son los conductores térmicos. ¿Y los aislantes térmicos? 5. Clasifica las siguientes sustancias como aislantes térmicos o conductores de calor: madera - hierro - lana - aluminio - plástico - acero

MEDICIÓN DE LA TEMPERATURA El punto de congelación del agua se asocia al cero y el punto de ebullición, al cien. En seguida, dicho intervalo se divide en cien partes iguales, por lo cual dicha escala se conoce como centígrada. Esto fue lo que hizo Anders Celsius, astrónomo sueco, en 1742. Por ese motivo cada una de esas partes iguales fue bautizada, en 1949, como grado Celsius. Esta escala es la que se utiliza en los países Sudamericanos y, en general, en el hemisferio sur.

MEDICIÓN DE LA TEMPERATURA Algunos años antes, en 1724, Gabriel Daniel Fahrenheit calibró la escala asignando 32 para el punto de congelación del agua y 212 para el punto de ebullición. De este modo, cada una de las 180 partes iguales se llamó grado Fahrenheit. Esta escala es la que se utiliza en Estados Unidos y en algunos países europeos.

CONVERSIÓN DE TEMPERATURA FAHRENHEIT A CENTÍGRADOS El sistema métrico utiliza la escala Celsius para medir la temperatura. Sin embargo la temperatura en Estados Unidos todavía se mide en grados Fahrenheit. El agua se congela a 0º Centígrados y hierve a 100º Centígrados, lo que indica una diferencia de 100º. El agua se congela a 32º Fahrenheit y hierve a 212º Fahrenheit, lo que indica una diferencia de 180º. Por lo tanto cada grado en la escala Fahrenheit es igual a 100/180 o 5/9 grados en la escala Celsius. Como convertir grados Fahrenheit a grados Celsius Resta 32º para adaptar el equivalente en la escala Fahrenheit. Multiplica el resultado por 5/9. Ejemplo: convierte 98. 6º Fahrenheit a Centígrados. 98. 6 - 32 = 66. 6 * 5/9 = 333/9 = 37 o C.

CONVERSIÓN DE TEMPERATURA KELVIN A CENTÍGRADOS Cero en la escala Celsius o de grados centígrados (0 °C) se define como el equivalente a 273, 15 K, con una diferencia de temperatura de 1 °C equivalente a una diferencia de 1 K, es decir, el tamaño de la unidad en cada escala es la misma. Esto significa que 100 °C, definido como el punto de ebullición del agua, se define como el equivalente a 373, 15 K. La escala Celsius es un sistema de intervalos pero no un sistema de proporciones, lo que significa que sigue una escala relativa y no una escala absoluta. Esto se puede ver porque el intervalo de temperatura entre 20 °C y 30 C es el mismo que entre 30 °C y 40 °C, pero 40 °C no tiene el doble de energía de calor del aire que 20 °C K = ℃ + 273. 15

CONVERSIÓN DE TEMPERATURA Existen tres tipos de escalas de temperatura: a) Escala de Celsius: Esta escala fue creada por Anders Celsius en el año 1742, también llamada escala centígrada. La relación entre grados centígrados a grados Fahrenheit se relaciona con la ecuación: °C = 5/ 9 (°F − 32) b) Escala de Fahrenheit: Esta escala fue propuesta por Gabriel Fahrenheit en el año 1724. La ecuación de esta en relación a °C, se representa con la ecuación: °F =( 9/ 5 °C) + 32 c) Escala Kelvin: Lord Kelvin. Tiene la siguiente ecuación: K = °C + 273, 15

EJERCICIOS Ejercicio 1. Convertir 340 grados Fahrenheit a centígrados. Ejercicio 2. Convertir 360°C a grados Fahrenheit Ejercicio 3. Convertir 90°C a Kelvin Ejercicio 4. Convertir 80 grados Kelvin a grados Centígrados

EJERCICIOS Los termómetros más habituales constan de un tubo de vidrio colocado junto a una escala graduada, cuyo extremo inferior está ensanchado y contiene mercurio o alcohol coloreado. Cuando la temperatura aumenta, el líquido (mercurio o alcohol) se dilata, ascendiendo por el tubo; cuando la temperatura disminuye ocurre lo contrario, el líquido se contrae y desciende. La temperatura se lee por la altura que alcanza el nivel de la columna de mercurio o alcohol en la escala graduada. ¿Por qué se utiliza mercurio en la fabricación de los termómetros?
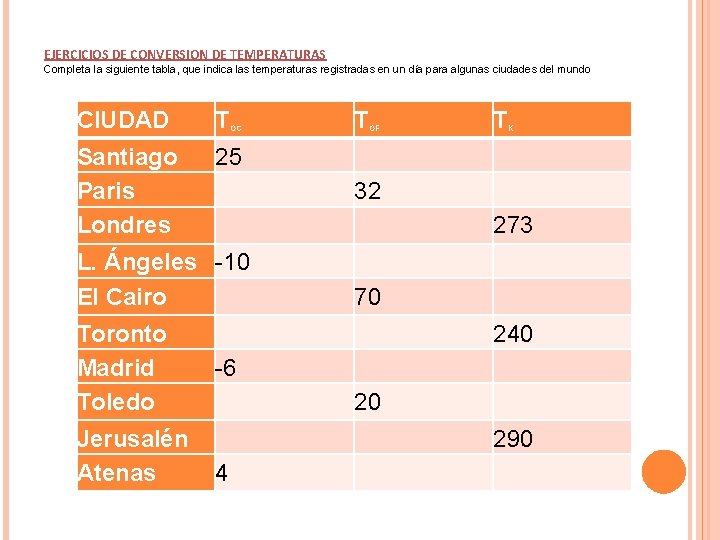
EJERCICIOS DE CONVERSION DE TEMPERATURAS Completa la siguiente tabla, que indica las temperaturas registradas en un día para algunas ciudades del mundo CIUDAD T Santiago Paris Londres 25 OC OF T K 32 273 L. Ángeles -10 El Cairo Toronto Madrid Toledo T 70 240 -6 Jerusalén Atenas 4 20 290

CALORIMETRÍA: CALOR ESPECIFICO Y CAPACIDAD CALÓRICA La calorimetría estudia la transferencia de calor durante procesos físicos y químicos, es una aplicación de la primera ley de la termodinámica. Calor especifico(s) es la cantidad de calor que se requiere para elevar en una unidad por unidad de masa, sin que ocurra un cambio de estado. Su unidad es el joule en un gramo por grado Celsius(J/g °C).
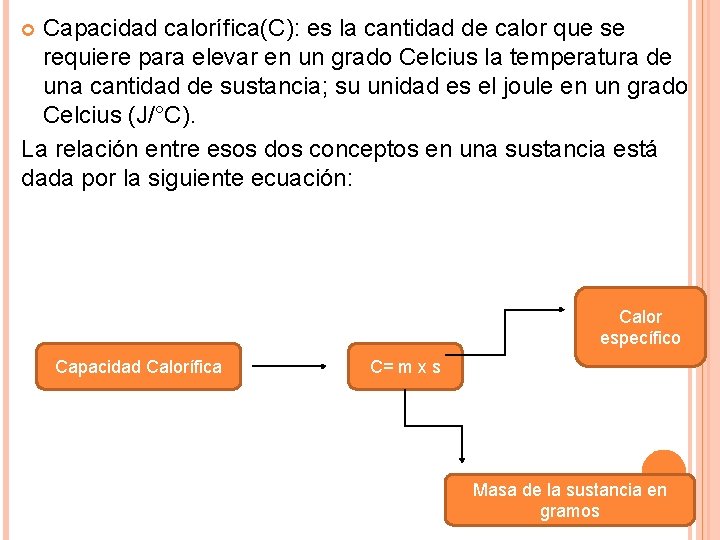
Capacidad calorífica(C): es la cantidad de calor que se requiere para elevar en un grado Celcius la temperatura de una cantidad de sustancia; su unidad es el joule en un grado Celcius (J/°C). La relación entre esos dos conceptos en una sustancia está dada por la siguiente ecuación: Calor específico Capacidad Calorífica C= m x s Masa de la sustancia en gramos

Consideremos el calor específico del agua es equivalente a 4, 184 J/g °C, por lo tanto la capacidad calorífica de 100 g de agua es: C= m x s C= (100 g) x (4, 184 J/g °C) C= 418, 4 J/°C
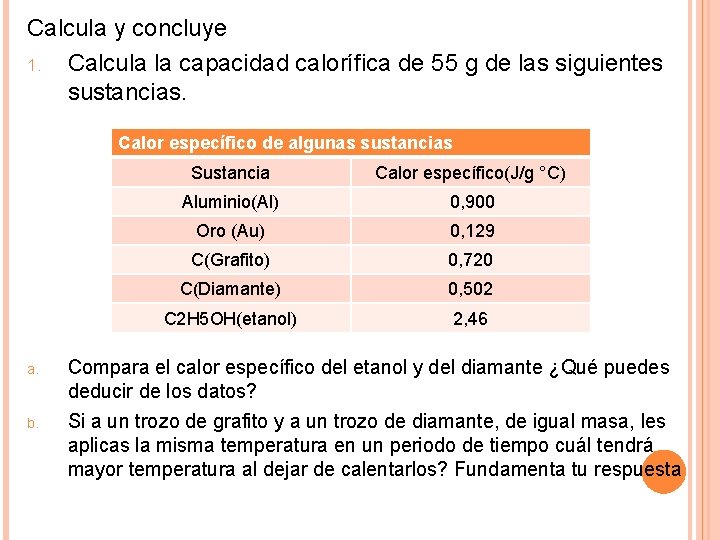
Calcula y concluye 1. Calcula la capacidad calorífica de 55 g de las siguientes sustancias. Calor específico de algunas sustancias a. b. Sustancia Calor específico(J/g °C) Aluminio(Al) 0, 900 Oro (Au) 0, 129 C(Grafito) 0, 720 C(Diamante) 0, 502 C 2 H 5 OH(etanol) 2, 46 Compara el calor específico del etanol y del diamante ¿Qué puedes deducir de los datos? Si a un trozo de grafito y a un trozo de diamante, de igual masa, les aplicas la misma temperatura en un periodo de tiempo cuál tendrá mayor temperatura al dejar de calentarlos? Fundamenta tu respuesta

El calor puede medirse con un calorímetro y la cantidad de calor que pueda poseer o liberar un cuerpo depende de la cantidad de materia(masa), naturaleza del cuerpo a través del calor especifico y de la diferencia de temperatura que se producen la transmisión de calor. La ecuación que permite determinar la cantidad de calor absorbido o liberado es: Q = m x ce x ∆ t Q = Cantidad de calor m = masa ce = calor especifico ∆t = variación de temperatura ¿Qué cantidad de calor absorbe un trozo de 1000 g de cobre al elevar su temperatura desde los 15°C a los 315 °C? ce del Cu= 0, 319 J/g °C?

¿Qué cantidad de calor libera un objeto de hierro que masa 5 oo g y reduce su temperatura de 400 °C a 25 °C? ce del Fe = 0, 47 J/g °C. Si Q > 0 el cuerpo absorbe calor Si Q < 0 el cuerpo libera calor El aluminio se caracteriza por ser un metal versátil, es maleable, un excelente conductor de electricidad, además posee un elevado calor especifico. Calcula la cantidad de calor liberado por una lámina de aluminio, cuya masa es 243 g y su calor especifico es 0, 900 J/g °C, si se enfría desde 60 °C hasta los 5 °C

El calor liberado de 125 g de oro cuando se enfría desde 65 °C a 41 °C (calor especifico = 0, 129 J/g °C) El calor absorbido de 85 g de grafito (calor especifico = 0, 720 J/g °C) cuando se calienta desde 14 °C a 54 °C) El calor absorbido de 100 g de hierro y de 100 g de agua, si cada uno se calienta desde 14 °C a 80 °C. Compara ambos calores y escribe tu conclusión.

PRINCIPIO DE RAUGNULT Si dos cuerpos de diferentes temperaturas se mezclan en un sistema termodinámicamente aislado, los cuerpos de menor temperatura absorberán calor, mientras que los de mayor temperatura liberarán calor, hasta alcanzar un equilibrio térmico. Q absorbido = - Q liberado Por lo tanto la cantidad liberada por un cuerpo debe ser la misma que absorba el o los otros cuerpos.

EJERCICIO En un vaso de vidrio de 150 g de masa que contiene 200 g de agua 10 °C se introduce una esfera de 170 g de níquel que esta a una temperatura de 250 °C. ¿Cuál es la temperatura final de la mezcla? Ce Ni = 0, 1146 cal/ g °C

REACCIONES QUÍMICAS Y ENERGÍA Objetivo de la clase: Se espera que los estudiantes sean capaces de comprender el concepto de entalpía como el calor implicado en un proceso físico como químico.
REACCIONES QUÍMICAS Y ENERGÍA Las reacciones se originan cuando los átomos o las moléculas reaccionantes alcanzan un elevado nivel de energía, con lo que comienzan a desplazarse rápidamente y a chocar una con otras, produciéndose el rompimiento de enlaces debilitados y la formación de otros más estables, originándose así nuevos compuestos. A+B C+D Reactantes Productos
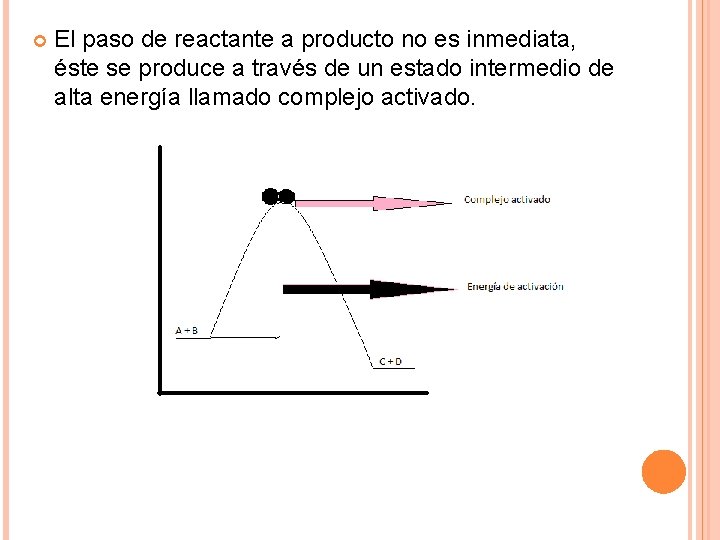
El paso de reactante a producto no es inmediata, éste se produce a través de un estado intermedio de alta energía llamado complejo activado.

PRIMER PRINCIPIO DE LA TERMODINÁMICA Este principio corresponde al de la “Conservación de la energía”, que establece que la cantidad de energía en el universo es constante y por lo tanto existen transformaciones de ellas, pero no creación ni destrucción de la energía. James Prescott Joule (1818 - 89) Julius Robert von Mayer (1814 – 78) Hermann Ludwing Ferdinand von Helmholtz (1821 – 94) En la década de 1840.

En las reacciones químicas en las que existen cambios de energía apreciables, pueden ocurrir dos situaciones: Si al producirse la reacción química se libera energía, entonces la reacción es de tipo EXERGÓNICA. En este caso la diferencia de energía entre los productos y los reactantes es menor que cero. Reactantes E 1 Productos + ∆ E E 2 ∆E = E 2 – E 1 ∆E < Q

En cambio si para que se verifique la reacción, esta tiene que absorber una gran cantidad de energía, esta es una reacción ENDERGÓNICA. En este caso la diferencia de energía es mayor que cero. Reactantes + ∆E Productos E 1 E 2 ∆E = E 2 – E 1 ∆E > Q

Si la energía que entra en juego en las reacciones químicas es la calórica, entonces las reacciones se denominan exotérmica cuando se. H)desprende calor, ENTALPÍA (∆ y endotérmica cuando lo absorbe. SI LA REACCIÓN QUÍMICA OCURRE A PRESIÓN CONSTANTE Y SE PRODUCE UN CAMBIO DE ENERGÍA CALÓRICA, ÉSTOS CAMBIOS SE CONOCEN CON EL NOMBRE DE CAMBIOS DE ENTALPÍA. Entalpía (∆ H) ∆ H = Q/ mol La entalpía se puede definir como el calor implicado en un proceso físico o químico a presión constante. ∆ H = Hf – Hi Si ∆ H > 0 significa que se le ha suministrado calor al sistema. Sí ∆ H < 0 significa que el sistema desprende calor, disminuyendo su contenido calórico. ENDOTÉRMICA EXOTÉRMICA

CALOR Y CAMBIOS DE ESTADO Para que un cambio de estado se efectúe es necesario cambiar la temperatura o la presión, o ambas. Sin embargo, casi siempre los cambios de estado se efectúan a presión constante, o sea, variando la temperatura por adición o sustracción del calor. Cuando se produce un cambio de estado, se presenta primero un equilibrio entre los dos estados involucrados en él.
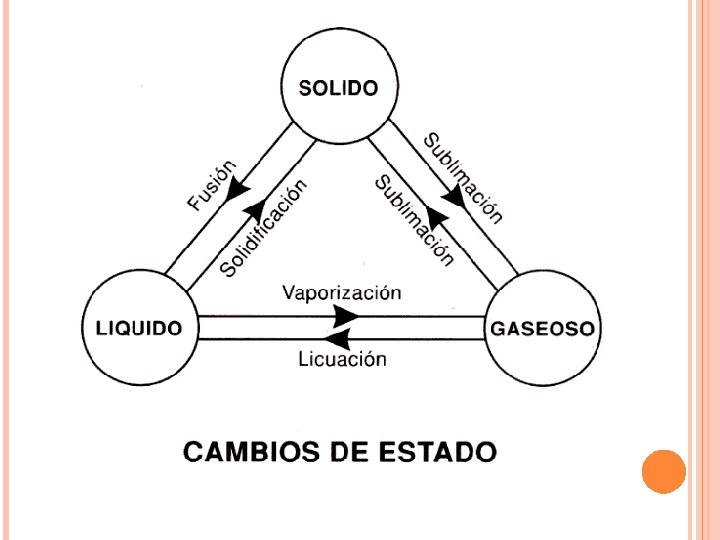
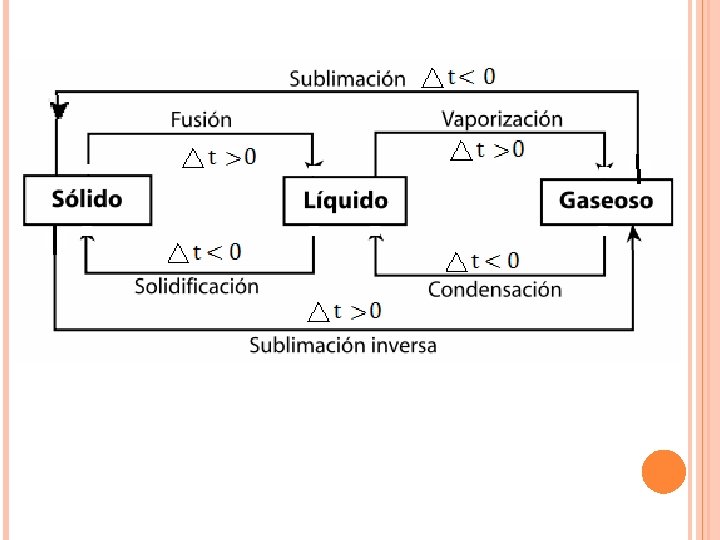
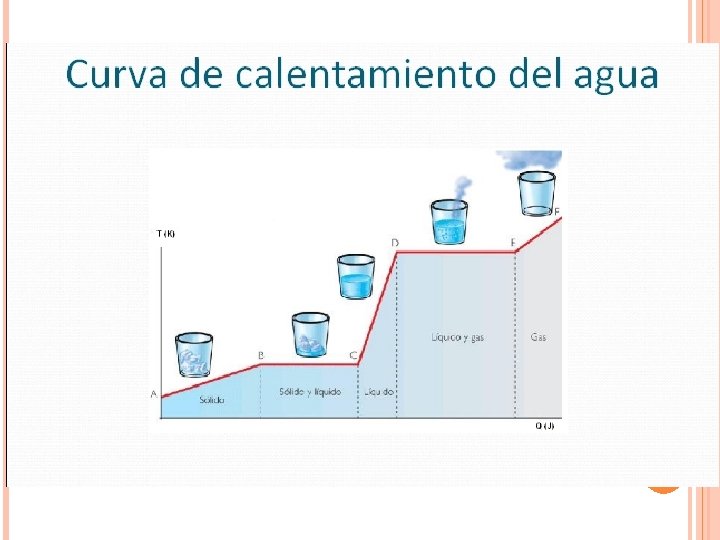

En la grafica anterior se presenta la curva de calentamiento completa desde el estado sólido, pasando por el líquido hasta el estado de vapor. Supongamos que se tiene en el estado sólido en un tiempo t 0 i. Si empezamos a agregar calor al sistema en forma progresiva su temperatura aumentara hasta una temperatura de fusión t°f, en el tiempo t 1. La cantidad de calor gastado es: Q 1 = m ce(s) ∆ T

Cuando la sustancia se encuentra en la temperatura de fusión, hay necesidad de aplicarle calor latente (∆ H fusión) Para convertirla en líquido (Intervalo de t 1 a t 2), el calor total de este intervalo depende de la masa. Q 2 = Q 1 = m ∆ H fusión Cuando todo el sólido se haya transformado en líquido (t 2), al aplicar nuevamente calor, se incrementa la temperatura hasta el tiempo(t 3), donde el líquido alcanza su temperatura de ebullición. El calor proporcionado entre t 2 y t 3 está determinado por la expresión. Q 3 = m ce(l) ∆ T

Cuando las sustancias se encuentra en el punto de ebullición, se le debe aplicar una cantidad de calor extra (∆ Hv) para convertirla en vapor entre los intervalo t 3 a t 4. El calor total de éste intervalo depende de la masa: Q 4 = Qv = m ∆ Hv Al estar todo el líquido en estado de vapor (t 4), se le aplica calor comenzando a incrementarse la temperatura hasta un tiempo t 5 y a una temperatura final (t°f). Entre estos dos últimos lapsos de tiempo se le aplicó una cantidad de calor cuya expresión es: Q 5 = m ce(v) ∆ T

Para determinar el calor total aplicado durante el proceso de calentamiento se deben sumar todos los calores involucrados en el proceso. QT = Q 1+Q 2+Q 3+Qv+Q 5 Ejemplo: Determine la cantidad de calor que se requiere para transformar 100 g de hielo a una temperatura de -10 °C en vapor de agua a 100 °C. Datos: T° fusión = 0 °C t° eb = 100 °C ce(f) = 0, 5 cal/g °C Ce(l) = 1 cal/g °C ce(v) = 0, 5 cal/ g°C ∆Hf = 80 cal/g ∆Hv = 540 cal/g

SEGUNDA LEY DE LA TERMODINÁMICA Objetivo de la clase: Comprender la entropía como la energía no aprovechada para realizar un trabajo

LEY DE HESS Para los sistemas químicos, cualquier compuesto en determinadas condiciones prefijadas tienen siempre la misma energía, independiente del proceso seguido para su obtención. Esto queda indicado en la ley de Hess: “El efecto térmico total que acompaña la transformación de un sistema en otro es independiente de los estados intermedios; solo son importantes el estado inicial y final de la transformación”

EJEMPLO: (1) (2) Calcular el calor de reacción correspondiente a la formación de dióxido de carbono a partir del carbono y oxígeno, utilizando los siguientes datos: 2 C(s) + O 2 2 CO(g) + O 2 2 CO 2(g) ∆H= -221 k. J ∆H= -566 k. J Solución: El calor de reacción (∆H) que se nos pide corresponde a: C(s) + O 2(g) CO 2(g) ∆H= X
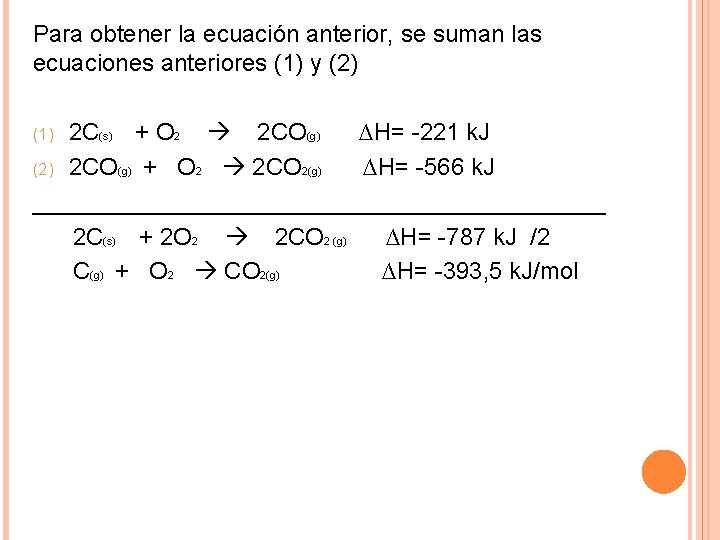
Para obtener la ecuación anterior, se suman las ecuaciones anteriores (1) y (2) 2 C(s) + O 2 2 CO(g) ∆H= -221 k. J (2) 2 CO(g) + O 2 2 CO 2(g) ∆H= -566 k. J ______________________ 2 C(s) + 2 O 2 2 CO 2 (g) ∆H= -787 k. J /2 C(g) + O 2 CO 2(g) ∆H= -393, 5 k. J/mol (1)

EJEMPLO Considera la ecuación química en un sentido: SO 2(g) + ½ O 2(g) SO 3(g) ∆ H = -99, 1 k. J R. E Al invertir la ecuación, se debe invertir el signo de la variación de entalpía, por lo que resulta una reacción endotérmica: SO 3(g) SO 2(g) + ½ O 2(g) ∆ H = +99, 1 k. J Si la ecuación se multiplica por un factor n, la variación de entalpía se debe multiplicar por el mismo valor n, debido a que la entalpía es una propiedad extensiva del sistema y depende de la cantidad de materia que se considere: 2 SO 2(g) + O 2(g) 2 SO 3(g) ∆ H = 2(-99, 1 k. J) = -198, 2 k. J

EJERCICIOS A partir de la información que se proporciona a continuación: (1) 2 Ca. O(s) 2 Ca(s) + O 2(g) ∆ H = +1270, 18 k. J/mol (2) C(grafito) + O 2(g) CO 2(g) ∆ H = -393, 51 k. J/mol (3) Ca. O(s) + CO 2(g) Ca. CO 3(s) ∆ H = -178, 32 k. J/mol Calcula la entalpía para la siguiente reacción: (4) 2 Ca(s) + 2 C(grafito) + 3 O 2(g) 2 Ca. CO 3(s)

SEGUNDA LEY DE LA TERMODINÁMICA Entropía Las moléculas tienen dos formas de almacenar energía: ►La primera corresponde al tipo de energía almacenada en los enlaces, y es un tipo de energía esencialmente útil para realizar un trabajo. ►La otra energía es la tendencia a tener el mayor numero de estados posibles que el estado final. Este tipo de energía es de un tipo desordenado, producido por la vibración, rotación y traslación de las moléculas. Como existen distintos tipos de moléculas, también existen distintas formas de almacenar energía desordenada.

Tomando en cuenta estos antecedentes, el segundo principio de la termodinámica establece que: “La entropía del universo (un sistema y su alrededor) siempre aumenta en los procesos espontáneos” ∆S sistema = q / T Para un sistema aislado puede ocurrir que: Reactantes Productos S 1 S 2 ∆S = S 2 – S 1 ∆S>0 En este caso en que la diferencia de entropía es mayor que cero, la transformación es espontanea

En cambio si Reactantes S 1 Productos S 2 Siempre ∆S = S 2 la – S 1 entropía del ∆S = 0 universo es positiva para los procesos que son Si existe un equilibrio entre el sistema totalmente aislado y suespontáneos. entorno cuando no hay variación de entropía. Por ejemplo, si tengo un gas y lo libero O Si caliento un metal

TERCERA LEY DE LA TERMODINÁMICA El valor de la entropía es cero en un solido cristalino perfecto en cero absoluto (0 kelvin) Así la tercera ley de la termodinámica permite determinar las entropías absolutas de sustancias, también llamadas entropías de la tercera ley, lo que no se logra para la energía interna o la entalpía. El valor de la entropía de una sustancia es absoluto, debido a que se determina a partir del valor de entropía cero en el cero absoluto, en el que se elimina el “desorden” molecular. En la siguiente reacción: N 2(g) + 3 H 2(g) 2 NH 3(g)
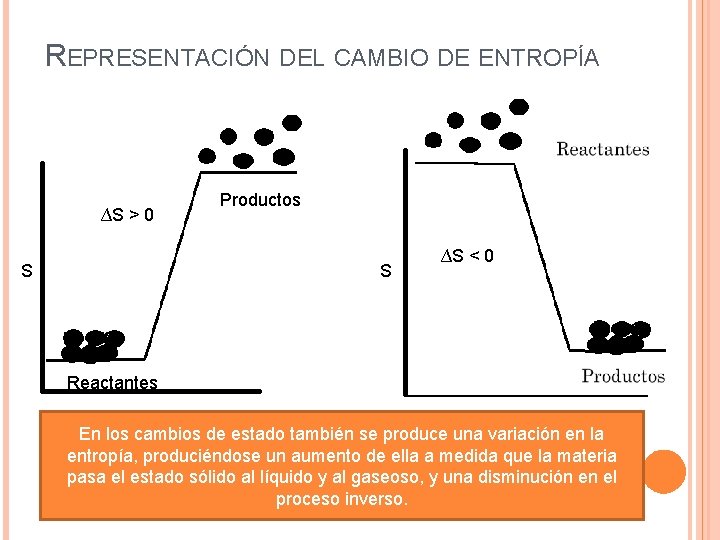
REPRESENTACIÓN DEL CAMBIO DE ENTROPÍA ∆S > 0 S Productos S ∆S < 0 Reactantes En los cambios de estado también se produce una variación en la entropía, produciéndose un aumento de ella a medida que la materia pasa el estado sólido al líquido y al gaseoso, y una disminución en el proceso inverso.

ENERGÍA LIBRE DE GIBBS Para predecir una reacción química ocurrirá espontáneamente, es necesario conocer y relacionar la transferencia de calor (Entalpía) entre el sistema y el ambiente. Si el sistema libera calor (∆H<0), el calor es absorbido por las moléculas del entorno, aumentando su entropía. A su vez si el entorno tiene una elevada temperatura (°K), la transferencia de calor desde el sistema al ambiente no tendrá un mayor impacto sobre la entropía.

La relación entre entropía del sistema y la entalpía está expresada en la siguiente expresión: ∆ S entorno = -∆H ambiente T Según el segundo principio de la termodinámica, una reacción será espontanea, siempre y cuando la entropía del universo aumente Para una reacción en equilibrio se cumple que: ∆ Suniverso = ∆ Ssistema + ∆ S ambiente > 0 Reemplazando tendríamos esto: ∆ Suniverso = ∆ Ssistema - ∆H ambiente T Multiplicado por –T: -T∆ S universo= -T∆ S sistema + ∆ H ambiente < 0

Por lo tanto, -T∆ S universo < 0 y como -T∆ S universo = ∆G, se cumple La función de estado energía libre de Gibbs (∆ G), se relaciona con la energía útil que posee un sistema∆G para y determina si una reacción es = ∆realizar H - T∆ trabajo S espontánea en un sentido o en el sentido inverso. Por lo tanto, la energía libre de Gibbs corresponde a la expresión: = H predictor – TS Por lo tanto, se cumple que. G es de la espontaneidad del proceso. En resumen, a presión y Ahora podemos usar un nuevo criterio de espontaneidad, que toma en cuenta temperatura constante solo el sistema, y que nossidice que la reacción espontánea ocurre con disminución de la energía de Gibbs. Por lo tanto, ∆ G del sistema es negativo para una reacción espontánea. ∆G < 0 si la reacción es espontánea ∆G > 0 la reacción es inducida ∆G = 0 la reacción esta en equilibrio
- Slides: 58