Endoscopic Mucosal Resection EMR AND Endoscopic Submucosal Dissection

Endoscopic Mucosal Resection (EMR) AND Endoscopic Submucosal Dissection (ESD) in 2016 Francesco Azzolini U. O. C. di Gastroenterologia Arcispedale S. Maria Nuova Reggio Emilia I. R. C. C. S
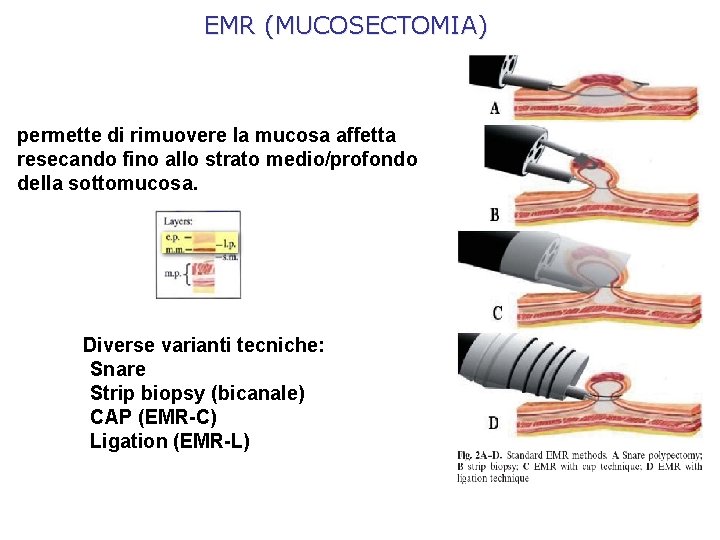
EMR (MUCOSECTOMIA) permette di rimuovere la mucosa affetta resecando fino allo strato medio/profondo della sottomucosa. Diverse varianti tecniche: • Snare • Strip biopsy (bicanale) • CAP (EMR-C) • Ligation (EMR-L)
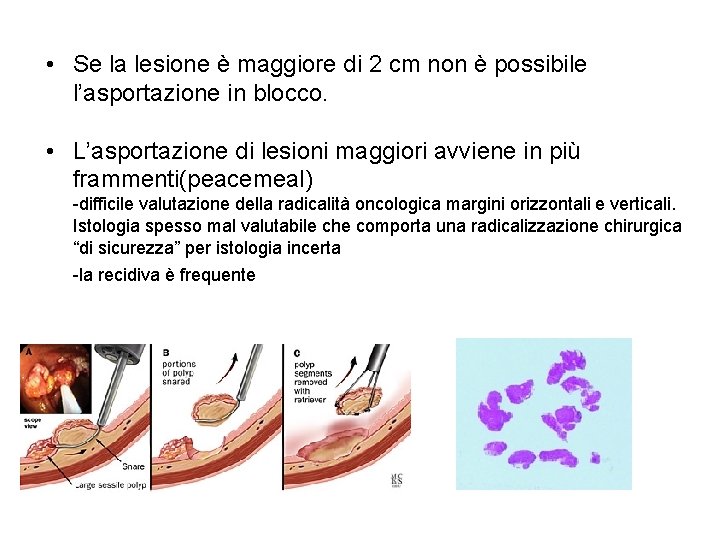
• Se la lesione è maggiore di 2 cm non è possibile l’asportazione in blocco. • L’asportazione di lesioni maggiori avviene in più frammenti(peacemeal) -difficile valutazione della radicalità oncologica margini orizzontali e verticali. Istologia spesso mal valutabile che comporta una radicalizzazione chirurgica “di sicurezza” per istologia incerta -la recidiva è frequente
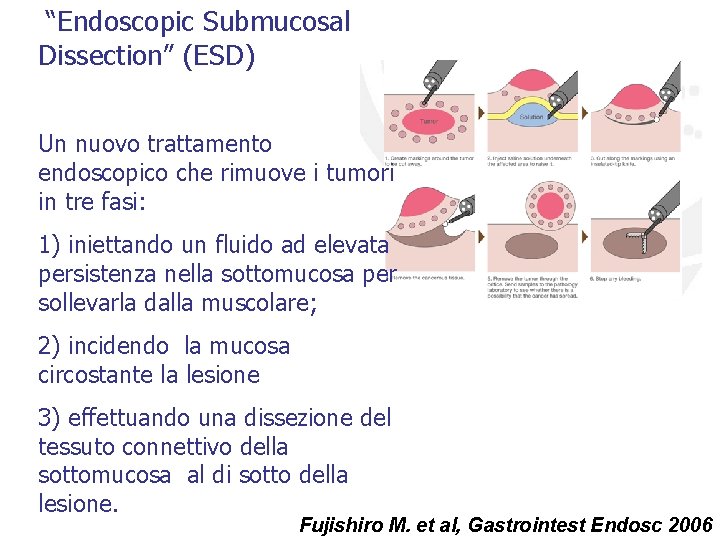
“Endoscopic Submucosal Dissection” (ESD) Un nuovo trattamento endoscopico che rimuove i tumori in tre fasi: 1) iniettando un fluido ad elevata persistenza nella sottomucosa per sollevarla dalla muscolare; 2) incidendo la mucosa circostante la lesione 3) effettuando una dissezione del tessuto connettivo della sottomucosa al di sotto della lesione. Fujishiro M. et al, Gastrointest Endosc 2006
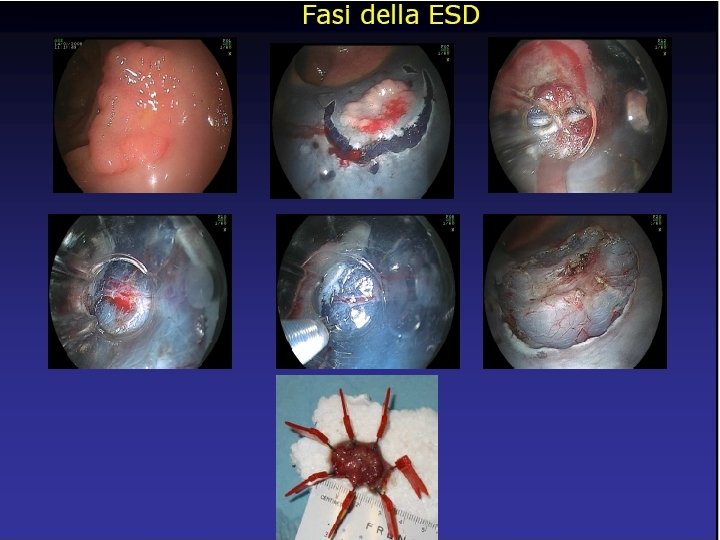
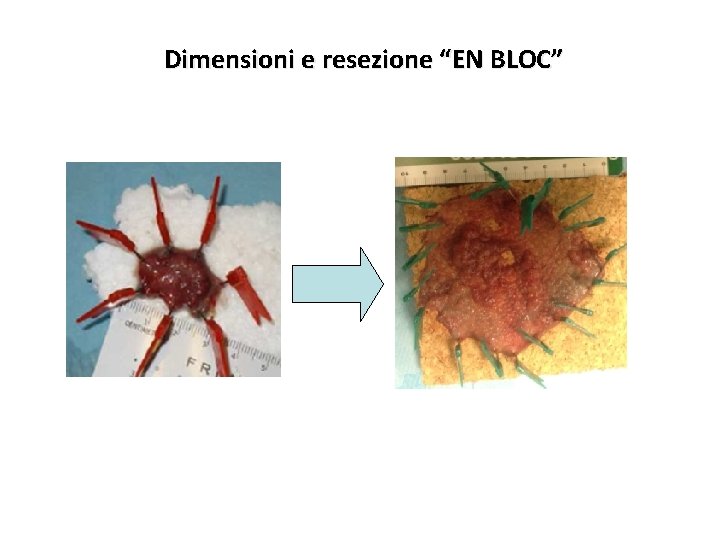
Dimensioni e resezione “EN BLOC”
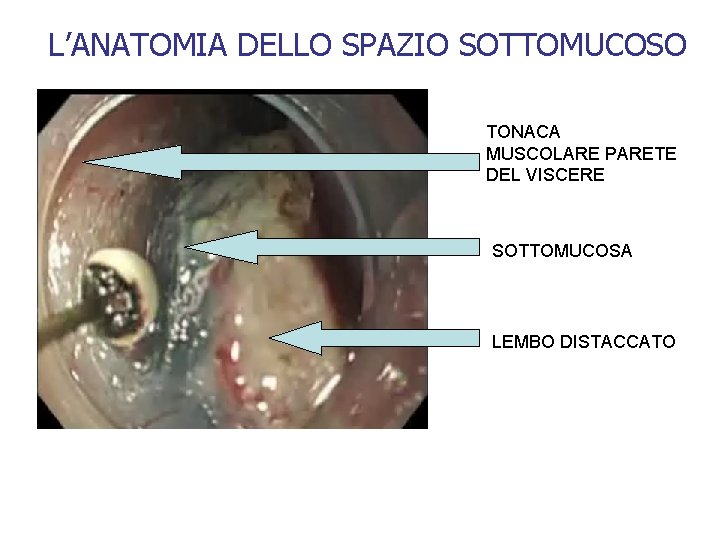
L’ANATOMIA DELLO SPAZIO SOTTOMUCOSO TONACA MUSCOLARE PARETE DEL VISCERE SOTTOMUCOSA LEMBO DISTACCATO

Carcinoma Squamocellulare Esofageo ESGE Guideline ESGE raccomanda la resezione en bloc per il carcinoma squamocellulare (SCC) superficiale ad eccezione di quelli con ovvio interessamento della sottomucosa (forte raccomandazione, moderata evidenza di qualità). La mucosectomia endoscopica (EMR) può essere considerata quando le lesioni sono inferiori ai 10 mm ed è garantita la rimozione en bloc. Tuttavia, ESGE consiglia la dissezione endoscopica sottomucosa (ESD) come prima opzione, in particolare perché garantisce la resezione en bloc ed un accurata stadiazione anatomopatologica evitando di perdere importanti caratteristiche istologica (forte raccomandazione, moderata evidenza di qualità) Endoscopy 2015; 47: 829

Carcinoma Squamocellulare Esofageo ESGE Guideline La resezione endoscopica è ormai considerata il trattamento di prima scelta per il SCC superficiale dell’esofago, ovvero m 1 (intraepiteliale) o m 2 (limitato alla lamina propria). La resezione en bloc è necessaria per garantire un’adeguata stadiazione della malattia, pertanto la decisione sulla tecnica di resezione è legata esclusivamente alle dimensioni della lesione. L’EMR dovrebbe essere presa in considerazione solo in caso di lesioni <10 mm, anche se la cap-assisted EMR si è dimostrata efficace in lesioni fino ai 15 mm. Grazie all’affinamento dell’ESD non esistono limiti dimensionali e possono essere resecate anche lesioni >30 mm e/o ad estensione circonferenziale. Per SCC m 3 (invasione muscolaris mucosae) e sm 1 (invasione sottomucosa <200 um) il rischio di metastasi linfonodali aumenta rispettivamente fino al 8 -15% e 11 -53%, pertanto la resezione endoscopica può essere presa in considerazione solo in pazienti anziani e/o con comorbidità significative Endoscopy 2015; 47: 829

Esofago di Barrett ESGE Guideline ESGE raccomanda la resezione endoscopica con intento curativo delle lesioni mucose visibili nel contesto di esofago di Barrett (forte raccomandazione, moderata evidenza di qualità). A differeza del SCC nche lesioni m 3 o sm 1 (invasione sottomucosa <500 um) possono avere un basso rischio di metastasi linfonodali ed essere radicalmente asportate La resezione con ESD non è stato dimostrato essere superiore all’EMR, pertanto quest’ultima dovrebbe essere la prima opzione. L’ESD è da preferire in casi selezionati, come lesioni >15 mm, con scarso sollevamento e lesioni a rischio per invasione sottomucosa 0 -Is e 0 -IIa+0 -IIc. 4 (forte raccomandazione, moderata evidenza di qualità). Endoscopy 2015; 47: 829

Esofago di Barrett ESGE Guideline • Resezione quasi sempre curativa (ma è necessario valutare la necessità di ulteriori terapie bilanciandone il rischio con quello di metastasi linfonodali in discussione multidisciplinare): ben o moderatamente differenziata, sm 1, senza invasione linfovascolare (forte raccomandazione, moderata evidenza di qualità) • Trattamento chirurgico: infiltrazione >sm 1 (>500 um), poco differenziata, invasione linfovascolare, margini verticali positivi (forte raccomandazione, moderata evidenza di qualità) • Sorveglianza endoscopica e ritrattamento: margini orizzontali positivi o resezione piecemeal (forte raccomandazione, moderata evidenza di qualità) • Altri trattamenti necessari (EMR, radiofrequenza): ablazione del Barrett residuo considerato il rischio di neoplasie metacrone (forte raccomandazione, moderata evidenza di qualità) Endoscopy 2015; 47: 829

Early Gastric Cancer L’EMR è un'opzione accettabile per le lesioni più piccole di 10 -15 mm con una probabilità molto bassa di istologia avanzata (Paris 0 -IIa). Le indicazioni alla ESD delle linee guida Giapponesi sono di fatto accettate dall’ESGE: • neoplasie non invasive (displasia) indipendentemente dalla dimensione • adenocarcinoma intramucoso di tipo differenziato, senza ulcerazioni (≤ 2 cm indicazione assoluta, > 2 centimetri indicazione estesa) • adenocarcinoma intramucoso di tipo differenziato ≤ 3 cm con ulcera (indicazione estesa) adenocarcinoma intramucosa indifferenziato ≤ 2 cm (indicazione estesa) • adenocarcinoma differenziato ≤ 3 cm con interessamento della sottomucosa superficiale, SM 1, ≤ 500μm (indicazione estesa) L’outcome della EMR è comunque inferiore alla ESD anche per lesioni di piccole dimensioni pertanto ESGE consiglia l’ ESD come trattamento di scelta per la maggior parte delle lesioni neoplastiche superficiali gastriche (forte raccomandazione, evidenza di qualità moderata) Endoscopy 2015; 47: 829

Early Gastric Cancer Una resezione in blocco R 0 di lesioni displastiche o di adenocarcinoma intramucoso di tipo intestinale senza ulcerazione o invasione linfovascolare deve essere considerata curativa (forte raccomandazione, evidenza di qualità moderata). Una resezione En bloc R 0 in caso di indicazione estesa è curativo nella maggior parte dei casi (forte raccomandazione, evidenze di qualità moderata). Tuttavia, in carcinomi scarsamente differenziati di tipo diffuso una gastrectomia deve sempre essere considerata decidendo su base individuale in un contesto multidisciplinare (forte raccomandazione, moderata evidenza di qualità). Si raccomanda la chirurgia in caso di invasione linfovascolare, infiltrazione profonda della sottomucosa (> 500μm), margini verticali positivi, ulcerazione in tumori> 30 millimetri (forte raccomandazione, evidenze di qualità moderata). Se vi è un margine orizzontale positivo o la resezione è frammentario, ma non c'è invasione sottomucosa o altri criteri ad alto rischio una sorveglianza endoscopica e un eventuale ritrattamento è maggiormente consigliato rispetto alla chirurgia (forte raccomandazione, evidenza di qualità moderata). Endoscopy 2015; 47: 829

Early Gastric Cancer Una resezione in blocco R 0 di lesioni displastiche o di adenocarcinoma intramucoso di tipo intestinale senza ulcerazione o invasione linfovascolare deve essere considerata curativa (forte raccomandazione, evidenza di qualità moderata). Una resezione En bloc R 0 in caso di indicazione estesa è curativo nella maggior parte dei casi (forte raccomandazione, evidenze di qualità moderata). Tuttavia, in carcinomi scarsamente differenziati di tipo diffuso una gastrectomia deve sempre essere considerata decidendo su base individuale in un contesto multidisciplinare (forte raccomandazione, moderata evidenza di qualità). Si raccomanda la chirurgia in caso di invasione linfovascolare, infiltrazione profonda della sottomucosa (> 500μm), margini verticali positivi, ulcerazione in tumori> 30 millimetri (forte raccomandazione, evidenze di qualità moderata). Se vi è un margine orizzontale positivo o la resezione è frammentario, ma non c'è invasione sottomucosa o altri criteri ad alto rischio una sorveglianza endoscopica e un eventuale ritrattamento è maggiormente consigliato rispetto alla chirurgia (forte raccomandazione, evidenza di qualità moderata). Endoscopy 2015; 47: 829

Duodeno L’ ESD duodenale o dell'intestino tenue lesioni va evitata a causa del suo alto rischio di perforazione (raccomandazione forte, moderata evidenza di qualità). Polipectomia standard e/o EMR anche frammentaria sono trattamenti preferibili in questa sede per il buon profilo di sicurezza (forte raccomandazione, evidenza di qualità moderata). Se è presente adenocarcinoma nel tessuto asportato il trattamento dovrebbe essere individualizzato, ed in particolare se c’è 'invasione sottomucosa dovrebbe essere presa in considerazione la chirurgia (forte raccomandazione, evidenza di bassa qualità). Endoscopy 2015; 47: 829

Duodeno L’ ESD duodenale o dell'intestino tenue lesioni va evitata a causa del suo alto rischio di perforazione (raccomandazione forte, moderata evidenza di qualità). Polipectomia standard e/o EMR anche frammentaria sono trattamenti preferibili in questa sede per il buon profilo di sicurezza (forte raccomandazione, evidenza di qualità moderata). Se è presente adenocarcinoma nel tessuto asportato il trattamento dovrebbe essere individualizzato, ed in particolare se c’è 'invasione sottomucosa dovrebbe essere presa in considerazione la chirurgia (forte raccomandazione, evidenza di bassa qualità). Endoscopy 2015; 47: 829

Colon La maggior parte delle lesioni superficiali colon e del retto può essere efficacemente rimosso in modo curativo con polipectomia standard ed EMR (forte raccomandazione, evidenza di qualità moderata). L’ESD è indicata per la rimozione di lesioni del colon e rettale con alto sospetto di cancerizzazione limitata alla sottomucosa superficiale. Queste lesioni sono identificate mediante criteri morfologici: • lesione depressa • irregular mucosal surface pattern Questo in particolare se le lesioni sono più grandi di 20 mm L’ ESD può essere inoltre indicata per lesioni che altrimenti non possono essere radicalmente rimosse con ansa (forte raccomandazione, evidenze di qualità moderata). Endoscopy 2015; 47: 829

ESD dove siamo in Italia e come migliorare la nostra pratica La dissezione sottomucosa (ESD) del colon è tecnicamente più difficile di quella gastrica ed è più complessa della EMR : • • Il colon presenta angolature e curve è più difficile lavorare con lo strumento ben raddrizzato per avere la massima risposta dei tiranti la parete e più sottile rispetto allo stomaco e quindi il rischio perforativo e di insulto termico è maggiore in caso di perforazione il liquido residuo della preparazione colica può portare rapidamente ad una peritonite

Colon La maggior parte delle lesioni superficiali colon e del retto può essere efficacemente rimosso in modo curativo con polipectomia standard ed EMR (forte raccomandazione, evidenza di qualità moderata). L’ESD è indicata per la rimozione di lesioni del colon e rettale con alto sospetto di cancerizzazione limitata alla sottomucosa superficiale. Queste lesioni sono identificate mediante criteri morfologici: • lesione depressa • irregular mucosal surface pattern Questo in particolare se le lesioni sono più grandi di 20 mm L’ ESD può essere inoltre indicata per lesioni che altrimenti non possono essere radicalmente rimosse con ansa (forte raccomandazione, evidenze di qualità moderata). Nel retto extraperitoneale è un approccio preferibile per lesioni superiori ai 20 mm soprattutto per l’impatto di una eventuale chirurgia a questo livello e per il rischio minore di complicanze severe rispetto al restante colon. Endoscopy 2015; 47: 829

Colon Una resezione in blocco R 0 di una lesione superficiale, con istologia di adenocarcinoma ben differenziato (G 1 / G 2), SM 1 (≤ 1 mm di invasione sottomucosa) senza invasione linfovascolare è considerata curativa (forte raccomandazione, evidenza di qualità moderata). Si raccomanda la chirurgia quando c’è invasione linfovascolare, l’interessamento della sottomucosa è più profondo di sm 1, i margini verticali positivi o non valutabili o il tumore poco differenziato con infiltrazione sottomucosa (forte raccomandazione, evidenze di qualità moderata). Se il margine orizzontale è positivo, ma non ci sono altri criteri ad alto rischio la sorveglianza e il ritrattamento endoscopico sono trattamenti adeguati (forte raccomandazione, evidenza di qualità moderata). ESGE raccomanda sorveglianza endoscopica 3 -6 mesi dopo il trattamento. Se non sono presenti recidive, una colonscopia completa di follow-up dovrebbe essere eseguita ad 1 anno (raccomandazione forte, moderata evidenza). Dopo resezione frammentaria o con presenza di margini laterali positivi in lesioni a basso rischio si consiglia la colonscopia con biopsie a 3 mesi (evidenza di bassa qualità) Endoscopy 2015; 47: 829

Clinical Outcomes of 500 colorectal ESD at NCCH “The endoscopic submucosal dissection technique, which enables en-bloc resection of large tumors, is accepted as a standard minimally invasive treatment for early gastric cancer in Japan. However, it is not widely used to treat superficial colorectal cancer because of technical difficulty and the higher risk of complications. Conventional EMR, therefore, is used for the resection of nonpolypoid colorectal neoplasm, including the large flat carpet lesions, called colorectal laterally spreading tumors” Saito, Gastrointest Clin N Am 2010; 515 -24

Learning Curve Associated With Colorectal Endoscopic Submucosal Dissection for Endoscopists Experienced in Gastric Endoscopic Submucosal Dissection Prerequisites for Performing Colorectal ESD (NCCH Tokyo): • high level of skill in the nonloop insertion colonoscopy technique • skill in conventional EMR or piecemeal EMR techniques • experience with >20 gastric ESD cases • assistance during >20 colorectal ESDs conducted by experienced endoscopists. Trainees require experience with>30 cases to perform colorectal ESD without guidance from an experienced specialist. Sakamoto DISEASES OF THE COLON & RECTUM 2011
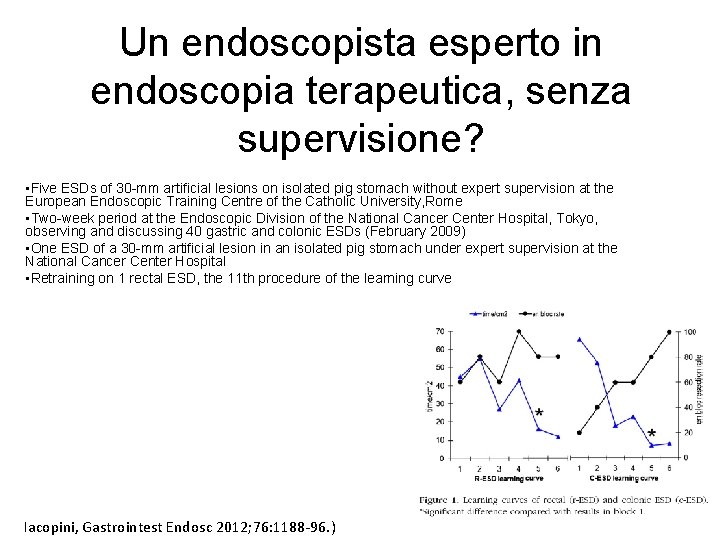
Un endoscopista esperto in endoscopia terapeutica, senza supervisione? • Five ESDs of 30 -mm artificial lesions on isolated pig stomach without expert supervision at the European Endoscopic Training Centre of the Catholic University, Rome • Two-week period at the Endoscopic Division of the National Cancer Center Hospital, Tokyo, observing and discussing 40 gastric and colonic ESDs (February 2009) • One ESD of a 30 -mm artificial lesion in an isolated pig stomach under expert supervision at the National Cancer Center Hospital • Retraining on 1 rectal ESD, the 11 th procedure of the learning curve Iacopini, Gastrointest Endosc 2012; 76: 1188 -96. )
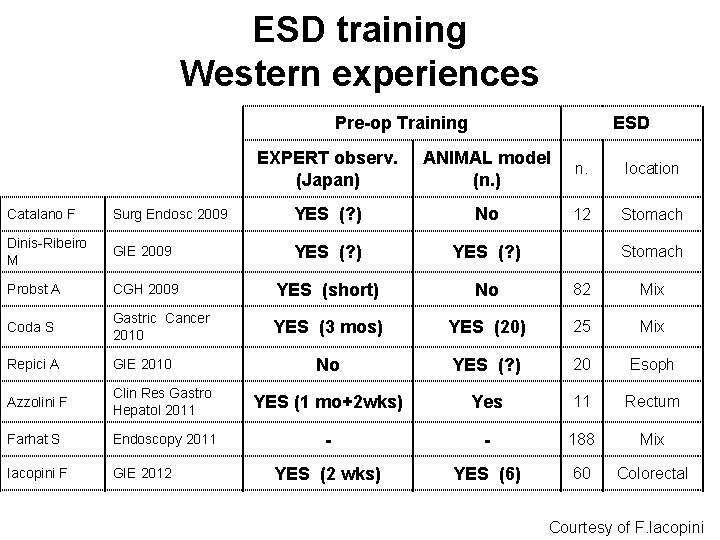
ESD training Western experiences Pre-op Training ESD EXPERT observ. (Japan) ANIMAL model (n. ) n. location 12 Stomach Catalano F Surg Endosc 2009 YES (? ) No Dinis-Ribeiro M GIE 2009 YES (? ) Probst A CGH 2009 YES (short) No 82 Mix Coda S Gastric Cancer 2010 YES (3 mos) YES (20) 25 Mix Repici A GIE 2010 No YES (? ) 20 Esoph Azzolini F Clin Res Gastro Hepatol 2011 YES (1 mo+2 wks) Yes 11 Rectum Farhat S Endoscopy 2011 - - 188 Mix Iacopini F GIE 2012 YES (2 wks) YES (6) 60 Colorectal Stomach Courtesy of F. Iacopini

My training program Pre-requested skills Observation Experts/assistance in Japan (Prof. H. Yamamoto) 40 ESD ( Stomach, Colon, Esoph) 2007 Animal models ESD Rectum Antrum explanted animal organs and live animal models ESD Stomach body/fundus/cardia ESD Colon - Esoph Animal models
My retraining program More than 150 ESD in Rectum an Stomach Observation Experts/assistance in Shanghai (Prof. P. Zhou) 22 POEM 20 ESD 7 STER + POEM AND ESD IN LIVE PIG Animal models 7 POEM ESD Colon - Esoph Supervision in Animal models

ESD training algorithm for Western endoscopists • ESD training offered to endoscopists already skilled in therapeutic endoscopy, particularly EMR • Knowledge about technique, instrumentation, and electrosurgical equipment, acquired by self-study and later reinforced by visiting centers with high volumes of ESD • Practice on animal models (explanted animal organs and live animal models) • Observing experts performing ESD, for a relatively short period in tertiary referral centers • Attendance at ESD workshops providing hands-on exposureand expert guidance • Commencing performance of ESD in humans on carefully selected lesions. Since early gastric cancer is rare in the. West, smaller (20– 30 mm) rectal laterally spreading tumors canserve as entry point to human ESD

Take-home Message: per partire • Visitare centro ad alto volume per almeno due settimane • Training sul modello animale fino ad effettuare la procedura agevolmente • Iniziare step-by step su lesioni selezionate di piccole dimensioni meglio se con la supervisione di un esperto. Portare il caso in un centro ad alto volume, assistere ed essere coinvolto gradualmente nella procedura per avere un risultato “garantito”

Take-home Message: per migliorare • Confronto con gli eastern endoscopists • Concentrare le procedure in centri con esperienza in modo da non disperdere la casistica • Standardizzare il più possibile la tecnica (device, correnti) • Affrontare un nuovo distretto solo quando l’esperienza cresce (antro+retto corpo gastrico cardias esofago e colon) • Continuare con il training sull’animale affrontando resezioni sempre più vaste
- Slides: 29