En el siguiente dibujo se idealiza el proceso
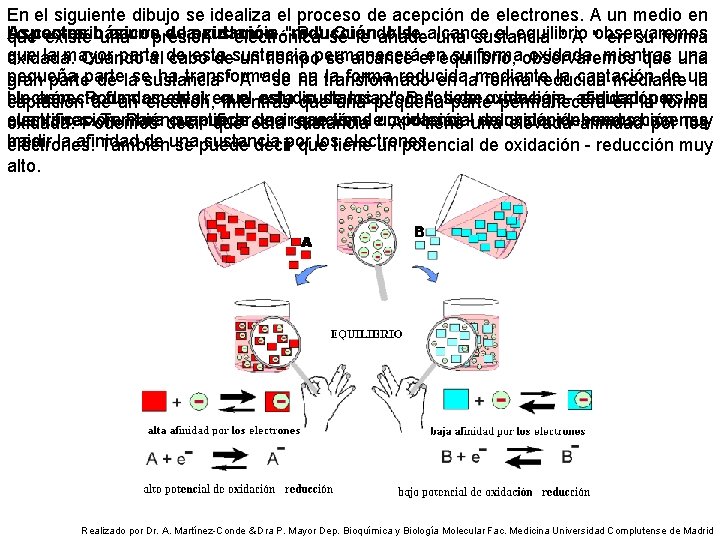
En el siguiente dibujo se idealiza el proceso de acepción de electrones. A un medio en Lo contrario ocurre a la sustancia " B ". Cuando se alcance el equilibrio observaremos Aspectos básicos de oxidación - reducción I I I que existe una " presión " electrónica se le añade una sustancia " A " en su forma que la mayor parte de esta sustancia permanecerá en su forma oxidada, mientras una oxidada. Cuando al cabo de un tiempo se alcance el equilibrio, observaremos que una pequeña parte se ha transformado en la forma reducida mediante la captación de un gran parte de la sustancia " A " se ha transformado en la forma reducida mediante la electrón. Un aspecto fundamental en el estudio de los procesos de oxidación - reducción es su Podemos decir que esta que sustancia " B " tiene baja afinidad por los captación de un electrón, mientras una pequeña parte una permanecerá en la forma electrones. También se puede decir que tiene un potencial de oxidación - reducción muy cuantificación. Para cuantificar una reacción de oxidación - reducción debemos hacer es oxidada. Podemos decir que esta sustancia " A " tiene una elevada afinidad por los bajo. medir la afinidad de una sustancia por los electrones. También se puede decir que tiene un potencial de oxidación - reducción muy alto. Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid

Hemos idealizado los acontecimientos con el objeto obtener una aproximación " intuitiva " a la noción de potencial de oxidación - reducción. Vamos a ver que es y como se realiza la cuantificación del potencial de oxidación - reducción standard en las siguientes diapositivas : aspectos básicos de oxidación - reducción IV Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid
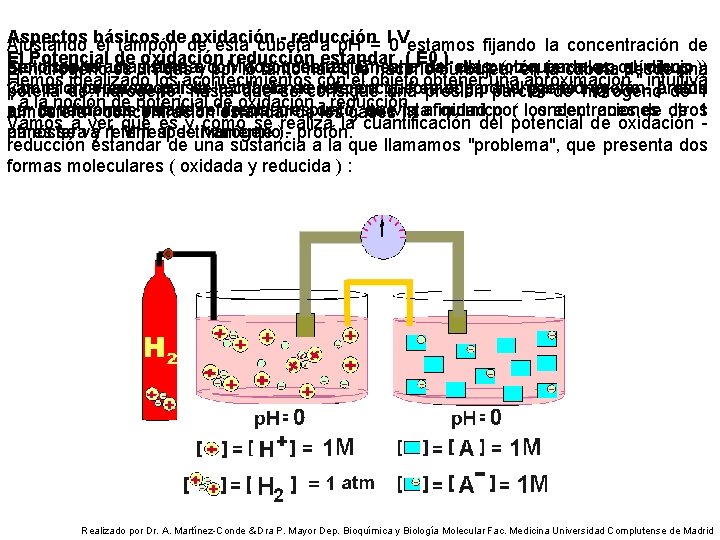
Aspectos básicos de oxidación - reducción I V Ajustando el tampón de esta cubeta a p. H = 0 estamos fijando la concentración de El Potencial de oxidación reducción estandar ( E 0 ). protones exactamente a 1 M ( concentración estandar del protón para los químicos ). Se dispone un sistema con dos cubetas. En una de ellas ( izquierda en el dibujo ) El hidrógeno es un gas y por lo tanto hay que hacerlo burbujear en la cubeta desde una Hemos idealizado los acontecimientos con el objeto obtener una aproximación " intuitiva Con ello ya tenemos lista la cubeta de referencia, formada por el par hidrógeno - protón vamos a poner un par de oxidación-reducción que es el par hidrógeno - protón. A este botella de hidrógeno, hasta que se consigue una presión parcial de hidrógeno de 1 " a la noción de potencial de oxidación - reducción. en condiciones estandar desde un punto de vista químico ( concentraciones de 1 par le llamamos par de referencia; es decir, que la afinidad por los electrones de otros atmósfera ( concentración estandar de los gases ). Vamos a ver que es y como se realiza la cuantificación del potencial de oxidación - atmósfera y 1 M respectivamente ). pares se va referir al de hidrógeno - protón. reducción estandar de una sustancia a la que llamamos "problema", que presenta dos formas moleculares ( oxidada y reducida ) : Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid
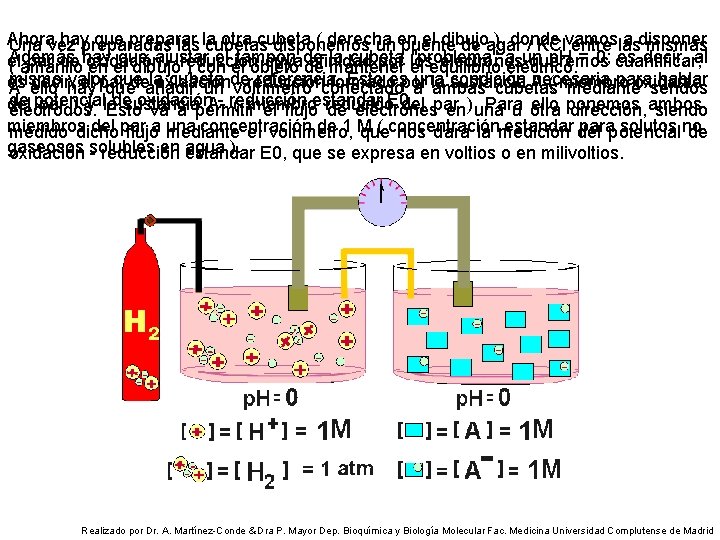
Ahora hay que preparar la otra cubeta ( derecha en el dibujo ), donde vamos a disponer Una vez preparadas las cubetas disponemos un puente de agar / KCl entre las mismas Además hay que ajustar el tampón de la cubeta "problema" a un p. H = 0; es decir, al el par de oxidación - reducción cuya afinidad por los electrones queremos cuantificar; ( amarillo en el dibujo ) con el objeto de mantener el equilibrio eléctrico. mismo valor que la cubeta de referencia. Esto es una condición necesaria para hablar es decir, el par de oxidación - reducción formado por la sustancia A ( miembro oxidante A ello hay que añadir un voltímetro conectado a ambas cubetas mediante sendos de potencial de oxidación - reducción estandar E 0. . del par ) y la sustancia A- ( miembro del par Para ello ponemos electrodos. Esto va a permitir el flujo reducido de electrones en ). una u otra dirección, ambos siendo miembros del par a una concentración de 1 M ( concentración estandar para solutos no medido dicho flujo mediante el voltímetro, que nos dará la medición del potencial de gaseosos solubles en agua ). oxidación - reducción estandar E 0, que se expresa en voltios o en milivoltios. Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid
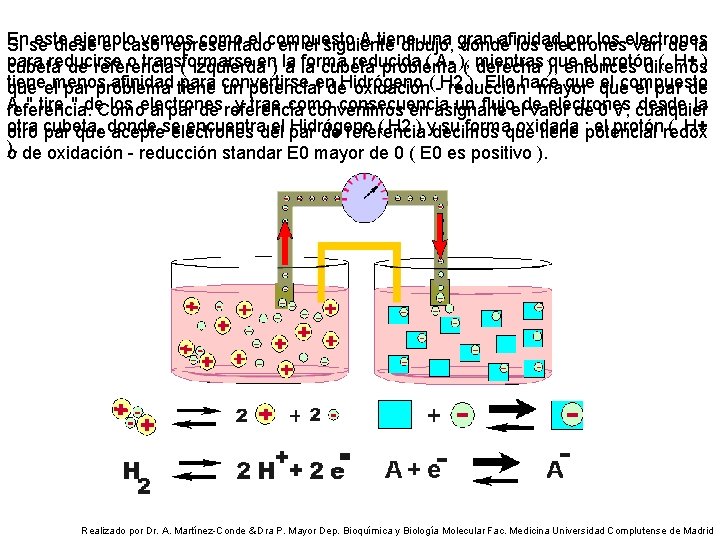
En este ejemplo vemos como el compuesto A tiene una gran afinidad por los electrones Si se diese el caso representado en el siguiente dibujo, donde los electrones van de la para reducirse o transformarse en la forma reducida ( A- ), mientras que el protón ( H+ ) cubeta de referencia ( izquierda ) a la cubeta problema ( derecha ), entonces diremos tiene menos afinidad para convertirse en Hidrógeno ( H 2 ). Ello hace que el compuesto que el par problema tiene un potencial de oxidación - reducción mayor que el par de A " tire " de los electrones, y trae como consecuencia un flujo de electrones desde la referencia. Como al par de referencia convenimos en asignarle el valor de 0 V, cualquier otra cubeta, donde se encuentra el Hidrógeno ( H 2 ) y su forma oxidada : el protón ( H+ otro par que acepte electrones del par de referencia decimos que tiene potencial redox ). o de oxidación - reducción standar E 0 mayor de 0 ( E 0 es positivo ). Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid
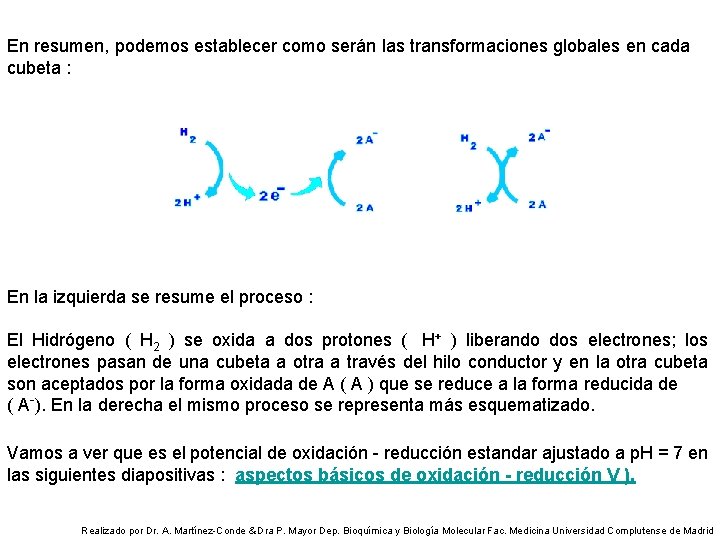
En resumen, podemos establecer como serán las transformaciones globales en cada cubeta : En la izquierda se resume el proceso : El Hidrógeno ( H 2 ) se oxida a dos protones ( H+ ) liberando dos electrones; los electrones pasan de una cubeta a otra a través del hilo conductor y en la otra cubeta son aceptados por la forma oxidada de A ( A ) que se reduce a la forma reducida de ( A-). En la derecha el mismo proceso se representa más esquematizado. Vamos a ver que es el potencial de oxidación - reducción estandar ajustado a p. H = 7 en las siguientes diapositivas : aspectos básicos de oxidación - reducción V ). Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid
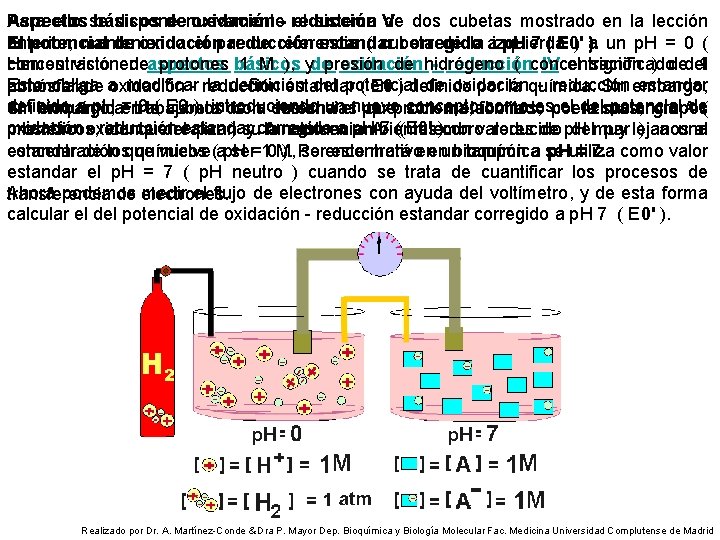
Para ello se dispone nuevamente el sistema de dos cubetas mostrado en la lección Aspectos básicos de oxidación - reducción V anterior, manteniendo el par de referencia ( cubeta de la izquierda ) a un p. H = 0 ( El potencial de oxidación reducción estandar corregido a p. H 7 ( E 0' ). concentración de aspectos protones básicos 1 M ), y presión de hidrógeno ( concentración ) de del 1 Hemos visto en de oxidación - reducción IV el significado Esto obliga a modificar la definición del potencial de oxidación - reducción estandar atmósfera. potencial de oxidación - reducción estandar ( E 0 ) definido por la química. Sin embargo, definido a p. H = 0 ( E 0 ), introduciendo un nuevo concepto como es el del potencial de Sin embargo, en la cubeta de la derecha el par problema, formado por la sustancia A ( en bioquímica trabajamos con sustancias que son metabolitos, coenzimas, grupos oxidación - reducción estandar corregido a p. H 7 ( E 0' ). miembro oxidante del par ) y la sustancia A- ( miembro reducido del par ), a una prostéticos, etc. que realizan su función en ambientes con valores de p. H muy lejanos al concentración que vuelve a ser 1 M, se encontrará en un tampón a p. H = 7. estandar de los químicos ( p. H = 0 ). Por este motivo en bioquímica se utiliza como valor estandar el p. H = 7 ( p. H neutro ) cuando se trata de cuantificar los procesos de Ahora podemos medir el flujo de electrones con ayuda del voltímetro, y de esta forma transferencia de electrones. calcular el del potencial de oxidación - reducción estandar corregido a p. H 7 ( E 0' ). Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid
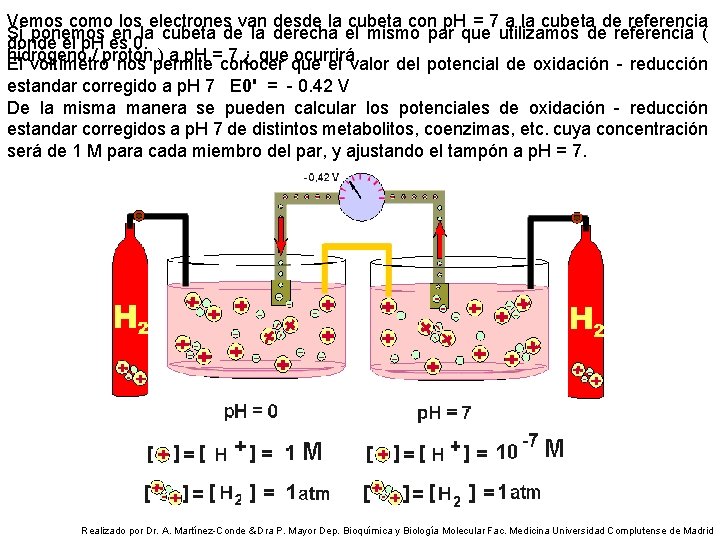
Vemos como los electrones van desde la cubeta con p. H = 7 a la cubeta de referencia Si ponemos en la cubeta de la derecha el mismo par que utilizamos de referencia ( donde el p. H es 0. hidrógeno / protón ) a p. H = 7 ¿ que ocurrirá El voltímetro nos permite conocer que el valor del potencial de oxidación - reducción estandar corregido a p. H 7 E 0' = - 0. 42 V De la misma manera se pueden calcular los potenciales de oxidación - reducción estandar corregidos a p. H 7 de distintos metabolitos, coenzimas, etc. cuya concentración será de 1 M para cada miembro del par, y ajustando el tampón a p. H = 7. Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid

En la siguiente tabla podemos observar los valores del potencial de oxidación - reducción estandar corregidos a p. H 7 de distintos metabolitos, coenzimas y grupos próstéticos : Realizado por Dr. A. Martínez-Conde & Dra P. Mayor Dep. Bioquímica y Biología Molecular Fac. Medicina Universidad Complutense de Madrid
- Slides: 9