Emogasanalisi ed equilibrio acidobase Prof Enrico Polati Anestesia

Emogasanalisi ed equilibrio acido-base Prof. Enrico Polati Anestesia e Rianimazione, Centro di Terapia Antalgica, Policlinico di Verona Direttore Prof. Enrico Polati
![Emogasanalisi ed equilibrio acido-base: p. H = - log [H+]: logaritmo negativo dell’attività ioni Emogasanalisi ed equilibrio acido-base: p. H = - log [H+]: logaritmo negativo dell’attività ioni](http://slidetodoc.com/presentation_image_h2/b2891f6fecbc7068a3d3cf0ec2f534e2/image-2.jpg)
Emogasanalisi ed equilibrio acido-base: p. H = - log [H+]: logaritmo negativo dell’attività ioni H+ Se p. H = 7, 4 [H+] = 40 nmol/L
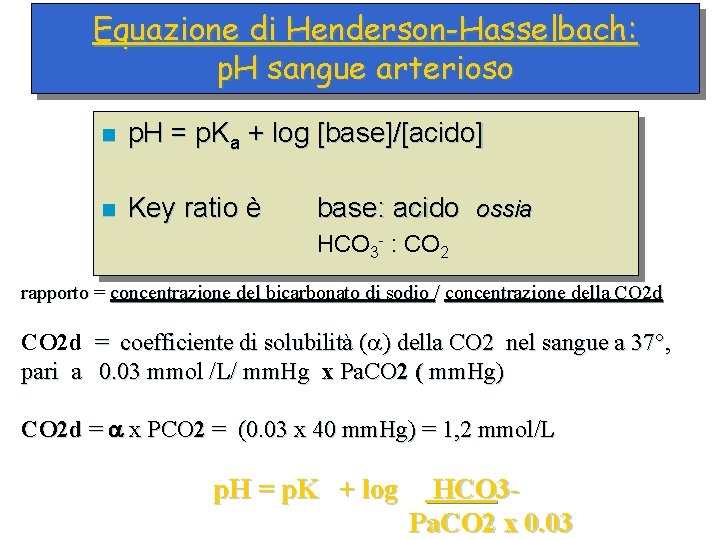
Equazione di Henderson-Hasselbach: p. H sangue arterioso n p. H = p. Ka + log [base]/[acido] n Key ratio è base: acido ossia HCO 3 - : CO 2 rapporto = concentrazione del bicarbonato di sodio / concentrazione della CO 2 d = coefficiente di solubilità ( ) della CO 2 nel sangue a 37°, pari a 0. 03 mmol /L/ mm. Hg x Pa. CO 2 ( mm. Hg) CO 2 d = x PCO 2 = (0. 03 x 40 mm. Hg) = 1, 2 mmol/L p. H = p. K + log HCO 3 Pa. CO 2 x 0. 03

Equazione di Henderson-Hasselbach: p. H sangue arterioso p. H = p. K + log HCO 3 Pa. CO 2 x 0. 03 Pa. CO 2 nel sangue arterioso Pa. CO 2 mm Hg 40 CO 2 d (mmol/L) = 40 x 0. 03 =1. 2 HCO 3 - nel sangue arterioso = 24 p. K tampone bicarbonato = 6, 1 p. H = 6, 1 + log 24 mmol/L / 1, 2 mmol/L p. H = 6, 1 + log 20 = 1. 3 p. H= 6. 1+1. 3 = 7. 4
![Il p. H è logaritmico p. H = log 1/[H+] n = - log Il p. H è logaritmico p. H = log 1/[H+] n = - log](http://slidetodoc.com/presentation_image_h2/b2891f6fecbc7068a3d3cf0ec2f534e2/image-5.jpg)
Il p. H è logaritmico p. H = log 1/[H+] n = - log 0. 00000004 = 40 nmol/L [H+] n p. H = 7. 4 n n Pensare al p. H come “potenza della [H+]”

![Il p. H è logaritmico Il p. H è inversamente proporzionale alla [H+] Piccole Il p. H è logaritmico Il p. H è inversamente proporzionale alla [H+] Piccole](http://slidetodoc.com/presentation_image_h2/b2891f6fecbc7068a3d3cf0ec2f534e2/image-7.jpg)
Il p. H è logaritmico Il p. H è inversamente proporzionale alla [H+] Piccole di p. H determinano ampie [H+] quando [H+] p. H & quando [H+] p. H 7. 4 = 40 nmol/L [H+] p. H 7. 1 = 80 nmol/L [H+] (è raddoppiato!)

Acidemia, alcalemia n p. H < 7, 35 acidemia n p. H > 7, 45 alcalemia Acidosi ed alcalosi: processi primitivi che causano la variazione della [H+ ] e quindi del p. H, determinata dal rapporto tra la componente metabolica e quella respiratoria (CO 2) del sistema di regolazione acido-base.

Equilibrio acido-base Regolazione precisa necessaria per tutte le attività enzimatiche (ATPasi Na-K lavora tra 6. 757. 75) n Dipendente da: – Sistemi Tampone – Sistema Respiratorio – Reni
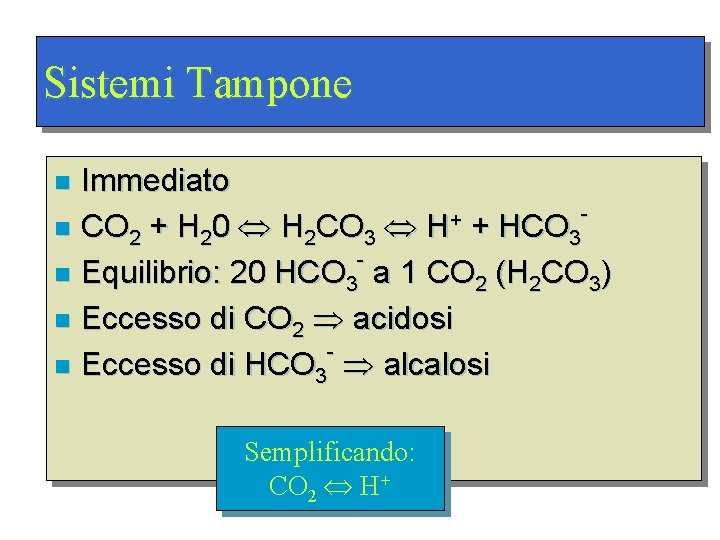
Sistemi Tampone Immediato + n CO 2 + H 20 H 2 CO 3 H + HCO 3 n Equilibrio: 20 HCO 3 a 1 CO 2 (H 2 CO 3) n Eccesso di CO 2 acidosi n Eccesso di HCO 3 alcalosi n Semplificando: CO 2 H+

Sistema Respiratorio • Meccanismo respiratorio mantenimento p. H via ventilazione polmonare: 1) trattenendo la CO 2 nell’alcalosi metabolica, 2) eliminando la CO 2 nell’acidosi metabolica. • H+ eccita il CR bulbare conseguente iperventilazione • Pa. CO 2 (acido volatile): CO 2 + H 2 O H 2 CO 3 H+ + HCO 3 -

Sistema Respiratorio n Pa. CO 2 Centro Respiratorio ventilazione alveolare n della Pa. CO 2 potente stimolo alla ventilazione alveolare, per cui l’acidosi respiratoria viene corretta rapidamente, a meno che fattori patologici non mantengano l’ipoventilazione !! n Aumento Pa. CO 2 non si traduce in acidosi se la ventilazione alveolare è efficiente; la causa principale di acidosi respiratoria è quindi una ridotta ventilazione alveolare !! n Se Pa. CO 2 è molto alta indurrà depressione del CR

Sistema Respiratorio Minuti n CO 2 H+ n Ventilazione : CO 2 : H+ n

Sistema Respiratorio n n Pa. O 2 : pressione parziale di ossigeno nel sangue arterioso (espressa in mm Hg). VN : 80 -100 mm Hg ; (dipende dall’età e dal BMI) n effetti sulla ventilazione polmonare si rendono evidenti quando la Pa. O 2 raggiunge valori < 60 mm. Hg n Spinta ipossica (hypoxic drive) : forte stimolo alla respirazione indotto dall’ipossia. n Attenzione quindi quando si inizia terapia con ossigeno!!!

Sistema Renale Da ore a giorni n Riassorbimento del bicarbonato n Escrezione di H+ n Escrezione di ammonio n

Valori normali p. H: 7. 35 - 7. 45 (meglio 7. 38 -7. 42) n Pa. CO 2: 38 – 42 mm. Hg n Pa. O 2: posizione seduta 104 mm. Hg – (0. 27 x età) n posizione supina 103 mm. Hg – (0. 45 x età) n HCO 3 : 24 mmol/l
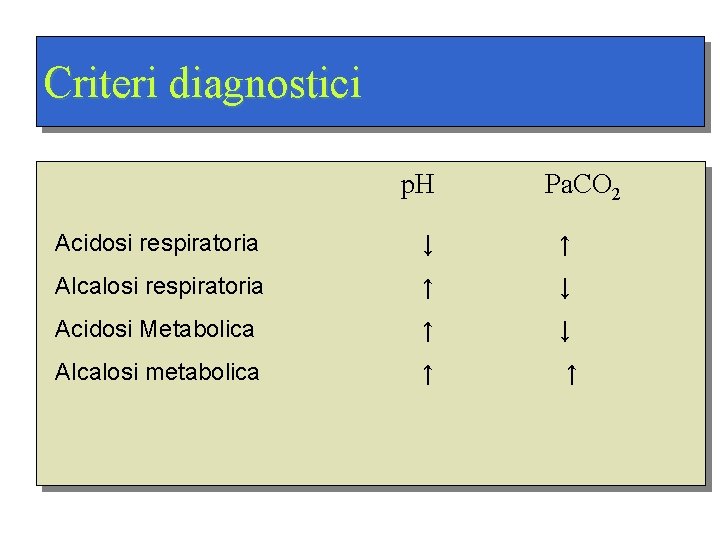
Criteri diagnostici p. H Pa. CO 2 Acidosi respiratoria ↓ ↑ Alcalosi respiratoria ↑ ↓ Acidosi Metabolica ↑ ↓ Alcalosi metabolica ↑ ↑
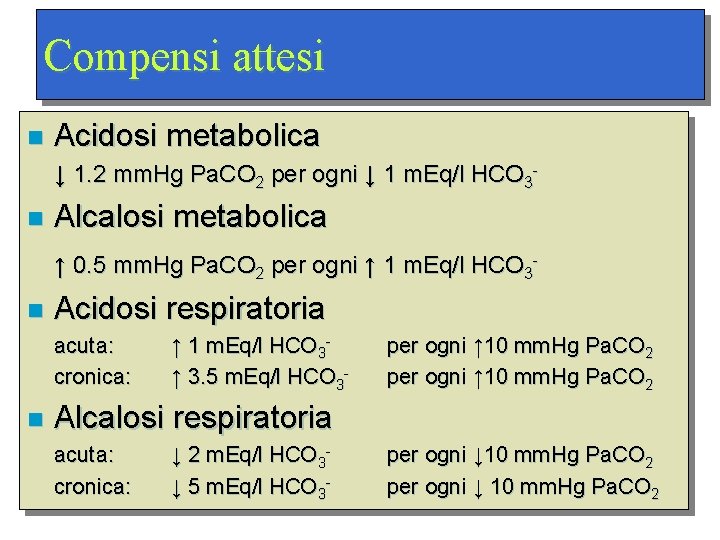
Compensi attesi n Acidosi metabolica ↓ 1. 2 mm. Hg Pa. CO 2 per ogni ↓ 1 m. Eq/l HCO 3 - n Alcalosi metabolica ↑ 0. 5 mm. Hg Pa. CO 2 per ogni ↑ 1 m. Eq/l HCO 3 - n Acidosi respiratoria acuta: cronica: n ↑ 1 m. Eq/l HCO 3↑ 3. 5 m. Eq/l HCO 3 - per ogni ↑ 10 mm. Hg Pa. CO 2 Alcalosi respiratoria acuta: cronica: ↓ 2 m. Eq/l HCO 3↓ 5 m. Eq/l HCO 3 - per ogni ↓ 10 mm. Hg Pa. CO 2

Disordini Acidosi Respiratoria n Alcalosi Respiratoria n Acidosi Metabolica n Alcalosi Metabolica n
![Acidosi Respiratoria Caratterizzata da un aumentata [CO 2] e di [H 2 CO 3 Acidosi Respiratoria Caratterizzata da un aumentata [CO 2] e di [H 2 CO 3](http://slidetodoc.com/presentation_image_h2/b2891f6fecbc7068a3d3cf0ec2f534e2/image-20.jpg)
Acidosi Respiratoria Caratterizzata da un aumentata [CO 2] e di [H 2 CO 3 ] con diminuzione del p. H. Disturbo primitivo: n aumento della [CO 2] per difetto della ventilazione o degli scambi gassosi alveolari.
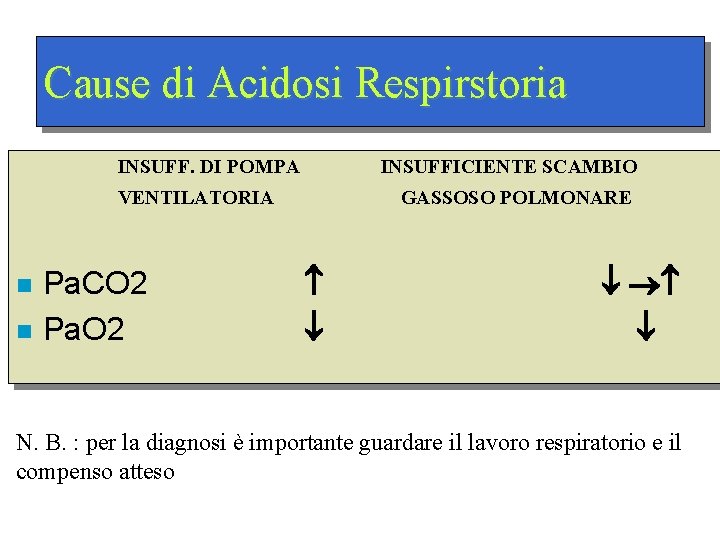
Cause di Acidosi Respirstoria INSUFF. DI POMPA INSUFFICIENTE SCAMBIO VENTILATORIA n n Pa. CO 2 Pa. O 2 GASSOSO POLMONARE N. B. : per la diagnosi è importante guardare il lavoro respiratorio e il compenso atteso
![Alcalosi Respiratoria Caratterizzata da diminuzione della [CO 2] e degli HCO 3 , con Alcalosi Respiratoria Caratterizzata da diminuzione della [CO 2] e degli HCO 3 , con](http://slidetodoc.com/presentation_image_h2/b2891f6fecbc7068a3d3cf0ec2f534e2/image-22.jpg)
Alcalosi Respiratoria Caratterizzata da diminuzione della [CO 2] e degli HCO 3 , con aumento del p. H. Disturbo primitivo: n aumento della ventilazione polmonare che determina ipocapnia e conseguente calo dei HCO 3 per meccanismo di compenso.

Cause di Alcalosi Respiratoria n Sepsi (mediatori) n SNC (sdr. ansiose, iperventilazione da stimoli dolorifici, …) n Ipossia con compenso ventilatorio in iperventilazione (es. embolia polmonare) n Altro (ventilazione meccanica, insufficienza epatica)

Acidosi Metabolica HCO 3 Caratterizata da diminuzione degli ed diminuzione del p. H (la CO 2 diminuisce per iperventilazione di compenso). Disturbo primitivo: n diminuzione della bicarbonatemia per eccesso di acidi (tamponati dagli HCO 3 ) n perdita consistente di basi (tratto intestinalediarrea-, o dal rene- es. acidosi tubulare renale)

Acidosi Metabolica Per differenziare i due tipi di acidosi è necessario calcolare il gap anionico e determinare la concentrazione sierica del cloro: n nella acidosi metabolica da consumo di bicarbonato il gap anionico è aumentato n nella acidosi metabolica da perdita di bicarbonato il gap anionico è normale ed è aumentato il cloro per ragioni di elettroneutralità

Gap anionico Nel siero le cariche + devono essere bilanciate da un egual numero di cariche -, ma le routinarie tecniche di laboratorio misurano più + + cationi(Na e K ) che anioni(Cl e HCO 3 ). Il gap anionico è costituito per circa due terzi da proteine e per un terzo da anioni inorganici L’intervallo anionico sarà quindi espresso da: [Na+ + K+] – [Cl- + HCO 3 -] = 10 -17 mmol/L

Cause di Acidosi Metabolica A gap anionico aumentato, o normocloremiche: q shock q chetoacidosi diabetica q acidosi lattica q avvelenamenti (introduzione di sostanze tossiche causano acidosi direttamente o tramite i loro metaboliti) q insufficienza renale acuta o cronica (diminuita escrezione acidi)

Cause di Acidosi Metabolica A gap anionico normale, o ipercloremiche: Ø q q da perdita di bicarbonati intestinale diarrea ureterosigmoidostomia da perdita di bicarbonati renale malattie tubulari renali (acidosi tubulare, malattie tubulointerstiziali) inibitori anidrasi carbonica da somministrazione di Cl cloruro d’ammonio soluzioni fisiologiche
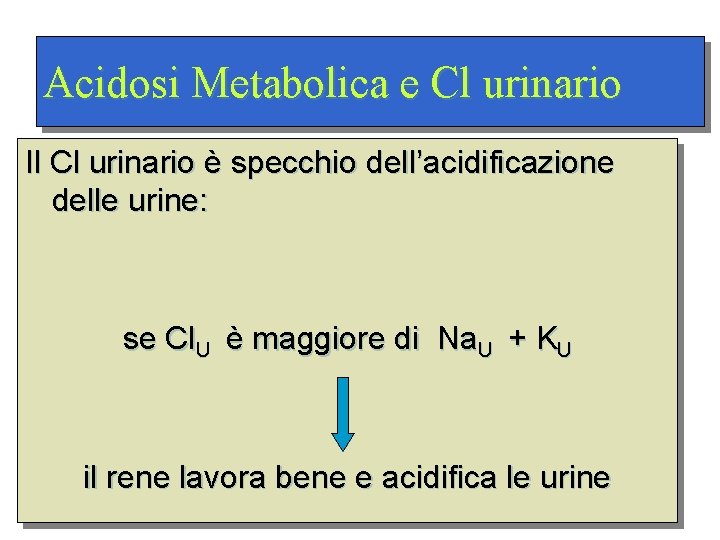
Acidosi Metabolica e Cl urinario Il Cl urinario è specchio dell’acidificazione delle urine: se Cl. U è maggiore di Na. U + KU il rene lavora bene e acidifica le urine
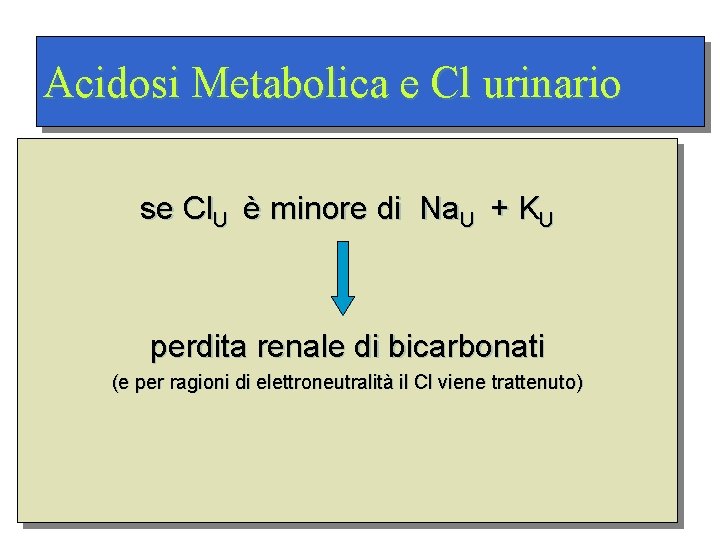
Acidosi Metabolica e Cl urinario se Cl. U è minore di Na. U + KU perdita renale di bicarbonati (e per ragioni di elettroneutralità il Cl viene trattenuto)
![Alcalosi metabolica - Caratterizzata da un’aumentata [HCO 3 ] con aumento del p. H Alcalosi metabolica - Caratterizzata da un’aumentata [HCO 3 ] con aumento del p. H](http://slidetodoc.com/presentation_image_h2/b2891f6fecbc7068a3d3cf0ec2f534e2/image-31.jpg)
Alcalosi metabolica - Caratterizzata da un’aumentata [HCO 3 ] con aumento del p. H e, per compenso, della Pa. CO 2 (ipoventilazione). Disordini fondamentali: q aumento primitivo della [HCO 3 ] di origine esogena o endogena q primitiva perdita di acidi conseguente aumento relativo degli HCO 3.

Cause di alcalosi metabolica q Il 90% delle volte sono ipovolemiche (alcalosi metabolica da contrazione di volume > attivazione aldosterone e sistema renina/angiotensina) q Se il volume circolante effettivo è alto: - iperaldosteronismo - cortisonici

Cause di alcalosi metabolica q Cloro responsive: vomito, perdite di secrezioni gastriche atrraverso il sondino naso-gastrico, diuretici, post-ipercapnia. q Cloro resistenti: iperaldosteronismo, sindrome di Cushing, liquirizia, grave deplezione potassica, uso protratto di corticosteroidei.

Cause di alcalosi metabolica Il cloro urinario permette di distinguere le due forme di alcalosi: q Cl urinario < 10 m. Eq/l = alcalosi metabolica cloro-responsiva q Cl urinario > 20 m. Eq/l = alcalosi metabolica cloro-resistente N. B. : in caso di diuretici in atto il Cl urinario può essere elevato

Alcalosi metabolica post-ipercapnica Attenzione!!! ↓ Mg K Ca > rischio aritmie!!!
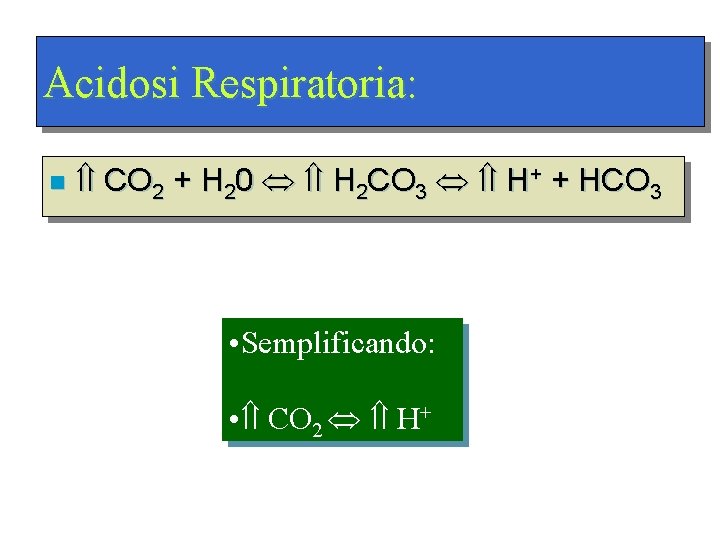
Acidosi Respiratoria: n CO 2 + H 20 H 2 CO 3 H+ + HCO 3 • Semplificando: • CO 2 H+
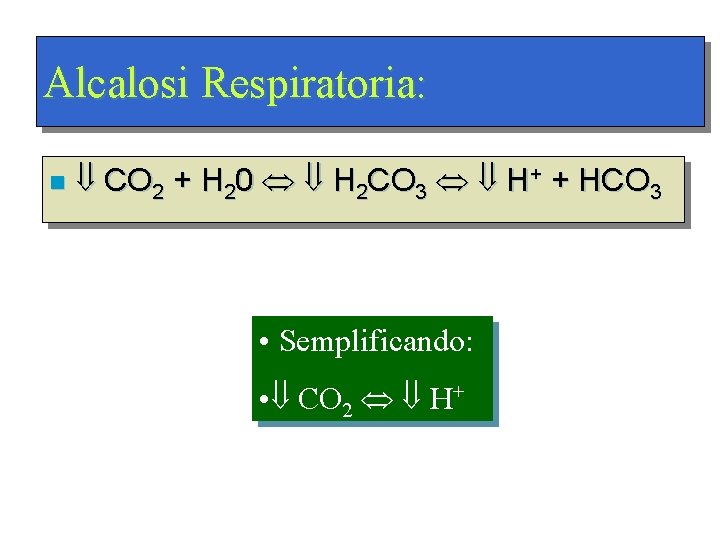
Alcalosi Respiratoria: n CO 2 + H 20 H 2 CO 3 H+ + HCO 3 • Semplificando: • CO 2 H+
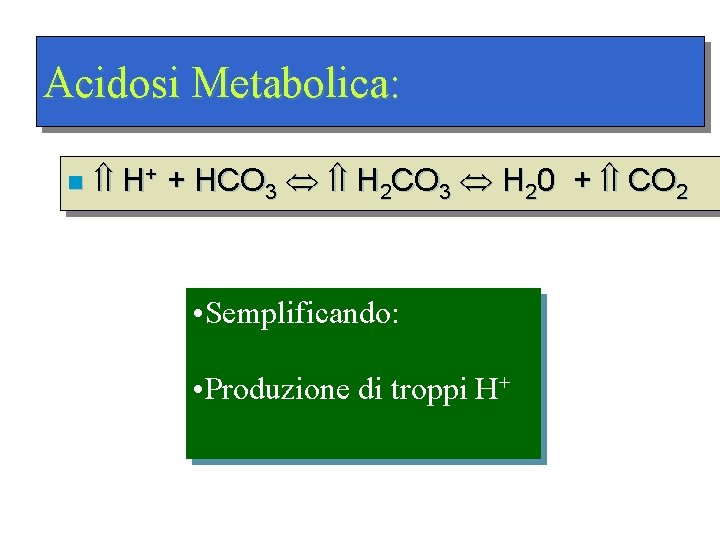
Acidosi Metabolica: n H+ + HCO 3 H 2 CO 3 H 20 + CO 2 • Semplificando: • Produzione di troppi H+
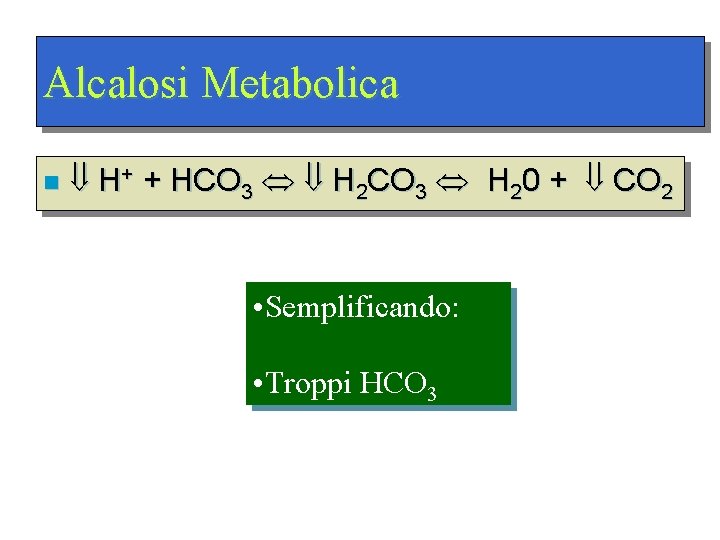
Alcalosi Metabolica n H+ + HCO 3 H 2 CO 3 H 20 + CO 2 • Semplificando: • Troppi HCO 3

Esempio: n n n p. H = 7. 25 PCO 2 = 60 mm. Hg HCO 3 - normale Acidosi respiratoria acuta!

Esempio: n n n p. H = 7. 35 PCO 2 = 60 mm. Hg HCO 3 - aumentato Acidosi respiratoria compensata!

Esempio: n n n p. H = 7. 50 PCO 2 = 38 mm. Hg HCO 3 - aumentato Alcalosi metabolica!

Esempio: n n n p. H = 7. 46 PCO 2 = 45 mm. Hg HCO 3 - aumentato Alcalosi metabolica compensata!

Esempio: p. H = 7. 60 n PCO 2 = 20 mm. Hg n Alcalosi respiratoria!

Esempio: n n n p. H = 7. 08 PCO 2 = 38 mm. Hg HCO 3 - diminuito Acidosi metabolica acuta!

Esempio: n n n p. H = 7. 33 PCO 2 = 27 mm. Hg HCO 3 - diminuiti Acidosi metabolica compensata!
- Slides: 46