EMBOLIE PULMONAIRE AIGUE PLAN INTRODUCTION v RAPPEL ANATOMIQUEPHYSIOPATHOLOGIE

EMBOLIE PULMONAIRE AIGUE

PLAN INTRODUCTION v RAPPEL ANATOMIQUE-PHYSIOPATHOLOGIE v ETIOLOGIES v FACTEURS DE RISQUE v DIAGNOSTIC POSITIF PRESOMPTION CLINIQUE BILAN DIAGNOSTIC v DIAGNOSTIC DIFFERENTIEL v DIAGNOSTIC ETIOLOGIQUE v EVOLUTION v STRATEGIE DIAGNOSTIQUE v TRAITEMENT v CONCLUSION v

INTRODUCTION � EPA: obstruction artérielle pulmonaire +/- importante , responsable d’une altération de l’hémodynamique droite et d’un trouble de l’échange gazeux. � Affection très fréquente: 3ème cause de pathologie cardio vasculaire aigue � Morbidité et mortalité non négligeable. � Lien étroit avec la thrombose veineuse des MI: concept de maladie veineuse thrombo embolique � Urgence diagnostique et thérapeutique � Diagnostic +: probabilité clinique + Scanner spiralé surtout volumique multi coupes: examen de référence

OBJECTIFS � Reconnaitre � Savoir les moyens d’exploration d’une EPA réaliser un angio scanner ++ � Reconnaitre les éléments sémiologiques de diagnostic d’EPA � Savoir établir une stratégie de diagnostic devant une EPA

RAPPEL ANATOMIQUE PHYSIOPATHOLOGIE
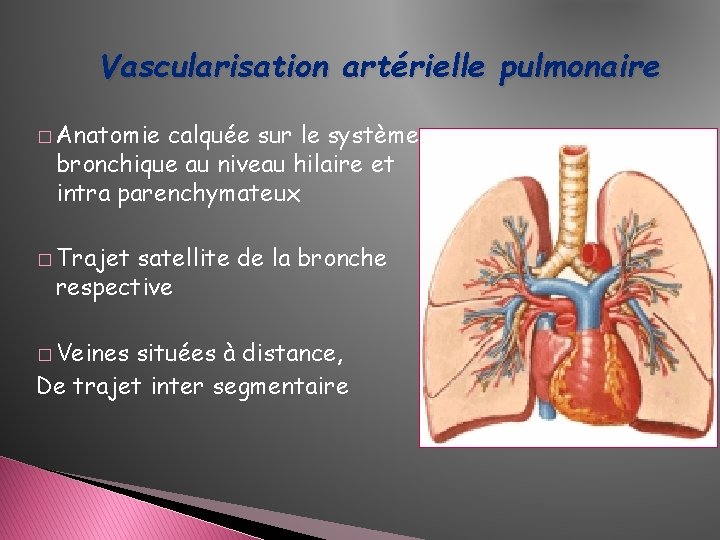
Vascularisation artérielle pulmonaire � Anatomie calquée sur le système bronchique au niveau hilaire et intra parenchymateux � Trajet satellite de la bronche respective � Veines situées à distance, De trajet inter segmentaire
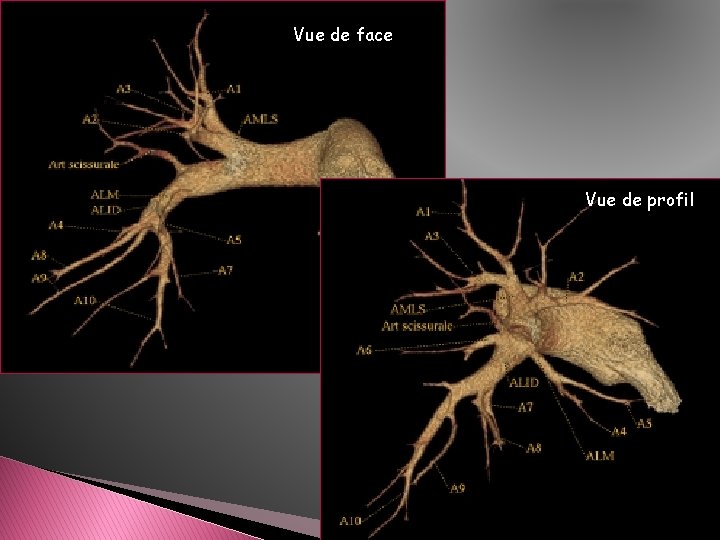
Vue de face Vue de profil
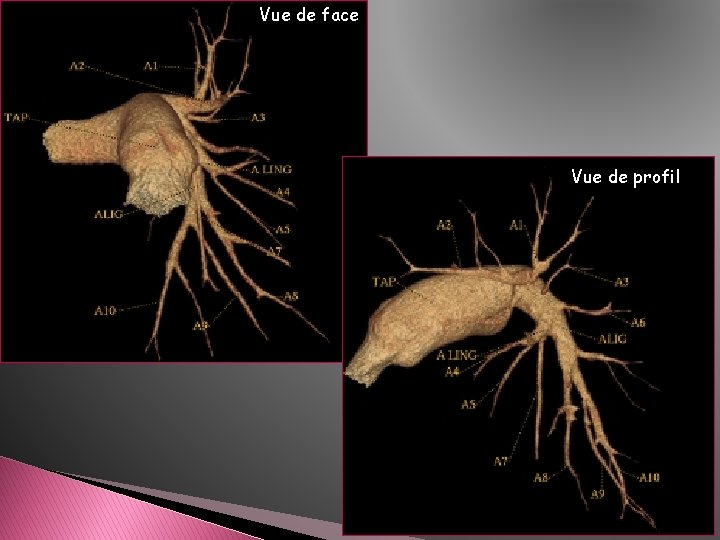
Vue de face Vue de profil

PHYSIOPATHOLOGIE Vascularisation arterielle pulmonaire est double: Système artériel pulmonaire: échanges gazeux Système bronchique systémique: vascularisation des voies aériennes inférieures Collatéralité peu développée entre les deux v v Obstruction d’une branche artérielle hypoperfusion vasodilatation du système bronchique reperfusion du territoire ischémié
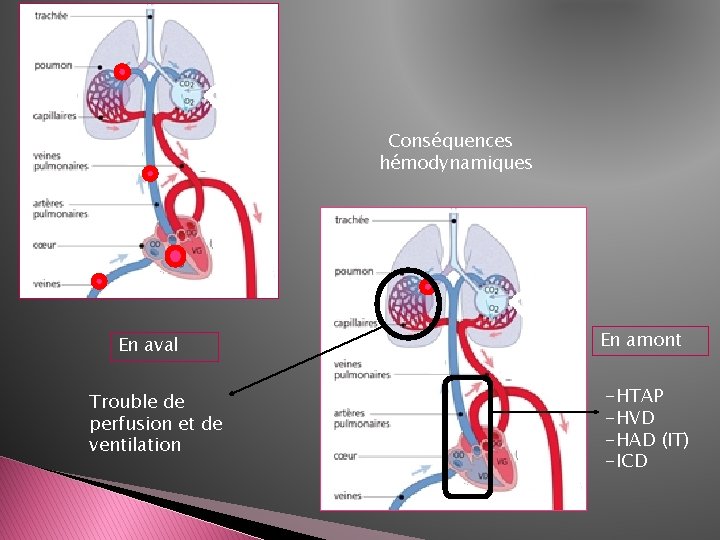
Conséquences hémodynamiques En aval Trouble de perfusion et de ventilation En amont -HTAP -HVD -HAD (IT) -ICD

ETIOLOGIES � Thrombus fibrino cruorique origine: phlébite des membres inférieurs (80%) étages sus et sous poplités � Thrombus non cruorique emboles graisseux, tumoraux, infectieux, ….

FACTEURS DE RISQUE � Chirurgie récente: orthopédie++, oncologie � Traumatisme des MI � Post partum (<3 mois) � Immobilisation prolongée de plus de 3 jours � Thrombophilie acquise: polyglobulie, Sd myéloprolifératifs, Sd Ac anti phospholipides… � Thrombophilie congénitale: Déficit en : Antithrombine III, protéine S/C, mutation des facteurs V ou II � Cancer actif � Sd néphrotique � Obésité, tabagisme, HTA � CO / THS

DIAGNOSTIC POSITIF

PROBABILITÉ CLINIQUE � Polymorphisme clinique � 3 Grands syndromes: - Douleur pleurétique / hémoptysie: Emboles périphériques hémorragie alvéolaire - Dyspnée isolée/ cyanose Emboles proximaux douleur rétrosternale oppressive - EPA grave Gros emboles centraux cœur pulmonaire aigu: tachycardie, turgescence jugulaire, RHJ, hypotension artérielle, signes de choc périphérique

Probabilité clinique

BILAN DIAGNOSTIC BIOLOGIE: Dosage plasmatique des D-Dimères Peu spécifique Valeur prédictive négative en dessous de 500 µg/L : 95% ECG: incts et non spécifiques Reflète une embolie pulmonaire grave: BBD, onde P, déviation axiale droite, complexe S 1 Q 3 Gaz du sang: incts et peu spécifiques Normaux: 20% Hypoxie (70 -80%) +/- hypercapnie
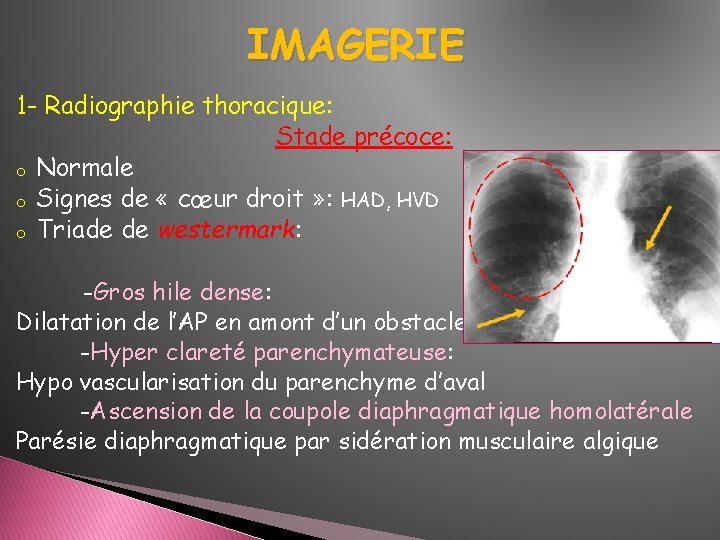
IMAGERIE 1 - Radiographie thoracique: Stade précoce: o Normale o Signes de « cœur droit » : HAD, HVD o Triade de westermark: -Gros hile dense: Dilatation de l’AP en amont d’un obstacle -Hyper clareté parenchymateuse: Hypo vascularisation du parenchyme d’aval -Ascension de la coupole diaphragmatique homolatérale Parésie diaphragmatique par sidération musculaire algique
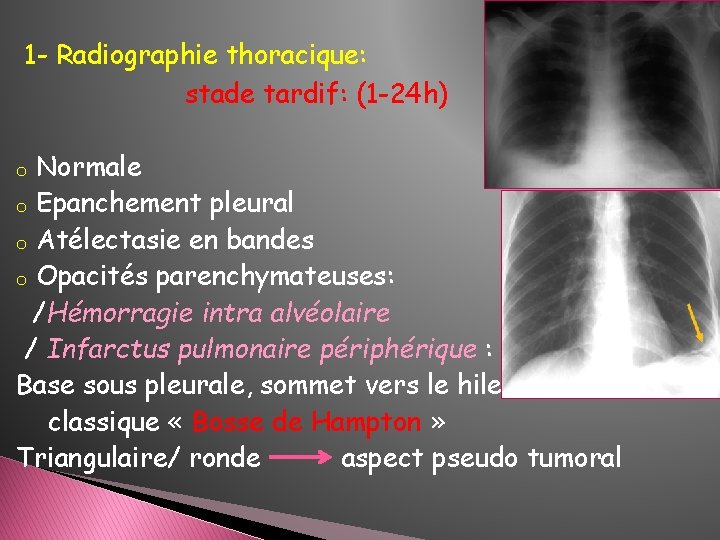
1 - Radiographie thoracique: stade tardif: (1 -24 h) Normale o Epanchement pleural o Atélectasie en bandes o Opacités parenchymateuses: /Hémorragie intra alvéolaire / Infarctus pulmonaire périphérique : Base sous pleurale, sommet vers le hile classique « Bosse de Hampton » Triangulaire/ ronde aspect pseudo tumoral o

Intérêt en pratique: -Éliminer un diagnostic différentiel -Évaluer l’état du parenchyme pulmonaire -Prévoir la rentabilité d’une scintigraphie de perfusion- ventilation

2 -Angioscanner � Examen de référence +++ � Diagnostic positif/ diagnostic de gravité / diagnostic différentiel � Non invasif, disponible, sensible et spécifique >90% avec Valeur prédictive négative est de 98% TECHNIQUE: -Apnée - Coupes sans injection de PDC de 5 mm de l’apex pulmonaire au coupoles diaphragmatiques -Acquisition hélicoïdale injectée: Épaisseur de coupes 1 mm/0, 8 mm (multibarettes) 2 -3 mm/1, 7 mm (monobarettes) Quantité: 90 -120 ml Débit de la seringue automatique: 4 -6 ml/s Couplage injection-acquisition
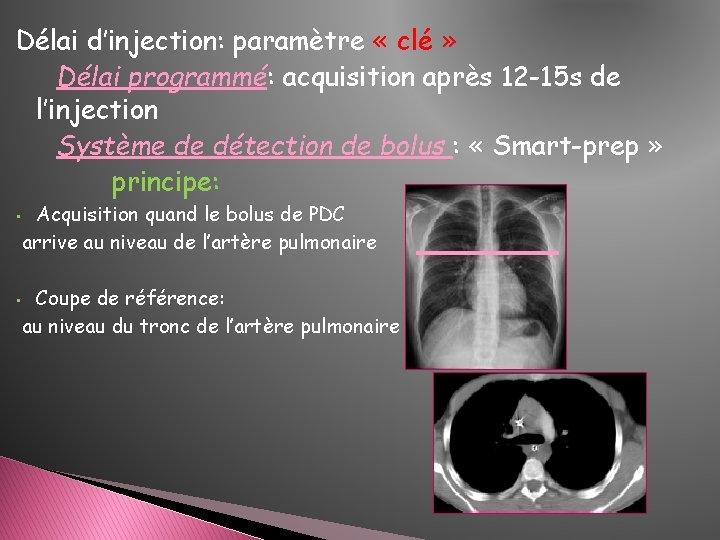
Délai d’injection: paramètre « clé » Délai programmé: acquisition après 12 -15 s de l’injection Système de détection de bolus : « Smart-prep » principe: • • Acquisition quand le bolus de PDC arrive au niveau de l’artère pulmonaire Coupe de référence: au niveau du tronc de l’artère pulmonaire
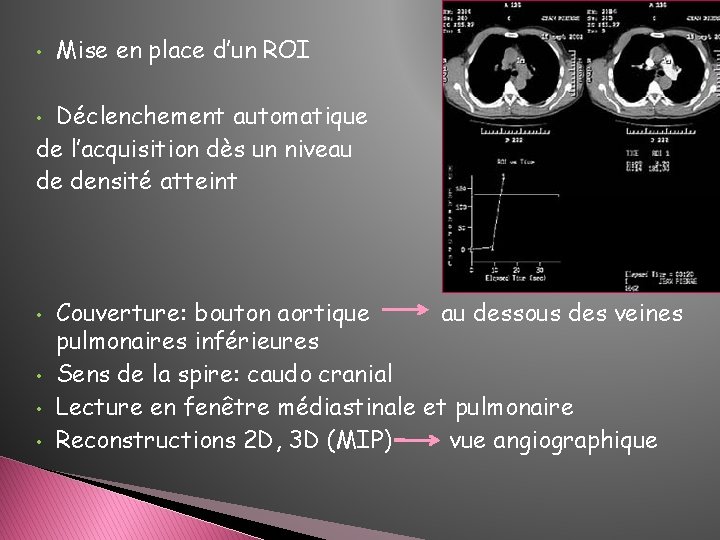
• Mise en place d’un ROI Déclenchement automatique de l’acquisition dès un niveau de densité atteint • • • Couverture: bouton aortique au dessous des veines pulmonaires inférieures Sens de la spire: caudo cranial Lecture en fenêtre médiastinale et pulmonaire Reconstructions 2 D, 3 D (MIP) vue angiographique
RESULTATS: Signes directs Signes indirects Signes de retentissement
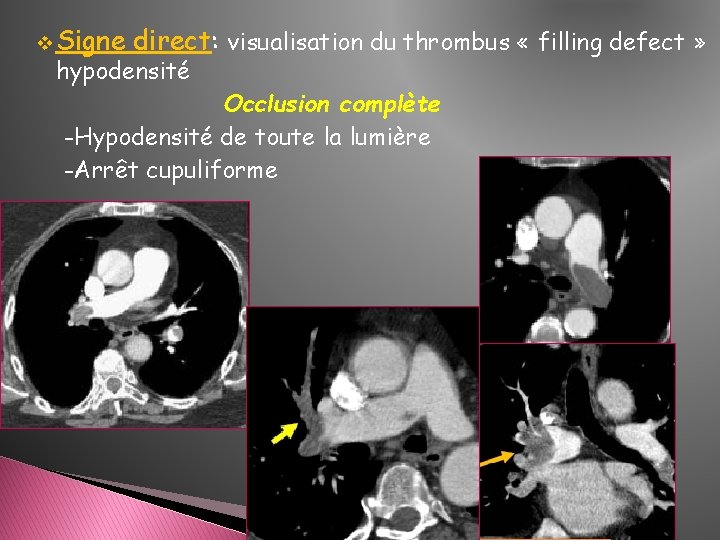
v Signe direct: visualisation du thrombus « filling defect » hypodensité Occlusion complète -Hypodensité de toute la lumière -Arrêt cupuliforme
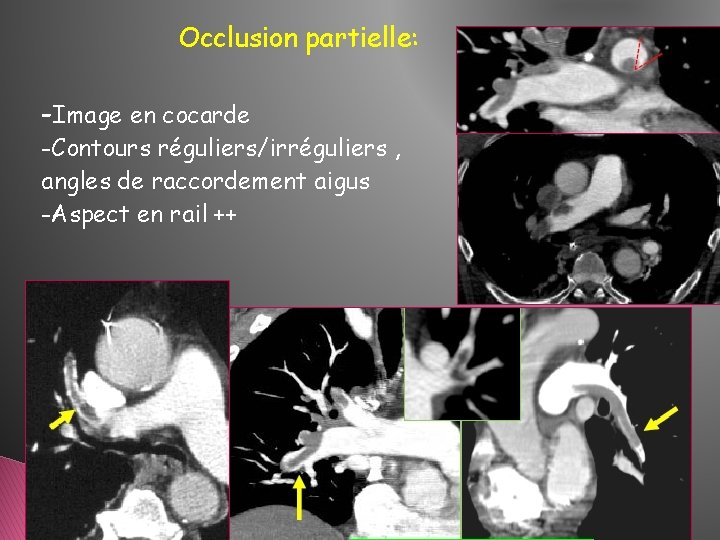
Occlusion partielle: -Image en cocarde -Contours réguliers/irréguliers , angles de raccordement aigus -Aspect en rail ++
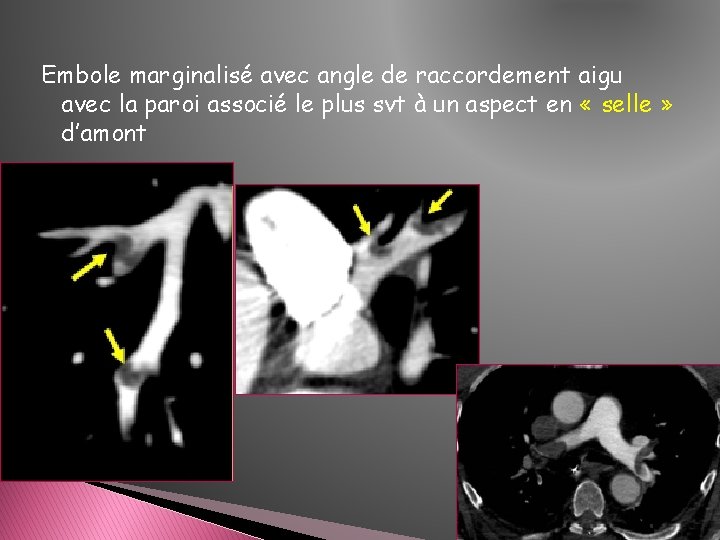
Embole marginalisé avec angle de raccordement aigu avec la paroi associé le plus svt à un aspect en « selle » d’amont
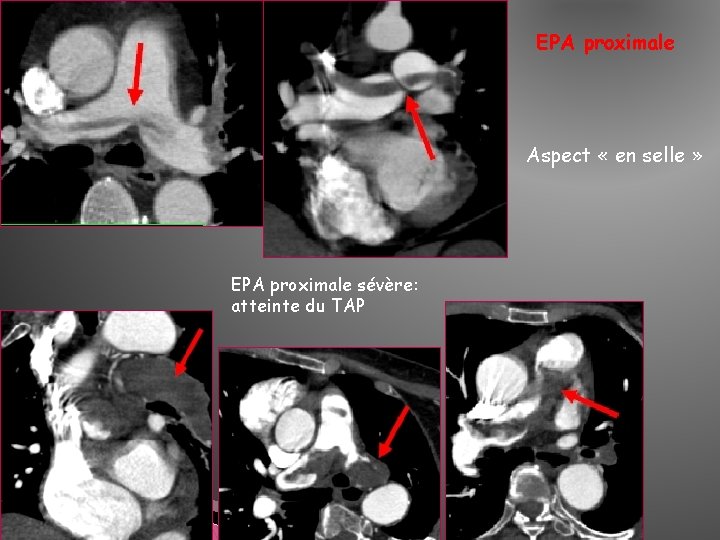
EPA proximale Aspect « en selle » EPA proximale sévère: atteinte du TAP
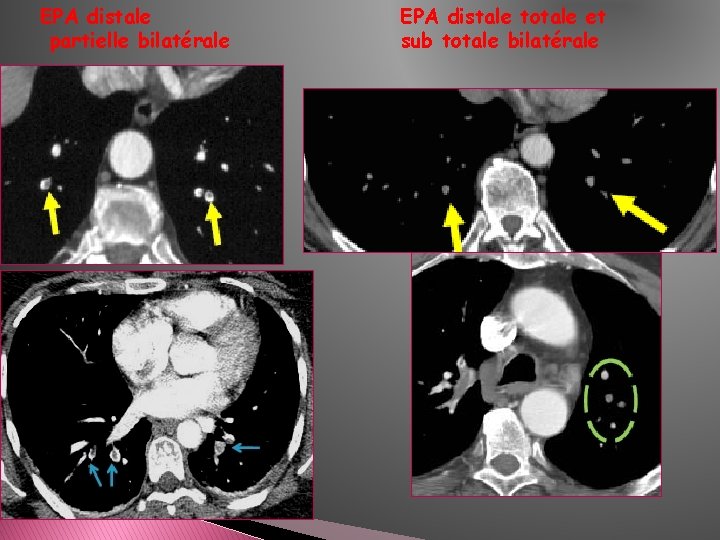
EPA distale partielle bilatérale EPA distale totale et sub totale bilatérale

Svt: augmentation du calibre du vaisseau thrombosé + œdème péri artériel du tissu interstitiel migration récente

RESULTATS: Signes directs Signes indirects Signes de retentissement
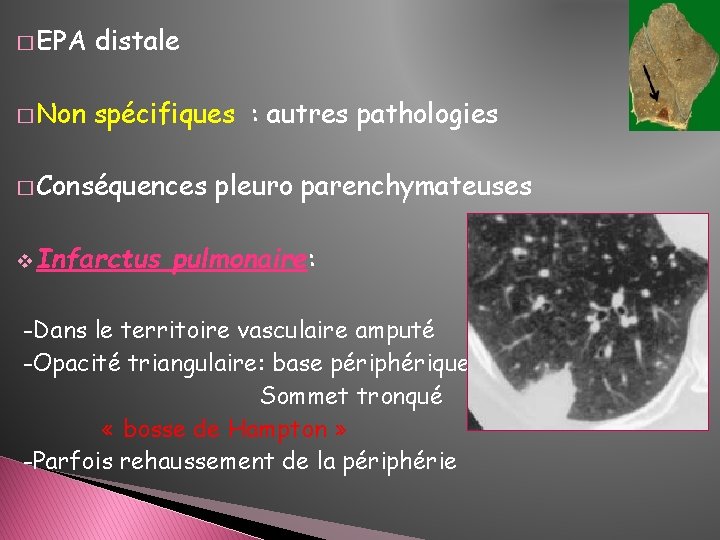
� EPA distale � Non spécifiques : autres pathologies � Conséquences v Infarctus pleuro parenchymateuses pulmonaire: -Dans le territoire vasculaire amputé -Opacité triangulaire: base périphérique, Sommet tronqué « bosse de Hampton » -Parfois rehaussement de la périphérie
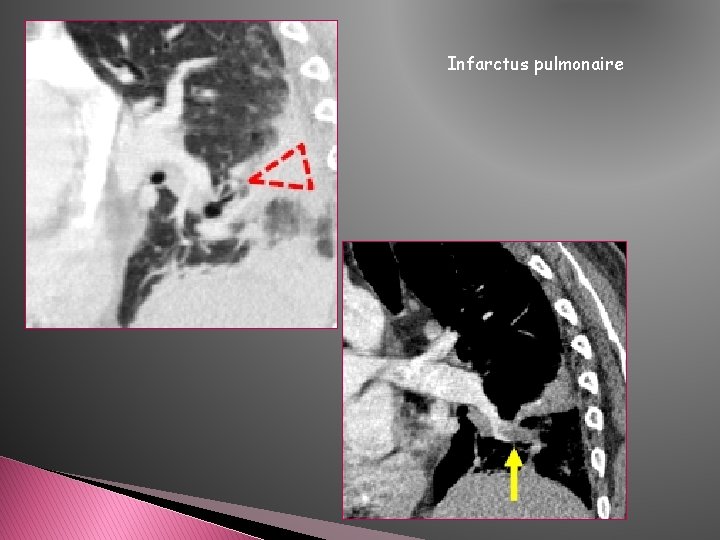
Infarctus pulmonaire
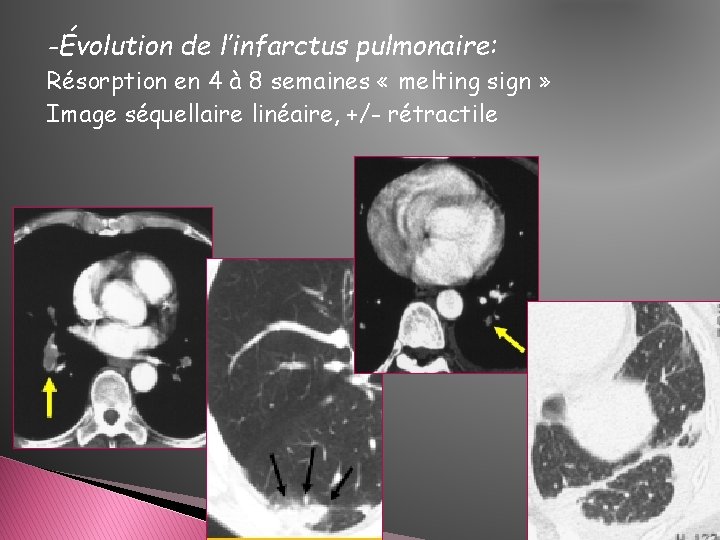
-Évolution de l’infarctus pulmonaire: Résorption en 4 à 8 semaines « melting sign » Image séquellaire linéaire, +/- rétractile
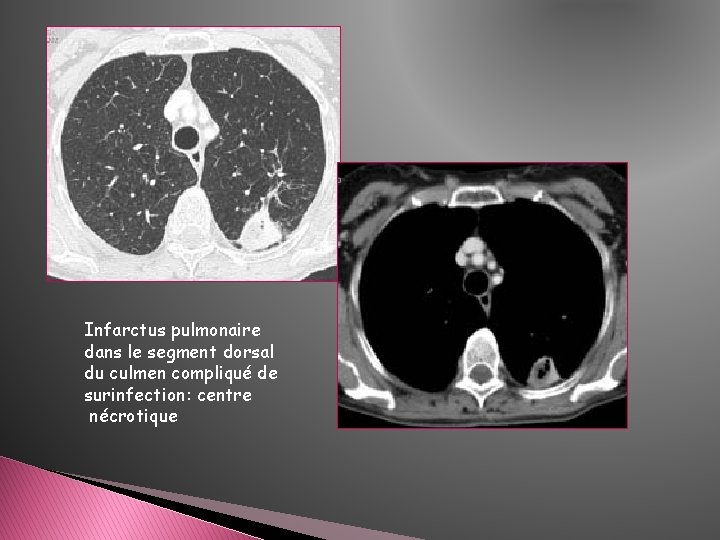
Infarctus pulmonaire dans le segment dorsal du culmen compliqué de surinfection: centre nécrotique

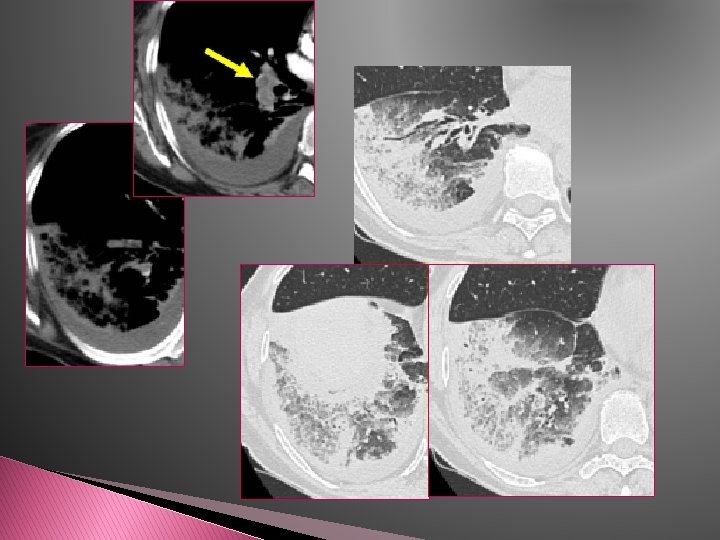
v Troubles de ventilation: -Atélectasie linéaire +/- Épanchement pleural -Hémorragie alvéolaire/alvéolite hémorragique : Image de verre dépoli aux alentours de l’infarctus pulmonaire
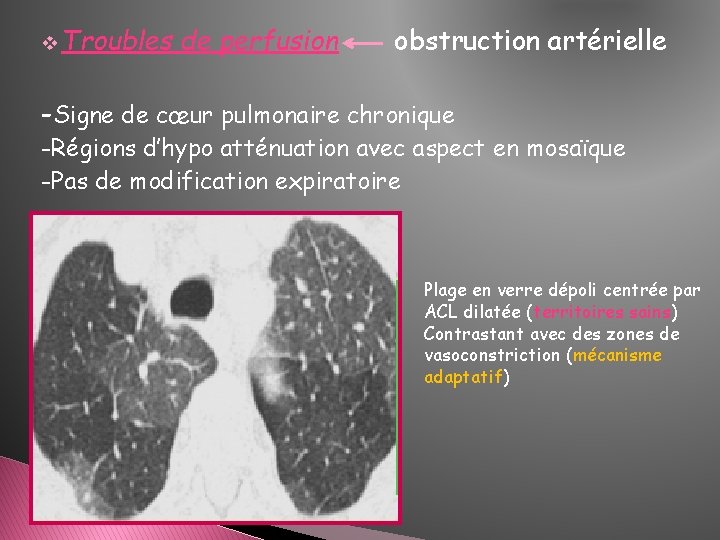
v Troubles de perfusion obstruction artérielle -Signe de cœur pulmonaire chronique -Régions d’hypo atténuation avec aspect en mosaïque -Pas de modification expiratoire Plage en verre dépoli centrée par ACL dilatée (territoires sains) Contrastant avec des zones de vasoconstriction (mécanisme adaptatif)
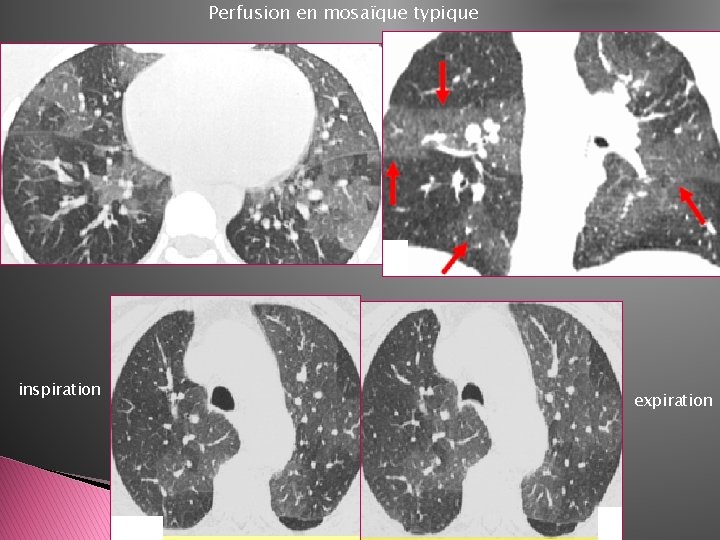
Perfusion en mosaïque typique inspiration expiration
RESULTATS: Signes directs Signes indirects Signes de retentissement

1 - Retentissement veineux d’amont -Dilatation veineuse juxta cardiaque: VCS, VCI, V AZ, VSH -Reflux cavo-sus-hépatique (IT fcl)
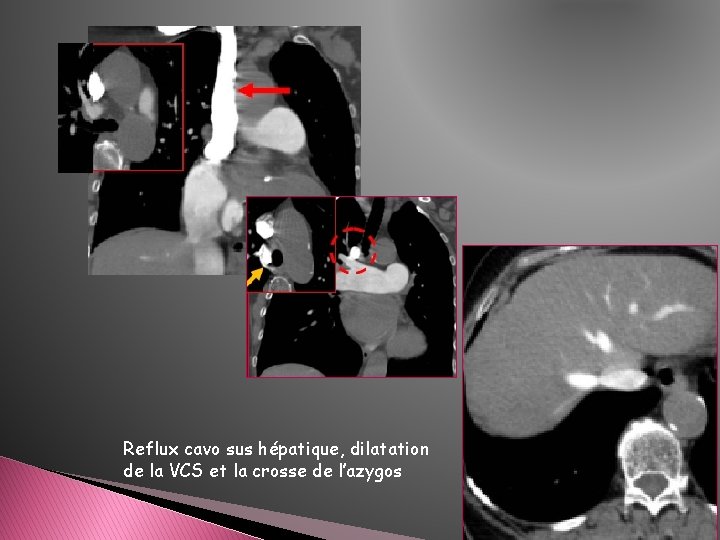
Reflux cavo sus hépatique, dilatation de la VCS et la crosse de l’azygos
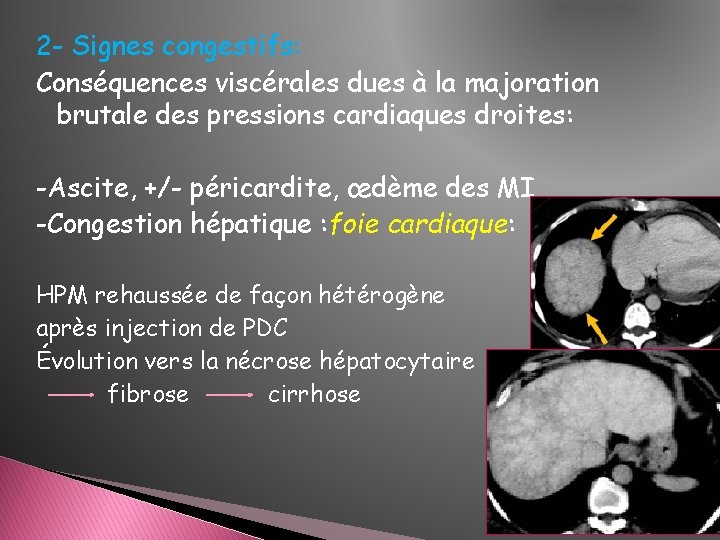
2 - Signes congestifs: Conséquences viscérales dues à la majoration brutale des pressions cardiaques droites: -Ascite, +/- péricardite, œdème des MI -Congestion hépatique : foie cardiaque: HPM rehaussée de façon hétérogène après injection de PDC Évolution vers la nécrose hépatocytaire fibrose cirrhose
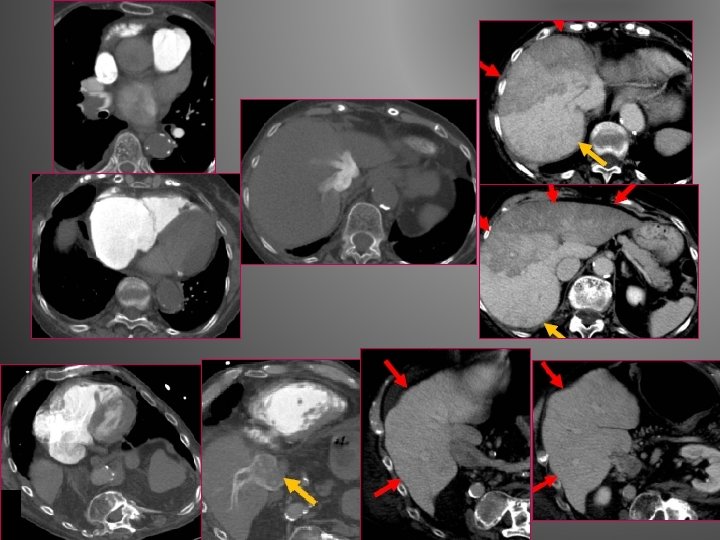

3 -Signes de souffrance ventriculaire droite -Dilatation atriale et/ou ventriculaire droite -Dysmorphie septale convexe vers le VG rectiligne, sigmoïde voire Cas d’examen synchronisé à l’ECG chiffrer la fonction globale des 2 ventricules voire recher des troubles de fonction segmentaire (dys/hypokinésie, akinésie)
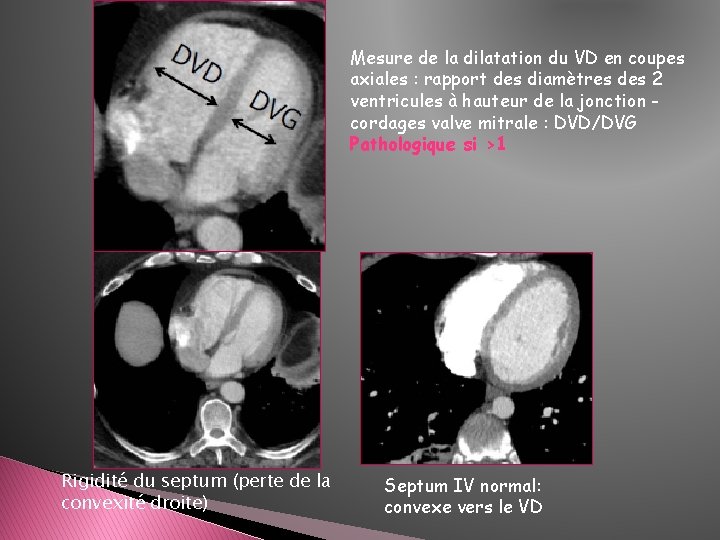
Mesure de la dilatation du VD en coupes axiales : rapport des diamètres des 2 ventricules à hauteur de la jonction cordages valve mitrale : DVD/DVG Pathologique si >1 Rigidité du septum (perte de la convexité droite) Septum IV normal: convexe vers le VD
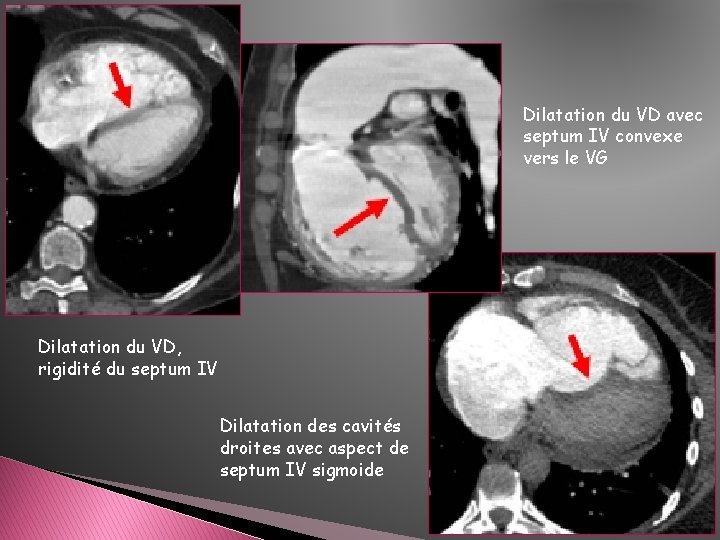
Dilatation du VD avec septum IV convexe vers le VG Dilatation du VD, rigidité du septum IV Dilatation des cavités droites avec aspect de septum IV sigmoide

4 - signes d’HTAP: Dilatation du tronc de l’AP >30 mm +/- signes d’insuffisance cardiaque

Pièges et difficultés d’interprétation +++ Facteurs patientsdépendants Facteurs techniques Facteurs anatomiques Facteurs pathologiques
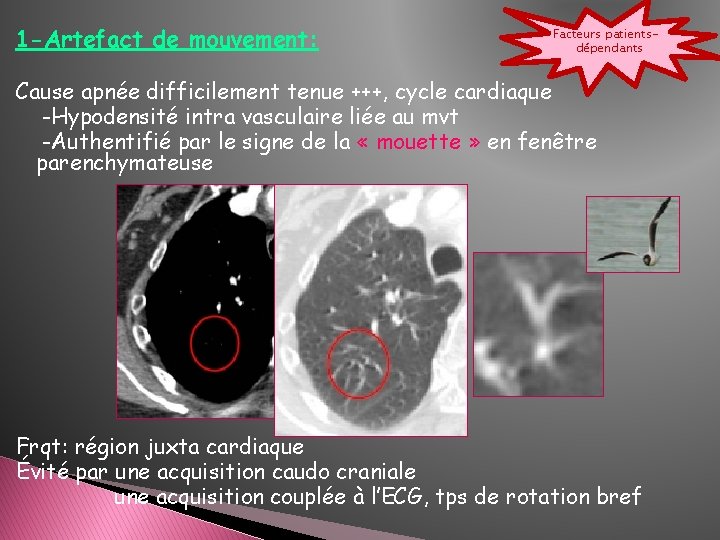
1 -Artefact de mouvement: Facteurs patientsdépendants Cause apnée difficilement tenue +++, cycle cardiaque -Hypodensité intra vasculaire liée au mvt -Authentifié par le signe de la « mouette » en fenêtre parenchymateuse Frqt: région juxta cardiaque Évité par une acquisition caudo craniale une acquisition couplée à l’ECG, tps de rotation bref
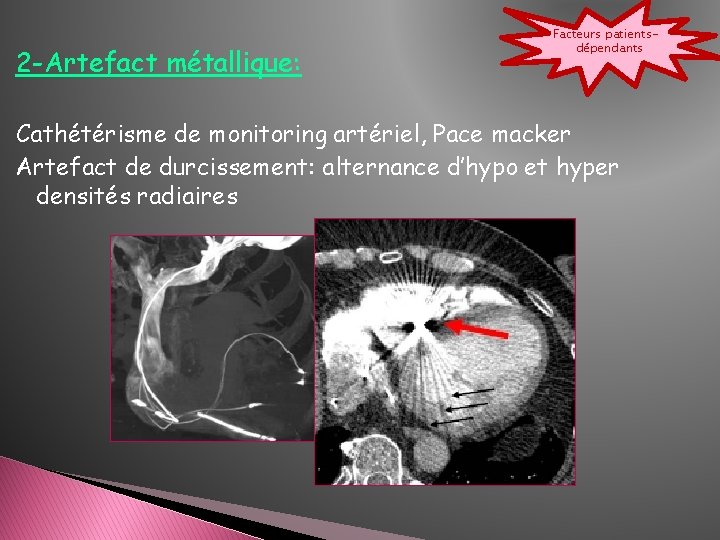
2 -Artefact métallique: Facteurs patientsdépendants Cathétérisme de monitoring artériel, Pace macker Artefact de durcissement: alternance d’hypo et hyper densités radiaires
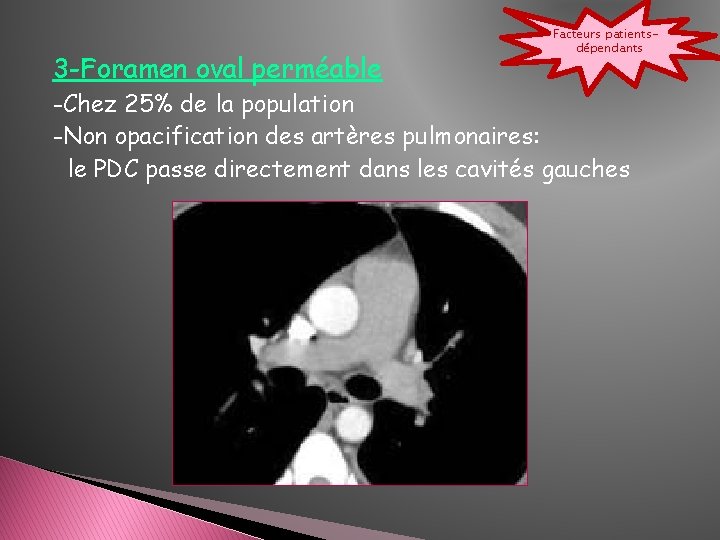
3 -Foramen oval perméable Facteurs patientsdépendants -Chez 25% de la population -Non opacification des artères pulmonaires: le PDC passe directement dans les cavités gauches
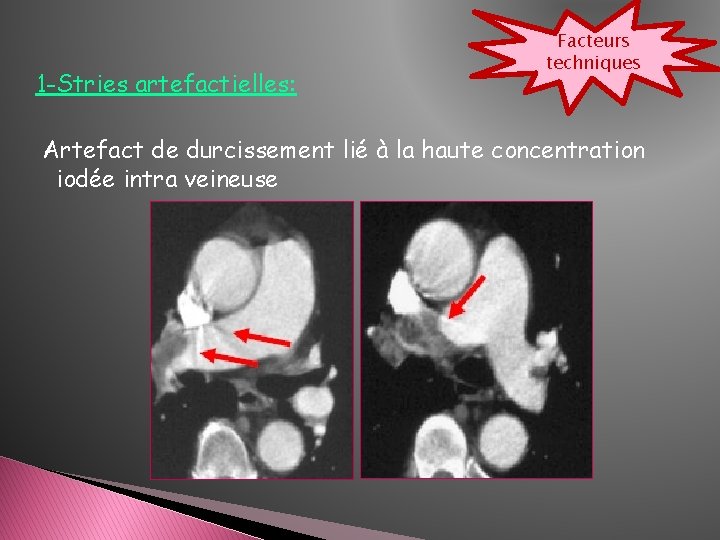
1 -Stries artefactielles: Facteurs techniques Artefact de durcissement lié à la haute concentration iodée intra veineuse
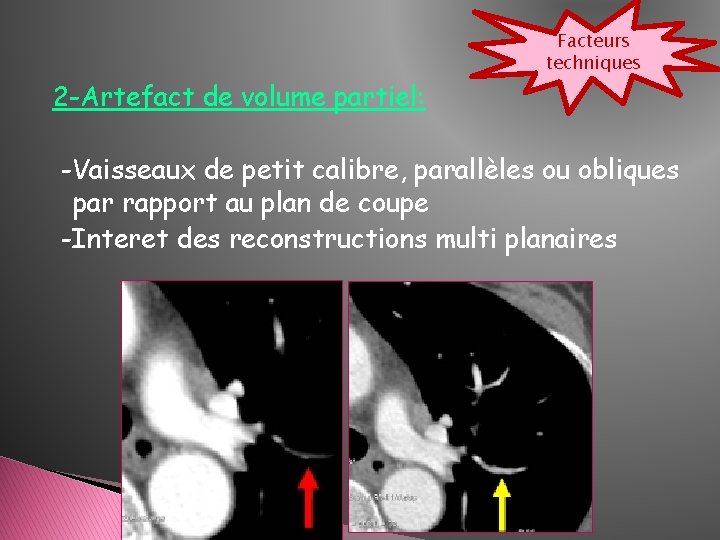
Facteurs techniques 2 -Artefact de volume partiel: -Vaisseaux de petit calibre, parallèles ou obliques par rapport au plan de coupe -Interet des reconstructions multi planaires
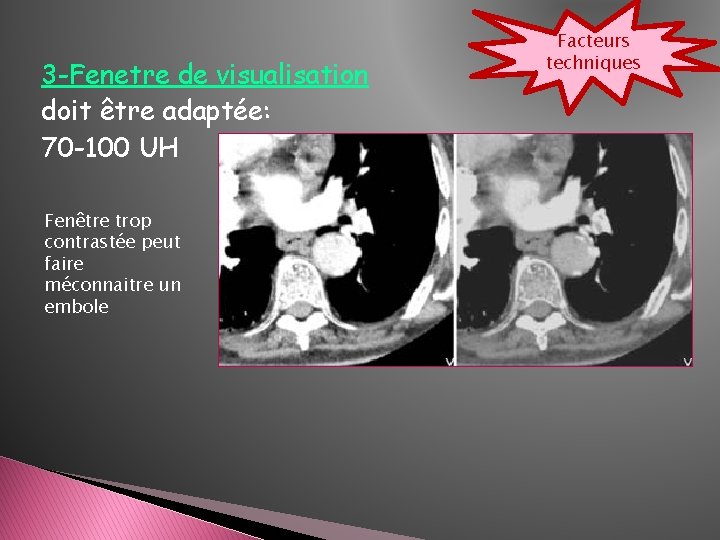
3 -Fenetre de visualisation doit être adaptée: 70 -100 UH Fenêtre trop contrastée peut faire méconnaitre un embole Facteurs techniques
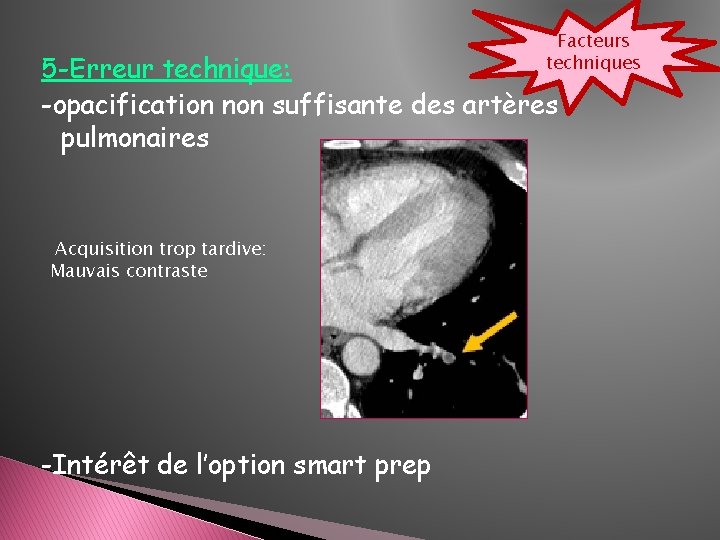
Facteurs techniques 5 -Erreur technique: -opacification non suffisante des artères pulmonaires Acquisition trop tardive: Mauvais contraste -Intérêt de l’option smart prep
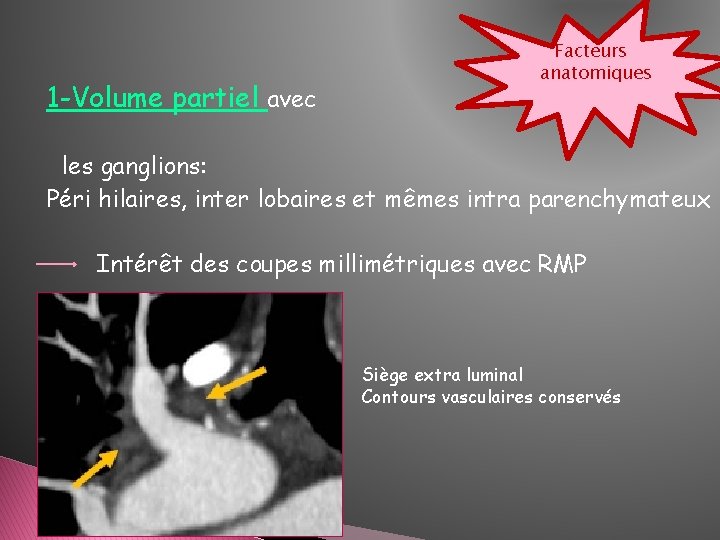
1 -Volume partiel avec Facteurs anatomiques les ganglions: Péri hilaires, inter lobaires et mêmes intra parenchymateux Intérêt des coupes millimétriques avec RMP Siège extra luminal Contours vasculaires conservés
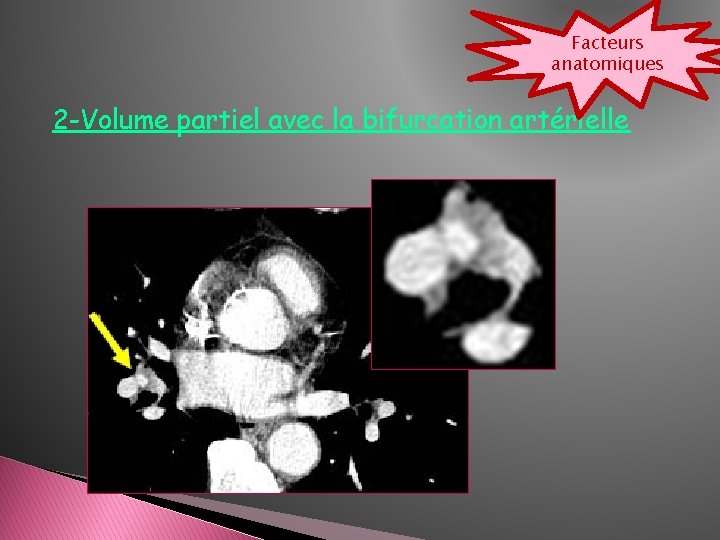
Facteurs anatomiques 2 -Volume partiel avec la bifurcation artérielle

Facteurs anatomiques 4 -Confusion entre les artères et les veines pulmonaires +++ Veines; absence de bronches contigües trajet convergeant vers l’auricule gauche
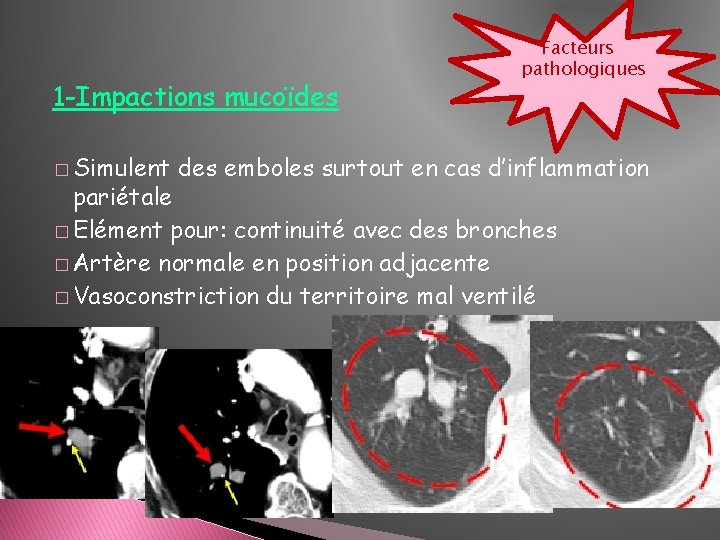
1 -Impactions mucoïdes � Simulent Facteurs pathologiques des emboles surtout en cas d’inflammation pariétale � Elément pour: continuité avec des bronches � Artère normale en position adjacente � Vasoconstriction du territoire mal ventilé
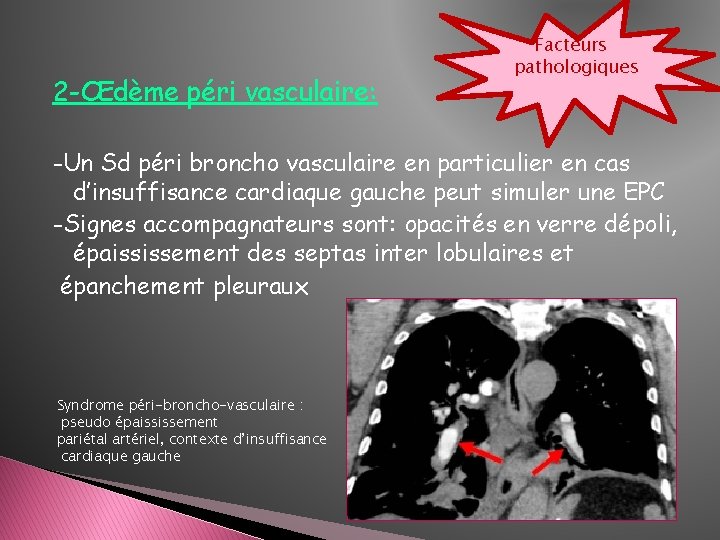
2 -Œdème péri vasculaire: Facteurs pathologiques -Un Sd péri broncho vasculaire en particulier en cas d’insuffisance cardiaque gauche peut simuler une EPC -Signes accompagnateurs sont: opacités en verre dépoli, épaississement des septas inter lobulaires et épanchement pleuraux Syndrome péri-broncho-vasculaire : pseudo épaississement pariétal artériel, contexte d’insuffisance cardiaque gauche
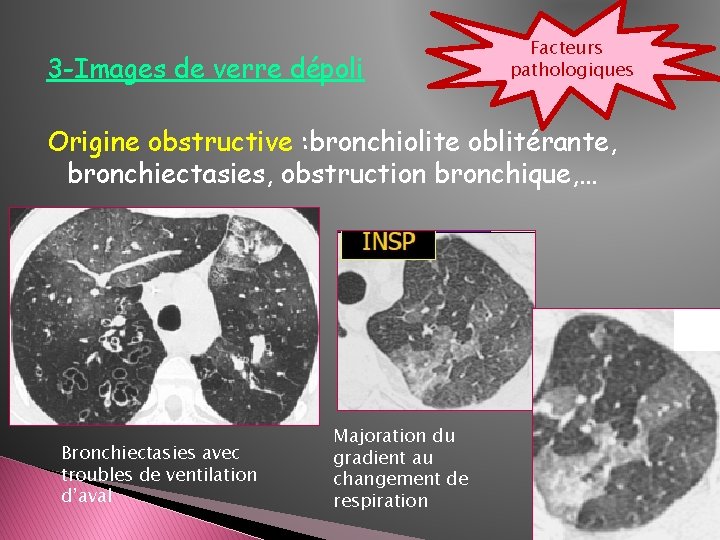
3 -Images de verre dépoli Facteurs pathologiques Origine obstructive : bronchiolite oblitérante, bronchiectasies, obstruction bronchique, … Bronchiectasies avec troubles de ventilation d’aval Majoration du gradient au changement de respiration

3 -Images de verre dépoli Facteurs pathologiques pathologie infiltrante interstitielle: protéinose alvéolaire, pneumopathie d’hypersensibilité

4 -Angiosarcome de l’artère pulmonaire: Facteurs pathologiques -Cause rare -Tableau identique à celui de l’EPA, ne disparait pas après TTT anticoagulant -Svt unilatéral, lobulé, rehaussé de façon hétérogène tardivement -Extension le long des axes vasculaires artériels -Extension trans murale vers le hile, médiastin et poumon
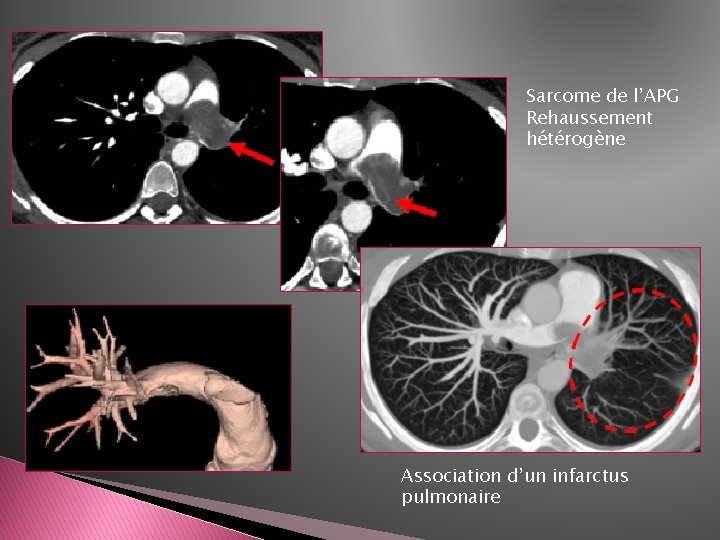
Sarcome de l’APG Rehaussement hétérogène Association d’un infarctus pulmonaire

3 -Scintigraphie ventilation/perfusion PRINCIPE: -Perfusion: images pulmonaires après injection d’une molécule radioactive Tech 99 m (6 incidences) tte interruption anatomique de la circulation defect -Ventilation: faire inhaler un aérosol marqué au Tech 99 m Recherche de mis match: zone non ou hyper perfusées et normalement ventilées Sensibilité mais non spécificité et Grande fréquence d’examens indeterminés

4 -Angio IRM -Séquence d’angio IRM ou ARM, combinaison des 2 -Plan: coronal -Intérêt: cas des CI à l’angioscanner, grossesse++ -Limite: durée d’examen/apnée gating cardiaque Angio IRM avec injection de Gado: -Séquence d’écho de gradient 3 D -Injection de Gado (0, 1 à 0, 2 mmol/kg) 5 -10 s début de l’acquisition

IRM de perfusion pulmonaire: � Utilisation de séquences avec temps d’écho court: Turbo flash images natives et avec soustraction � Estimation qualitative de la perfusion pulmonaire � Bonne concordance avec la scintigraphie pulmonaire de perfusion � Possibilité de mesure de courbe et de pourcentage de rehaussement

5 -Angiographie pulmonaire � Ancien examen de référence � Technique invasive � Plateau technique lourd � Thérapeutique éventuelle ++: thrombolyse, filtre cave � Permet: -Visualisation directe des emboles (temps artériel) -Appréciation fine des troubles de perfusion (temps parenchymateux) -Informations hémodynamiques (prise de pression)

6 - Echo cœur cas d’embolie pulmonaire grave: - Caillot intracardiaque et Signes de cœur pulmonaire aigu - Éliminer un diagnostic différentiel: Infarctus ventriculaire droit Tamponnade Dissection aortique
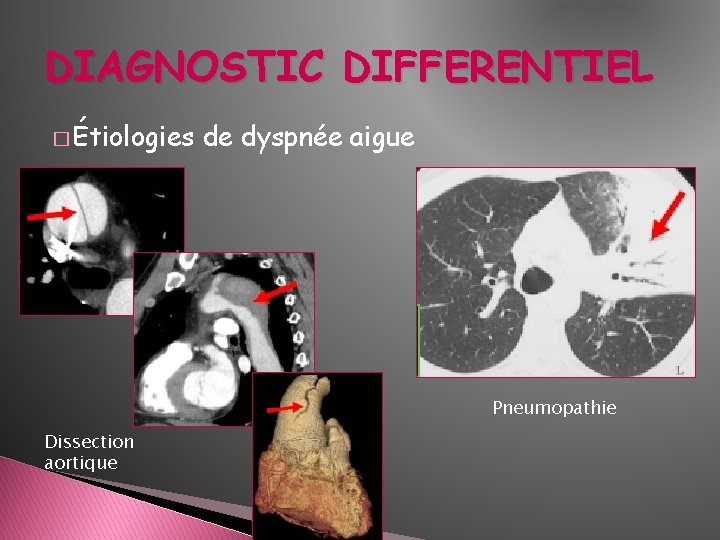
DIAGNOSTIC DIFFERENTIEL � Étiologies de dyspnée aigue Pneumopathie Dissection aortique
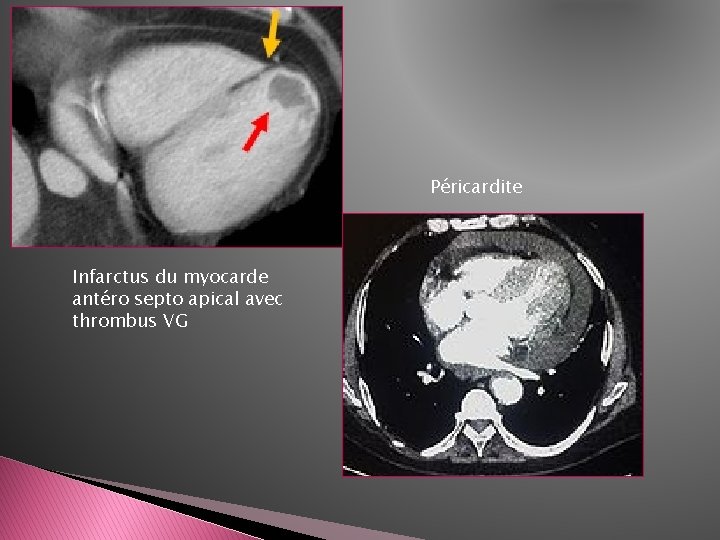
Péricardite Infarctus du myocarde antéro septo apical avec thrombus VG

DIAGNOSTIC ÉTIOLOGIQUE
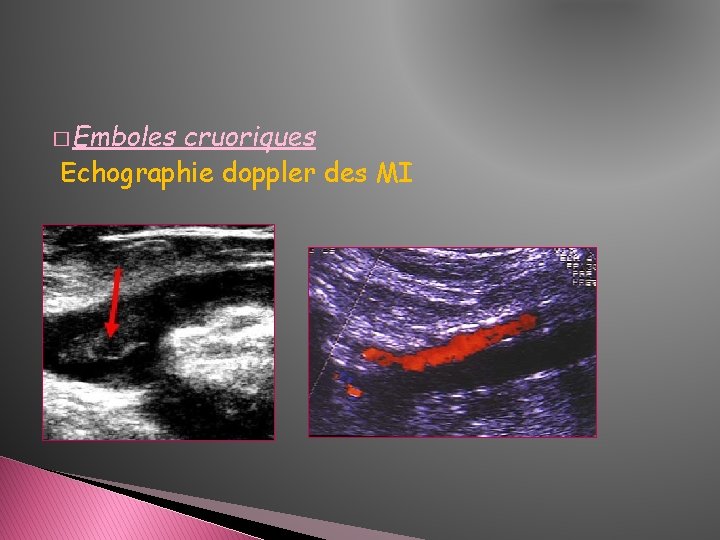
� Emboles cruoriques Echographie doppler des MI
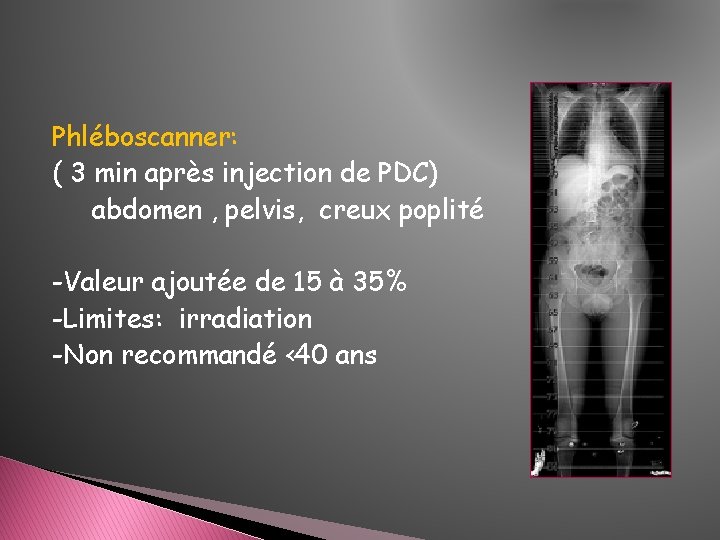
Phléboscanner: ( 3 min après injection de PDC) abdomen , pelvis, creux poplité -Valeur ajoutée de 15 à 35% -Limites: irradiation -Non recommandé <40 ans
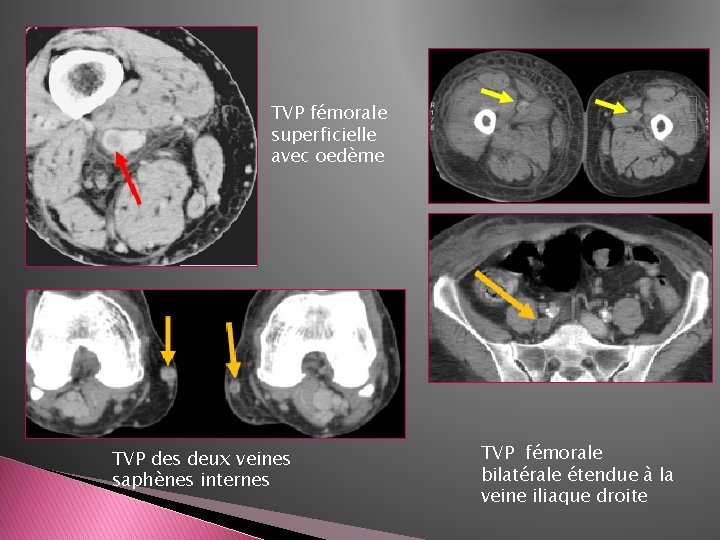
TVP fémorale superficielle avec oedème TVP des deux veines saphènes internes TVP fémorale bilatérale étendue à la veine iliaque droite

� Emboles tumoraux: -Le plus svt embolie périphérique sous segmentaire -Plus rarement EPA proximale (envahissement cave inférieur de CHC, d’ADK rénal ou de chorio carcinome) -Rehaussé par le PDC
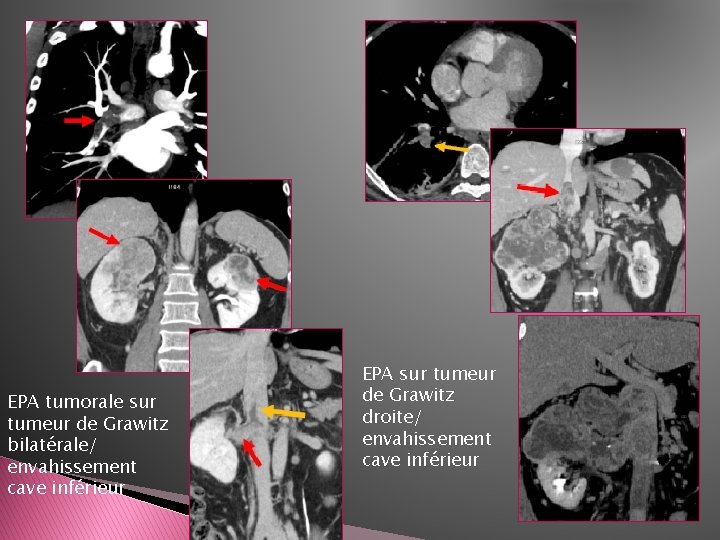
EPA tumorale sur tumeur de Grawitz bilatérale/ envahissement cave inférieur EPA sur tumeur de Grawitz droite/ envahissement cave inférieur
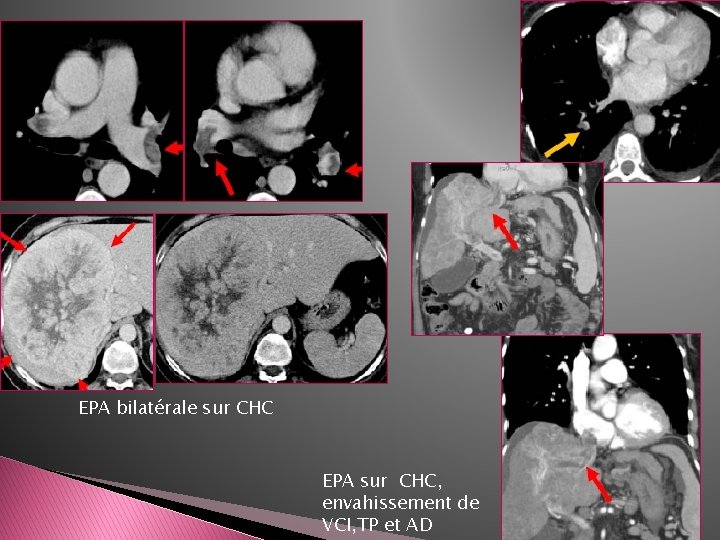
EPA bilatérale sur CHC EPA sur CHC, envahissement de VCI, TP et AD

EVOLUTION

EVOLUTION � Dans 0, 1 à 0, 4% des cas embolie pulmonaire chronique = cœur pulmonaire chronique post embolique Absence de résorption des caillots � Echo cœur HTAP, retentissement sur les cavités cardiaques, insuffisance tricuspidienne et shunt droit gauche par réouverture du foramen ovale � Angio scanner +++ éléments sémiologiques
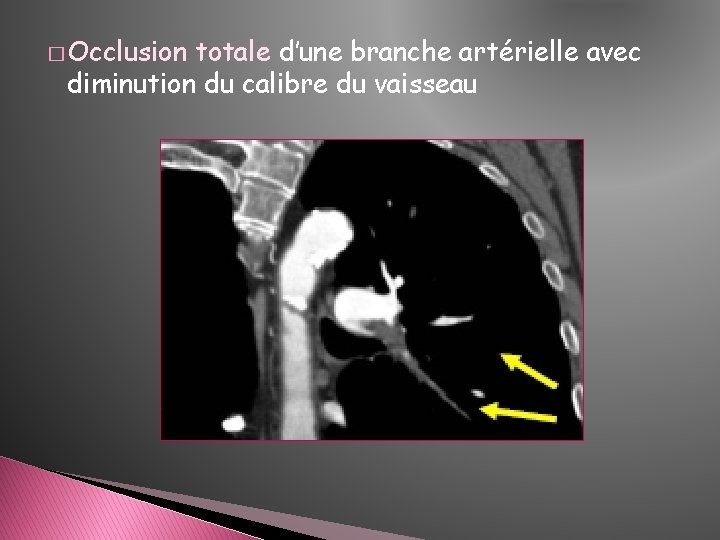
� Occlusion totale d’une branche artérielle avec diminution du calibre du vaisseau
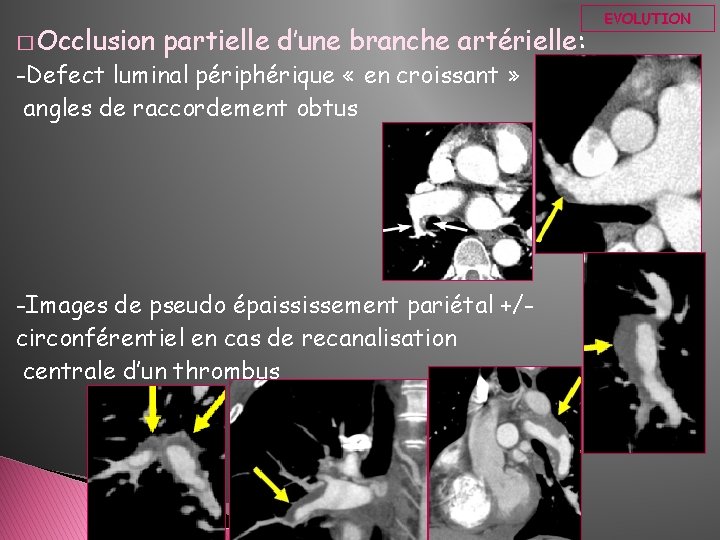
� Occlusion partielle d’une branche artérielle: -Defect luminal périphérique « en croissant » angles de raccordement obtus -Images de pseudo épaississement pariétal +/circonférentiel en cas de recanalisation centrale d’un thrombus EVOLUTION
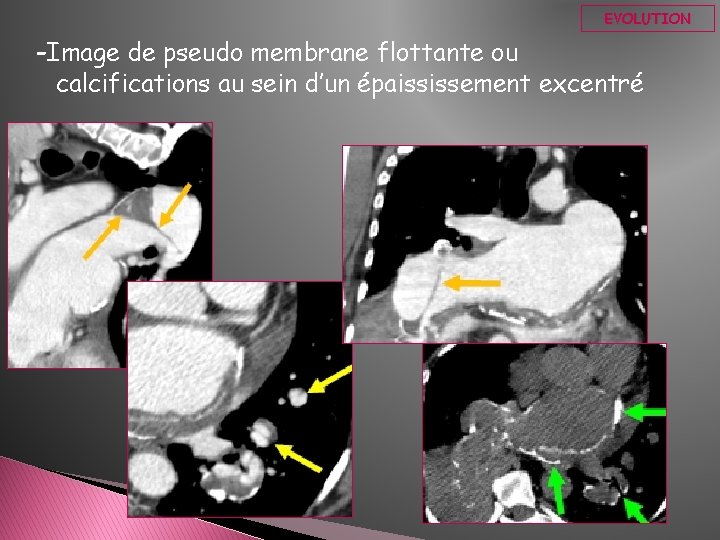
EVOLUTION -Image de pseudo membrane flottante ou calcifications au sein d’un épaississement excentré
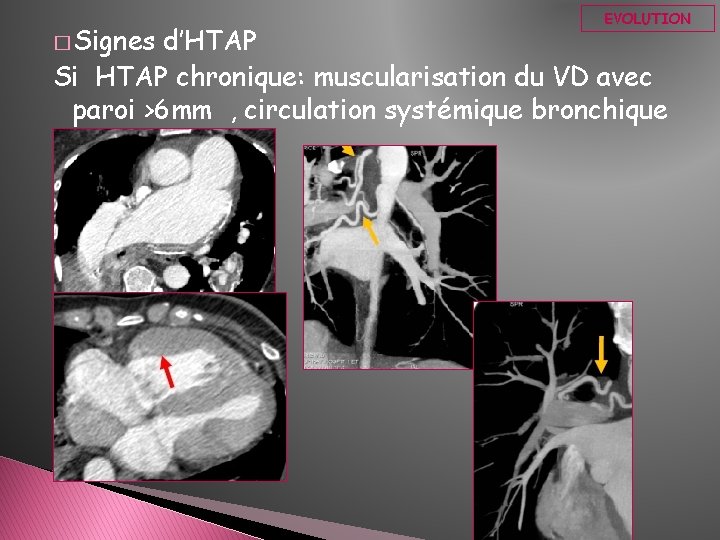
� Signes EVOLUTION d’HTAP Si HTAP chronique: muscularisation du VD avec paroi >6 mm , circulation systémique bronchique

STRATEGIE DIAGNOSTQUE
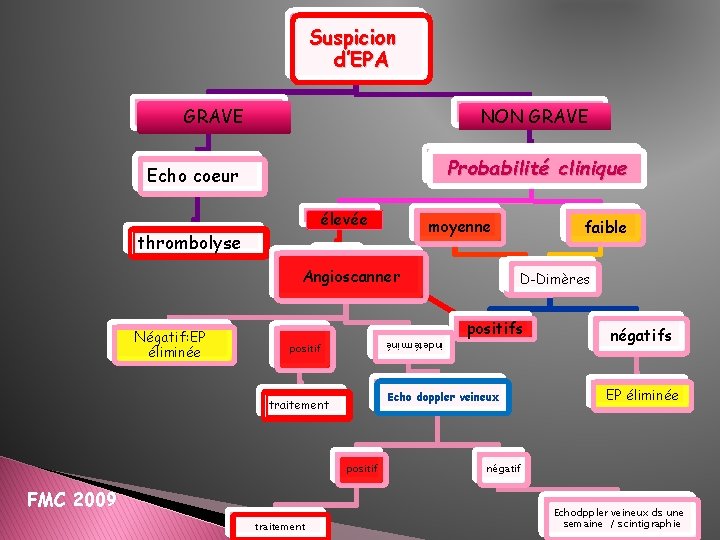
Suspicion d’EPA NON GRAVE Probabilité clinique Echo coeur élevée thrombolyse moyenne Angioscanner indetérminé Négatif: EP éliminée positif traitement D-Dimères positifs Echo doppler veineux traitement FMC 2009 faible négatifs EP éliminée négatif Echodppler veineux ds une semaine / scintigraphie

TRAITEMENT � EPA non grave: Héparinothérapie avec relais précoce avec AVK � EPA grave: Thrombolyse (contre – indications) embolectomie chirurgicale si CI à la thrombolyse Filtre cave inférieur: EPA non grave +CI aux anticoagulants Récidive d’EPA malgré un TTT bien conduit EPC

CONCLUSION � Le diagnostic de l’embolie pulmonaire repose sur une probabilité clinique et sur l’angioscanner: examen de choix dans l’étude des artères pulmonaires � Intérêt risque de la prévention en cas de facteurs de

MERCI
- Slides: 89