Elettrochimica Elettrochimica Lelettrochimica una branca della chimica che

Elettrochimica

Elettrochimica L’elettrochimica è una branca della chimica che studia le trasformazioni chimiche avvengono in un sistema in concomitanza con il passaggio di cariche elettriche esternamente al sistema. Tale passaggio può essere spontaneo (corrente elettrica generata dal sistema in esame) ovvero indotto dall’esterno. Nei processi elettrochimici l’energia chimica viene convertita in energia elettrica (invece che, ad esempio, in energia termica) o viceversa.

Reazioni di Ossido-riduzione • Le reazioni di ossido-riduzione generano un flusso di elettroni. • La reazione di Ossidazione libera elettroni • La reazione di Riduzione cattura elettroni

Applicazioni Il movimento di elettroni genera corrente elettrica. • 6 H++2 Mn. O 4 -+ 5 H 2 O 2 ® 2 Mn 2+ + 5 O 2 +8 H 2 O Scrivendo in due semireazioni avremo: • 2(8 H++Mn. O 4 -+5 e- ® Mn 2+ +4 H 2 O) • 5 ( H 2 O 2 ® O 2 + 2 e- + 2 H+ ) Nella stessa soluzione le due semireazioni non producono lavoro, ma se le semireazioni avvenissero in due soluzioni separate ……
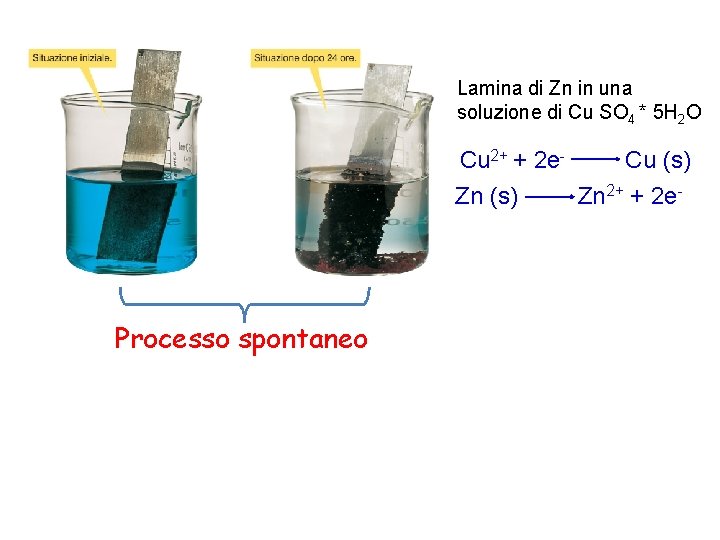
Lamina di Zn in una soluzione di Cu SO 4 * 5 H 2 O Cu 2+ + 2 e. Cu (s) Zn 2+ + 2 e- Processo spontaneo

Cosa succede se invece mettiamo una lamina di Cu in una soluzione di Zn. SO 4? Non si osserva nessun processo A dimostrazione del fatto che per far avvenire spontaneamente un processo redox, le specie devono essere scelte opportunamente. Questo dato sperimentale ci indica che: Potere ossid. della coppia Cu 2+/Cu > potere ossid. della coppia Zn 2+/Zn
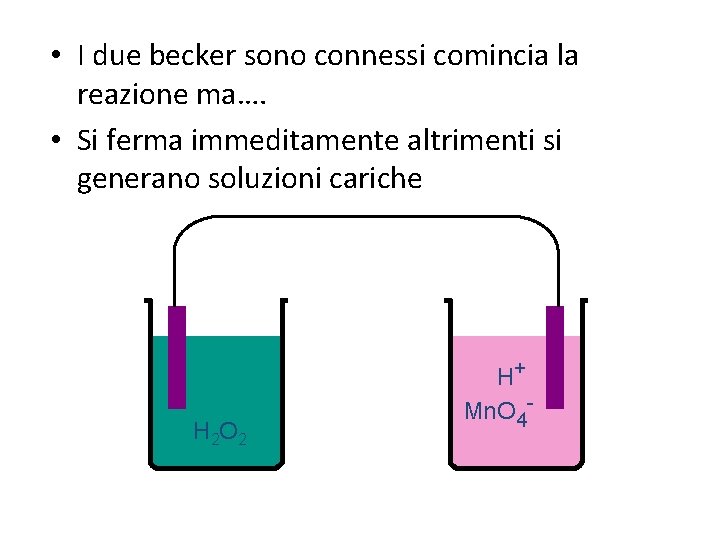
• I due becker sono connessi comincia la reazione ma…. • Si ferma immeditamente altrimenti si generano soluzioni cariche H 2 O 2 H+ Mn. O 4 -
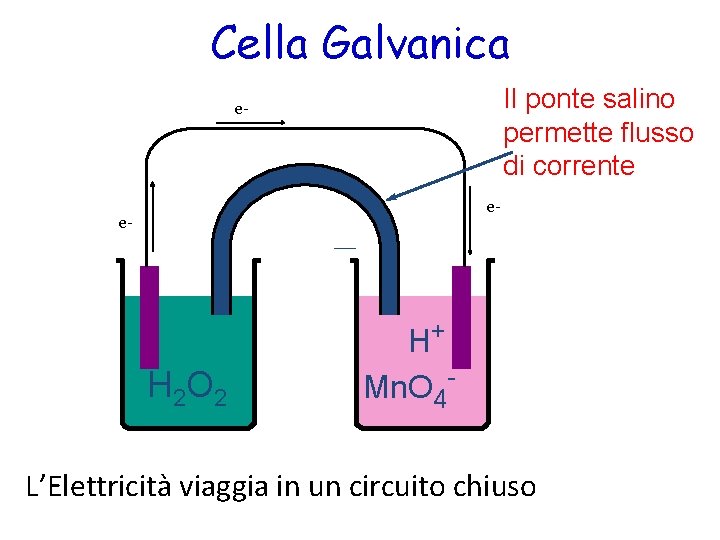
Cella Galvanica Il ponte salino permette flusso di corrente e- e- e- H 2 O 2 H+ Mn. O 4 - L’Elettricità viaggia in un circuito chiuso
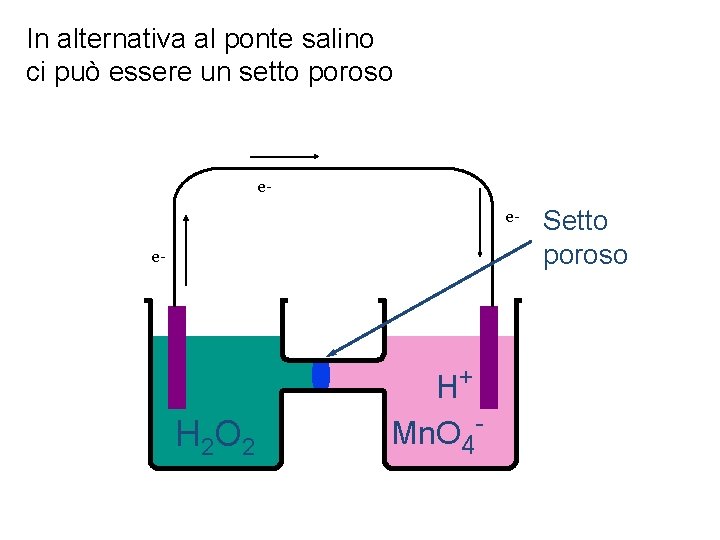
In alternativa al ponte salino ci può essere un setto poroso eee- H 2 O 2 H+ Mn. O 4 - Setto poroso

Pila Daniel Zn (s) | Zn 2+ || Cu 2+ | Cu (s) una pila è costituita da due semi-celle: in ciascuna semi-cella è presente un elemento chimico in due stati di ossidazione diversi (coppia red-ox) A circuito interrotto, il voltmetro misura una differenza di potenziale elettrico tra le due semicelle ( E). Se il circuito viene chiuso: gli elettroni che si liberano dal processo di ossidazione dello zinco fluiranno all’elettrodo dell’altra semicella dove si verificherà la riduzione degli ioni rame a rame metallico.

Notazione lineare solido½Acquoso½solido Anodo a sinistra½½Catodo a destra Fasi differente linea singola. Setto poroso o ponte salino doppia linea. Se tutte le specie sono in soluzione in una delle due semicelle allora c’è un elettrodo inerte ad esempio di Platino • Per esempio Cu(s)½Cu 2+ (aq)½½Fe 2+ (aq), Fe 3+(aq)½Pt(s) • • •

Il Potenziale elettrico E’ in un punto il valore dell'energia potenziale elettrica rilevato da una carica elettrica positiva di prova posta in quel punto per unità di carica. Ossia …. il lavoro che deve compiere una forza dovuta al campo elettrico per spostare una o più cariche da quel punto fino all'infinito (ove si assume potenziale nullo).

Potenziale della Cella • La specie che si ossida libera elettroni. • La specie che si riduce acquista elettroni. • Queste azioni generano una differenza di potenziale della cella Ecella (anche chiamata forza elettromotrice (fem) • Ecella = lavoro /carica • Unità di misura del potenziale è il volt(V) • Un volt = 1 joule/coulomb
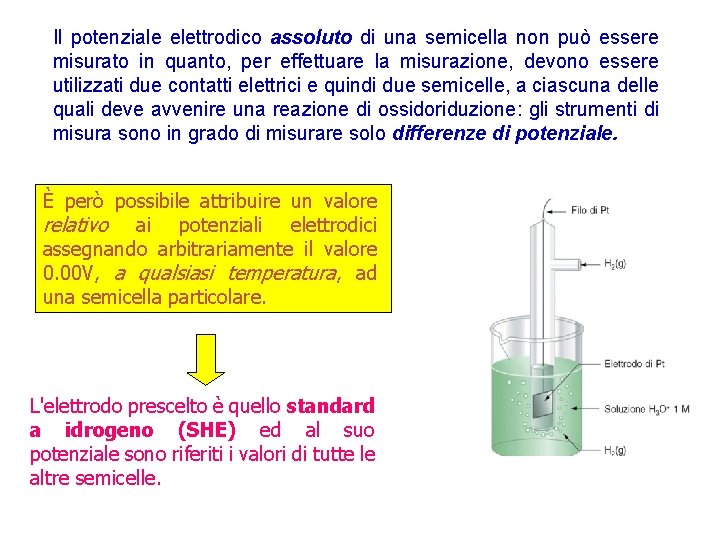
Il potenziale elettrodico assoluto di una semicella non può essere misurato in quanto, per effettuare la misurazione, devono essere utilizzati due contatti elettrici e quindi due semicelle, a ciascuna delle quali deve avvenire una reazione di ossidoriduzione: gli strumenti di misura sono in grado di misurare solo differenze di potenziale. È però possibile attribuire un valore relativo ai potenziali elettrodici assegnando arbitrariamente il valore 0. 00 V, a qualsiasi temperatura, ad una semicella particolare. L'elettrodo prescelto è quello standard a idrogeno (SHE) ed al suo potenziale sono riferiti i valori di tutte le altre semicelle.
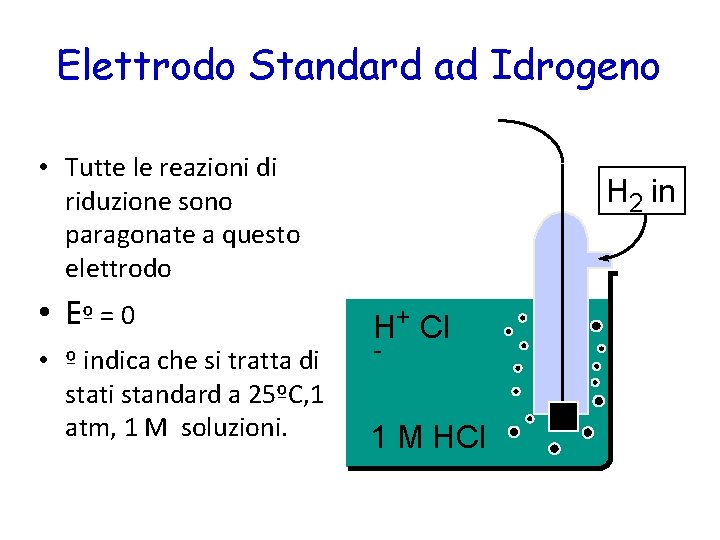
Elettrodo Standard ad Idrogeno • Tutte le reazioni di riduzione sono paragonate a questo elettrodo • Eº = 0 • º indica che si tratta di stati standard a 25ºC, 1 atm, 1 M soluzioni. H 2 in H+ Cl - 1 M HCl

L'assegnazione del valore 0. 000 V al potenziale standard dell'elettrodo standard a idrogeno è arbitraria, ma consente di definire una serie elettrochimica di potenziali elettrodici standard relativi. Questi possono essere usati nei calcoli. Per assegnare il potenziale ad una certa semicella, M/Mn+, si costruisce una cella elettrochimica formata da un elettrodo standard a idrogeno e dalla semicella in esame, e se ne misura la differenza di potenziale, Ecella Per una qualsiasi cella galvanica è possibile calcolare il potenziale standard della come somma dei potenziali di ossidazione e di riduzione secondo la relazione: Ecella = E° oss + E° rid
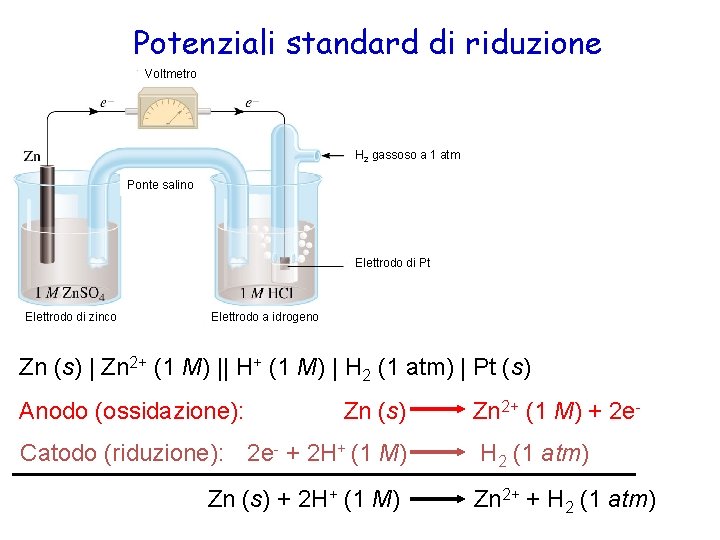
Potenziali standard di riduzione Voltmetro H 2 gassoso a 1 atm Ponte salino Elettrodo di Pt Elettrodo di zinco Elettrodo a idrogeno Zn (s) | Zn 2+ (1 M) || H+ (1 M) | H 2 (1 atm) | Pt (s) Anodo (ossidazione): Zn (s) Catodo (riduzione): 2 e- + 2 H+ (1 M) Zn (s) + 2 H+ (1 M) Zn 2+ (1 M) + 2 e. H 2 (1 atm) Zn 2+ + H 2 (1 atm)

• E 0 si riferisce alla reazione così come scritta • Più E 0 è positivo, maggiore è la tendenza della sostanza ad essere ridotta • Le reazioni di semicella sono reversibili • Il segno di E 0 cambia quando è invertita la reazione • Variando i coefficienti stechiometrici di una reazione di semicella non si modifica il valore di E 0
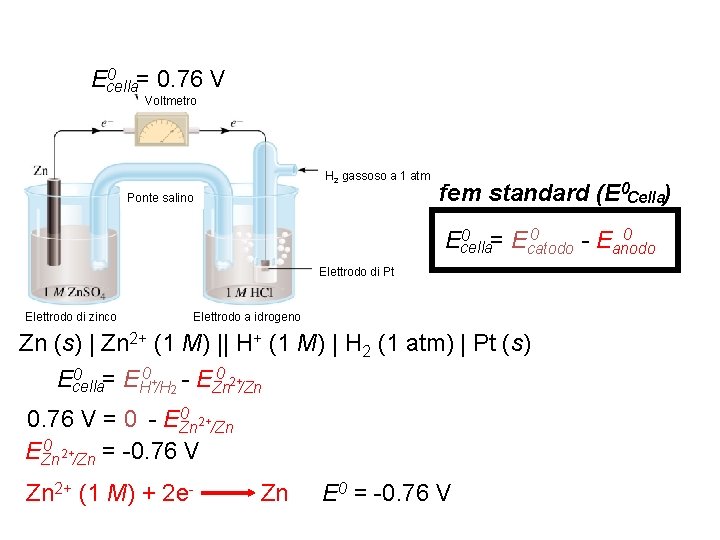
0 = 0. 76 V Ecella Voltmetro H 2 gassoso a 1 atm Ponte salino fem standard (E 0 Cella) 0 0 = E 0 Ecella catodo - Eanodo Elettrodo di Pt Elettrodo di zinco Elettrodo a idrogeno Zn (s) | Zn 2+ (1 M) || H+ (1 M) | H 2 (1 atm) | Pt (s) 0 = E 0 + - E 0 2+ Ecella H /H 2 Zn /Zn 0 2+ 0. 76 V = 0 - EZn /Zn 0 2+ EZn /Zn = -0. 76 V Zn 2+ (1 M) + 2 e- Zn E 0 = -0. 76 V

Potenziali standard di riduzione 0 = 0. 34 V Ecella Voltmetro 0 0 = E 0 Ecella catodo - Eanodo 0 0 0 2+/Cu – EH +/H Ecella = ECu 2 H 2 gassoso a 1 atm 0 2+ 0. 34 = ECu /Cu - 0 Ponte salino 0 2+ ECu /Cu = 0. 34 V Elettrodo a idrogeno Elettrodo di rame Pt (s) | H 2 (1 atm) | H+ (1 M) || Cu 2+ (1 M) | Cu (s) Anodo (ossidazione): Catodo (riduzione): H 2 (1 atm) 2 e- + Cu 2+ (1 M) H 2 (1 atm) + Cu 2+ (1 M) 2 H+ (1 M) + 2 e. Cu (s) + 2 H+ (1 M)

Pila a secco - Pila Leclanché Spaziatore di carta Pasta umida di Zn. Cl 2 e NH 4 Cl Strato di Mn. O 2 Catodo di grafite Anodo: Zn 2+ + 2 e. Catodo: 1° 2 NH 4 Cl + 2 e- H 2 + 2 NH 3 +2 Cl. Catodo: 2° 2 Mn. O 2 + H 2 + 2 e- Mn 2 O 3 + H 2 O Anodo di zinco Pila alcalina Anodo: Zn + 2 OH- Zn(OH)2 + 2 e. Catodo: +2 e- +2 Mn. O 2 + 2 H 2 O 2 Mn. O(OH) + 2 OH-

Batterie sono Celle Galvaniche Batteria al piombo Batteria Nichel-Cadmio 2 H 2 SO 4 +Pb + Pb. O 2 2 Pb 2+ + 2 SO 42 - + 2 H 2 O 2 Ni. O(OH) + Cd + 2 H 2 O Cd(OH)2 + 2 Ni(OH)2

Batterie al Litio Le batterie al litio sono superiori alle altre batterie in commercio perché hanno: 1. una d. d. p. elevata fra gli elettrodi (3, 5– 4, 5 V); 2. un’elevata densità di energia (150 Wh/kg); 3. un numero elevato di cicli di rica/scarica (circa 500); 4. un voltaggio che rimane costante durante il funzionamento degli apparecchi che le utilizzano.

Cella Galvanica • • 1) 2) 3) 4) Le reazioni si svolgono spontaneamente sempre nella direzione che produce un potenziale positivo della cella. Per una completa descrizione di una cella bisogna: Determinare il Potenziale della cella Determinare la direzione del flusso di elettroni Designare l’anodo e il catodo Natura di tutti i componenti elettrodi e ioni
Definizione del G G Fornisce la direzione del processo Fornisce il massimo lavoro utilizzabile di un processo

Energia di Gibbs e Spontaneità n n n G < 0 - la reazione di definisce esoergonica e procede spontaneamente nella direzione in cui è scritta, ossia da sinistra a destra G > 0 - la reazione si definisce endoergonica e procede spontaneamente nella direzione opposta. G = 0 - la reazione è all'equilibrio

Potenziale della Cella • La specie che si ossida libera elettroni. • La specie che si riduce acquista elettroni. • Queste azioni generano una differenza di potenziale della cella Ecella (anche chiamata forza elettromotrice (fem) • Ecella = lavoro /carica • Unità di misura del potenziale è il volt(V) • Un volt = 1 joule/coulomb

Potenziale Lavoro e G • F. e. m. = potenziale (V) = lavoro (J) / Carica(C) • E = lavoro compiuto dal sistema/Carica • E = -w/q w = -q. E • Una mole di elettroni avrà una carica 96485 C q = 1, 602*10 -19 x 6, 022*1023 = 96485 C/mol e 96485 C = 1 Faraday • q = n. F = moli di e- x carica/mole e • w = -q. E = -n. FE = G

Lavoro elettrico e lavoro chimico ΔG = − n. FΔE Il lavoro elettrico è uguale al prodotto del numero di elettroni messi in gioco (n) per la carica di un numero di Avogadro di elettroni (F) per la forza elettromotrice della pila (DE).

Potenziale Lavoro e G G° = -n. F E° Se: DG° < 0 DG° > 0 DE° < 0 processo spontaneo processo non spontaneo Quindi quando il potenziale è negativo vuol dire che quel processo non è spontaneo nel verso in cui è scritto, ma è spontaneo il processo inverso.

Qual’ è la fem standard di una cella elettrochimica costituita da un elettrodo di Cd in una soluzione 1. 0 M di Cd(NO 3)2 e un elettrodo di Cr in una soluzione 1. 0 M di Cr(NO 3)3? Cd 2+ (aq) + 2 e- Cd (s) E 0 = -0. 40 V Cd è un ossidante più forte Cr 3+ (aq) + 3 e- Cr (s) Anodo (ossidazione): Catodo (riduzione): E 0 = -0. 74 V Cd ossiderà Cr Cr 3+ (1 M) + 3 e- x 2 Cr (s) 2 e- + Cd 2+ (1 M) 2 Cr (s) + 3 Cd 2+ (1 M) Cd (s) x 3 3 Cd (s) + 2 Cr 3+ (1 M) 0 0 = E 0 Ecella catodo - Eanodo 0 = -0. 40 – (-0. 74) Ecella 0 = 0. 34 V Ecella

la ‘propensione’ di un elemento a ridursi è quantificata dalla grandezza potenziale standard di riduzione E° (volt ) Cu 2+ + 2 e- = Cu Zn 2+ + 2 e- = Zn E° = 0. 342 volt E° = - 0. 762 volt la propensione del rame a ridursi è maggiore della propensione dello zinco a ridursi, e così Zn + Cu 2+ = Zn 2+ + Cu = Zn + Cu 2+ E°= 1. 1 V la reazione è spontanea E°= - 1. 1 V la reazione non è spontanea Esercizio: Vogliamo sapere se la reazione che segue è spontanea oppure no 5 Fe 3+ + Mn 2+ + 4 H 2 O = Mn. O 4 - + 5 Fe 2+ + 8 H+ E°Mn. O 4 -/Mn 2+ = 1. 51 V; E° F 3+/Fe 2+ = 0. 771 V

Nello stato standard: G° = -n. F E° Tuttavia nel mondo reale le celle elettrochimiche raramente operano nello stato standard. Anche se la cella è costruita utilizzando tutte le specie a concentrazione 1 M, nel corso della reazione le concentrazioni di reagent e prodotti cambiano. Le variazioni di concentrazione, così come anche la variazione di temperature, influenzano il potenziale della cella. In condizioni non standard si ricorre “all’equazione di Nerst” ovvero un’equazione in cui il lavoro elettrico dipende anche dalla concentrazione di prodotti e reagent e dalla temperatura.

Equazione di Nernst Per una soluzione lo stato non standard è: G = G° + RT ln. Q Sostituendo: G = -n. FEcella G 0 = -n. FE°cella -n. FE = -n. FE° + RT ln. Q cambiando il segno e dividend tutto per n. F E= E 0 E = E 0 - RT ln Q n. F 0. 0257 n 0. 0592 n ln Q log Q t = 298 K R= 8, 314 J·K-1 mol-1 ln = 2. 303 log

E (fem) è la differenza dei potenziali di riduzione relativi a ciascuna semireazione, è una quantità sempre positiva e misura la tendenza della reazione red-ox ad avvenire Cu 2+ + Zn = Cu + Zn 2+ Ox 1 + Red 2 = Red 1 + Ox 2 f. e. m. = E = E° - 0. 0592 log [Ox 2] [Red 1] 2 [Ox 1] [Red 2] E semicella 1 - E semicella 2 Esemicella 1 = E° 1 - 0. 0592 log [Red 1] 2 [Ox 1] Esemicella 2 = E° 2 - 0. 0592 log [Red 2] 2 [Ox 2]

Una pila è capace di erogare corrente continua con una differenza di potenziale che, via che la pila funziona, decresce fino diventare pari a zero. A questo punto la reazione che alimenta la pila (ad es. ) Zn + Cu 2+ = Zn 2+ + Cu è all’equilibrio, nel senso che non ha più alcuna tendenza a spostarsi in un senso o nell’altro. Quindi E = 0 e Q= Keq. Sostituendo nell’equazione di Nerst si ha: E = 0 = E° - 0. 0592 log Keq 2 Keq = Quindi E° = 0. 059 log Keq 2 E’ possibile determinare il valore della costante di equilibrio Keq = 10 (2 E°/0. 059) = 2. 0 x 1037 [Zn 2+] [Cu 2+]

Corrosione • Ruggine – spontaneo processo di ossidazione. • I metalli che hanno potenziali di riduzione meno positivi dell’ O 2 subiscono l’ossidazione all’atmosfera. • Fe ® Fe 2+ +2 e • O 2 + 2 H 2 O + 4 e- ® 4 OH- E°= 0. 44 V E°= 0. 40 V • Fe 2+ + O 2 + H 2 O ® Fe 2 O 3 + H+ • Reazione avviene in due tempi.


Elettrolisi • E’ possibile far svolgere un processo non spontaneo? • Si!! • Inserendo nel circuito un generatore di corrente ad un voltaggio più elevato del potenziale della cella. In questo modo si inverte la direzione del flusso di elettroni nella reazione redox.
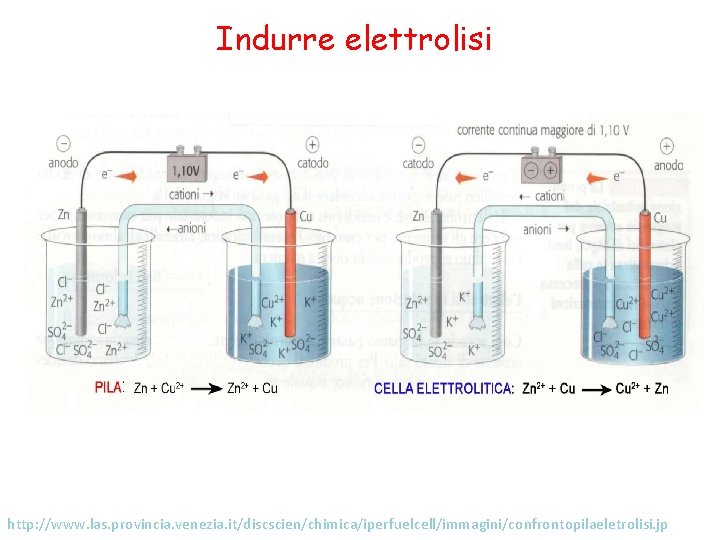
Indurre elettrolisi http: //www. las. provincia. venezia. it/discscien/chimica/iperfuelcell/immagini/confrontopilaeletrolisi. jp
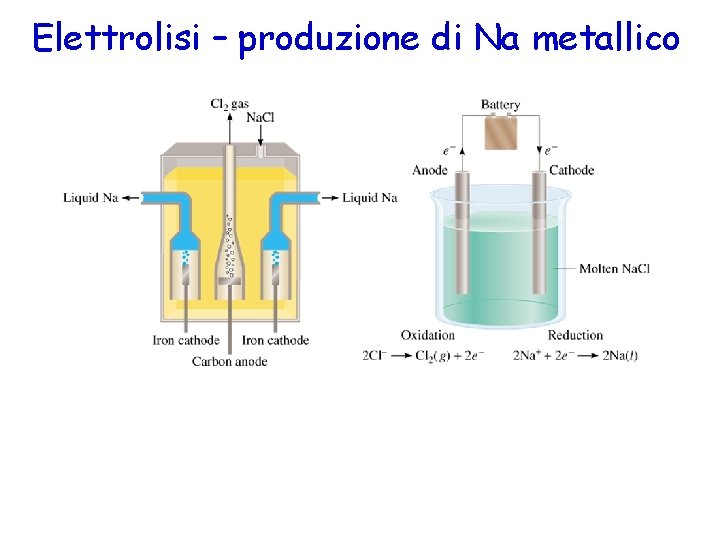
Elettrolisi – produzione di Na metallico
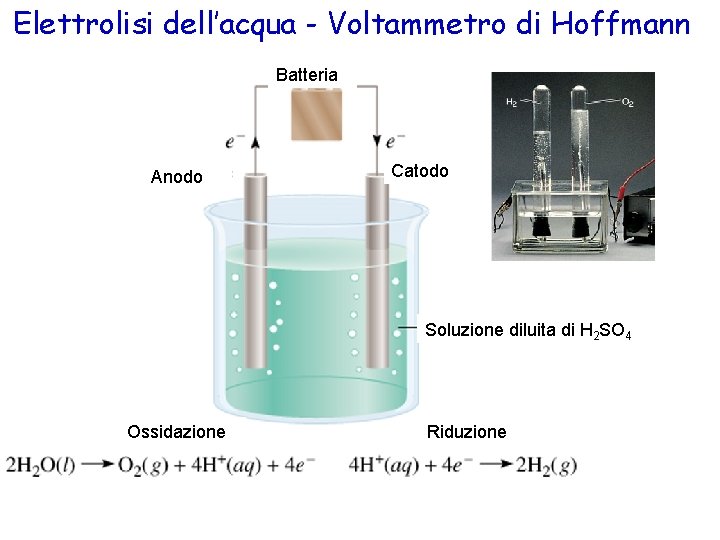
Elettrolisi dell’acqua - Voltammetro di Hoffmann Batteria Anodo Catodo Soluzione diluita di H 2 SO 4 Ossidazione Riduzione

Leggi di Faraday elaborò una relazione quantitativa tra la quantità di corrente (q= i*t) che circola in una cella elettrolitica e l’entità della trasformazione chimica. I° Legge di Faraday: Le quantità delle specie chimiche formate o consumate agli elettrodi durante l’elettrolisi sono proporzionali alle quantità di corrente II° Legge di Faraday: Le quantità delle specie chimiche formate o consumate per il passaggio di una stessa quantità di corrente agli elettrodi sono proporzionali alla massa delle specie interessate all’elettrolisi Massa del metallo = (I * t /n. F) Ma

Relazione tra quantità di elettricità e quantità di prodotti di reazione Na+ + e- → Na Cl- → ½ Cl 2 + e. Con il passaggio di una carica elettrica pari a quella trasportata da una mole di elettroni ( 96500 C), si avrà la produzione di 1 mole di sodio e di ½ mole di cloro gassoso. Supponiamo di far circolare attraverso la cella, una corrente I da 0. 30 A per un tempo t di 40 minuti. La carica complessivamente fatta circolare corrisponde a: Q (C) = I (A) x t (s) = 0. 30 C/s x (40 x 60) s = 720 coulomb corrispondono alla carica trasportata da : 720 C /96500 C mol -1= 7. 5 x 10 -3 moli Si produrranno 7. 5 x 10 -3 moli di sodio metallico e 3. 73 x 10 -3 moli di Cl 2 1 mole di elettroni trasporta 96485 C
- Slides: 44

































































