Elementi Iagrupe Alkalni metali Li Na K Rb

Elementi Ia-grupe Alkalni metali Li, Na, K, Rb, Cs, Fr ns 1 ↑ ns np 1
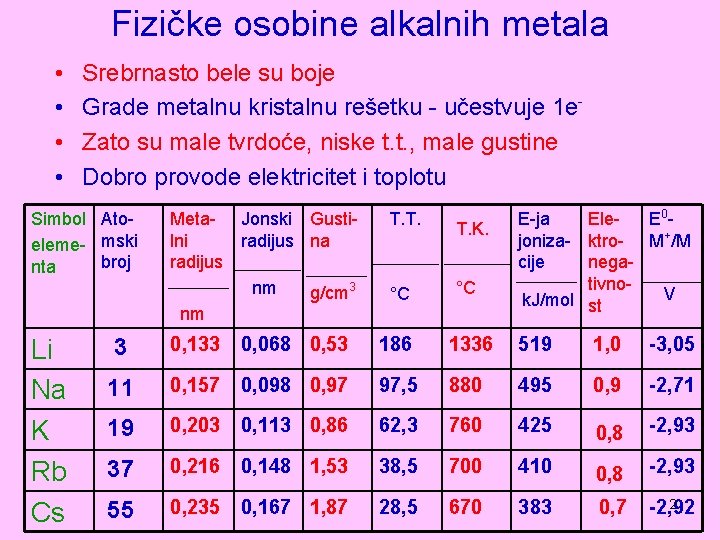
Fizičke osobine alkalnih metala • • Srebrnasto bele su boje Grade metalnu kristalnu rešetku - učestvuje 1 e. Zato su male tvrdoće, niske t. t. , male gustine Dobro provode elektricitet i toplotu Simbol Atoeleme- mski broj nta Li Na K Rb Cs Meta- Jonski Gustilni radijus na radijus nm g/cm 3 nm T. T. K. °C °C E-ja Ele. E 0 joniza- ktro- M+/M cije negativno. V k. J/mol st 3 0, 133 0, 068 0, 53 186 1336 519 1, 0 -3, 05 11 0, 157 0, 098 0, 97 97, 5 880 495 0, 9 -2, 71 19 0, 203 0, 113 0, 86 62, 3 760 425 0, 8 -2, 93 37 0, 216 0, 148 1, 53 38, 5 700 410 0, 8 -2, 93 55 0, 235 0, 167 1, 87 28, 5 670 383 0, 7 2 -2, 92

Svi akalni metali se čuvaju u petroleumu ili parafinskom ulju litijum rubidijum natrijum kalijum cezijum 3
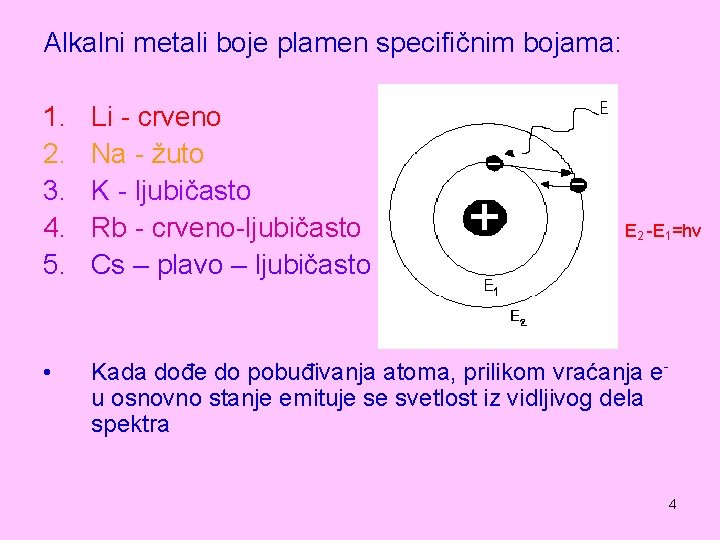
Alkalni metali boje plamen specifičnim bojama: 1. 2. 3. 4. 5. Li - crveno Na - žuto K - ljubičasto Rb - crveno-ljubičasto Cs – plavo – ljubičasto • Kada dođe do pobuđivanja atoma, prilikom vraćanja eu osnovno stanje emituje se svetlost iz vidljivog dela spektra E 2 -E 1=hν 4

Rasprostranjenost i nalaženje u prirodi • • 1. 2. 3. Zbog svoje reaktivnosti se NE nalaze u prirodi slobodni, već samo u obliku jedinjenja Natrijum: Na. Cl – kamena so Na. NO 3 – čilska šalitra Na 3 Al. F 6 – kriolit Kalijum: KCl - silvin KCl · Mg. Cl 2 · 6 H 2 O – karnalit KAl. Si 3 O 8 – ortoklas 5 ortoklas

Dobijanje alkalnih metala • Zbog svojih veoma negativnih redokspotencijala mogu se dobiti jedino elektrolizom rastopa njihovih soli ili hidroksida Na. Cl → Na+ + Cl. K(-): 2 Na+ + 2 e- → 2 Na - redukcija A(+): 2 Cl- → Cl 2 + 2 e- - oksidacija 6
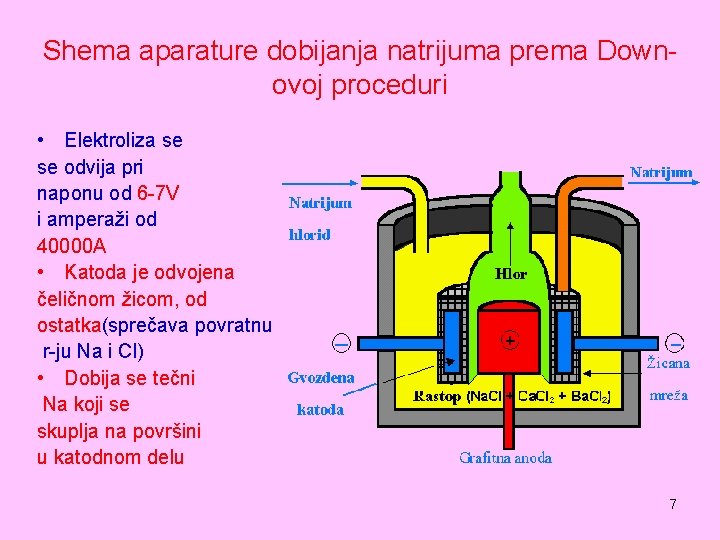
Shema aparature dobijanja natrijuma prema Downovoj proceduri • Elektroliza se se odvija pri naponu od 6 -7 V i amperaži od 40000 A • Katoda je odvojena čeličnom žicom, od ostatka(sprečava povratnu r-ju Na i Cl) • Dobija se tečni Na koji se skuplja na površini u katodnom delu 7

Primena • Litijum: 1. Kao redukciono i dehidrataciono sredstvo 2. Kao katalizator 3. Za izradu suvih galvanskih elemenata • Natrijum: 1. Industrijska primena se zasniva na redukcionim osobinama Na 2. U industriji boja, sintetičkog kaučuka, u raznim sintezama (B, Si, Na. NH 2, Na. CN, Na. H…) 3. Izradu Na-sijalica (emituju žutu boju koja prodire kroz prašinu i maglu) Litijumova baterija Na-sijalica 8

• Kalijum 1. Za dobijanje superoksida, KO 2 , koji vezuje ugljendioksid i oslobađa kiseonik 4 KO 2 + 2 CO 2 → 2 K 2 CO 3 + 3 O 2 Ova r-ja se koristi kao izvor kisonika u podmornicama i kosmičkim brodovima Rastvorne soli K se koriste kao vestačka đubriva U industriji sapuna (K-sapuni su mekši od Na-sapuna) Ima važnu ulogu u biološkim sistemima zajedno sa Na - regulišu krvi pritisak - regulišu zadržavanje vode - utiču na pravilan rad srca - promena koncentracije jona Na+ i K+ izaziva prenošenje nervnih impulsa 2. 3. 4. 9
- Slides: 9