Elemente si combinatii chimice Sistem periodic Proprietati periodice

Elemente si combinatii chimice Sistem periodic Proprietati periodice Hidrogen & Oxigen & Combinatii (ale acestora) http: //vl. academicdirect. org/general_chemistry/periodic_system
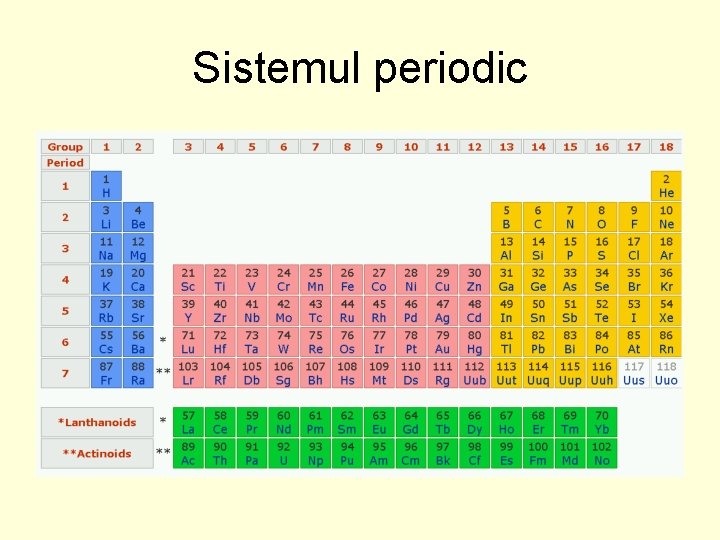
Sistemul periodic
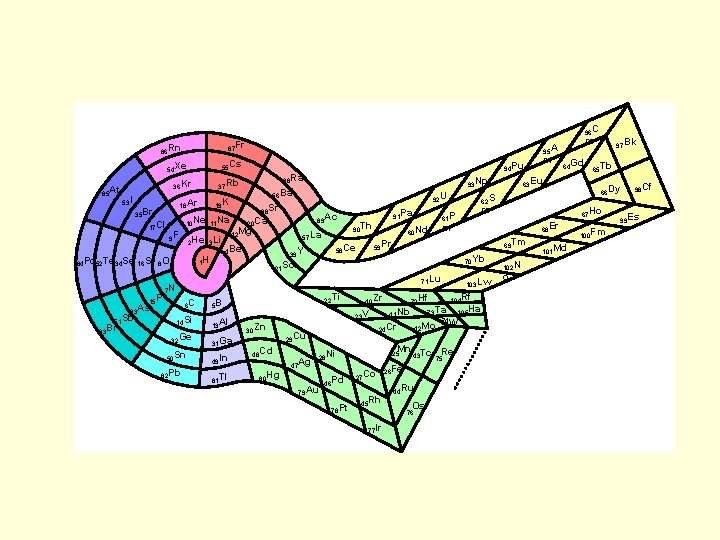
96 C 87 Fr 86 Rn 55 Cs 54 Xe 85 At 53 I 17 Cl 84 Po 52 Te 34 Se 16 S 51 Sb 83 Bi 10 Ne 9 F 11 Na 2 He 3 Li 1 H 8 O 15 P 33 As 19 K 18 Ar 35 Br 93 Np 56 Ba 92 U 38 Sr 89 Ac 20 Ca Mg 12 57 La 4 Be 91 Pa 90 Th 58 Ce 39 Y 14 Si 32 Ge 50 Sn 82 Pb 22 Ti 13 Al 31 Ga 49 In 81 Tl 30 Zn 69 Tm 70 Yb 48 Cd 47 Ag 40 Zr 105 Ha 73 Ta 74 W 79 Au 46 Pd 78 Pt 42 Mo Mn Tc Re 43 28 Ni 80 Hg 103 Lw 104 Rf 72 Hf 41 Nb 23 V 24 Cr 29 Cu 68 Er 59 Pr 25 27 Co 45 Rh 75 26 Fe 44 Ru Os 76 77 Ir 97 Bk 65 Tb 66 Dy 67 Ho m 71 Lu 5 B 63 Eu m 61 P 60 Nd 64 Gd 62 S 21 Sc 7 N 6 C m 94 Pu 88 Ra 37 Rb 36 Kr m 95 A 102 N o 101 Md 100 Fm 98 Cf 99 Es

• Criteriul de bază al clasificării elementelor este numărul atomic, Z care reprezintă numărul total de electroni ai atomilor, respectiv numărul de protoni din nucleu • Elementele în sistemul periodic sunt aşezate în coloane verticale - grupe - respectiv şiruri orizontale - perioade. Succesiunea perioadelor respectă succesiunea nivelelor principale de energie sau a straturilor electronice din atomi. Deci numărul perioadei din sistem este egal cu numărul cuantic principal (a stratului în curs de ocupare). Numărul grupei reprezintă numărul electronilor de pe ultimul înveliş, care determină proprietăţile chimice ale elementelor. Astfel se explică similitudinea proprietăţilor chimice în grupe. • Proprietăţile chimice ale elementelor sunt determinate în primul rând de tendinţa atomilor de a realiza configuraţii electronice cât mai stabile şi de a-şi folosi cât mai complet orbitalele de valenţă.

• The periodic "law" of chemistry recognises that properties of the chemical elements are periodic functions of their atomic number (that is, the number of protons within the element's atomic nucleus). The periodic table is an arrangement of the chemical elements ordered by atomic number in columns (groups) and rows (periods) presented so as to emphasize their periodic properties. • There are many different ways, sometimes ingenious, of arranging the chemical elements according to which properties are of particular interest but that shown here is a standard form of the periodic table. The relative merits of various other periodic table organisations is still the subject of debate.

Marimi si proprietati • Anion: atom sau grup de atomi care contin mai multi electroni decat protoni – consecinta - orice sistem incarcat negativ este referit ca anion; Cation: idem opus • Raza atomica: masura dimensiunii relative a atomilor (vezi O 2 si H 2 O) • Afinitatea electronica: masura a abilitatii sau tendintei unui atom de a primi electroni – concept energetic – definitia formala refera un electron: X + 1 e- → X-1 + E. A. • Electronegativitatea: abilitatea unui atom legat de a atrage electroni; la nivel de legatura, electronul poate fi pus in comun sau transferat; Scara Pauling postuleaza electronegativitatea F: 4. 0 si H: 1. 0; Ies din scara metalele; ex Fr: 0. 7. • Potential de ionizare: proces energetic ce refera formarea cationului: X + I. P. → X+ + 1 e-; exista si potentiale de ionizare suplimentare (ex. X+ +I. P. 2 → X 2+ + 1 e-

Tendinte periodice • Refera schimbarea proprietatilor atomilor care au loc in la deplasarea in interiorul grupelor si perioadelor • In perioada de la stanga la dreapta: I. P. , E. A. , electronegativitatea cresc; Dimensiunea (raza) scade; • In grupa de sus in jos: I. P. , E. A. , electronegativitatea scad; Dimensiunea (raza) creste; • Factori de stabilitate – electroni cedati sau primiti de atomi in procesul de formare de legaturi chimice cu scopul de a creste stabilitatea prin legatura: – Tendinta de a ajunge la configuratia electronica a unui gaz nobil; – Tendinta de a pierde toti electronii de valenta (uneori in special cei de pe subnivelul p); – Tendinta de a mentine: Ocupati, jumatate ocupati si neocupati seturile de orbitali
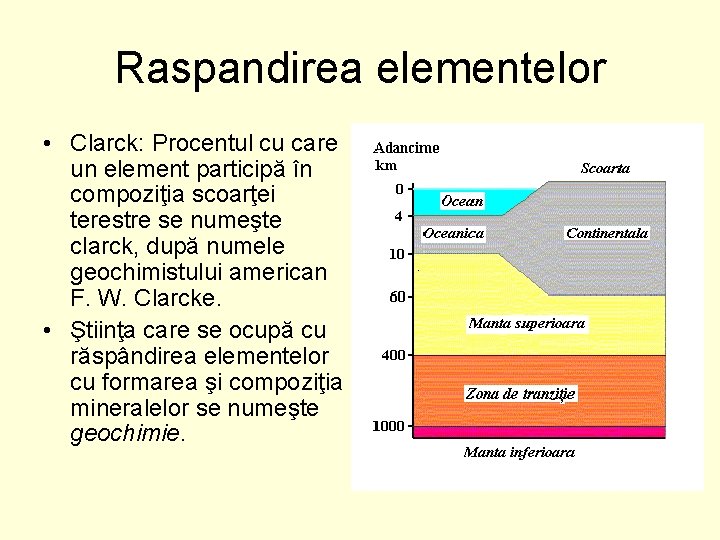
Raspandirea elementelor • Clarck: Procentul cu care un element participă în compoziţia scoarţei terestre se numeşte clarck, după numele geochimistului american F. W. Clarcke. • Ştiinţa care se ocupă cu răspândirea elementelor cu formarea şi compoziţia mineralelor se numeşte geochimie.

Răspândirea elementelor in scoarţă În scoarţa terestră 15 elemente, majoritatea de la începutul sistemului periodic, cu Z mic, formează aproximativ 99. 8%, pe când restul elementelor abia însumează 0. 52%. Cele mai răspândite elemente din scoarţă sunt oxigenul, siliciul şi aluminiul, care reprezintă peste 82%.

Raspandirea elementelor in atmosfera • Învelişul gazos din imediata vecinătate a Pământului este atmosfera. Atmosfera este formată mai ales din azot (78%) şi oxigen (21%), alături de alte elemente în cantităţi foarte mici.

Minereuri
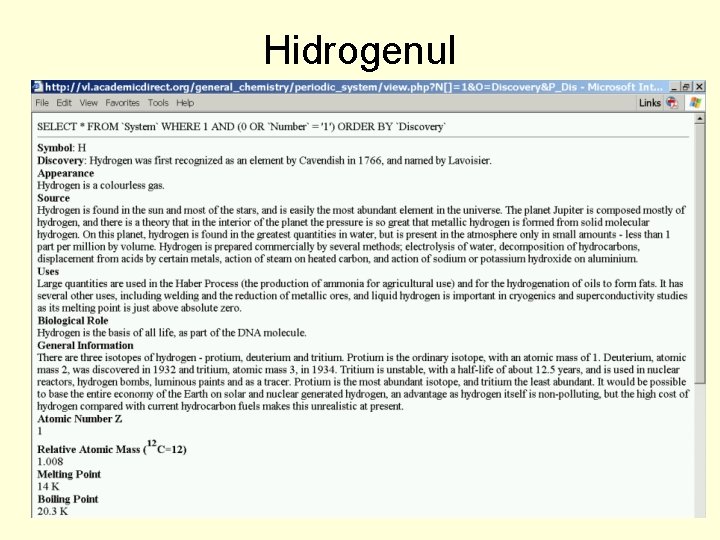
Hidrogenul
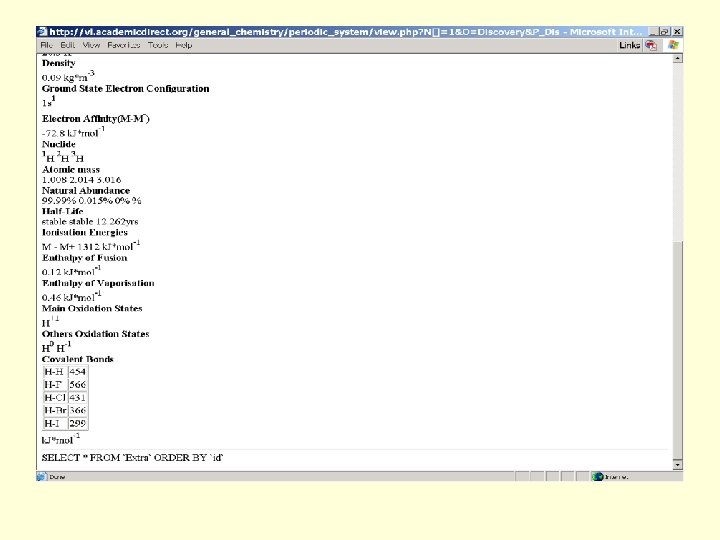

• configuraţia 1 s 1 şi stabilitatea la ionizare fac ca hidrogenul să formeze în majoritatea combinaţiilor legături covalente. • Ionii H+ şi : H- sunt instabili - chimic se traduce prin a afirma că sunt foarte reactivi • Astfel, din cauza câmpului electrostatic extrem de intens generat în jurul, său protonul nu poate exista singur în aceeaşi soluţie cu moleculele polare, sau specii ce se pot polariza, reacţionând instantaneu. • In apă, ionul H+ se stabilizează devenind ionul hidroniu, notat H 3 O+, iar în amoniac devine ionul amoniu, NH 4+, legătura coordinativă datorându-se unei perechi de electroni neparticipanţi. • Clasic: H+ + H 2 O → H 3 O+, ΔH= -1093 k. J·mol-1 • In realitate există mai multe specii hidroniu ce conţin 3, 4, . . . , 12 molecule de apă legate împreună, cea mai probabilă fiind: (H 2 O)4 H+, dar pentru simplitate toate aceste specii se notează simplificat H 3 O+

• Hidrogenul are trei izotopi purtând nume distincte: protiul, deuteriul şi tritiul respectiv: 11 H, 12 H (notat D) şi 13 H (notat T). Evident masa deuteriului este de două ori masa protiului iar a tritiului de trei ori masa acestuia. 99. 985% din hidrogenul scoarţei terestre este reprezentat de protiu şi doar 0. 015% este deuteriu. Acesta este motivul pentru care masa atomică hidrogenului este fracţionară (1. 008). Izotopul natural cel mai greu - tritiul - este βradioactiv, având un timp de înjumătăţire T 1/2 = 12. 26 ani, trecând prin dezintegrare în heliu. De aceea poate fi utilizat fără pericol în calitate de trasor radioactiv, pentru că face posibilă urmărirea manierei în care loc o succesiune complicată de reacţii sau etape tehnologice în care este implicat şi hidrogenul.

Obtinerea hidrogenului • O primă cale pleacă de la hidrocarburi cu masă moleculară joasă. În procesele industriale de rafinare a benzinelor, hidrogenul rezultă ca produs secundar. Astfel în procesul de sinteză a octanului, C 8 H 18, pornindu-se de la molecule mai mici se obţine şi hidrogen: 2 C 2 H 6 + C 4 H 8 C 8 H 18 + H 2 • Un alt procedeu, în care sunt implicate de asemenea hidrocarburi, este cracarea - o tehnologie de transformare a moleculelor de hidrocarburi mari în molecule mai mici - rezultând atât hidrogen cât şi molecule de hidrocarburi nesaturate. De exemplu: C 12 H 26 C 5 H 10 + C 4 H 8 + C 3 H 6 + H 2

• Alte metode de obţinere a hidrogenului utilizează, pe lângă hidrocarburi, vapori de apă şi catalizatori. Unul dintre aceste procedee este reformarea catalitică. Astfel, dacă se utilizează metan şi vapori de apă rezultă monoxid de carbon şi hidrogen: CH 4 + H 2 O CO + 3 H 2 • Produsul (amestecul CO + H 2) este cunoscut şi sub numele de gaz de sinteză întrucât se poate folosi ca materie primă într-o serie de sinteze industriale, ca de exemplu în cea a alcoolului metilic. Printr-o a doua reacţie catalitică oxidul de carbon se poate converti cu vapori de apă, în dioxid de carbon şi hidrogen fenomenul fiind cunoscut sub numele de reacţia gazului de apă: CO + H 2 O Fe/Cu→ 500°C CO 2 + H 2 Fe/Cu - fier activat cu cupru.

Proprietăţi chimice ale hidrogenului. Reacţii cu nemetale
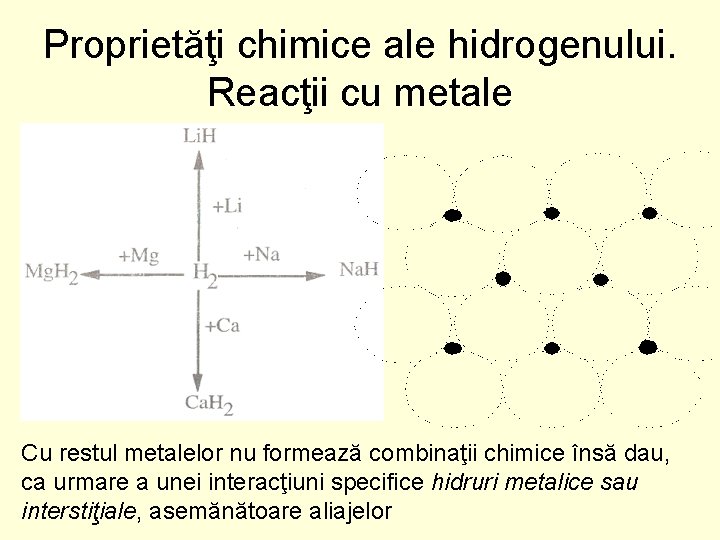
Proprietăţi chimice ale hidrogenului. Reacţii cu metale Cu restul metalelor nu formează combinaţii chimice însă dau, ca urmare a unei interacţiuni specifice hidruri metalice sau interstiţiale, asemănătoare aliajelor

Caracterul reducător al hidrogenului • Cu foarte multe combinaţii, inclusiv organice, hidrogenul prezintă un caracter reducător, în principiu asemănător celui din reacţia cu nemetalele (oxidanţi). Pe baza acestui caracter reducător, hidrogenul se utilizează în extracţia hidro-metalurgică a cuprului sau a altor metale: Cu 2+(aq) + H 2(g) = Cu(s) + 2 H+(aq) • Astfel, după ce cuprul, provenit din minereu, este transformat în sulfat de cupru, prin barbotare de hidrogen se poate separa cuprul metalic. Cam 1/3 din tot hidrogenul fabricat industrial este utilizat pentru astfel de reduceri. Condiţia necesară pentru a fi posibilă o astfel de reducere este ca potenţialul redox al metalului (ε°) să fie pozitiv. • De asemenea, un mare număr de oxizi se poate reduce cu hidrogen la metal, evident la o temperatură ridicată, servind la obţinerea acestora. De exemplu, trioxidul de wolfram se poate reduce la metal: WO 3 + 3 H 2 W + 3 H 2 O
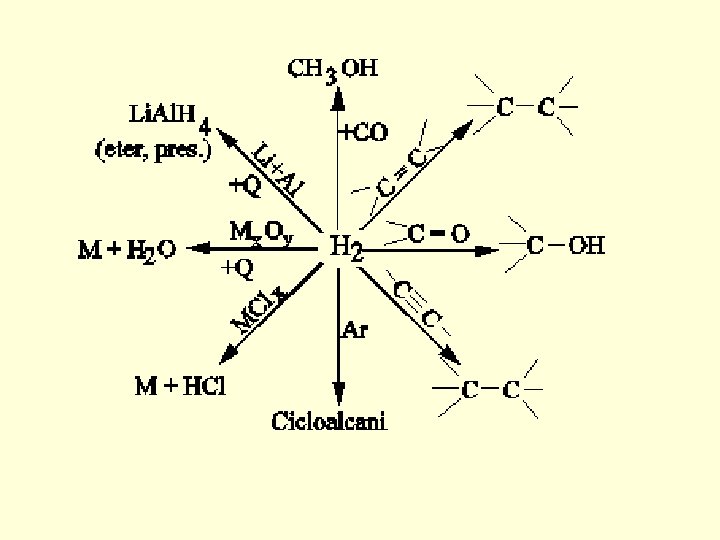

• Pe de altă parte o mare cantitate de hidrogen este utilizată în industria alimentară pentru hidrogenarea uleiurilor vegetale, acestea având o legătură dublă izolată în interiorul unui lanţ saturat, R, dintr-un acid gras (R-COOH): H 2 + …-CH 2 -CH= CH-CH 2 - … …-CH 2 – CH 2 -CH 2 -··· • Procesul este de asemenea o reducere. În urma acestui tratament uleiurile (grăsimile lichide), ce conţin legături duble (fig. 2. 1. 4), devin grăsimi solide (margarina) din cauza faptului că, împachetându-se mai bine, interacţiunile catenelor (moleculelor) se intensifică • Hidrogenul este folosit în practica industrială datorită reacţiilor de hidrogenare catalitică dintre care se disting ca importanţă hidrogenările azotului, oxidului de carbon şi uleiurilor naturale: – – – • azotului (procedeul Haber); oxidului de carbon: CO + 2 H 2 → CH 3 OH (metanol); uleiurilor nesaturate cu formare de catene hidrocarbonate saturate (aplicată în obţinerea margarinei). Toate reacţiile amintite se petrec catalitic în condiţii energice.

Oxigenul • Oxigenul este primul element al grupei 16 având configuraţia electronică 2 s 22 p 4; este al doilea element, din punct de vedere al electronegativităţii, după fluor • Oxigenul este elementul cel mai răspândit în natură (46. 59%) atât în aer în stare liberă (20. 9% volum), în apă (88. 89%) şi în scoarţa terestră intrand în compoziţia majorităţii rocilor şi mineralelor (46. 6%). • Existenţa oxigenului a făcut posibilă apariţia formelor superioare ale vieţii pe pământ. Oceanele acoperă trei sferturi din suprafaţa Pământului. În scoarţă oxigenul se găseşte mai ales sub formă de oxo-săruri – silicaţi şi alumino-silicaţi, carbonaţi, sulfaţi, nitraţi, şi sub formă de oxizi. • Oxigenul are 3 izotopi: 16 O (99. 759%), 17 O (0. 0374%), 18 O (0. 239%). Prin distilarea fracţionată a apei se pot concentra până la 97% atomice în cazul 18 O sau 4% atomice de 17 O. Izotopul 18 O foloseşte ca trasor în studiul mecanismelor de reacţie ale compuşilor cu oxigen. 17 O are spin nuclear şi se poate utiliza în studii de rezonanţă, de exemplu pentru a face distincţie între apa din complecşi, de exemplu: Co(NH 3)5∙H 2 O, şi apa ca solvent.

• Stări alotropice. Oxigenul are două stări alotropice: O 2 – dioxigen, şi O 3 – trioxigen sau ozon. • Reacţia de formare a O 3 din O 2 este de asemenea endotermă iar inversul acesteia, firesc este una exotemă: 3 O 2 → 2 O 3 ΔH = +8. 1 k. J·mol-1 2 O 3 → 3 O 2 ΔH = -142 k. J·mol-1 • Se mai poate forma O 3 şi prin disocierea termică a O 2 peste 1500°C, când O 2 disociază în 2 atomi de O care cu O 2 dau O 3. • Acţiunea radiaţiilor ultraviolete (UV) asupra O 2 produce urme de O 3 în atmosfera superioară (stratosferă). Concentraţia maximă de ozon în stratosferă se află la altitudinea de ~25 km. Prezenţa ozonului în atmosfera superioară este de importanţă vitală pentru protejarea scoarţei terestre de expunere excesivă la radiaţii UV.

• • Metode de obţinere a O 2 Industrial Distilarea fracţionată a aerului lichid. O 2 are p. f. = -182. 9 °C iar N 2 are p. f. = -195. 7 °C, astfel încât se pot separa destul de uşor. Oxigenul se îmbuteliază în tuburi de oţel la presiuni de 150 atm, care se pot astfel transporta şi utiliza în multe domenii. Electroliza apei acidulate sau alcalinizate, de exemplu soluţii de Na. OH 15 -20%, folosind catod de Fe şi anod de grafit. La catod se separă H 2 iar la anod O 2. În laborator Se poate obţine O 2 în cantităţi mici prin descompunerea termică a unor combinaţii: - oxizi: 2 Hg. O → O 2 + 2 Hg, 3 Mn. O 2 → O 2 + Mn 3 O 4 - peroxizi: 2 Ba. O 2 → O 2 + 2 Ba. O - săruri: KCl. O 3→ 3/2 O 2 + KCl, 2 KMn. O 4 → O 2 + Mn. O 2 + K 2 Mn. O 4 O altă cale de obţinere este utilizarea unor reacţii redox: 4 Mn. O 4 - + 12 H+ → 5 O 2 + 4 Mn 2+ + 6 H 2 O
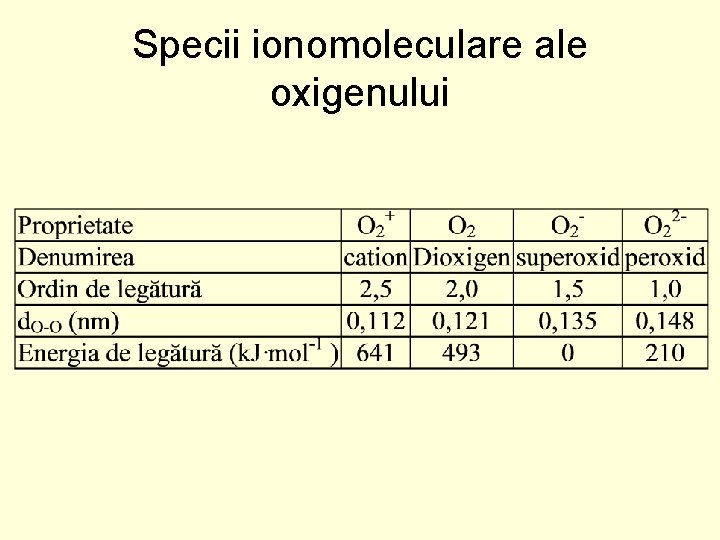
Specii ionomoleculare ale oxigenului

Arderi • Unele elemente reacţionează energic cu oxigenul cu degajare mare de căldură şi lumină (arderi vii). Aceste reacţii sunt şi mai violente în O 2 curat decât în aer. Dintre nemetale, fosforul, carbonul şi sulful ard uşor în O 2, iar dintre metale, Mg, Al, Fe (aduse la incandescenţă). • Arderea cărbunilor fosili şi a hidrocarburilor constituie principala sursă de căldură şi indirect de energie a civilizaţiei umane. • Arderea unui amestec de H 2 sau hidrocarburi cu O 2 sau aer este o reacţie explozivă (mecanismul este de reacţie în lanţ, prin atomi şi radicali liberi, cu o fază de iniţiere prin scânteie sau flacără).

• oxidarea halogenurilor la halogen elementar: Si. Cl 4 + O 2 = 2 Cl 2 + Si. O 2 Mg. Cl 2 + O 2 = Cl 2 + 2 Mg. O 2 Al. Br 3 + 3/2 O 2 = 3 Br 2 + Al 2 O 3 • oxidarea sulfurilor (prăjirea), importantă în metalurgie: 2 Fe. S + 7/2 O 2 = Fe 2 O 3 + 2 SO 2 Zn. S + 3/2 O 2 = Zn. O + SO 2 • oxidarea unor oxizi inferiori: CO +1/2 O 2 = CO 2 2 Fe. O + 1/2 O 2 = Fe 2 O 3 SO 2 + 1/2 O 2 → SO 3 (în prezenţă de catalizator) NO +1/2 O 2 = NO 2 • oxidarea hidrurilor covalente (ale nemetalelor) 2 HX + 1/2 O 2 → X 2 + H 2 O, X = Cl, Br, I SH 2 + 1/2 O 2 → S + H 2 O 2 NH 3 + 3/2 O 2 → N 2 +3 H 2 O CH 4 + O 2 → CO 2 + 2 H 2 O

• Astăzi se admite că sunt posibile mai multe reacţii în soluţie apoasă: O 2 + 4 H+ + 4 e- = 2 H 2 O ε 0 = +1. 229 V O 2 + 2 H 2 O + 4 e- = 4 OH- ε 0 = +0. 401 V O 2 + 2 H+ + 2 e- = H 2 O 2 ε 0 = +0. 682 V O 2 + H 2 O + 2 e- = OH- + HO 2 - ε 0 = -0. 076 V

Biochimia oxigenului • Existenţa oxigenului în atmosfera terestră este esenţială pentru viaţa de pe Pământ. Cea mai mare parte a oxigenului din atmosferă este produs în procesul de fotosinteză de către plantele verzi, în care clorofila foloseşte energia solară, sintetizând zaharuri. Procesul se numeşte asimilaţie clorofiliană: 6 CO 2 + 6 H 2 O → C 6 H 12 O 6 + 6 O 2 • Aceasta este o reacţie endotermă care poate avea loc numai în prezenţa luminii solare, unica sursă de energie care întreţine viaţa pe pământ. Vieţuitoarele consumă oxigenul din atmosferă, în procesul de respiraţie, cu eliminare de CO 2: C 6 H 12 O 6 + 6 O 2 → 6 CO 2 + 6 H 2 O

Oxizi • Oxizi ionici, Oxizi covalent – ionici, Oxizi covalenţi • Ionici: – Elementele din grupele 1 şi 2 formează oxizi cu legături predominant ionice – Metalele blocului d şi f, de regulă în stări inferioare de oxidare, formează de asemenea oxizi ionici, având tot un caracter bazic – Aceşti oxizii cristalizează în reţele ionice, compuse din ioni O 2 - şi cationii metalelor respective – Ionul O 2 - există numai în stare solidă, iar în prezenţa apei hidrolizează: O 2 - + H 2 O = 2 OH-

• Covalenţi: – sunt oxizii nemetalelor şi au caracter acid – aceştia sunt formaţi în general din molecule covalente simple, de exemplu CO, CO 2, NO 2, SO 3 – Oxizii cu caracter covalent formează şi unele metale tranziţionale în trepte superioare de oxidare – Cei solubili dau cu apa acizi (sunt deci anhidride de acizi): SO 2 + H 2 O = H 2 SO 3 – Cei insolubili reacţionează cu bazele formând săruri ale acizilor corespunzători: Sb 2 O 5 + 2 OH- + 5 H 2 O = 2[Sb(OH)6] • Covalent-ionici: – Sunt formati cu restul elementelor – Au proprietati intermediare (amfoteri) Al 2 O 3 + 6 H+ = 2 Al 3+ + 3 H 2 O Al 2 O 3 + 2 OH- + 3 H 2 O = 2[Al(OH)4]-
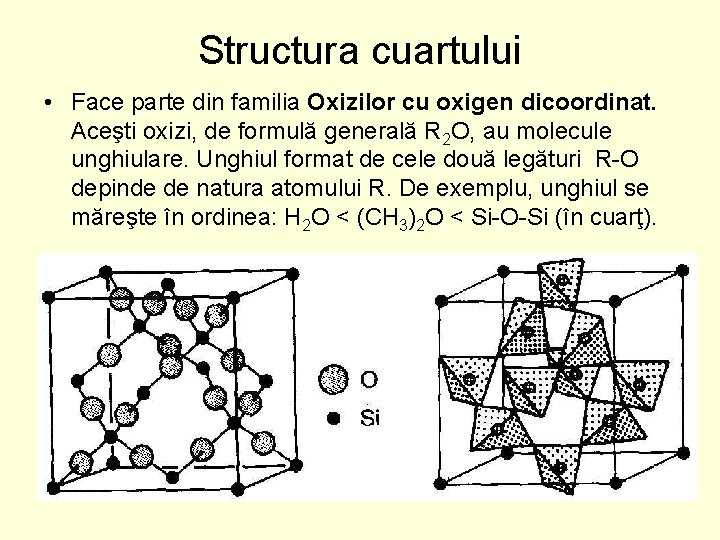
Structura cuartului • Face parte din familia Oxizilor cu oxigen dicoordinat. Aceşti oxizi, de formulă generală R 2 O, au molecule unghiulare. Unghiul format de cele două legături R-O depinde de natura atomului R. De exemplu, unghiul se măreşte în ordinea: H 2 O < (CH 3)2 O < Si-O-Si (în cuarţ).
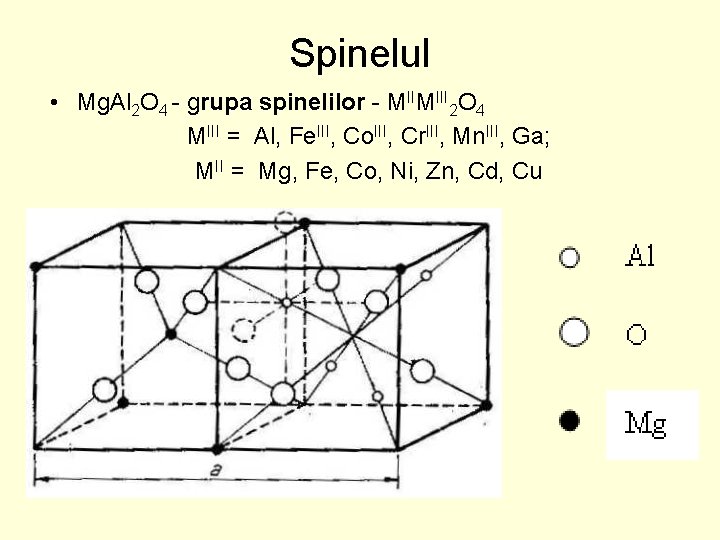
Spinelul • Mg. Al 2 O 4 - grupa spinelilor - MIIMIII 2 O 4 MIII = Al, Fe. III, Co. III, Cr. III, Mn. III, Ga; MII = Mg, Fe, Co, Ni, Zn, Cd, Cu
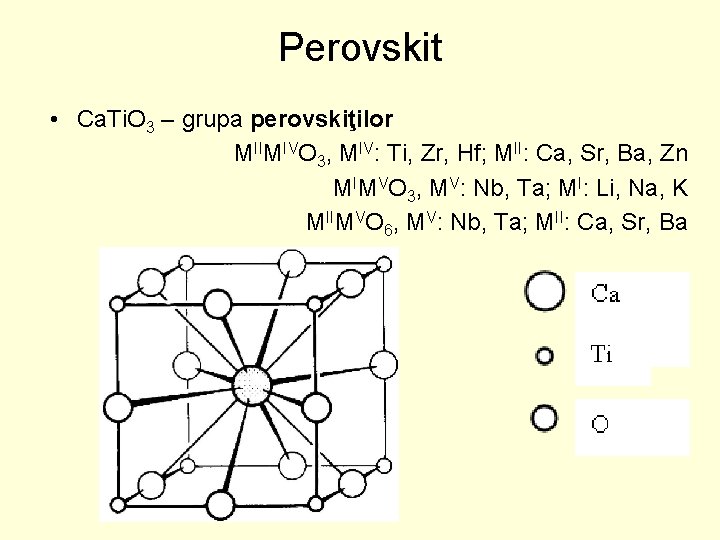
Perovskit • Ca. Ti. O 3 – grupa perovskiţilor MIIMIVO 3, MIV: Ti, Zr, Hf; MII: Ca, Sr, Ba, Zn MIMVO 3, MV: Nb, Ta; MI: Li, Na, K MIIMVO 6, MV: Nb, Ta; MII: Ca, Sr, Ba
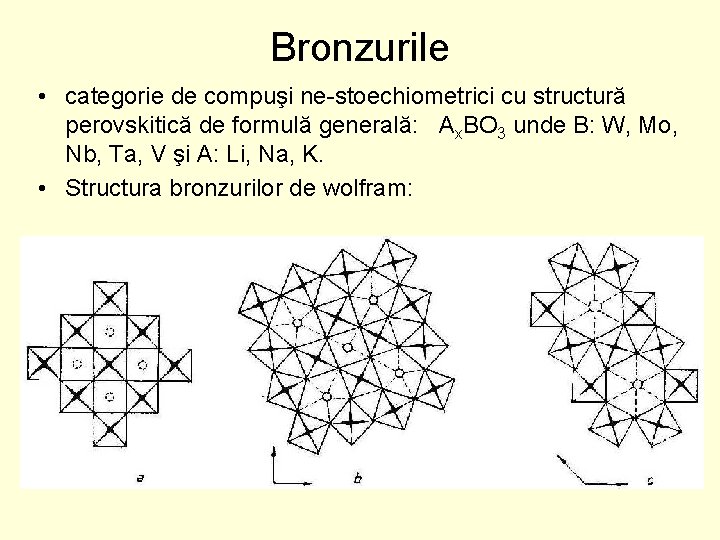
Bronzurile • categorie de compuşi ne-stoechiometrici cu structură perovskitică de formulă generală: Ax. BO 3 unde B: W, Mo, Nb, Ta, V şi A: Li, Na, K. • Structura bronzurilor de wolfram:
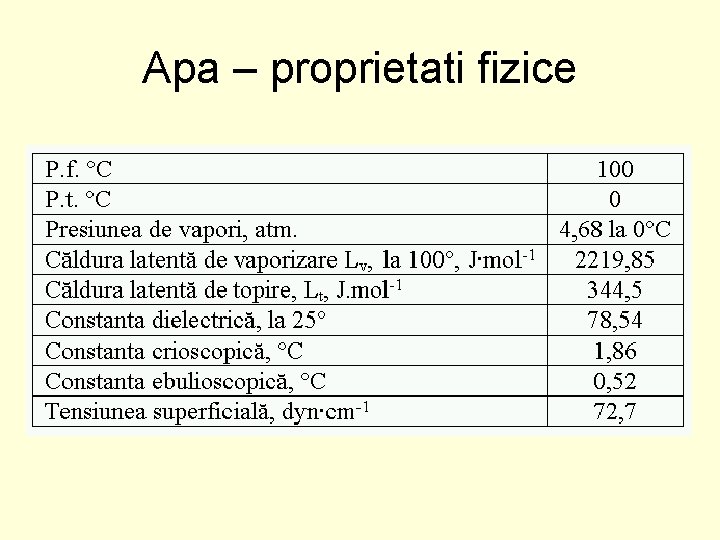
Apa – proprietati fizice

Apa – proprietati chimice

Water properties: p. H • No, you don't often hear your local news broadcaster say "Folks, today's p. H value of Dryville Creek is 6. 3"! But p. H is an important measurement of water. Maybe for a science project you have taken the p. H of water samples in your chemistry class. . . and here at the U. S. Geological Survey we take a p. H measurement whenever water is studied. Not only does the p. H of a stream affect organisms living in the water, a changing p. H in a stream can be an indicator of increasing pollution or some other environmental factor. • As this diagram shows, p. H ranges from 0 to 14, with 7 being neutral. p. Hs less than 7 are acidic while p. Hs greater than 7 are alkaline (basic). You can see that acid rain can be very acidic, and it can affect the environment in a negative way.

- Slides: 40